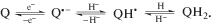Химия высоких энергий, 2021, T. 55, № 4, стр. 318-320
О взаимодействии семихинонов с ионами железа (III)
В. С. Кособуцкий *
Белорусский государственный университет
220030 Минск, просп. Независимости, 4, Беларусь
* E-mail: kasabutski@bsu.by
Поступила в редакцию 17.02.2021
После доработки 10.03.2021
Принята к публикации 12.03.2021
Семихиноны (Q–•) образуются при одноэлектронном восстановлении хинонов (Q) или окислении гидрохинонов (QH2):
Хиноны являются активными участниками важнейших биохимических окислительно-восстановительных процессов. Именно этот процесс обратимого восстановления лежит в основе биологического использования хинонов. При транспорте электронов по дыхательной цепи в присутствии восстановителей типа НАД убихиноны переходят из хинонной формы в гидрохинонную и обратно через образование семихинонов. Аналогичные превращения претерпевают пластохиноны при транспорте электрона в процессах фотосинтеза [1–3]. Природные и синтетические антиоксиданты на основе бифенолов в процессах ингибирования перекисного окисления липидов превращаются в семихиноны
Многие хиноны используются как лекарственные препараты для лечения онкологических и других заболеваний [4–6]. В биосистемах существуют ферментативные и неферментативные системы восстановления хинонов, витаминов К. Их восстановление идет через образование семихинонов. В работе исследуется возможность окисления семихинонов ионами железа. Этот процесс может приводить к нарушению хинон-гидрохинонных превращений в биосистемах, а также к нарушению процессов антиоксидации с участием дифенолов в живых и неживых системах.
Таблица 1
| ${{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{{\text{ + 3}}}}}}}}$ × 104, М | Gац, молекула/100 эВ | ${{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{{\text{ + 2}}}}}}}}$, ион/100 эВ |
|---|---|---|
| 0 | 3.41 ± 0.21 | 0 |
| 1 | 4.17 ± 0.22 | 0.80 ± 0.19 |
| 2 | 4.64 ± 0.21 | 2.27 ± 0.18 |
| 3 | 4.79 ± 0.25 | 2.87 ± 0.27 |
| 4 | 5.03 ± 0.28 | 3.85 ± 0.51 |
| 6 | 6.02 ± 0.28 | 4.24 ± 0.33 |
Семихиноны генерировали действием γ-излучения на водные 1 моль/л растворы пропанола-2, содержащие 0.001 моль/л тетраметил-1,4-бензохинон. Для приготовления растворов использовали бидистиллированную воду. Концентрацию Fe2(SO4)3 варьировали в интервале (1–6) × × 10–4 моль/л. Перед облучением растворы многократно насыщали аргоном в шприце, при этом воздух в растворах замещался аргоном. Облучение проводили в запаянных стеклянных ампулах. Мощность поглощенной дозы по ферро-сульфатному дозиметру составляла 0.11 Гр/с. Ацетон анализировали методом ГЖХ с пламенно-ионизационным детектором. Ионы Fe+2 анализировали калориметрическим методом с использованием 2,2'-дипиридила [7]. Коэффициент экстинкции раствора малиновой окраски составил 8700 л моль–1 см–1 при длине волны 522 нм.
Под действием излучения в воде образуются радикальные частицы радиолиза воды: •ОН, eaq, Н с радиационно-химическими выходами 2.8, 2.8, 0.55 молекула/100 эВ соответственно [8]. Образование семихинонов в исследованных системах осуществлялось непосредственно по быстрой реакции (1) и за счет окисления гидроксиизопропильных радикалов хиноном (реакция (4)).
(1)
${{{\text{e}}}_{{{\text{aq}}}}}~~ + ~~{\text{Q}}~~ \to ~\,{{{\text{Q}}}^{{-- \bullet }}}~\,\,\,3.1 \times {{10}^{{10~}}}{\text{л мол}}{{{\text{ь}}}^{{--1}}}\,{{{\text{с}}}^{{--1}}}\,\,\,\left[ {9,{\text{ }}10} \right],$(3)
$\begin{gathered} ^{ \bullet }{\text{OH}} + {{\left( {{\text{С}}{{{\text{Н}}}_{{\text{3}}}}} \right)}_{{\text{2}}}}{\text{CHOH}}~~ \to \left( {{\text{С}}{{{\text{Н}}}_{{\text{3}}}}} \right)_{2}^{\centerdot }{\text{COH}}~\, + ~\,{{{\text{H}}}_{{\text{2}}}}{\text{O}}~ \\ 2.1 \times {{10}^{9}}\,\,{\text{л мол}}{{{\text{ь}}}^{{--1}}}\,{{{\text{с}}}^{{--1}}}\,\,\,\left[ 8 \right], \\ \end{gathered} $(4)
$\begin{gathered} \left( {{\text{С}}{{{\text{Н}}}_{{\text{3}}}}} \right)_{2}^{{}}{{{\text{C}}}^{\centerdot }}{\text{OH}}~\, + \,{\text{Q}} \to {{\left( {{\text{С}}{{{\text{Н}}}_{{\text{3}}}}} \right)}_{2}}{\text{CO}}\,\,~ + \,\,{{{\text{Q}}}^{{-- \bullet }}}~ + \,~{{{\text{H}}}^{{ + ~}}} \\ 3.6 \times {{10}^{9}}\,\,{\text{л мол}}{{{\text{ь}}}^{{--1}}}\,{{{\text{с}}}^{{--1}}}\,\,\,\left[ {10,{\text{ }}11} \right]. \\ \end{gathered} $Семихиноны присутствовали в растворе (рН 7) преимущественно в анионной форме, так как рК их диссоциации 4.95 (реакция (5))
(5)
${{{\text{Q}}}^{{-- \bullet }}}~~ + ~{\text{\;}}{{{\text{H}}}^{ + }}~~ \leftrightarrow ~~{\text{Q}}{{{\text{H}}}^{ \bullet }}~\,\,\,{\text{pK}}~\,\,4.95\,\,\,\left[ {13} \right].$Образование ацетона происходило по реакции (4). Окисление радикалов (СН3)2•COH ионами Fe+3 (реакция (6)) практически не протекало, так как константы скоростей реакций (4) и (6), а также концентрации Q и Fe+3 различаются на порядок
(6)
$\begin{gathered} \left( {{\text{С}}{{{\text{Н}}}_{{\text{3}}}}} \right)_{2}^{\centerdot }{\text{COH}}\,~ + \,{\text{F}}{{{\text{e}}}^{{ + 3}}}~ \to {{\left( {{\text{С}}{{{\text{Н}}}_{{\text{3}}}}} \right)}_{2}}{\text{CO}}\,~ + ~\,{\text{F}}{{{\text{e}}}^{{ + 2}}} + {{{\text{H}}}^{{ + ~}}}~ \\ 4.5 \times {{10}^{8}}\,\,{\text{л мол}}{{{\text{ь}}}^{{--1}}}\,{{{\text{с}}}^{{--1}}}~\,\,\,\left[ {10} \right]. \\ \end{gathered} $Образование ионов Fe+2, преимущественно, шло по реакции (7)
(7)
${{{\text{Q}}}^{{-- \bullet }}}~~ + ~~{\text{F}}{{{\text{e}}}^{{ + 3}}}~~ \to ~~{\text{Q}}~~ + ~~{\text{F}}{{{\text{e}}}^{{ + 2}}},$так как возможная реакция (8) имеет меньшую скорость по сравнению с реакцией (1) из-за преобладания концентрации хинона над концентрацией ионов Fe+3.
(8)
${{{\text{e}}}_{{{\text{aq}}}}}{\text{\;}}~ + ~~{\text{F}}{{{\text{e}}}^{{ + 3}}}~~ \to \,\,{\text{F}}{{{\text{e}}}^{{ + 2}}}\,\,~6.0 \times {{10}^{{10~}}}{\text{л мол}}{{{\text{ь}}}^{{--1}}}\,{{{\text{с}}}^{{--1}}}\,\,\,\left[ {10} \right].$Параллельно реакции (7) протекала и реакция (9) диспропорционирования семихинонов
(9)
$\begin{gathered} {{{\text{Q}}}^{{-- \bullet }}}~\, + {{{\text{Q}}}^{{-- \bullet }}}~ + {\text{ }}2{{{\text{H}}}_{{\text{2}}}}{\text{O}} \to {\text{Q}} + {\text{Q}}{{{\text{H}}}_{2}} + {\text{H}}{{{\text{O}}}^{--}} + {\text{H}}{{{\text{O}}}^{{--~}}}~ \\ 1.6 \times {{10}^{7}}\,\,{\text{л мол}}{{{\text{ь}}}^{{--1}}}\,{{{\text{с}}}^{{--1}}}\,\,\,\left[ {12} \right]. \\ \end{gathered} $Полученные зависимости выходов ацетона (Gац) и ионов Fe+2 (${{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{{\text{ + 2}}}}}}}}$) от концентрации ионов Fe+3 приведены в табл. 1.
Возрастание выхода ацетона, в основном, связано с образованием в растворах ионов Fe+2 и их реакцией (10) с пероксидом водорода
(10)
${\text{F}}{{{\text{e}}}^{{ + 2}}} + ~\,\,{{{\text{Н}}}_{{\text{2}}}}{{{\text{О}}}_{2}}~~ \to ~~{\text{F}}{{{\text{e}}}^{{ + 3}}}~~ + ~~{\text{О}}{{{\text{H}}}^{ \bullet }}~\, + ~\,{\text{H}}{{{\text{O}}}^{--}}.$Для оценки константы скорости (k7) реакции (7) окисления семихинонов ионами Fe+3 применим метод стационарных концентраций, согласно которому скорость образования радикалов равна скорости их гибели в реакциях. В условиях радиационного инициирования скорость образования частиц (Vо) выражается соотношением: Vо = (G P)/(100N), где G – радиационно-химический выход частицы, молекула/100 эВ; P – мощность поглощенной дозы, 6.9 × 1017 эВ/(л с); N – число Авогадро, 6 × 1023 молекула/моль. Тогда, из условий стационарности и в соответствии с реакциями (1), (2) и (3) следует, что
(11)
${{{{{\text{G}}}_{{{\text{eaq}}}}}{\text{P}}} \mathord{\left/ {\vphantom {{{{{\text{G}}}_{{{\text{eaq}}}}}{\text{P}}} {100{\text{N}}}}} \right. \kern-0em} {100{\text{N}}}} = {{k}_{1}}{{[{{{\text{e}}}_{{{\text{aq}}}}}{\text{]}}}_{{{\text{ст}}}}}{\text{[Q]}}~,$(12)
${{{{{\text{G}}}_{н}}{\text{P}}} \mathord{\left/ {\vphantom {{{{{\text{G}}}_{н}}{\text{P}}} {{\text{100N}}}}} \right. \kern-0em} {{\text{100N}}}} = {{k}_{2}}{{[{\text{H}}]}_{{{\text{ст}}}}}[{{({\text{C}}{{{\text{H}}}_{{\text{3}}}}{\text{)}}}_{{\text{2}}}}{\text{CHOH}}],$(13)
${{{{{\text{G}}}_{{{\text{он}}}}}{\text{P}}} \mathord{\left/ {\vphantom {{{{{\text{G}}}_{{{\text{он}}}}}{\text{P}}} {100{\text{N}}}}} \right. \kern-0em} {100{\text{N}}}} = {{k}_{3}}{{[{\text{ОН}}]}_{{{\text{ст}}}}}[{{({\text{C}}{{{\text{H}}}_{{\text{3}}}}{\text{)}}}_{{\text{2}}}}{\text{CHOH}}].$Для семихинонов Q–• с учетом реакций (1), (4), (7) и (9) получаем уравнение (14)
(14)
$\begin{gathered} {{k}_{1}}{{[{{{\text{e}}}_{{{\text{aq}}}}}]}_{{{\text{ст}}}}}[{\text{Q}}]~\, + ~\,{{k}_{4}}{{[({\text{C}}{{{\text{H}}}_{{\text{3}}}})_{2}^{{}}{{{\text{C}}}^{\centerdot }}{\text{OH}}]}_{{{\text{ст}}}}}[{\text{Q}}]~\,\, = \\ = \,\,2{{k}_{9}}[{{{\text{Q}}}^{{-- \bullet }}}]_{{{\text{ст}}}}^{2} + {{k}_{7}}{{[{{{\text{Q}}}^{{-- \bullet }}}]}_{{{\text{ст}}}}}[{\text{F}}{{{\text{e}}}^{{ + 3}}}]. \\ \end{gathered} $С другой стороны, в соответствии с реакцией (7) получаем выражение (15):
(15)
${{{{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{ + 2}}}}}}{\text{P}}} \mathord{\left/ {\vphantom {{{{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{ + 2}}}}}}{\text{P}}} {100{\text{N}}}}} \right. \kern-0em} {100{\text{N}}}} = {{k}_{7}}{{[{{{\text{Q}}}^{{-- \bullet }}}]}_{{{\text{ст}}}}}[{\text{F}}{{{\text{e}}}^{{ + 3}}}].$С учетом выражений (11) и ${{k}_{4}}{{[({\text{C}}{{{\text{H}}}_{3}})_{2}^{{}}{{{\text{C}}}^{\centerdot }}{\text{OH]}}}_{{{\text{ст}}}}}[{\text{Q}}]~$ = GацP/100N уравнение (14) приобретает вид (16)
(16)
$\begin{gathered} {{{{{\text{G}}}_{{{\text{eaq}}}}}{\text{P}}} \mathord{\left/ {\vphantom {{{{{\text{G}}}_{{{\text{eaq}}}}}{\text{P}}} {{\text{100N}}}}} \right. \kern-0em} {{\text{100N}}}} + {{{{{\text{G}}}_{{{\text{ац}}}}}{\text{P}}} \mathord{\left/ {\vphantom {{{{{\text{G}}}_{{{\text{ац}}}}}{\text{P}}} {100{\text{N}}}}} \right. \kern-0em} {100{\text{N}}}} = \\ = \,\,2{{k}_{9}}[{{{\text{Q}}}^{{-- \bullet }}}]_{{{\text{ст}}}}^{2} + {{k}_{7}}{{[{{{\text{Q}}}^{{-- \bullet }}}]}_{{{\text{ст}}}}}[{\text{F}}{{{\text{e}}}^{{ + 3}}}]. \\ \end{gathered} $Из уравнения (15) находим: [Q–•]ст = = (${{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{{\text{ + 2}}}}}}}}$P/100N)/ k7[Fe+3], подставляем в выражение (16) и получаем (17)
(17)
$\begin{gathered} {{({{{\text{G}}}_{{{\text{eaq}}}}} + {{{\text{G}}}_{{{\text{ац}}}}}){\text{P}}} \mathord{\left/ {\vphantom {{({{{\text{G}}}_{{{\text{eaq}}}}} + {{{\text{G}}}_{{{\text{ац}}}}}){\text{P}}} {100{\text{N}}~}}} \right. \kern-0em} {100{\text{N}}~}} = \\ = \,\,2{{k}_{9}}[{{({{{{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{ + 2}}}}}}{\text{P}}} \mathord{\left/ {\vphantom {{{{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{ + 2}}}}}}{\text{P}}} {100{\text{N}}~}}} \right. \kern-0em} {100{\text{N}}~}})} \mathord{\left/ {\vphantom {{({{{{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{ + 2}}}}}}{\text{P}}} \mathord{\left/ {\vphantom {{{{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{ + 2}}}}}}{\text{P}}} {100{\text{N}}~}}} \right. \kern-0em} {100{\text{N}}~}})} {{{k}_{7}}[{\text{F}}{{{\text{e}}}^{{ + 3}}}]{{]}^{2}}}}} \right. \kern-0em} {{{k}_{7}}[{\text{F}}{{{\text{e}}}^{{ + 3}}}]{{]}^{2}}}}~ + ~\,{{{{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{{\text{ + 2}}}}}}}}{\text{P}}} \mathord{\left/ {\vphantom {{{{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{{\text{ + 2}}}}}}}}{\text{P}}} {{\text{100N}}}}} \right. \kern-0em} {{\text{100N}}}}. \\ \end{gathered} $Преобразованием выражения (17) получаем уравнение (18)
(18)
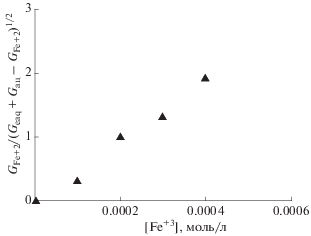
$\begin{gathered} {{{{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{{\text{ + 2}}}}}}}}} \mathord{\left/ {\vphantom {{{{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{{\text{ + 2}}}}}}}}} {{\text{(}}{{{\text{G}}}_{{{\text{eaq}}}}}}}} \right. \kern-0em} {{\text{(}}{{{\text{G}}}_{{{\text{eaq}}}}}}} + {{{\text{G}}}_{{{\text{ац}}}}}--{{{\text{G}}}_{{{\text{F}}{{{\text{e}}}^{{{\text{ + 2}}}}}}}}{{)}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}~ = \\ = \,\,{{10{{k}_{7}}{{{\text{N}}}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}} \mathord{\left/ {\vphantom {{10{{k}_{7}}{{{\text{N}}}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}} {{{{(2{{k}_{9}}P)}}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}[{\text{F}}{{{\text{e}}}^{{ + 3}}}]}}} \right. \kern-0em} {{{{(2{{k}_{9}}P)}}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}[{\text{F}}{{{\text{e}}}^{{ + 3}}}]}}. \\ \end{gathered} $На рис. 1 приведено графическое решение уравнения (18) в координатах ${{G}_{{{\text{F}}{{{\text{e}}}^{{{\text{ + 2}}}}}}}}$/(Geaq + Gац – ‒ ${{G}_{{{\text{F}}{{{\text{e}}}^{{{\text{ + 2}}}}}}}}$)1/2 – [Fe+3], из которого получаем, что 10k7N1/2/(2k9 P)1/2 = 4646 ± 860. Отсюда k7 = (2.8 ± ± 0.5) × 103 л моль–1 с–1. Тангенс угла наклона прямой рассчитывали по начальным точкам приведенной зависимости, исключая последнюю точку, выпадающую из линейной зависимости. При высоких концентрациях Fe+3 эти ионы существенно конкурируют с хиноном за eaq по реакции (8), вызывая выпадение последней точки.
Таким образом ионы железа (III) способны окислять семихиноны. Константа скорости этой реакции составляет (2.8 ± 0.5) × 103 л моль–1 с–1.
Список литературы
Бурлакова Е.Б., Храпова Н.Г. // Успехи химии. 1985. Т. 54. № 9. С. 1540.
Beyer R.E. // Free Rad. Biol. Med. 1990. V. 8. № 6. P. 545.
Ленинджер А. Основы биохимии. Т. 2. М.: Мир, 1985. 368 с. / Lehninger A.L. Principles of Biochemistry. Worth Publishers, Inс. 1982.
Silverman R.B. Organic chemistry of drug design and drug action. San Diego: Academic Press, 1992. 422 p.
Wardman P. Free radical mechanisms in anti-cancer drug research. In “Radiation chemistry: Present Status and Future Trends.”/ Ed. by Jonah C.D., Madhava Rao B.S. The Netherlands: Elsevier Science B.V. 2001. 739 p.
Mukherjee T. Radiation chemistry of quinones. In “Radiation chemistry: Present Status and Future Trends.”/ Ed. by Jonah C.D., Madhava Rao B.S. The Netherlands: Elsevier Science B.V. 2001. 739 p.
ГОСТ 4011-72. Вода питьевая. Методы измерения массовой концентрации общего железа (с Изменениями N 1, 2). Группа Н09.
Пикаев А.К. Современная радиационная химия. Радиолиз газов и жидкостей. М: Наука, 1986. 440 с.
Ilan Y.A., Czapski G., Meisel D. // Biochim. Biophys. Acta. 1976. V. 430. P. 209.
https://kinetics.nist.gov/solution/
Patel K.B., Willson R.L. // J. Chem. Soc. Farad. Trans. 1. 1973. № 4. P. 814.
Denisov E.T., Khudyakov I.V. // Chem. Rev. 1987. V. 87. № 6. P. 1313.
Patel K.B., Willson R.L. // J. Chem. Soc. Farad. Trans. 1. 1973. № 4. P. 814.
Дополнительные материалы отсутствуют.
Инструменты
Химия высоких энергий