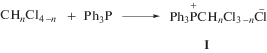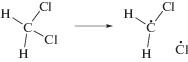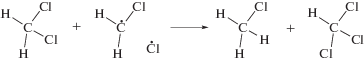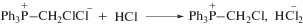Химия высоких энергий, 2022, T. 56, № 1, стр. 70-80
Синтез декорированных углеродных структур с инкапсулированными компонентами при действии низковольтных электрических разрядов
И. В. Бодриков a, Е. Ю. Титов a, *, А. В. Воротынцев a, В. И. Пряхина b, Д. Ю. Титов a
a Нижегородский государственный технический университет им. Р.Е. Алексеева
603950 Нижний Новгород, ул. Минина, 24, Россия
b УрФУ им. первого Президента России Б.Н. Ельцина
620002 Екатеринбург, ул. Мира, 19, Россия
* E-mail: E.titov@nntu.ru
Поступила в редакцию 27.06.2021
После доработки 23.08.2021
Принята к публикации 28.08.2021
- EDN: HRSAXW
- DOI: 10.31857/S0023119322010041
Аннотация
При поликонденсации комплексов хлорметанов с трифенилфосфином под действием низковольтных электрических разрядов в жидкой фазе получаются наноразмерные твердофазные продукты. Изучен элементный состав с построением карт распределения элементов (SEM-EDS mapping) и компонентный состав (Direct EGA-MS) твердофазных продуктов. Элементный и компонентный составы образующихся структур изменяются в широких пределах в зависимости от содержания хлора в исходных субстратах и добавок трифенилфосфина. При проведении термодесорбционного анализа выявлено аномальное поведение HCl и бензола, находящихся в составе твердофазных продуктов. В спектрах термической десорбции эти компоненты появляются при нехарактерно высокой температуре. Наблюдаемая аномалия в поведении HCl обусловлена связыванием HCl в комплекс твердого аниона ${\text{HCl}}_{2}^{ - }$ с трифенил(хлорметил)фосфоний хлоридом для разложения которого требуется относительно высокая температура (до 800 К). Аномальное поведение бензола связано с его капсулированным состоянием в наноструктурах. Появление бензола начинается с 650 К и продолжается до температур свыше 1300 К.
ВВЕДЕНИЕ
В конце прошлого века началось быстрое развитие теории и практики создания наноструктурированных материалов. Достигнутый прогресс стимулировал формирование новых междисциплинарных направлений в химии, физике, материаловедении, медицине и открытие новых аллотропных модификаций углерода (фуллерены, карбин, нанотрубки, графен и др.) [1–4]. Так, добавление в полимерную матрицу углеродных нанотрубок придает полученному материалу принципиально новые свойства, обусловленные уникальными характеристиками нанотрубок. Например, одностенные нанотрубки имеют модуль Юнга 320–1470 ГПа [5], многостенные нанотрубки имеют модуль Юнга 270–950 ГПа [6]. Таким образом, открывается возможность создания на основе полимеров и присадок углеродных нанотрубок композитных материалов, имеющих принципиально новые характеристики, которые способны обеспечить только присадки наноструктур.
Основная трудность, стоящая на пути решения этой проблемы, заключается в необходимости обеспечения хорошего механического сопряжения между поверхностью нанотрубки и материалом. Для преодоления этой трудности необходимо создание химической связи между поверхностью нанотрубок и матрицы, что требует поверхностной функционализации нанотрубок.
Известно, что фуллерены и нанотрубки легко модифицируются различными прекурсорами с получением декорированных наноструктур, в которых прекурсоры фиксируются на поверхности наноструктур химическими связями. Как оказалось, этим не исчерпываются трансформативные способности наноструктур. Установлено, что фуллерены и нанотрубки могут реагировать не только с аналогами и различными прекурсорами, но и друг с другом с образованием уникальных симбиозных структур – нанотрубок, внутри которых находятся фуллерены. Эти структуры были получены при лазерном испарении графита с металлическими катализаторами [7]. Нанопиподы – это гибридные системы, состоящие из углеродной нанотрубки (стручка) с молекулами или атомами (горошинами), размещенными в ее полости. Вместо фуллеренов внутри нанотрубок могут капсулироваться и другие вещества в различных фазовых состояниях [8–10]. Примером является недавнее открытие явления самоорганизации молекул воды, помещенных внутрь углеродной нанотрубки диаметром 1.05 нм, в цепочки и их замерзание при температуре системы 130–138°С [11–13]. Такая самоорганизация и удерживание веществ внутри нанотрубок с выстраиванием их в цепи, по-видимому, имеет общую основу с формированием пиподов.
Модификация наноструктур с формированием заданных функциональных групп является эффективным приемом вовлечения этих соединений в практическую область и формирование новых материалов с заданными свойствами [14, 15]. Модификация углеродных структур с включением гетероатомов непосредственно в углеродный остов также обеспечивает расширение функциональных возможностей наноструктурных частиц [16–20]. Одним из методов функционализации углеродных материалов является введение производных фосфина [21–23]. Они являются важными лигандами в координационной химии, особенно в элементоорганических соединениях. Фрагменты фосфинов часто являются ценными прекурсорами для получения негорючих материалов, смазочных добавок, экстрагентов и флотационных реагентов [24].
Альтернативный метод модификации наночастиц – вовлечение в синтез наноструктур комплексных субстратов, содержащих целевые декорирующие фрагменты, до настоящего времени не получил системного развития. В этом принципе модифицирования углеродных структур гетероатомный компонент – трифенилфосфин координирован с субстратами перед действием низковольтных импульсных разрядов (предразрядно). Трифенилфосфин является орбитальноконтролируемым (мягким) основанием [25]. При поликонденсации хлорметанов PPh3 выполняет три функции: электронодонорного компонента в комплексах с субстратами, замещая одну из нуклеофугных групп в субстратах (мягких кислотах), повышая их реакционную способность; источника водорода, обеспечивая межмолекулярное элиминирование HCl, а также источника фрагментов наноструктур для функционализации активных частиц, образующихся при действии низковольтных импульсных разрядов в жидких средах. Таким образом, в индуцированной низковольтными разрядами поликонденсации участвуют не индивидуальные хлорметаны, а донорно-акцепторные комплексы субстратов с трифенилфосфином. Предварительные результаты по активирующему действию трифенилфосфина на субстраты приведены в работах [26, 27].
В настоящем сообщении приводится карта распределения элементов (SEM-EDS mapping) в наноструктурах, а также термоадсорбционное (Direct EGA-MS) определение состава компонентов твердых структур, полученных индуцированной низковольтными разрядами поликонденсации комплексов хлорметанов с трифенилфосфином. По карте распределения элементов наноструктур полученных при действии низковольтных импульсных разрядов на комплексные субстраты оценивается содержание элементов (C, P, Cl) в локальных областях и на всей поверхности наноструктур. По спектрам термодесорбционного анализа определен состав образовавшихся нелетучих продуктов и компонентов, распределенных в твердой фазе. При этом порядок проявления фрагментов в спектре с учетом их молекулярной массы использован для оценки возможности взаимодействия компонентов с поверхностью наноструктур (декорированные наноструктуры) или нахождения компонентов в полости наноструктур (капсулированные компоненты).
ЭКСПЕРИМЕНТ
Для проведения эксперимента использовались реактивы: дихлорметан (температура кипения 39.6°C, 99.9 мол. %), трихлорметан (температура кипения 61.2°C, 99.9 мол. %), тетрахлорметана (температура кипения 76.7°C, 99.9 мол. %) и трифенилфосфин (температура кипения 377°C., 99.0 мол. %). В опытах индуцированной низковольтным разрядами поликонденсации исследовались бинарные системы CH2Cl2, CHCl3, и CCl4 с PPh3 (9 мас. %). Для иллюстрации вклада вносимое PPh3 в изменение элементного и компонентного состава продуктов поликонденсации хлорметанов в настоящее работе приводятся результаты индуцированной разрядами поликонденсации чистого CHCl3.
На рис. 1 показана схема экспериментальной установки с объемом 40 см3. Внутри реактора установлены графитовые электроды диаметром 6 мм. Источник постоянного напряжения 60 В (VS) емкостью 2200 мкФ использовался для генерации разрядов низкого напряжения путем изменения расстояния между электродами. Продолжительность и мощность разряда контролировали с помощью блока управления. При этих условиях энергии разряда достаточно для разрыва связей и протекания химических реакций [28]. Подробное описание блока управления разрядом и расчет энергии приведено в работе [29].
Рис. 1.
Схема экспериментальной установки. R, реактор; RC, обратный холодильник; Е, электроды; М, манометр; V, клапан; GT, газоуловитель; C, муфта; SM, шаговый двигатель; D, драйвер шагового двигателя; БП – блок питания шагового двигателя; CS, датчик тока; MCS, микропроцессорная система управления; VS, источник напряжения.
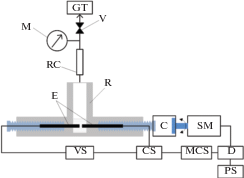
Реагент загружали в реактор при температуре окружающей среды в атмосфере гелия, чтобы предотвратить его окисление. Уровень жидкости в реакторе был намного выше, чем уровень электродов E. Для предотвращения испарения реагента использовался обратный холодильник RC (температура 4°C). Температура в реакторе не превышает температуру кипения реагента. Образующийся газ охлаждали и улавливали в газовой ловушке (GТ). Давление в реакторе атмосферное.
Для оценки эффекта добавления трифенилфосфина к хлорметану на конверсию под действием низковольтного разряда были исследованы воздействия реагентов и реагентов с добавлением трифенилфосфина в плазму. В табл. 1 представлены экспериментально измеренные значения конверсии, выхода газа и твердых продуктов для соответствующих систем.
Таблица 1.
Характеристики трансформации трихлорметана и бинарных систем с PPh3
| Субстрат | Время реакции, мин | Конверсия, % мас. | Выход газа, % мас. | Выход твердых продуктов, % мас. |
|---|---|---|---|---|
| CH2Cl2 + PPh3 | 20 | 33 | 41 | 58 |
| CHCl3 | 30 | 22 | 30 | 69 |
| CHCl3 + PPh3 | 20 | 35 | 34 | 65 |
| CCl4 + PPh3 | 20 | 71 | 45 | 54 |
Термодесорбционный анализ (Direct EGA-MS) для состав твердых продуктов выполняли на программируемом по температуре пиролизере Double-Shot EGA/PY-3030D (Frontier Laboratories, Япония), встроенном в GC-MS QP-2010Plus (Shimadzu, Япония). Для проведения анализа загружали 100 мкг образца в чашу из нержавеющей стали и погружали в кварцевую трубку для пиролиза. Кварцевая трубка была окружена трубчатой печью, которая обеспечивала равномерный нагрев. Первый этап анализа – выдержка при 323 К в течение 10 мин, после этого образец нагревался в интервале 323–773 К (10 К/мин). На втором этапе идентификация полученных хроматографических пиков проводилась с помощью масс-селективного детектора. Ионизацию в масс-спектрометре проводили путем электронной ионизации (EI) при 70 эВ, и сканировали в диапазоне масс от 12 до 500 а. е. м. Продукты реакции идентифицировали с помощью базы данных масс-спектров NIST-11 и программы “GCMS Real Time Analysis®”.
Для определения элементного состава образцов проведено исследование поверхности методом энергодисперсионной рентгеновской спектроскопии (ЭДС) на сканирующем электронном микроскопе JSM-6700F (JEOL, Япония). Образцы были закреплены на держателе образца с помощью проводящей углеродной клейкой ленты и покрыты пленкой Au/Pd толщиной 3 нм методом магнетронного распыления (Q150R S, Quorum, UK) для компенсации заряда, вызванного электронным пучком. Морфологические и визуальные характеристики внешнего вида визуализировали с помощью сканирующей электронной микроскопии (Merlin, Carl Zeiss, Germany) с использованием встроенного в линзу вторичного электронного детектора при энергии ускорения электронов 5–7 кВ. Вакуум в камере микроскопа составлял ~10–6 мбар. На образцы наносили проводящий слой золота толщиной 20 нм.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
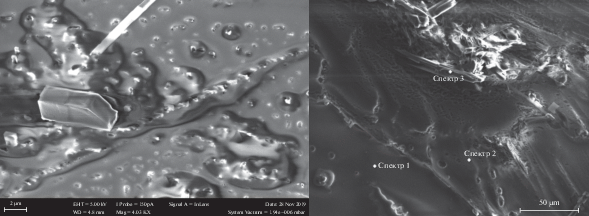
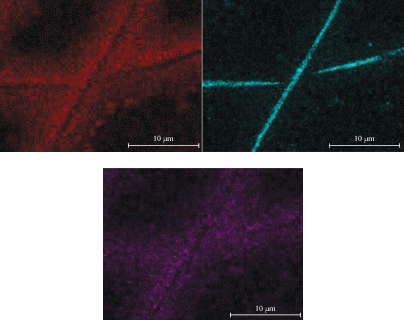
Электронные изображения твердых структур (рис. 2) показывают, что при действии низковольтных разрядов на комплексную систему CH2Cl2 + PPh3 просматриваются области наноструктур, которые имеют несимметрично организованные по форме участки структур (вискеры, ламели и др). Эти области сильно разнятся элементным составом (табл. 2). Участок структур на электронном изображении (рис. 2) в области спектра 3 имеет форму ламелей с содержанием фосфора и углерода 26.3 и 73.7 ат. % соответственно. В этих наноструктурах атомы фосфора равномерно распределены на всем участке (рис. 3). Участок карты (рис. 2, спектр 2) образован структурами с низким содержанием фосфора (содержание углерода, хлора и фосфора равно 94.8, 0.5 и 4.7 ат. % соответственно).
Таблица 2.
Соотношение элементов в твердом продукте поликонденсации CH2Cl2 + PPh3, ат. %
| Элемент | Номер спектра | ||
|---|---|---|---|
| 1 | 2 | 3 | |
| С | 97.1 | 94.8 | 73.7 |
| Cl | 0.6 | 0.5 | – |
| P | 2.3 | 4.7 | 26.3 |
Высокое содержание фосфора и низкое содержание хлора (рис. 3) в твердофазных продуктах индуцированной поликонденсации системы CH2Cl2 + PPh3 обусловлены участием PPh3 как непосредственно в формировании цепочки наноструктур (образовании связей С–Р), так и в декорировании образующихся структур фосфорсодержащими фрагментами.
Результаты трансформации CHCl3 приводятся для иллюстрации изменений характеристик трансформации хлорметанов, вносимых трифенилфосфином. Из сравнения локальных областей (табл. 3, спектры 10–12 и 4–9) твердофазных продуктов хорошо прослеживается влияние добавок трифенилфосфина на элементный состав. При индуцированной поликонденсации чистого трихлорметана образуются структуры (рис. 4, спектр 9) в форме кактуса с диаметром 15–25 мкм с содержанием углерода 56.8 ат. % и высоким содержанием хлора – 43 ат. %. Эти шары соединяются одиночными (диаметр 400–600 нм) и сплетенными (диаметр до 7 мкм) нитями с содержанием углерода и хлора 84.3 ат. % и 15.7 ат. % соответственно (спектр 6). Наноструктуры индуцированной низковольтными разрядами поликонденсации бинарной системы CHCl3 + PPh3 (рис. 5) значительно отличаются от структур поликонденсации чистого CHCl3 (рис. 6) очень низким содержанием хлора (0.6–0.9 ат. %). По форме локальные группировки структур имеет вид длинных трубок (спектр 10) или мелкодисперсных частиц (спектры 11, 12).
Таблица 3.
Соотношение элементов в твердом продукте поликонденсации CHCl3 (спектр 4–9) and CHCl3 + PPh3 (спектр 10–12), aт. %
| Элемент | Номер спектра | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | |
| С | 98.3 | 81.3 | 84.3 | 93.5 | 98.4 | 56.8 | 94.8 | 100.00 | 95.3 |
| Cl | 1.7 | 18.7 | 15.7 | 6.5 | 1.6 | 43.2 | 0.6 | – | 0.9 |
| P | – | – | – | – | – | – | 4.6 | – | 3.8 |
Эффект трифенилфосфина особенно ярко проявляется при поликонденсации CCl4. Без “предразрядной” активации PPh3 тетрахлорметан трансформируется очень медленно [26]. В присутствии PPh3 (9 мас. %) при действии разрядов конверсия бинарной системы CCl4 + PPh3 за 20 мин достигает 71%. Основными твердофазными продуктами конденсации системы CCl4 + PPh3 являются соединения структурированного углерода – формы вискеров (рис. 7). По изображению в электронном микроскопе углеродные наноструктуры занимают основную часть твердой фазы.
При индуцированной низковольтными разрядами поликонденсации системы PPh3 + CCl4 добавка PPh3 выполняет функцию предразрядного активатора и источника водорода для межмолекулярного элиминирования HCl. При трансформации комплексной системы, образование молекулярного хлора по типу α-элиминирования при фрагментации тетрахлорметана, по-видимому, затруднено ввиду легкости вовлечения элиминируемого хлора в продолжение реакции. При действии импульсных разрядов, такое элиминирование без источников водорода фактически становится обратимым [30].
Элементный анализ твердого образца показывает, что основная часть сгруппированных структур сформирована из одного углерода (рис. 8 и табл. 4, спектры 13 и 15). Только в отдельных областях (спектр 14) структуры включают атомы хлора (8.7 ат. %) и фосфора (4.4 ат. %).
Таблица 4.
Соотношение элементов в твердом продукте поликонденсации CCl4 + PPh3, aт. %
| Элемент | Номер спектра | ||
|---|---|---|---|
| 13 | 14 | 15 | |
| С | 100 | 86.9 | 100 |
| Cl | – | 8.7 | – |
| P | – | 4.4 | – |
Бинарные системы представляют собой комплексы донорно-акцепторного типа, в которых один из атомов хлора хлорметанов замещен трифенилфосфином с образованием связи P–C [26]. Образование бинарной системы ди-, три- и тетрахлорметанов с PPh3 под действием низковольтных импульсных разрядов можно представить как Sn2 процесс (реакция (1)).
Таким образом, в бинарных системах добавки PPh3 выполняют роль источника фосфорсодержащих декорирующих фрагментов. При этом PPh3 вводится в реакцию в форме компонента комплексных систем с хлорметанами перед действием низковольтных разрядов (предразрядно).
При действии низковольтных импульсных разрядов на комплексы I в растворе соответствующих хлорметанов образуются супермолекулярные углеродные структуры типа вискеров, сфер, ламелей. Атомный состав структур в локальных областях приведен в табл. 2–4. Хотя комплексы ди-, три- и тетрахлорметанов с PPh3 близки по структуре, но образующиеся при действии разрядов структуры отличаются по морфологии, элементному и компонентному составу. Морфология структур сильно меняются при переходе от одного субстрата к другому (рис. 2, 4, 7).
В спектре термической десорбции наноструктур, полученных в индуцированной низковольтными импульсными разрядами поликонденсации дихлорметана, предразрядно активированного PPh3, проявляется часть соединений, образование которых трудно прогнозировать. При этом внутри структур типа нанотрубок часто капсулируются компоненты в твердом, жидком и газообразном состояниях. Как показано в работах [31–33], происходит самоорганизация молекул и удерживание как простых, так и сложных веществ внутри нанотрубок и выстраивание их в цепочки (peapods), которые представляют собой структуры, состоящие из фуллеренов, капсулированных в нанотрубках.
Из спектра (табл. 5) видно, что дихлорметан при действии низковольтных разрядов трансформируется по нескольким маршрутам. В образовании трихлорметана молекула дихлорметана вовлекается в двух состояниях: триплетном и синглетном [26]. В триплетное состояние хлорметаны частично переходят при действии низковольтных разрядов по схеме 1 (реакция (2)). Рекомбинация дихлорметил и хлор радикала протекает безбарьерно (реакция (3))
Таблица 5.
Состав продуктов поликонденсации CH2Cl2 + PPh3
| Tmax, K | Ион, m/z | Вещество |
|---|---|---|
| 461 | 83 | Трихлорметан |
| 728 | 262 | Трифенилфосфин |
| 615 | 284 | Перхлорбензол |
| Гексахлорфульвен | ||
| 749 | 183 | Трифенил(хлорметил)фосфония хлорид |
| 543 | 36 | Хлористый водород |
| 713 | 277 | Оксид трифенилфосфина |
| 891 | 153 | Аценафтен |
Генерируемые хлорметильные радикалы вовлекаются в “сборку” наноструктур непосредственно на стадии релаксации или после дополнительной трансформации. Второй маршрут конверсии дихлорметана (реакция (4)) – участие в образовании трифенил(хлорметил)фосфония хлорида при действии электрических разрядов.
Проявляющийся в спектре хлороводород, удерживаемый при десорбции до температуры 400 К, по-видимому, в структурах связан в комплексный анион с трифенил(хлорметил)фосфония хлоридом (реакция (5)) [34, 35].
Трифенилфосфиноксид наиболее вероятно образуется после действия низковольтных импульсных разрядов в результате окисления PPh3 атмосферным кислородом при высушивании твердой фазы. Образование ацетонафтена, осуществляется, наиболее вероятно, сборкой валентноненасыщенных активных частиц, генерируемых при действии низковольтных разрядов в жидкой среде.
Из сравнения спектров термической десорбции продуктов индуцированной низковольтными разрядами конденсации CHCl3 (табл. 6) и CHCl3 + PPh3 (табл. 7) прослеживается эффект PPh3, проявляющийся в изменении компонентного состава продуктов поликонденсации. PPh3 драматически изменяет спектр термической десорбции наноструктур, получаемых при индуцировании низковольтными разрядами поликонденсации трихлорметана. Основными компонентами, появляющимися в спектре наноструктур поликонденсации трихлорметана, являются гексахлорэтан и гексахлорбензол. В спектре термодесорбции в небольших количествах появляются также гексахлорбутадиен и октахлорнафталин.
Таблица 6.
Состав продуктов поликонденсации CHCl3
| Tmax, K | Ион, m/z | Вещество |
|---|---|---|
| 403 | 119 | Гексахлорэтан |
| 470 | 225 | Гаксахлорбутадиен |
| 497 | 237 | Гексахлорциклопентадиен |
| 614 | 284 | Гексахлорбензол |
| 703 | 57 | Бис(тридецил)фталат |
| 785 | 404 | Октахлорнафталин |
Таблица 7.
Состав продуктов поликонденсации CHCl3 + + PPh3
| Tmax, K | Ион, m/z | Вещество |
|---|---|---|
| 473 | 83 | Трихлорметан |
| 600 | 36 | Хлористый водород |
| 673 | 284 | Перхлорбензол |
| Гексахлорфульвен | ||
| 757 | 262 | Трифенилфосфин |
| 993 | 277 | Оксид трифенилфосфина |
| 1073 | 108 | Трифенил (хлорметил) фосфония хлорид |
В спектре термической десорбции твердофазных продуктов поликонденсации системы CHCl3 + + PPh3 в качестве основных продуктов появляются трифенилфосфин, трифенилфосфиноксид и трифенилхлорметилфосфоний хлорид. В продуктах обнаруживается также хлороводород, который удерживается в твердых продуктах до температуры 850 К. Эта аномалия в поведении HCl, согласно работе [34], обусловлена связыванием HCl в комплексный анион (реакция (5)). Применение трифенилфосфина как активирующего компонента при превращении хлорметанов позволяет получать востребованные в производстве хлорсодержащие продукты, другие методы получения которых сложны [35].
В такой ситуации может нарушаться порядок проявления компонентов или их фрагментов при термодесорбционном анализе твердых структур. На основе полученных результатов можно качественно представить связь между фрагментами в твердофазной части продуктов и состав адсорбированных и капсулированных компонентов.
Химический аспект эффекта трифенилфосфина особенно четко прослеживается при анализе спектров термической десорбции наноструктур, получаемых при поликонденсации системы CCl4 + + PPh3 под действием электрических разрядов. Фенильные фрагменты выполняют роль доноров водорода для межмолекулярного элиминирования хлороводорода и акцептором атомов хлора, поставляемых тетрахлорметаном. Образование дихлор-, трихлор-, пентахлор- и гексахлорбензолов является наглядной иллюстрацией последовательного замещения атомов водорода ароматического ядра хлором. Генерируемые под действием низковольтных разрядов активные частицы углерода формируют наноструктуры, декорированные атомами хлора и частично фрагментами трифенилфосфина. При термической десорбции, декорирующий фрагмент трифенилфосфина, обладая высокой нуклеофугностью, подвергается фрагментации с образованием трифенилфосфина. Частично, как уже отмечено, трифенилфосфин получается при фрагментации декорирующих наноструктур фосфорсодержащих фрагментов. Проявляющийся в спектрах термической десорбции трифенилфосфин оксид при индуцированной разрядами поликонденсации всех изученных хлорметанов с добавкой PPh3 получается окислением трифенилфосфина кислородом воздуха при сушке образцов.
Из спектров термической десорбции наноструктур (табл. 8), полученных при индуцированной разрядами поликонденсации бинарной системы CCl4 + PPh3, на ряду с HCl обнаружена другая аномалия, связанная с поведением бензола в твердофазных продуктах. По физическим характеристикам бензол как низкокипящий компонент не должен присутствовать в твердофазных продуктах после сушки образцов при пробоподготовке. Остаточные количества бензола после сушки должны проявляться при температуре 350–400 К. В действительности при анализе бензол проявляется при температуре 997 K. Эта аномалия наиболее вероятно связана с нахождением бензола в капсулированном состоянии внутри нанотрубок. Молекулы бензола удерживаются в капсулах подобно кокосу (молоко внутри скорлупы) до температуры, при которой стенки или заглушки нанотрубок частично разрушаются и бензол диффундирует через эти дефекты [36, 37]. Возможна также самоорганизация молекул бензола внутри наноструктур, которая обуславливает изменения в физических свойствах бензола. Подобное явление, названное самоорганизацией молекул, недавно открыто для молекул воды [11–13].
ЗАКЛЮЧЕНИЕ
Полученные в настоящей работе результаты показывают, что индуцированная низковольтными импульсными разрядами поликонденсация обеспечивает формирование наноструктур из хлорметанов. Форма образующихся структур изменяется в широких пределах в зависимости от содержания хлора в субстратах. Приведенные в работе результаты показывают также, что добавки трифенилфосфина не только предразрядно активируют субстраты, но и вносят принципиальные изменения в морфологию, элементный и компонентный состав твердофазных продуктов. Этот эффект PPh3 особенно четко иллюстрируется результатами индуцированной трансформации чистых CHCl3 и CCl4 и их бинарных систем с трифенилфосфином. Чистый тетрахлорметан практически не реагирует при действии электрических разрядов. Конверсия бинарной системы CCl4 + PPh3 при действии низковольтных разрядов за 20 мин достигает 71 мас. %.
Трихлорметан при индуцированной низковольтными разрядами поликонденсации образует шарообразные структуры с иглами в форме кактусов диаметром 15–25 мкм, соединенные одиночными (диаметр 400–600 нм) и сплетенными (диаметр до 7 мкм) нитями. Бинарная система CHCl3 + PPh3 в тех же условиях образует наноструктуры в форме ламелей. Из сравнения спектров термической десорбции твердофазных продуктов поликонденсации CHCl3 и CHCl3 + PPh3 видно, что в первом случае обнаруживаются только перхлорированные углеводороды с различным остовом (линейным, циклическим, ароматическим). При поликонденсации бинарной системы CHCl3 + PPh3 в спектрах проявляются: CHCl3, C6Cl6, трифенил(хлорметил)фосфония хлорид, а также HCl, который выделяется в температурном интервале 450–850 К. При анализе твердофазных продуктов поликонденсации систем CH2Cl2 + + PPh3 методом термической десорбции также обнаруживается интенсивное выделение хлороводорода в интервале 360–800 К. Задержка появления HCl вызвана связыванием с Cl– в комплексный анион ${\text{HCl}}_{2}^{ - }.$ При нагревании во время анализа продуктов поликонденсации систем CH2Cl2 + PPh3 и CHCl3 + PPh3 происходит медленное разложение комплекса трифенил(хлорметил)фосфония хлорида с твердым анионом ${\text{HCl}}_{2}^{ - }$ с образованием HCl [34].
В спектре термической десорбции твердофазного продукта поликонденсации системы CCl4 + + PPh3 обнаружены аномалия, связанная с высокой температурой выхода (997 К) бензола. Наиболее вероятно эта аномалия связана с капсулированным состоянием бензола внутри наноструктур.
ИСТОЧНИКИ ФИНАНСИРОВАНИЯ
Исследование выполнено при финансовой поддержке РФФИ в рамках научного проекта № 18-29-24008.
Часть работы, связанная с термическим анализом, была выполнена в рамках базовой части государственного задания (тема FSWE-2020-0008, проект 0728-2020-0008).
В работе использовано оборудование УЦКП “Современные нанотехнологии” УрФУ.
Список литературы
Novoselov K.S., Geim A.K., Morozov S.V., Jiang D., Zhang Y., Dubonos S.V., Grigorieva I.V., Firsov A.A. // Science. 2004. V. 306. P. 666.
Novoselov K.S., Jiang D., Schedin F., Booth T.J., Khotkevich V.V., Morozov S.V., Geim A.K. // Proc. Natl Acad. Sci. USA. 2005. V. 102. P. 10451.
Hersam M.C. // Nat. Nanotechnol. 2008. V. 3. P. 387.
Nanot S., Hároz E.H., Kim J.H., Hauge R.H., Kono J. // Adv. Mater. 2012. V. 24. P. 4977.
Yu M.F., Files B.S., Arepalli S., Ruoff R.S. // Phys. Rev. Lett. T. 2000. V. 84. P. 5552.
Yu M.F., Lourie O., Dyer M.J., Moloni K., Kelly R.F., Ruoff R.S. // Science. 2000. V. 287. P. 637.
Smith B.W., Monthioux M., Luzzi D.E. // Nature. 1998. V. 396. P. 323.
Loi M.A., Gao J., Cordella F., Blondeau P., Menna E., Bartova B., Hebert C., Lazar S., Botton G., Milko M., Ambrosch-Draxl C. // Adv. Mater. 2010. V. 22. P. 1635.
Orellana W., Vasquez S.O. // Phys. Rev. B. T. 2006. V. 74. 125419.
Wang Y., Huang Y., Yang B., Liu R. // Carbon. 2008. V. 46. P. 276.
Agrawal K.V., Shimizu S., Drahushuk L.W., Kilcoyne D., Strano M.S. // Nat. Nanotechnol. 2017. V. 12. P. 267.
Kurita T., Okada S., Oshiyama A. // Phys. Rev. B. 2007. V. 75. 205424.
Agrawal B.K., Singh V., Pathak A., Srivastava R. // Phys. Rev. B. 2007. V. 75. 195420.
Liu H.Y., Zhang L.N., Yan M., Yu J.H. // J. Mater. Chem. B. 2017. V. 5. P. 6437.
Yao X.P., Li J., Kong L., Wang Y. // Nanotechnology. 2015. V. 26. P. 1.
Biju V. // Chem. Soc. Rev. 2014. V. 43. P. 744.
Fan W., Yung B., Huang P., Chen X. // Chem. Rev. 2017. V. 17. P. 13566.
Chen F., Cai W. // Small. 2014. V. 10. P. 1887.
Alshehri R., Ilyas A. M., Hasan A. // J. Med. Chem. 2016. V. 59. P. 8149.
Pooresmaeil M., Namazi H. // Colloid Surf. B Biointerfaces. 2018. V. 172. P. 17.
Biagiotti G., Lange V., Ligi C., Caporali S., Muniz-Miranda M., Flis A., Pietrusiewicz K.M., Ghini G., Brandi A., Cicchi S. // Beilstein J. Nanotechnol. 2017. V. 8. P. 485.
Muleja A.A., Mbianda X.Y., Krause R.W., Pillay K. // Carbon. 2012. V. 50. P. 2741.
Muleja A.A. // Environ. Sci. Pollut. Res. 2008. V. 25. P. 20032.
Marklund A., Andersson B., Haglund P. // Chemosphere. 2003. V. 53. 1137e1146.
Klopman G. Chemical Reactivity and Reaction Paths. M.: Wiley, 1974.
Bodrikov I.V., Titov E.Y., Subbotin A.Y., Grinvald I.I., Titov D.Y., Razov E.N. // Plasma Process Polym. 2020. V. 17. e1900247.
Bodrikov I.V., Titov E.Y., Grinval’d I.I., Titov D.Y., Kurskii Y.A., Razov E.N. // High Energy Chem. 2020. V. 54. № 1. P. 72.
Bodrikov I.V., Kut’in A.M., Titov E.Yu., Titov D.Yu., Kurskii Yu.A., Gazizulin R.R. // Plasma Process. Polym. 2018. V. 15. e1800094.
Titov E.Y., Titov D.Y., Bodrikov I.V., Kut’in A.M., Kurskii Y.A., Gazizzulin R.R. // High Energy Chem. 2018. V. 52. № 6. P. 512.
Kovács T., Turányi T., Föglein K., Szépvölgyi J. // Plasma Chem. Plasma Process. 2005. V. 25. P. 109.
Cao J., Wang Y., Chai J., Shi J. // Comput. Mater. Sci. 2019. V. 160. P. 403.
Smith B.W., Luzzi D.E. // Chem. Phys. Lett. 2000. V. 321. P. 169.
Shiraishi M., Takenobu T., Yamada A., Ata M., Kataura H. // Chem. Phys. Lett. 2002. V. 358. P. 213.
Nikitin K., Muller-Bunz H., Muldoon J., Gilheany D.G. // Chem. Eur. J. 2017. V. 23. P. 4794.
Vetter A.C., Nikitin K., Gilheany D.G. // Chem. Commun. 2018. V. 54. P. 5843.
Wang Z. // J. Phys. Chem. 2020. V. 124. P. 3851.
Heo S., Sinnott S.B. // J. Appl. Phys. 2007. V. 102. 064307.
Дополнительные материалы отсутствуют.
Инструменты
Химия высоких энергий