Химия высоких энергий, 2023, T. 57, № 2, стр. 91-99
Долгоживущая замедленная флуоресценция тройных комплексов нафталин-β-циклодекстрин–циклогексан при комнатной температуре
Д. С. Ионов a, *, И. В. Ионова a, М. А. Мазалов a, b, М. В. Алфимов a, b
a Центр фотохимии РАН, ФНИЦ “Кристаллография и фотоника” РАН
119421 Москва, ул. Новаторов, д. 7А, корп. 1, Россия
b Московский физико-технический институт (Государственный университет)
141701 Московская область, Долгопрудный, Институтский пер., д. 9, Россия
* E-mail: dmitriy.ionov@gmail.com
Поступила в редакцию 12.08.2022
После доработки 05.09.2022
Принята к публикации 05.09.2022
- EDN: PMKFEO
- DOI: 10.31857/S0023119323010060
Аннотация
Исследована долгоживущая замедленная флуоресценция дисперсий микрокристаллов тройных комплексов нафталин–β-циклодекстрин–циклогексан. Установлено, что замедленная флуоресценция обусловлена процессом Т-Т аннигиляции. Кинетика замедленной флуоресценции имеет неэкспоненциальный характер, среднее время жизни составляет 0.68 с. Форма кинетических кривых затухания замедленной флуоресценции не зависит от интенсивности возбуждающего света. Неэкспоненциальный характер замедленной флуоресценции предположительно связан с наличием в кристаллах парных молекул нафталина с различным взаимным расположением и энергией образования пары.
ВВЕДЕНИЕ
Процесс триплет-триплетной аннигиляции (T-T аннигиляция) интенсивно исследуется последнее десятилетие в связи с возможностью создания на его основе эффективных ап-конверсионных систем (up-conversion systems), эффективно работающих при низких интенсивностях возбуждающего света [1], а также из-за возможности использования замедленной флуоресценции для создания эффективных органических светоизлучающих диодов (OLED) [2]. Одним из необходимых требований для эффективного процесса T-T аннигиляции является наличие значительной концентрации триплетных состояний, что может быть реализовано в системах, обладающих фосфоресценцией при комнатной температуре [3]. Ранее было показано, что комплексы нафталина с β-циклодекстрином и различными третьими компонентами обладают долгоживущей фосфоресценцией при комнатной температуре, близкой по своим временам жизни к значениям для нафталина в замороженных растворах при 77 K [4, 5], кроме этого, в таких системах возможен процесс триплет-триплетного переноса энергии [6]. Данный факт говорит о том, что в таких комплексах значительно подавлены процессы безызлучательного распада триплетных состояний и возможно создание больших концентраций молекул в триплетном состоянии.
МЕТОДИКА ЭКСПЕРИМЕНТА
В работе были использованы следующие соединения: β-циклодекстрин (β-CD) производства Sigma-Aldrich, нафталин (Naph) (Sigma-Aldrich), циклогексан (CyH) (Sigma-Aldrich). Все соединения использовались без предварительной очистки. К 6 мл раствора β-CD (8 мМ) добавляли 10 мкл раствора Naph в CyH разной концентрации. Мольное соотношение Naph : β-CD в образцах варьировалось в интервале от 1 : 3 до 1 : 100 соответственно. После интенсивного перемешивания на турбулентной мешалке (6000 об/мин) в течение 3 мин образец переносили в кварцевую кювету с длиной оптического пути 1 см. Перед проведением оптических измерений кювету в течение 20 мин продували аргоном. Для приготовления водного раствора β‑СD использовали деионизированную воду с удельным сопротивлением 18 Мом см (t = 25°C).
Для оптических измерений спектров люминесценции образцов использовали спектрофлуориметр “Cary Exlipse” (Agilent Technologies, США). Перед входной щелью спектрофлуориметра размещали светофильтр HOYA UV30. Кювету размещали под углом 45° к возбуждающему лучу. Кинетику люминесценции исследовали с помощью спектрофлуориметра FluoTime 300 (PicoQuant, Германия). При измерении времени жизни флуоресценции в качестве источника возбуждающего света использовался диод PLS-270 (λex = 275 нм). Для измерения кинетики затухания фосфоресценции и замедленной флуоресценции в качестве источника возбуждающего света использовали ртутно-ксеноновую лампу LC-80 (Hammatsu, Япония), свет от лампы проходил через монохроматор MC-20 (Solar, Белорусия), который был настроен на 280 нм. Свет от лампы с помощью конденсора монохроматора фокусировался на его входной щели. Изображение выходной щели монохроматора с помощью системы линз проецировалось на поверхность кюветы, расположенной под углом 20° к входной щели монохроматора спектрофлуориметра, перед которой стоял фильтр HOYA UV30. Образец в течение 1 с облучали возбуждающим светом, затем затвор лампы закрывался (время закрытия затвора составляло <10 мс), одновременно с этим подавался синхроимпульс начала измерения. В случае измерения замедленной флуоресценции на время облучения закрывался затвор ФЭУ. Максимальная мощность возбуждающего света в этом случае составляла 1 мВт, интенсивность приблизительно составляла 0.01 Вт/см2.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При добавлении CyH к раствору β-CD в воде происходит образование слаборастворимых комплексов включения. Почти сразу комплексы CyH@β-CD выпадают в виде белого кристаллического осадка. Если при этом в CyH растворен Naph, то при смешивании с раствором β-CD наряду с двойными комплексами CyH@β-CD образуются тройные комплексы Naph-CyH@β-CD, которые в виде примеси распределены в матрице из двойных комплексов. Предположительная структура комплекса ранее была рассчитана квантово-химическим методом MNDO/PM3 [7]. Средний размер кристаллов в таких суспензиях зависит от условий получения. Для исследуемых образцов он составлял 10–20 мкм. Микрофотографии кристаллов представлены на рис. 1.
Рис. 1.
(а) Микрофотография кристаллов CyH@β-CD, содержащих тройные комплексы Naph-CyH@β-CD; (б) суспензия, содержащая тройные комплексы Naph-CyH@β-CD, в кювете.

В рассматриваемой системе наблюдается долгоживущая фосфоресценция при комнатной температуре (ФКТ) и, как было обнаружено, при высоких интенсивностях возбуждающего света наблюдается замедленная флуоресценция. Спектры флуоресценции, фосфоресценции и замедленной флуоресценции представлены на рис. 2а.
Рис. 2.
(а) Спектры флуоресценции (1), замедленной флуоресценции (2) (интенсивность спектра увеличена в 10 раз) и фосфоресценции (3) водной дисперсии, содержащей комплексы Naph-CyH@β-CD; (б) кинетика затухания флуоресценции (λFl = 340 нм) (1) и форма импульса возбуждающего света (λEx = 275 нм ) (2); (в) кинетики затухания фосфоресценции (λPh = 505 нм) (1) и замедленной флуоресценции (λDFl = 340 нм) (2) в водной дисперсии Naph-CyH@β-CD (λex = 280 нм).
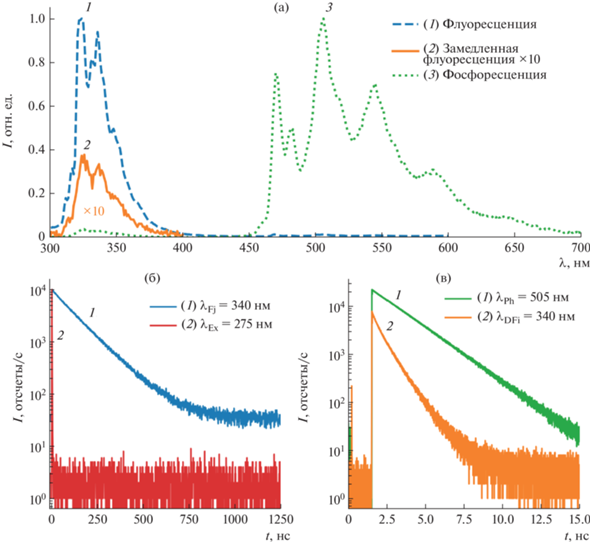
Кинетика затухания флуоресценции моноэкспоненциальна, время жизни флуоресценции τFl = = 120 нс (рис. 2б). Кинетика затухания фосфоресценции может быть описана моноэкспоненциальной зависимостью с временем жизни τP = 1.97 с (рис. 2в). Для аппроксимации кинетики затухания замедленной флуоресценции необходима двухэкспоненциальная модель с временами $\tau _{1}^{{{\text{DF}}}}$ = = 0.39 с и $\tau _{2}^{{{\text{DF}}}}$ = 0.95 с. Отношение τP/$\tau _{2}^{{{\text{DF}}}}$ ≈ 2 свидетельствует о том, что наблюдаемая замедленная флуоресценция происходит по механизму T-T аннигиляции.
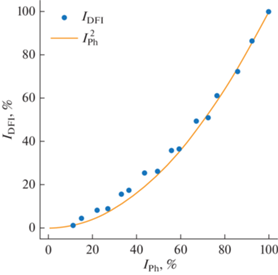
Интенсивность фосфоресценции линейно зависит от интенсивности возбуждающего излучения, в то время как интенсивность замедленной флуоресценции зависит квадратично (см. рис. 3). Этот факт наряду с результами, приведенными выше, свидетельствует о том, что наблюдаемая замедленная флуоресценция связана с процессом триплет-триплетной аннигиляции.
Система уравнений, описывающих кинетику гибели триплетных состояний, в случае наличия процесса триплет-триплетной аннигиляции, может быть записана в следующей форме:
(1)
$\left\{ {\begin{array}{*{20}{c}} {\frac{{dT\left( t \right)}}{{dt}} = - k_{{{\Sigma }}}^{T}T\left( t \right) - \gamma T{{{\left( t \right)}}^{2}} + k_{{{\text{ISC}}}}^{S}S\left( t \right)} \\ {\frac{{dS\left( t \right)}}{{dt}} = - k_{{{\Sigma }}}^{S}S\left( t \right) + \gamma T{{{\left( t \right)}}^{2}} = 0} \end{array}} \right.,$Систему уравнений (1) можно переписать в виде:
(2)
$\left\{ {\begin{array}{*{20}{c}} {\frac{{dT\left( t \right)}}{{dt}} = - k_{{{\Sigma }}}^{T}T\left( t \right) - \left( {1 - {{\varphi }_{{{\text{ISC}}}}}} \right)\gamma T{{{\left( t \right)}}^{2}}} \\ {S\left( t \right) = \frac{{\gamma T{{{\left( t \right)}}^{2}}}}{{k_{{{\Sigma }}}^{s}}}} \end{array}} \right..$В общем случае описания кинетики гибели возбужденных состояний с учетом процессов диффузии выражения (1) и (2) сохраняют свой вид, если считать, что $\gamma $ зависит от времени. Например, в случае диффузии возбуждения в изотропной трехмерной среде (с коэффициентом диффузии D), если два возбуждения аннигилируют, находятся на расстоянии $a$, бимолекулярная константа скорости может быть записана с помощью уравнения, полученного Смолуховским [8]:
В более общем случае $\gamma $ записывают в виде [9]:
где ${{\gamma }_{0}}$ – постоянная, h – параметр, зависящий от размерности пространства, в котором происходит диффузия возбуждения.Решая систему (2) при начальном условии $T\left( 0 \right) = {{T}_{0}}$, можно получить выражение для кинетики гибели триплетных состояний в виде:
(5)
$T\left( t \right) = \frac{{{{T}_{0}}{{e}^{{ - k_{{{\Sigma }}}^{T}t}}}}}{{1 + {{T}_{0}}\left( {1 - {{\varphi }_{{{\text{ISC}}}}}} \right)\int\limits_0^t {\gamma \left( \tau \right){{e}^{{ - k_{{{\Sigma }}}^{T}\tau }}}d\tau } }}.$Кинетика замедленной флуоресценции имеет вид:
(6)
$\begin{gathered} {{I}_{{{\text{Df}}}}} = k_{f}^{s}S\left( t \right) = \varphi \gamma \left( t \right)T{{\left( t \right)}^{2}} = \\ = \,\,\frac{{\varphi \gamma \left( t \right){{T}_{0}}^{2}{{e}^{{ - 2k_{{{\Sigma }}}^{T}t}}}}}{{{{{\left( {1 + {{T}_{0}}\left( {1 - {{\varphi }_{{{\text{ISC}}}}}} \right)\int\limits_0^t {\gamma \left( \tau \right){{e}^{{ - k_{{{\Sigma }}}^{T}\tau }}}d\tau } } \right)}}^{2}}}}, \\ \end{gathered} $Важным свойством систем, описываемых уравнениями (5) и (6), является существенная зависимость формы кинетических кривых от интенсивности возбуждающего света. В рассматриваемом случае кинетики замедленной флуоресценции, полученные на одном и том же образце при различной интенсивности возбуждающего света, могут быть с хорошей точностью аппроксимированы моделью с постоянной $\gamma \left( t \right) = ~{{\gamma }_{0}}$. При этом уравнение (6) будет иметь хорошо известный вид:
(7)
${{I}_{{{\text{Df}}}}} = \frac{{\varphi {{\gamma }_{0}}{{T}_{0}}^{2}k_{{{\Sigma }}}^{T}{{e}^{{ - k_{{{\Sigma }}}^{T}t}}}}}{{{{{\left( {k_{{{\Sigma }}}^{T} + \left( {1 - {{\theta }_{{{\text{ISC}}}}}} \right){{\gamma }_{0}}{{T}_{0}}\left( {1 - {{e}^{{ - k_{{{\Sigma }}}^{T}t}}}} \right)} \right)}}^{2}}}}.$Данное уравнение удобно представить в виде:
где(9)
$\begin{array}{*{20}{c}} {\begin{array}{*{20}{c}} {\begin{array}{*{20}{c}} {a = \frac{{k_{\Sigma }^{T}{{T}_{0}}}}{{k_{\Sigma }^{T} + \left( {1 - {{\theta }_{{{\text{ISC}}}}}} \right){{\gamma }_{0}}{{T}_{0}}}}} \\ {b = \frac{{\left( {1 - {{\theta }_{{{\text{ISC}}}}}} \right){{\gamma }_{0}}{{T}_{0}}}}{{k_{\Sigma }^{T} + \left( {1 - {{\theta }_{{{\text{ISC}}}}}} \right){{\gamma }_{0}}{{T}_{0}}}}} \end{array},} \\ {c = {{a}^{2}}\frac{{{{\gamma }_{0}}}}{{k_{{{\Sigma }}}^{S}}},} \end{array}} \\ {k = k_{\Sigma }^{T}.} \end{array},$Результаты аппроксимации кинетических кривых, полученных при различных интенсивностях возбуждающего света, представлены в табл. 1. Также в таблице представлены расчетные значения параметра bр, которые получены на основе уравнения (9) и значений параметров, полученных из кинетических кривых, измеренных при интенсивности источника I = Imax. Из уравнений (9) следует, что при уменьшении интенсивности, а следовательно, и ${{T}_{0}}$ в 10 раз, параметр b должен измениться от первоначального значение b (100%) = 0.58 до bр (10%) = 0.12, однако экспериментальный параметр почти не изменяется.
Таблица 1.
Результаты аппроксимации кинетики затухания замедленной флуоресценции уравнением (8), полученные при различной интенсивности возбуждающего света
| I/Imax, % | $k_{\Sigma }^{T}$, c–1 | c, отсч. | b | bр* |
|---|---|---|---|---|
| 100 | 0.37 | 1236 | 0.58 | 0.58 |
| 90 | 0.37 | 1032 | 0.58 | 0.55 |
| 80 | 0.37 | 899 | 0.57 | 0.52 |
| 70 | 0.37 | 763 | 0.56 | 0.49 |
| 60 | 0.37 | 631 | 0.56 | 0.45 |
| 50 | 0.37 | 511 | 0.55 | 0.40 |
| 40 | 0.37 | 385 | 0.55 | 0.35 |
| 30 | 0.37 | 253 | 0.54 | 0.29 |
| 20 | 0.37 | 166 | 0.53 | 0.21 |
| 10 | 0.37 | 71 | 0.49 | 0.12 |
* Значения параметра bp рассчитаны на основе уравнения (9) и значений параметров, полученных при аппроксимации кинетической кривой, измеренной при интенсивности источника I = Imax.
Кинетика процессов аннигиляции в твердофазных системах может быть описана с использованием статистического подхода [10, 11]. В рамках данного подхода рассматриваемая система представляет собой набор изолированных кластеров (доменов) молекул, в каждом из которых в начальный момент времени находится в среднем ${{T}_{0}}$ возбуждений. В начальный момент времени число возбуждений в доменах имеет вид распределения Пуассона. Возбуждения из разных кластеров не взаимодействуют. В одном домене возбуждения могут исчезать путем аннигиляции или мономолекулярного распада. Эти процессы приводят к изменению распределения возбуждения по доменам во времени. При этом кинетика дезактивации возбужденных состояний описывается средним числом возбуждений на домен и имеет вид:
(10)
$T = {{T}_{0}}\mathop \sum \limits_{p = 0}^\infty {{\left( { - 1} \right)}^{p}}{{A}_{p}}{{e}^{{ - \left( {p + 1} \right)\left( {p + r} \right)\frac{{\gamma t}}{2}}}},$(11)
${{A}_{p}} = \mathop \sum \limits_{k = p}^\infty \frac{{{{{\left( { - 1} \right)}}^{k}}k!{{Z}^{k}}\left( {r + 1 + 2p} \right)}}{{p!\left( {k - p} \right)!\left( {r + p + 1} \right) \ldots \left( {r + p + k + 1} \right)}},$Кинетика замедленной флуоресценции может быть найдена по формуле:
Результаты фитинга, полученные с использованием рассматриваемой модели, представлены в табл. 2. Из таблицы можно видеть, что при изменении интенсивности возбуждающего свет в 10 раз среднее число фотонов на домен Z и другие параметры, изменяются незначительно, в пределах ошибки.
Таблица 2.
Результаты аппроксимации кинетики затухания замедленной флуоресценции уравнениями (10)–(12), полученные при различной интенсивности возбуждающего света
| I/Imax, % | $k_{\Sigma }^{T}$, c–1 | γ, c–1 | Z |
|---|---|---|---|
| 100 | 0.52 | 0.77 | 1.06 |
| 90 | 0.52 | 0.97 | 0.87 |
| 80 | 0.52 | 1.01 | 0.83 |
| 70 | 0.52 | 0.93 | 0.87 |
| 60 | 0.50 | 0.65 | 1.17 |
| 50 | 0.50 | 0.87 | 0.89 |
| 40 | 0.49 | 0.82 | 0.97 |
| 30 | 0.48 | 0.84 | 1.00 |
| 20 | 0.47 | 0.97 | 0.88 |
| 10 | 0.44 | 0.87 | 0.90 |
Таким образом, независимость формы кинетики затухания замедленной флуоресценции от интенсивности возбуждающего света свидетельствует, что скорость бимолекулярного процесса мала по сравнению с мономолекулярными процессами. Это предположение также хорошо согласуется с моноэкспоненциальным характером фосфоресценции. Неэкспоненциальный характер кинетики замедленной флуоресценции обусловлен, по-видимому, наличием центров с разной вероятностью Т-Т аннигиляции. Предположим, что кристаллы комплексов CyH@β-CD имеют структуру подобную комплексам трет-бутилтолуол@β-CD [12, 13] или адамантан@β-CD [14], в которой β-CD образует каналы. При таком строении молекула нафталина может взаимодействовать в процессе Т-Т аннигиляции с молекулами, расположенными как в одном с ней канале, так и в соседнем (см. рис. 4). Константа скорости Т-Т аннигиляции экспоненциально зависит от расстояния между молекулами [15]:
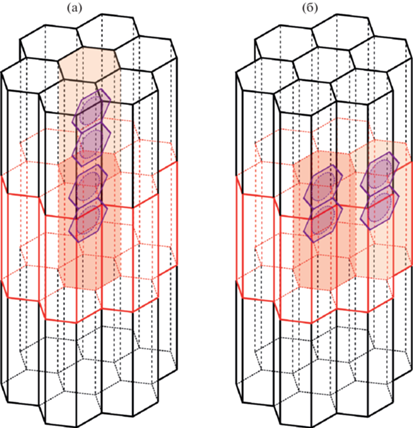
Рис. 4.
Схематичное изображение канальной структуры комплекса Naph-CyH@β-CD с возможными вариантами расположения Naph. Молекулы CyH, находящиеся в пустых ячейках, не показаны.
Поэтому можно предположить, что константы скорости Т-Т аннигиляции для молекул нафталина внутри канала будут больше из-за меньшего расстояния между ними.
Выражение для кинетики Т-Т аннигиляции для двух типов пар молекул нафталина, находящихся в соседних ячейках, можно получить из следующей системы уравнений:
(14)
$\left\{ {\begin{array}{*{20}{c}} {\frac{{d{{T}_{1}}\left( t \right)}}{{dt}} = - k_{{{\Sigma }}}^{T}{{T}_{1}}\left( t \right) + 2\mathop \sum \limits_{i = 1}^2 k_{{{\Sigma }}}^{T}T_{2}^{i}\left( t \right) + k_{{{\text{ISC}}}}^{S}S\left( t \right)} \\ {\frac{{dT_{2}^{i}\left( t \right)}}{{dt}} = - 2k_{{{\Sigma }}}^{T}T_{2}^{i}\left( t \right) - {{\gamma }_{i}}T_{2}^{i}\left( t \right),~~i = 1,2} \\ {\frac{{dS\left( t \right)}}{{dt}} = - k_{{{\Sigma }}}^{S}S\left( t \right) + \mathop \sum \limits_{i = 1}^2 {{\gamma }_{i}}T_{2}^{i}\left( t \right) = 0,} \end{array}} \right.$(15)
${{I}_{{{\text{Df}}}}} = k_{f}^{s}S\left( t \right) = \varphi \sum\limits_{i = 1}^2 {{{\gamma }_{i}}T_{2}^{i}\left( t \right)} = \sum\limits_{i = 1}^2 {T_{2}^{i}\left( 0 \right){{e}^{{ - \left( {2k_{{{\Sigma }}}^{T} + {{\gamma }_{i}}} \right)t}}}} ,$Если предположить, что химический потенциала молекулы нафталина в кристалле CyH@β-CD не зависит от наличия в соседних ячейка других молекул нафталина, то в этом случае кристалл, содержащий Naph-CyH@β-CD, можно считать набором из N эквивалентных ячеек, в которых размещены М молекул нафталина. В случае если у каждой молекулы нафталина может быть n соседних молекул, которые могут участвовать в процессе T-T аннигиляции. При этом ns из них могут иметь константу скорости ${{\gamma }_{1}}$, а $n - {{n}_{s}}$ – константу скорости $~{{\gamma }_{2}}$ можно получить следующие выражения для концентрации пар возбужденных молекул различного типa в начальный момент времени (см. Приложение 1).
(16)
$T_{2}^{1}\left( 0 \right) = T_{0}^{2}\frac{{{{n}_{s}}}}{n}\left( {1 - {{{\left( {1 - \alpha } \right)}}^{n}}} \right),$(17)
$T_{2}^{2}\left( 0 \right) = T_{0}^{2}\frac{{n - {{n}_{s}}}}{n}\left( {1 - {{{\left( {1 - \alpha } \right)}}^{n}}} \right),$Из выражений (16) и (17) следует, что соотношение возбужденных пар двух типов не должно зависеть от количества нафталина в кристалле. В табл. 3 приведены результаты двухэкспоненциального фитинга кинетических кривых замедленной флуоресценции, полученных при различных концентрациях нафталина. Среднее время жизни замедленной флуоресценции растет по мере увеличения концентрации нафталина.
Таблица 3.
Результаты аппроксимации кинетики затухания замедленной флуоресценции двухэкспоненциальной моделью и средние времена жизни флуоресценции при различном соотношении Naph : β-CD
| α, Naph : β-CD | $2k_{\Sigma }^{T} + {{\gamma }_{1}}$, c–1 | $2k_{\Sigma }^{T} + {{\gamma }_{2}}$, c–1 | A1, % | A2, % | τAv.Amp, c* |
|---|---|---|---|---|---|
| 1 : 3 | 1.15 | 3.30 | 67 | 33 | 0.68 |
| 1 : 10 | 1.15 | 3.23 | 65 | 35 | 0.67 |
| 1 : 20 | 1.14 | 3.34 | 63 | 37 | 0.66 |
| 1 : 40 | 1.12 | 3.52 | 57 | 43 | 0.63 |
| 1 : 100 | 1.11 | 3.39 | 53 | 47 | 0.61 |
* Среднее время жизни флуоресценции, рассчитанное по формуле: ${{{{\tau }}}_{{{\text{Av}}.{\text{Amp\;}}}}} = {{\sum\limits_{i = 1}^2 {{{A}_{i}}{{\tau }_{i}}} } \mathord{\left/ {\vphantom {{\sum\limits_{i = 1}^2 {{{A}_{i}}{{\tau }_{i}}} } {\sum\limits_{i = 1}^2 {{{A}_{i}}} }}} \right. \kern-0em} {\sum\limits_{i = 1}^2 {{{A}_{i}}} }}$.
Как следует из таблицы, значение амплитуды ${{A}_{1}} = \frac{{T_{2}^{1}\left( 0 \right)}}{{T_{2}^{1}\left( 0 \right) + T_{2}^{2}\left( 0 \right)}} = \frac{{{{n}_{s}}}}{n}$ возрастает, а ${{A}_{2}} = $ $\frac{{T_{2}^{2}\left( 0 \right)}}{{T_{2}^{1}\left( 0 \right) + T_{2}^{2}\left( 0 \right)}} = \frac{{n - {{n}_{s}}}}{n}$ падает по мере увеличения количества нафталина в образце. Наблюдаемые изменения происходят, по-видимому, вследствие нарушения предположения о независимости химического потенциала молекул нафталина внутри кристалла CyH@β-CD от наличия соседних молекул нафталина. Если предположить, что в кристалле все ячейки полностью заполнены нафталином и у каждого нафталина есть 8 соседних молекул, две из которых находятся в том же канале, то получим следующие значения амплитуд: A1 = 75%, A2 = 25%. По-видимому, расположение пары молекул нафталина в одном канале (рис. 4а) является более энергетически выгодным по сравнению с расположением пары молекул нафталина в соседних каналах (рис. 4б). Вследствие этого, при малых концентрациях Naph доля пар с более быстрой константой скорости Т-Т аннигиляции, находящихся в одном канале, больше. По мере роста концентрации число таких пар быстрее достигает своего максимально возможного значение, а число пар, расположенных в соседних каналах, растет медленнее, что предположительно и объясняет наблюдаемую зависимость A1 и A2 от концентрации.
ВЫВОДЫ
Обнаружено, что, наряду с долгоживущей фосфоресценцией, в микрокристаллах тройных комплексов нафталин-циклогексан-β-циклодекстрин при комнатной температуре наблюдается замедленная флуоресценция. Показано, что причиной наблюдаемой замедленной флуоресценции является процесс Т-Т аннигиляции. Проанализированы зависимости кинетики замедленной флуоресценции от интенсивности возбуждающего света и мольного соотношения нафталина и β‑циклодекстрина. Независимость формы кинетических кривых от интенсивности возбуждающего света указывает на то, что наблюдаемый неэкспоненциальный характер замедленной флуоресценции связан с наличием в образце центров с различной эффективностью Т-Т аннигиляции. Влияние концентрации нафталина на форму кинетических кривых связано, предположительно, с различиями в энергиях образования пар молекул нафталина различной геометрии.
Список литературы
Zhao J., Ji S., Guo H. // RSC Adv. 2011. V. 1. № 6. P. 937.
Kondakov D.Y. // Philos. Trans. R. Soc. A Math. Phys. Eng. Sci. 2015. V. 373. № 2044. P. 20140321.
Hirata S. // Adv. Opt. Mater. 2017. V. 5. № 17. P. 1.
Nazarov V.B., Vershinnikova T.G., Alfimov M.V. // Russ. Chem. Bull. 1999. V. 48. № 10. P. 1998.
Назаров В.Б., Авакян В.Г., Багрий Е.И. и др. // Известия Академии Наук. Серия Химическая. 2005. № 12. С. 2661.
Nazarov V.B., Avakyan V.G., Alfimov M.V. // J. Lumin. 2020. V. 219. P. 116909.
Назаров В.Б., Авакян В.Г., Алфимов М.В. и др. // Известия Академии Наук. Серия Химическая. 2003. С. 1.
Chandrasekhar S. // Rev. Mod. Phys. 1943. V. 15. № 1. P. 1.
Gulbinas V., Chachisvilis M., Valkunas L., et al. // J. Phys. Chem. 1996. V. 100. № 6. P. 2213.
Paillotin G., Swenberg C.E., Breton J., et al. // Biophys. J. 1979. V. 25. № 3. P. 513.
Bodunov E.N., Berberan-Santos M.N., Martinho J.M.G. // Chem. Phys. 2005. V. 316. № 1–3. P. 217.
Mavridis I.M., Hadjoudis E. // Carbohydr. Res. 1992. V. 229. № 1. P. 1.
Herbstein F.H., Marsh R.E. // Acta Crystallogr. Sect. B Struct. Sci. 1998. V. 54. № 5. P. 677.
Enright G.D., Udachin K.A., Ripmeester J.A. // Cryst-EngComm. 2010. V. 12. № 5. P. 1450.
Curutchet C., Voityuk A.A. // J. Phys. Chem. C. 2012. V. 116. № 42. P. 22179.
Дополнительные материалы отсутствуют.
Инструменты
Химия высоких энергий