Физикохимия поверхности и защита материалов, 2019, T. 55, № 3, стр. 237-246
Мезопористые сферические углеродные адсорбенты для сорбционного концентрирования и извлечения никотина и других компонентов сигаретного дыма
Т. С. Губецкая 2, О. А. Хайнакова 2, Н. Г. Кобылинская 1, *, Х. Р. Гарсиа 2
1 Кафедра аналитической химии, химический факультет, Киевский национальный университет
имени Тараса Шевченко
01601 Киев, ул. Владимирская, 64/13, Украина
2 Кафедра общей и неорганической химии, химический факультет, Университет Овьедо
33006 Овьедо, Х. Клаверия, 8, Испания
* E-mail: kobilinskaya@univ.kiev.ua
Поступила в редакцию 26.12.2017
После доработки 06.03.2018
Принята к публикации 18.04.2018
Аннотация
Получены сферические углеродные адсорбенты с использованием мезопористого MCM-48 и исследована их адсорбционная активность по отношению к токсичным компонентам сигаретного дыма, в том числе никотина, с целью их использования в качестве наполнителей фильтров в курительных кабинах. Методами низкотемпературной ад/десорбции азота, рентгеновской фотоэлектронной и ИК-спектроскопии, рН- и кондуктометрического титрований исследованы структурно-сорбционные свойства поверхности, а также состав поверхностного слоя углеродных материалов. Показано, что после карбонизации и активации, поверхностный слой полученных углеродных адсорбентов содержит протолитически-активные карбоксильные (0.1; 0.35 ммоль/г) и гидроксильные группы, а также широкий спектр других кислородсодержащих групп. Для полученного материала наблюдается узкое распределение пор по размерам (5–9 нм), микропоры практически отсутствуют. Установлено, что лучшие характеристики, превосходящие таковые у промышленного материала, имеет, полученный нами мезопористый сферический активированный уголь с развитой удельной поверхностью (1680 м2/г) и сорбционной емкостью по отношению к никотину на уровне 9.2 ммоль/г. Полная химическая регенерация адсорбентов (до 5–7 циклов) достигается экстрагированием органическими растворителями (хлороформ или метанол) без последующей термообработки. Взаимодействие газообразных продуктов горения сигарет со сферическими углеродными образцами проходит по всему объему, а не только на его внешней поверхности. Показано, что изученные адсорбенты могут быть применены, как в стационарных курительных кабинах, так и в кабинах оснащенных автономной вентиляцией.
1. ВВЕДЕНИЕ
Согласно данным Всемирной организации здравоохранения, ежегодно от непосредственного употребления табачных сигарет умирает более пяти миллионов людей, а около 600 000 умирает от вторичного воздействия табачного дыма [1]. Сигаретный дым является многокомпонентной смесью газов и твердой фазы (взвесь), в которой на газовую фазу приходится 92–95 мас. % [2], которую сложно разделить и идентифицировать. В сигаретном дыме обнаружено около 4000 компонентов, среди которых наиболее опасным для здоровья человека, и в тоже время, самым важным компонентом табака, а следовательно, и сигаретного дыма является никотин — алкалоид пиридинового ряда, содержащийся преимущественно в листьях и стеблях табака (от 0.3 до 5 мас. %), который вызывает зависимость от курения у человека и относится к первому классу безопасности [3].
Многие компоненты табачного дыма могут сохраняться и накапливаться в помещении, образуя еще более токсичные вещества [4], поэтому необходимо принимать и осуществлять эффективные меры для защиты населения от воздействия табачного дыма внутри помещений, на рабочих местах, а также в общественных местах, например, в аэропортах [5], так как обычные вентиляционные системы не обеспечивают полноценную очистку воздуха в таких помещениях [6].
В основном очистка воздуха в курительных кабинах осуществляется в несколько этапов. На первом этапе, с помощью фильтра грубой очистки, улавливаются содержащиеся в воздухе крупные частицы (электростатический фильтр), затем воздух проходит через аэрозольный фильтр, задерживающий остатки мелких частиц. На последнем этапе воздух доочищается на сменных фильтрах “тонкой” очистки от газообразных компонентов, выделяющихся во время курения сигарет. Вещества, которые используются в качестве наполнителя для фильтров, должны обладать высокими сорбционными характеристиками и коэффициентами массопереноса, легко регенерироваться, быть механически прочными, а также экономически выгодными. Диапазон фильтрующих материалов в основном ограничен использованием силикатных материалов, сепиолита, окиси алюминия, а также различных композиций на их основе. Однако чаще всего применяют различные виды угольных наполнителей [7, 8] из-за их высоких сорбционных характеристик, термической и механической прочности в сочетании с относительно невысокой стоимостью. В большинстве случаев для этих целей используют бурые древесные активированные угли. В литературе достаточно широко представлены исследования адсорбции никотина с использованием различных наноматериалов – графена [9], диоксида кремния, углеродных нанотрубок, полимерных нановолокон [10] и т.д. как газообразного [10, 11], так и из его водных растворов [12–15]. Несмотря на это, практическое использование этих материалов, на данный момент, ограничивается их высокой стоимостью, сложностью промышленного получения, особенно для наполнителей в курительных кабинах приемлемого объема, а также усложнением инженерных конструкций фильтров, не обеспечивающих, из-за плотной упаковки и неэффективного массопереноса, нормальный доступ к нижним слоям адсорбента.
Ранее были опубликованы данные об использовании пиролизированных пористых полимерных материалов, в т.ч. стирола и его производных, в качестве источника углерода для гранулированных углей [16], обладающий микро-, мезо- и макропористой структурой с удельной площадью поверхности 1110–1180 м2/г, используемых для очистки химических растворов и биологических жидкостей от тяжелых и радиоактивных металлов, а также в качестве энтеросорбента [17]. Knox с сотр. в своей работе [18] описали методику получение пористого аморфного угля с использованием кремнезема как матрицы/темплата. Согласно этой методике, силикагель пропитывался полимерными производными, которые при термической обработке полимеризовались с образованием сплошной сети, окружающей частицы двуокиси кремния. Kарбонизация полимерного покрытия и последующее растворение кремнеземной матрицы превращало его в пористый уголь. В 2000 г. Ryoo и его группа [19] использовали мезопористые кремнеземы для синтеза упорядоченного мезопористого углерода (CMK-1) из сахарозы, фурфурилового спирта или фенольной смолы путем взаимодействия материала на основе углерода с H2SO4 внутри мезопор MCM-48 [20]. Аналогичный подход был применен для синтеза пористых углей c использованием матрицы SBA-15 [21]. Напротив, MCM-41 – представитель того же класса соединений, оказался менее пригоден для этих целей [22], хотя позже были описаны и более удачные его применения [23], но массового использования для синтеза пористого углерода он так и не обрел. В большинстве исследований, где сахароза или фурфуриловый спирт использовались в качестве источника углерода, на финальной стадии получали графитоподобный мезопористый углерод [24]. Получение мезопористых углеродных сфер (гранул), с использованием матрицы мезопористой двуокиси кремния также описаны в [25], однако такие материалы обладали низкими структурно-сорбционными характеристиками и незначительной механической прочностью. В связи с этим актуальной остается задача создания активированных углей, обладающих комплексом механических и сорбционных параметров, а именно: высокой прочностью гранул, развитой пористостью и направленно изменяемой химической природой поверхностного слоя.
Общеизвестно [26, 27], что в большинстве своем углеродные материалы гидрофобны, что не способствует сродству по отношению к никотину и другим компонентам сигаретного дыма. Одним из возможных путей решения проблемы гидрофобности является введение в углеродную сетку гетероатомов. Так, например, азотсодержащий активированный уголь проявляет повышенную способность к поглощению анионов и слабых кислот, таких как кофеин [15] газообразный диоксид серы или сероводород [28]. Относительно невысокое количество кислородсодержащих поверхностных групп приводит к появлению гидрофильных центров на поверхности угля и придает способность к катионному обмену [29]. Наиболее простым способом окисления углеродных материалов является обработка азотной кислотой – сильным окислителем с медленным действием, реже используются концентрированные соляная и серная кислоты [30]. Альтернативными подходами может быть применение концентрированных растворов перекиси водорода [31] и персульфата аммония [14].
В настоящей работе проведена сравнительная оценка эффективности извлечения никотина промышленным активированным углем, используемым как наполнитель в фильтрах курительных кабин и сферическим угольным адсорбентом, полученным при карбонизации сополимера стирола и дивинилбензола с использованием в качестве темплата мезопористого кремнезема типа МСМ-48 для придания углеродному адсорбенту регулируемой мезопористой структуры. Такой адсорбент, благодаря своей сферической форме в сочетании с развитой поверхностью и механической прочностью может обладать хорошими массообменными характеристиками, что, вероятно, позволит существенно увеличить сорбционную емкость к газообразным продуктам горения сигарет.
Целью работы была разработка методологии получения мезопористых упорядоченных сферических углеродных адсорбентов и исследование их эффективности для извлечения и концентрирования основных компонентов сигаретного дыма с целью оценки возможности их использования в качестве наполнителей для фильтров в помещениях, предназначенных для курения. Контроль эффективности адсорбентов проводили по основному алкалоиду табака – никотину методом газовой хроматографии.
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
2.1. Реагенты
В работе использовали хлороформ (CHCI3), метанол (MeOH) хроматографической чистоты, стандарты никотина (99.8%, “Aldrich”) и хинолина (99.8%, “Aldrich”). Стандартные растворы никотина и хинолина готовили растворением точных навесок веществ в соответствующих растворителях (1 мг/мл). Минеральные кислоты и щелочи: Н2SO4 (х. ч., 96%), NaOH (ч. д. а.). В синтезе использовали свежеперегнанный толуол (х. ч.).
2.2. Методики синтеза углеродных адсорбентов
Для получения сферических углеродных материалов с регулируемой мезопористой структурой использовали кремнеземный темплат. В качестве темплата использовали упорядоченный мезопористый кремнезем с кубической структурой, ранее используемый для получения аморфного упорядоченного мезопористого углерода [32].
Мезопористый сферический активированный уголь (Ссфер), получали по комбинированной методике [32, 33]. Эксперименты по карбонизации проводили путем двухступенчатой пропитки МСМ-48 полистиролом и дивинилбензолом. В типичном эксперименте полистирол (5.0 г) и серную кислоту (1.0 г) растворяли в толуоле (40.0 г) и этот раствор затем добавляли к MCM-48 (0.2, 0.5; 1 г). Полученную смесь нагревали при 100°С в течение 0.5 ч, с последующим повышением до 160°С и выдерживали в течении 6 ч. Затем к кремнезем/полимерному остатку добавляли раствор, состоящий из дивинилбензола (5.0 г) и серной кислоты (1.0 г) в толуоле (40.0 г). Затем повторяли цикл ступенчатого нагрева смеси сначала до 100°С, а потом – до 160°С. Образец выдерживали при этой температуре, пока он не становился темно-коричневым (около 6 ч). Образовавшийся материал подвергали пиролизу в кварцевом реакторе при 850°C в течение 2-х ч. Полученный углерод/силикатный композит промывали раствором 2 М NaOH до полного растворения кремнеземной матрицы. Затем образцы фильтровали, промывали дистиллированной водой, после чего активировали в статическом режиме водяным паром в течение 4–6 ч и сушили при 100°С ((Ссфер)неакт).
На следующем этапе сферический углеродный материал кипятили с обратным холодильником в присутствии 50% раствора перекиси водорода при перемешивании на механической мешалке на протяжении 24 ч с последующей карбонизацией при температуре 800°С. После карбонизации уголь отмывали дистиллированной водой. В результате был получен сферический материал (Ссфер) со средним диаметром гранул 0.45–0.50 мм.
Для сравнения параллельно проводили исследования коммерчески доступного активированного древесного угля (Спром) (Filtroc, Италия), используемого в фильтрах для курительных кабин. По форме это уголь представляет собой полидисперсные частицы размером 0.7–1.2 мм.
2.3. Методы исследования адсорбентов
ИК-спектры регистрировали на ИК-Фурье спектрометре “NEXUS Thermo Nicolet 470” в диапазоне 400–4000 см–1 в режиме пропускания в таблетках из KBr (1 : 10). Анализ пористой структуры проводили путем снятия изотерм ад/десорбции азота при 77 К на приборе “ASAP 2020 Micromeritics” (США). Рентгеновские фотоэлектронные спектры снимали на приборе Kratos Analytycal “Series-800” с использованием монохроматического Mg (Kα = 1253.6 эВ) излучения.
Для кондуктометрического и потенциометрического титрования использовали “метод одной навески” [34]: навеску образца (0.15 г) помещали в 25 мл бидистилированной воды на 12 ч. Полученную суспензию титровали раствором гидроксида натрия (0.01 моль/л) в термостатированном сосуде при одновременном измерении удельной электропроводности (Metler Toledo MPC227) и рН суспензии при перемешивании на магнитной мешалке. рН суспензии измеряли на иономере “И-160М” с комбинированным стеклянным электродом.
2.4. Условия газохроматографического определения никотина и хинолина
Анализ проводили на газовом хроматографе “Agilent 6890”; детектор – пламенно-ионизационный; колонка – HP-5, 30 м × 0.32 мм × 0.25 мкм; газ-носитель – гелий (ТУ 51-40-80) расход 2.0 мл/мин. Скорость нагрева печи с 50 до 200°С составляла 10°С/мин. Температура инжектора и детектора составляли 270 и 350°С, соответственно. Объем аликвоты составлял 1 мкл. Пробы вводили в режиме “без деления потока” (Splitless). Концентрацию никотина в пробе определяли по градуировочному графику: CHCI3: S = (13.5 ± 0.9) + + (10 880.7 ± 0.2) C мг/мл (r2 = 0.9998); MeOH: S = = (52.3 ± 6.6) + (9434 ± 10.1) C (мг/мл) (r2 = 0.9999), а концентрацию хинолина – CHCI3S = = (78.49 ± 280.6) + (12 405 ± 428) C мг/мл (r2 = = 0.9996).
2.5. Сорбция сигаретного дыма на углеродных сорбентах
Исследования проводили с популярными на табачном рынке сигаретами: “Прима” (0.7 мг никотина, без фильтра, крепкие), “Marlboro” (0.7 мг никотина, с фильтром, крепкие), “Winston” (0.1 мг никотина, с фильтром, экстра легкие).
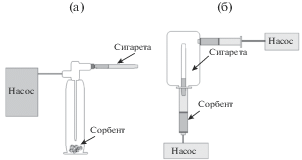
Концентрирование продуктов горения сигарет проводили с помощью курительных устройств в динамических и статических режимах (рис. 1). Используемые курительные устройства моделируют реальные условия при курении сигарет и близки по своим характеристикам к курительным машинам, применяемых при контроле качества сигарет, а также позволяют одновременно отбирать пробы побочного и основного сигаретного дыма, легко менять картриджи с адсорбентами для адсорбционных измерений.
При адсорбционных исследованиях в статическом режиме на дно стеклянной колбы помещали навеску исследуемого сорбента (0.1 г), после чего вставляли сигарету, включали насос, создающий тягу, поджигали сигарету и засекали время (рис. 1a). Время сорбции дыма 4-х сигарет составляло 20 мин для адсорбента массой 0.1 г. При исследованиях в динамическом режиме (рис. 1б) сорбция побочного дыма проводилась в течение 30 мин – время, за которое весь образованный побочный дым проходил через наполнитель. Сорбция основного дыма проводилась в течение 5–7 мин, что равно среднему времени выкуривания одной сигареты. Оптимальная масса сорбента в лабораторных условиях составила 0.1 г. Объем затяжки 20 мл, время между затяжками– 5–7 с. Проведена апробация методики в помещении (120 м2) с 30 курящими с использованием мембранного насоса и фильтра наполненного 100 г синтезированного образца (Ссфер).
2.6. Десорбция никотина с поверхности адсорбентов и их регенерация
В виалы с сорбентом массой 0.1 г добавляли 0.5, 1, 2, 3 мл органического растворителя (СНСІ3, МеОН), и оставляли на 30, 45, 60, 90 мин при комнатной температуре. Для отделения экстракта от твердой фазы проводили фильтрование на бумажном фильтре “синяя лента”. Полученные экстракты анализировали на полноту извлечения компонентов сигаретного дыма газохроматографическим методом. Кроме того, для удаления органических загрязнителей с поверхности адсорбента-наполнителя, проводили термообработку в муфельной печи при температуре 600–800°С в присутствии водяного пара и без него.
3. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
3.1. Пористая структура углеродных адсорбентов-наполнителей
Размер пор и их распределение, удельная поверхность имеют существенное влияние на массообменные и сорбционные характеристики наполнителей-адсорбентов при поглощении табачного дыма в помещении. Для изучения структурно-сорбционных характеристик адсорбентов применяли метод низкотемпературной ад/десорбции азота (рис. 2). Изотерму ад/десорбции Спром можно отнести к ленгмюровскому I типу по классификации IUPAC [35] с более крутым подъемом изотермы в начальной области р/р0. Это свидетельствует о преимущественно микропористой природе этого материала.
Рис. 2.
Изотермы низкотемпературной ад/десорбции N2 на поверхности: Спром (1), (Ссфер)неакт (2) и Cсфер(3).

Изотермы ад/десорбции азота для МСМ-48 и полученного углеродного образца Ссфер (рис. 2) имеют S-образный вид с четко выраженной петлей капиллярно-конденсационного гистерезиса в области относительных давлений 0.5–0.9 и относятся к IV типу по классификации IUPAC [35] и характерны для мезопористых материалов с узким распределением пор по размерам.
Этот вывод подтверждается при анализе структурно-сорбционных параметров адсорбентов (табл. 1) рассчитанных по десорбционной кривой изотерм методами ВЕТ (S, м2/г) и BJH (V, cм3/г; d, нм) [36], как наиболее полно описывающей морфологию пор углеродных материалов [37].
Таблица 1.
Структурно-сорбционные характеристики (удельная площадь поверхности (S), объем пор (Vобщ, Vмезо, Vмикро), диаметр пор (d)) пористых углеродных материалов, рассчитанные по данным изотерм низкотемпературной ад/десорбции азота методами БЕТ и BJH
| Образец | S, м2/г | Vобщ, см3/г | Vмезо, cм3/г | Vмикро, cм3/г | d, нм |
|---|---|---|---|---|---|
| Ссфер | 1680 | 1.19 | 0.93 | 0.24 | 5.02 |
| Спром | 970 | 0.95 | 0.35 | 0.87 | (2.2)3.6 |
| (Ссфер)неакт | 1330 | 1.03 | 0.88 | 0.21 | 4.95 |
| МСМ-48 | 1800 | 1.21 | 1.00 | 0.1 | 5.11 |
Примечание. Классификация пор согласно рекомендаций IUPAC [50].
Изученные материалы обладают разной пористой структурой и удельной поверхностью, которые существенно зависят от способа получения образцов (табл. 1). Taк, Ссфер полученный с использованием темплата МСМ-48 обладает высокой удельной площадью поверхности (1680 м2/г), что почти в два раза превышает соответствующие параметры для промышленного образца, при характерном мезопористом распределении размера пор у первого материала. И если в случае промышленного угля вклад микропористой составляющей велик, то у сферического материала, как и следовало ожидать исходя из метода получения, превалируют мезопоры. Вклад микропор для сферического угля не превышает 20.2%, тогда как для промышленного образца более 60% от общего объема пор.
Окисление раствором перекиси водорода поверхности Ссфер приводит к незначительному увеличению среднего диаметра пор, размер которых, свидетельствуют о мезопористом характере пористости этих образцов. Аналогичная пористая структура наблюдается и для образца МСМ-48, использованного в качестве темплата (табл. 1). Для Спром характерна бипористая структура, с преобладанием микропористой составляющей (рис. 2). Среди изученных образцов максимальный объем пор наблюдается в полученном Ссфер.
Следует отметить, что по структурно-адсорбционным характеристикам полученный мезопористый сферический углеродный адсорбент значительно превышает ранее описанные аналоги, например [19, 20], и даже некоторые углеродные наноматериалы [9].
3.2. Анализ функциональных групп поверхности адсорбентов-наполнителей
Идентификацию функциональных групп адсорбентов осуществляли методом ИК-спектроскопии (рис. 3).
В ИК-спектрах Спром и Cсфер присутствие метиленовых групп проявляется в виде нескольких полос поглощения в области 2850–2960 см–1, которые, несомненно, отвечают νas(С–Н) и νs(С–Н), а наличие полосы при 3445 см–1 относится к колебаниям νs(ОН) связанных гидроксильных групп [38]. Полосы поглощения при 1010 и 1096 см–1 образца Cсфер и уширенная полоса поглощения при 1120 см–1 для промышленного углеродного материала относятся к колебаниям νs(С–О–С) эфирных груп. Малоинтенсивные полосы поглощения при 1430 см–1, скорее всего, обусловлены колебаниями δ(С=С) углеродного каркаса. Наличие в ИК-спектрах Cсфер и Спром полос поглощения различной интенсивности в области 1750–1650 см–1 обусловлены наличием в углеродных материалах функциональных –COО- или С=О-групп. В ИК-спектре Cсфер, по сравнению со спектром Спром, несколько увеличивается интенсивность полос принадлежащих валентным колебаниям связи С–Н (2850–2960 см–1). Наличие малоинтенсивных узких полос в спектре Cсфер при 800 и 1275 см–1 вероятно относится к δ(Si–С) и νs(Si–С), соответственно, и свидетельствует о присутствии в углеродном каркасе незначительных количеств карбида кремния. Присутствие в ИК-спектре Cсфер полосы принадлежащий валентным колебаниям связи Si–С говорит о том, что дальнейшее повышение температуры карбонизации нежелательно [39]. Уширенные полосы поглощения образцов при 3445 см–1 указывают на различную степень гидратированности поверхности исследованных адсорбентов. Следует отметить, что адсорбированная вода (δ(ОН) 1630 см–1) присутствует в поверхностном слое всех изученных материалов.
Результаты ИК-спектроскопических исследований состава функциональных групп в углеродных образцах подтверждаются методами РФЭС путем анализа профиля С1s и О1s линий спектра в области 280–292 эВ. Разложение С1s полос спектра на гауссовы составляющие дает пять компонентов: составляющая с энергиями связи (Есв) 284.6 эВ, что отвечают С–С-группам углеродных слоев, с Есв ≈ 286.1 эВ относящейся к С–О связи в фенольной или эфирной группе, с Есв ≈ 287.3 эВ – С=О связи в карбонильной или эфирной группе, с Есв ≈ 288.4 эВ – С=О связи в карбоксильных или сложноэфирных группах, а также углероду в карбонатных группах или адсорбированном СО2 [40]. В спектре С1s полос не обнаружено компоненты относящуюся к Si–C (при 282.6 эВ [41]), возможно, из-за незначительного количества фазы SiC в образце. Разложение линии спектра О1s дает три компоненты: первая, интенсивная составляющая с максимумом при 531.2 эВ относящаяся к связи С=О в кетонных, сложноэфирных или карбонильных группах, вторая компонента средней интенсивности, при 532.2 эВ относящаяся к С–О связи в гидроксильных, эфирных группах, а также малоинтенсивная компонента относящаяся к молекулам воды при Есв = 535.0 эВ.
Таким образом, анализ РФЭС и ИК-спектров изученных углеродных образцов показал, что их поверхностный слой содержит в том или ином количестве имеют различныe функциональные группы, в том числе кислородсодержащиe: карбоксильные, карбонильные, неконденсированные фенольные (гидроксильные), эфирные, хинонные группы, а также молекулы воды (схема 1 ), что согласуется с данными полученными для ранее полученных углеродных адсорбентов [14].
Схема 1 . Поверхностный слой углеродных адсорбентов.
Высоким сродством к никотину и другим компонентам сигаретного дыма могут обладать кислородсодержащие группы, среди которых наиболее активными являются протолитически-активные функциональные группы. Исследования их природы и концентрации поверхностном слое углеродных и кремнеземных материалов были проведены методом кислотно-основного титрования (рис. 4).
Рис. 4.
Кривые кондуктометрического (1) и рН-метрического (2) титрований Спром (а) и Ссфер (б) щелочью (С(NaOH) = = 0.011 М, g = 0.15 г, V = 20 мл).
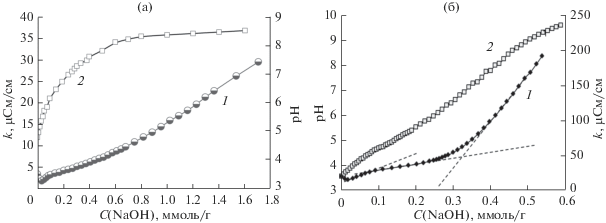
При титровании водной суспензии углеродных адсорбентов раствором NaOH на кривых кондуктометрического титрования присутствует минимум, характерный для слабокислотных карбоксильных групп в растворе [42] и на поверхности твердых носителей [34]. Дальнейшее увеличение электропроводности суспензии, после достижения точки эквивалентности, вызвано нейтрализацией еще более слабокислотных групп поверхности, скорее всего гидроксильных. Это подтверждает факт присутствия различных кислотных групп в фазе углеродного материала.
По перегибам на кривой кондуктометрического титрования (рис. 4) рассчитана концентрация протолитически-активных функциональных групп на поверхности адсорбентов: концентрация карбоксильных групп на поверхности Ссфер составляет около 0.35 ммоль/г, а гидроксильных – около 1.0 ммоль/г, в то время как, поверхностный слой образца Спром более однороден и содержит незначительное количество слабокислотных карбоксильных групп на уровне 0.1 ммоль/г.
3.3. Условия извлечения никотина и других компонентов сигаретного дыма углеродными адсорбентами
Для количественного определения никотина в сигаретном дыме используют газовую и высокоэффективную жидкостную хроматографию с различными типами детектирования (масс-, пламенно-ионизационным, азотно-селективным, диодно-матричным) [43, 44]. Все выше перечисленные методы, из-за сложного состава дыма, требуют предварительной пробоподготовки, включающей стадию твердофазного концентрирования [45], с последующей жидкостной экстракцией адсорбата органическими растворителями (метанол, хлороформ, изопропанол) [4, 5, 46, 47] или термодесорбцией при высоких температурах.
Парофазное газохроматографическое определение термодесорбированной газовой фазы сигаретного дыма проблематично из-за сложности идентификации составляющих в многокомпонентной смеси и перекрывания их пиков при хроматографическом анализе, поэтому для количественного определения проводили экстракцию никотина и других компонентов адсорбированных на поверхности углерода с помощью органических растворителей. После подбора оптимальных условий газохроматографического определения, (рис. 7) при которых другие компоненты экстракта не мешают определению, и происходит разделение пиков никотина (tR = 9.38 мин) и других сопутствующих веществ, входящих в состав дыма от сигарет, в соответствии с Rs критерием (Rs ≥ 1.5). Вместе с тем в экстракте сигаретного дыма обнаружен (при tR = 8.4 мин) и идентифицирован пик, соответствующий хинолину (рис. 7) [2], который является побочным продуктом синтеза никотина [3, 43], и не менее вредный для здоровья человека, чем никотин [48, 49]. То есть можно предположить, что один из путей попадания его в сигаретный дым является введение в табачное сырье искусственно синтезированного никотина.
Адсорбцию сигаретного дыма на поверхности материалов проводили в динамическом и статическом режимах. Согласно результатам газохроматографических исследований (рис. 5), тестируемые адсорбенты достаточно эффективно извлекают никотин в обоих режимах, поэтому могут быть применены в качестве наполнителей как в стационарных, так и в моделях кабин оборудованных вентиляцией. Также следует отметить, что эффективность извлечения никотина из газовой фазы в динамическом режиме в два раза выше, чем в статическом (рис. 5).
Рис. 5.
Хроматограммы экстракта сигаретного дыма после сорбции в динамическом (1) и в статическом (2) режимах (сорбент: Ссфер, экстрагент – СНCI3).

Обнаружено, что существенное значение при извлечении газообразных веществ имеет геометрия гранул адсорбента-наполнителя. Варьирование наполнителей в виде сферических гранул и зерен неправильной формы в динамических и статических условиях показали, что сферическая форма частиц углеродного наполнителя в наибольшей мере подходит для динамических условий поглощения сигаретного дыма в помещениях для курения. В этом случае обеспечивается наименьшее сопротивление газовому потоку в фильтрах и значительно уменьшается насыпная плотность наполнителя. Кроме того, облегчается возможность осуществления противоточных процессов в фильтрационном слое.
В табл. 2 приведены сравнительные данные эффективности углеродных сорбентов при сорбции никотина и хинолина из основной фракции сигаретного дыма в динамических условиях. Обнаружено наличие хинолина в сигаретном дыме практически всех марок сигарет, в среднем на уровне приблизительно 10% от общего содержания никотина.
Таблица 2.
Сравнение эффективности углеродных сорбентов при сорбции никотина и хинолина (г/г) из основной фракции сигаретного дыма по данным ГХ-ПИД (P = 0.95, n = 3)
| Марка сигарет | Ссфер | Спром | (Ссфер)неакт | |||
|---|---|---|---|---|---|---|
| никотин | хинолин | никотин | хинолин | никотин | хинолин | |
| Прима | 1.50 ± 0.02 | 0.12 ± 0.03 | 0.78 ± 0.04 | 0.08 ± 0.1 | 1.11 ± 0.04 | 0.12 ± 0.03 |
| Мarlboro | 0.98 ± 0.03 | 0.08 ± 0.02 | 0.59 ± 0.04 | 0.10 ± 0.1 | 0.54 ± 0.02 | 0.08 ± 0.02 |
| Winston | 0.88 ± 0.02 | 0.06 ± 0.02 | Не проводилось | 0.52 ± 0.01 | 0.05 ± 0.02 | |
Необходимо отметить, что наблюдается зависимость между структурно-сорбционными характеристиками угольных адсорбентов и их способностью поглощать никотин и другие компоненты сигаретного дыма (табл. 2). Наименее эффективным, из исследованных нами сорбентов, был коммерческий углеродный адсорбент. Это может быть вызвано как относительно более низкими структурно-сорбционными характеристиками, так и плохими массообменными характеристиками из-за неоднородности размера гранул и слишком плотной их упаковкой. Синтезированный же нами сферический адсорбент обладал высокой эффективностью удаления никотина из сигаретного дыма в воздухе. Максимальная сорбционная емкость для Ссфер по отношению к никотину составляла до 9.2 и до 6.8 ммоль/г – для образца полученного без дополнительного окисления перекисью водорода (табл. 2). По сорбционным характеристикам полученный мезопористый сферический углеродный адсорбент в несколько раз превышает ранее описанные окисленные активированные угли при менее развитой площади поверхности [14], и даже модифицированные мезопористые угли [15]. Это может быть обусловлено различными факторами, в частности своим массообменным и структурно-сорбционным характеристикам, высокому сродству поверхности адсорбента к адсорбату за счет электростатических и протолитических взаимодействий.
3.4. Десорбция никотина и сопутствующих компонентов с поверхности углеродных адсорбентов и их регенерация
Оптимизацию условий десорбции адсорбата с поверхности исследованных адсорбентов проводили путем жидкостной экстракции (экстракционно-химическая регенерация), изменяя природу и объем органического растворителя, время контакта фаз (рис. 6), состоящая из следующих этапов: 1 этап – отмывка углеродного материала органическим растворителем; 2 этап – повторная отмывка свежим растворителем с последующим газохроматографическим анализом смывов; 3 этап – высушивание адсорбента при температуре 100–120°С. Эффективность регенерации углеродного материала контролировалась методом термогравиметрического анализа, а также анализом пористой структуры и сорбционной активности материала.
Рис. 6.
Зависимость полноты извлечения никотина углеродным адсорбентом от времени контакта фаз (адсорбент: Ссфер, растворитель: СНCI3).

Установлено, что при экстракции хлороформом полное извлечение аналита проходит в течение одного часа (рис. 6). Тогда как при экстракции метанолом в тех же условиях для достижения полноты десорбции 1 ч недостаточно. Процесс химической регенерации позволяет извлечь 90–95% содержащегося сорбата с сохранением сорбционных параметров материала. Сферические углеродные материалы возможно регенерировать без значительного снижения эффективности от 5 до 7-ми циклов, далее наблюдалось ухудшение механических свойств адсорбента и деформация гранул. Контроль полноты регенерации проводили методом термогравиметрического анализа.
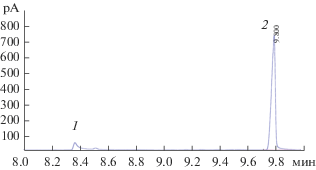
Рис. 7.
Хроматограмма экстракта сигаретного дыма хинолин (1), никотин (2) (сигарета: Marlboro, адсорбент: Ссфер, элюент: СНСІ3).
Для удаления органических загрязнителей с поверхности адсорбента-наполнителя проводили дополнительную регенерацию сорбентов путем термодесорбции (термическая регенерация). Эффективное удаление сорбата с поверхности адсорбентов происходит при температурах, превышающих 600°С. Полное восстановление пористой структуры и сорбционной активности углеродных адсорбентов может быть обеспечено термообработкой в течение 10–30 мин при 800–850°С в атмосфере водяного пара. Показано, что углеродные материалы возможно регенерировать без значительного снижения эффективности от 2 до 3-х циклов регенерации. Для промышленного углеродного наполнителя не удалось достичь полной десорбции адсорбата с поверхности и, соответственно, его полной регенерации, скорее всего, из-за большого количества червячных микропор (табл. 2). Этот факт позволяет предположить, что молекулы никотина и другие газообразные продукты горения табака проникают в мезопоры углеродных материалов и взаимодействие проходит по всему объему, а не лишь на их внешней поверхности.
ВЫВОДЫ
Проведена оценка эффективности синтезированных мезопористых сферических углеродных адсорбентов для удаления, контроля, извлечения и концентрирования никотина из газовой фазы. Проведен мониторинг извлечения никотина из сигаретного дыма с целью использования в фильтрах для курительных кабин, в сравнении с промышленным углеродным адсорбентом-наполнителем используемый в таких фильтрах. Установлено, что окисление углеродных образцов перекисью водорода приводит к формированию функционального слоя, который состоит из протолитически-активных карбоксильных и гидроксильных групп, а также других кислородсодержащих групп. Обнаружено, что из исследованных углеродных адсорбентов наиболее эффективным по отношению к никотину является полученный нами мезопористый сферический активированный уголь после стадии окисления. Сферическая форма частиц углеродного наполнителя в наибольшей мере подходит для динамических условий поглощения сигаретного дыма в помещениях для курения. Оптимизированы условия количественной экстракции никотина из исследуемых объектов. При газохроматографическом определении в сигаретном дыме обнаружен хинолин. Показана перспективность такого материала для использования в качестве наполнителей для курительных кабин, который поражает своей эффективностью и простотой регенерации. Полученные мезопористые сферические адсорбенты могут быть применены, как в стационарных курительных кабинах, так и в кабинах оснащенных автономной вентиляцией, эффективность которых в 2 раза выше, благодаря улучшенному массопереносу в адсорбционном слое углеродного материала.
Список литературы
Uchiyama Sh., Hayashida H., Izu R., Inaba Y. et al. // J. Chrom. 2015. V. 1426. P. 48–55.
Moir D., Rickert W.S., Levasseur G., Larose Y. et al. // Chem. Res. Toxicol. 2008. V. 21. № 2. P. 494.
Misra M., Leverette R.D., Cooper B.T., Bennett M.B. et al. // Intern. J. Environ. Research Pub. Health. 2014. V. 11. P. 11 325.
Ramírez N., Vallecillos L., Alastair C. et al. // J. Chrom. A. 2015. V. 1426. P. 191.
Pérez-Ortuño R., Martínez-Sánchez J.M., Fernández E. et al. // Anal. Bioanal. Chem. 2015. V. 407. № 28. P. 8463.
ISO Standard 3308, International Organization for Standardization. Routine Analytical Cigarette-Smoking Machine–Definitions and Standard Conditions. International Organization for Standardization, 2012. Geneva, Switzerland.
Вентиляционные Hepa и Ulpa фильтры Envirco, http://www.envirco.com.ua.
Курительные кабины, столы и комнаты для курения, http://www.scabins.ru.
Mahpishanian Sh., Sereshti H. // Talanta. 2014. V. 130. P. 71–77.
Guo Zh., Wu X., Dong J., Su H., Cai R. // Analytical Methods. 2014. V. 6. № 14. P. 5120.
Marcilla A., Beltran M.I., Gomez-Siurana A., Berenguer D., Martinez-Castellanos I. // J. Anal. Appl. Pyrol. 2016. V. 119. P. 162.
Majidi R., Karami A.R. // Diamond and Related Materials. 2016. V. 66. P. 47–51.
Lu C., Li H., Xu M., Wang S., Li G., Zhong W., Qin S. // Separation Science and Technology (Philadelphia, PA, United States). 2015. V. 50. № 14. P. 2124.
Pi K., Xia M., Wu P., Yang M., Chen Sh. et al. // J. Ind. Eng. Chem. (Amsterdam, Netherlands). 2015. V. 31. P. 112.
Cai J., Bennici S., Shen J., Auroux A. // Wat. Air Soil Poll. 2014. V. 225. P. 2088–2094.
Бурушкина Т.Н., Алейников В.Г., Kислицин Н.А. и др. // Адсорбция и адсорбенты. 1979. № 7. C. 15.
Картель М.Т., Козинченко О.П., Пузий О.М., Михаловський С.В., Стрелко В.В. // Патент України № 3396. 1994.
Knox J.H, Kaur B., Millward G.R. // J. Chromatogr. 1986. V. 352. P. 3.
Kruk M., Jaroniec M., Ryoo R., Joo S.H. // J. Phys. Chem. B. 2000. V. 104. P. 7960–7968.
Mbileni Ch.N., Prinsloo F.F., Witcomb M.J., Coville N.J. // Carbon. 2006. V. 44. P. 1476.
Fuertes A.B., Nevskaia D.M. // Micropor Mesopor Mater. 2003. V. 62. P. 177.
Jun S., Joo S.H., Ryoo R., Kruk M., Jaroniec M., Liu Z. et al. // J. Am. Chem. Soc. 2000. V. 122. P. 10712.
Perez L.D., Lopez J.F., Orozco V.H., Kyu T., López B.L. // J. Appl. Polym. Sci. 2009. V. 111. P. 2229.
Xia Y., Mokaya R. // Adv. Mater. 2004. V. 16. P. 1553.
Oda Y., Fukuyama K., Nishikawa K., Namba S., Yoshitake H., Tatsumi T. // Chem. Mater. 2004. V. 16. P. 3860.
Tascon J. Novel Carbon Adsorbents. 1st Edition. Elseveir. 600 p.
Adsorption by Carbons. Edited by E.J. Bottani, J.M.D. Tascón. Elseveir. 2008. 773 p.
Adib F., Bagreev A., Bandosz T.J. // Langmuir. 2000. V. 16. P. 1980.
Николаев В.Г., Стрелко В.В. Гемосорбция на активированных углях. Киев. Наукова думка, 1979. 360 с.
Hong C.-E., Lee J.-H., Kalappa P., Advani S.G. // Comp. Sci. Technol. 2007. V. 67. P. 1027.
Miyata Y., Maniwa Y., Kataura H. // J. Phys. Chem. B. 2006. V. 110. P. 25.
Telbiz G.M., Gerda V.I., Kobylinska N.G., Zaitsev V.M. et al. // NATO Science for Peaceand Security Series C: Environm. Secur. Springer. 2011. V. 2. C. 499.
Бурушкина Т.Н., Алейников В.Г., Kислицин Н.А. и др. // Адсорбция и адсорбенты. 1979. № 7. C. 15–18.
Зайцев В.Н., Кобылинская Н.Г., Костенко Л.С., Герда В.И. // Журн. аналит. химии. 2008. Т. 63. № 8. С. 304. (Zaitsev V.N., Kobylinskaya N.G., Kostenko L.S., Gerda, V.I. // Russian J. Analytical Chemistry. 2008. V. 63. № 8. P. 779.)
Sing K.S.W., Everett D.H., Haul R.A.W., Moscou L. et al. // Pure Appl. Chem. 1985. V. 57. № 4. P. 603.
Bunenauer S., Emmett H., Teller E. // Amer. J. Chem. Soc. 1938. V. 60. P. 309.
Rouquerol J., Rouquerol K.S.W., Sing P. et al. Adsorption by Powders and Porous Solids. Principles, Methodology and Applications, 2014. Elsevier Ltd. 626 p.
Infrared and Raman Characteristic Group Frequencies: Tables and Charts. 3rd ed By George Socrates (The University of West London, Middlesex, U.K.) / J. Wiley and Sons: Chichester, 2001. 348 p.
Colombo P., Paulson T.E., Pantano C.G. // J. Am. Ceram. Soc. 1997. V. 80. № 9. P. 2333.
Yue Z.R., Jiang W., Wang L., Gardner S.D. et al. // Carbon. 1999. V. 37. P. 1785.
https://srdata.nist.gov/xps/ElmSpectralSrch.aspx?selEnergy=PE.
Худякова Т.А., Крешков А.П. Теория и практика кондуктометрического и хронокондуктометрического анализа. М.: Химия, 1976. 304 с.
Gorrod J.W., Jacob P. Analytical determination of nicotine and related compounds and their metabolites. Elsevier, 1999. 772 p.
Trehy M.L., Ye W., Hadwiger M.E., Moore T.W. et al // J. Liq. Chrom. & Relat. Technol. 2011. V. 34. P. 1442.
Xiong W., Hou H., Jiang X., Tang G. et al. // Anal. Chim. Acta. 2010. V. 674. P. 71–78.
Marco E., Grimalt J.O. // J. Chrom. A. 2015. V. 1410. P. 51.
Varlet V., Farsalinos K., Augsburger M., Thomas A. et al. // Internal. J. Environ. Res. Pub. Health. 2015. V. 12. № 5. P. 4796.
Notice regarding requirement for annual submission of the quantity of nicotine contained in smokeless tobacco products manufactured, imported, or packaged in the United States. Centers for Disease Control and Prevention (CDC), Department of Health and Human Services. Notice // Federal Register. 1999. V. 64. № 55. P. 712.
Stanfill S.B., Jia L.T., Ashley D.L., Watson C.H. // J. Chrom. Sci. 2009. V. 47. № 10. P. 902.
IUPAC Manual of Symbols and Terminology for Physicochemical Quantities and Units, Appendix II: Definitions, Terminology and Symbols in Colloid and Surface Chemistry // Pure Appl. Chem. 1972. V. 31. № 4. P. 577.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов