Физикохимия поверхности и защита материалов, 2019, T. 55, № 3, стр. 234-236
Абсолютные изотермы адсорбции компонентов бинарных жидких растворов на макро- и микропористых адсорбентах
А. М. Толмачев 1, *, Д. А. Фирсов 1, Н. Г. Крюченкова 1, Т. А. Кузнецова 1
1 Московский государственный университет им. М.В. Ломоносова, химический факультет
199992 Москва, ГСП-2, Ленинские Горы, дом 1, строение 3, Россия
* E-mail: amtolmach@yandex.ru
Поступила в редакцию 29.04.2018
После доработки 18.06.2018
Принята к публикации 14.08.2018
Аннотация
В рамках решеточной модели рассмотрены методы описания абсолютных изотерм адсорбции компонентов бинарных растворов неэлектролитов на микро- и макропористых адсорбентах.
ВВЕДЕНИЕ
При экспериментальном изучении адсорбции растворов получают изотермы избыточной адсорбции. Однако для решения технологических задач необходимы абсолютные изотермы адсорбции компонентов растворов. Пересчет избыточных в абсолютные изотермы адсорбции компонентов растворов может быть проведен на основании соотношений [1]:
(1)
${{\bar {c}}_{1}} = \frac{{\Gamma _{1}^{x} + {{x}_{1}}\bar {c}_{2}^{0}}}{{1 - {{x}_{1}}\left( {1 - {{\bar {c}_{2}^{0}} \mathord{\left/ {\vphantom {{\bar {c}_{2}^{0}} {\bar {c}_{1}^{0}}}} \right. \kern-0em} {\bar {c}_{1}^{0}}}} \right)}};\,\,\,\,{{\bar {c}}_{2}} = \frac{{ - \Gamma _{1}^{x} + {{x}_{2}}\bar {c}_{1}^{0}}}{{1 - {{x}_{2}}\left( {1 - {{\bar {c}_{1}^{0}} \mathord{\left/ {\vphantom {{\bar {c}_{1}^{0}} {\bar {c}_{2}^{0}}}} \right. \kern-0em} {\bar {c}_{2}^{0}}}} \right)}}.$В работах [2, 3] было показано, что исходные избыточные изотермы на микро- и макропористых адсорбентах количественно описываются уравнениями решеточной модели с физически достоверными значениями параметров. В настоящем сообщении впервые показано, что абсолютные “экспериментальные” изотермы компонентов растворов, рассчитанные по соотношениям (1), также количественно описываются уравнениями этой модели.
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Уравнения избыточной адсорбции на микро- и макропористых адсорбентах (2), (3) и абсолютной адсорбции компонентов растворов (2), (4) имеют вид [2, 3]:
(2)
$\begin{gathered} \ln {{Y}_{1}}\left( {1 - {{X}_{1}}} \right){\text{/}}{{X}_{1}}\left( {1--{{Y}_{1}}} \right)--B + \\ + \,\,\Delta {\text{/}}kT\left( {A{{Y}_{{\text{1}}}}{\text{-- 12}}{{X}_{{\text{1}}}}} \right) = 0, \\ \end{gathered} $(4)
${{Y}_{1}} = {a \mathord{\left/ {\vphantom {a {{\text{N}}{{{\text{a}}}_{{1m}}}}}} \right. \kern-0em} {{\text{N}}{{{\text{a}}}_{{1m}}}}}.$(5)
$\begin{gathered} B = - {\text{[}}{{{\varepsilon }}_{{{\text{02}}}}} - {{{\varepsilon }}_{{{\text{01}}}}} + {{z}_{{\text{В }}}}{\text{(}}{{{\varepsilon }}_{{{\text{22}}}}} - {{{\varepsilon }}_{{{\text{12}}}}}{\text{)]/}}kT{\text{,}} \\ {\Delta } = {\text{2}}{{{\varepsilon }}_{{{\text{12}}}}} - {{{\varepsilon }}_{{{\text{11}}}}} - {{{\varepsilon }}_{{{\text{22}}}}}, \\ \end{gathered} $Для нахождения параметров системы уравнений (2), (3) и (2), (4) при численном моделировании изотерм адсорбции был использован нелинейный вариант метода наименьших квадратов (МНК) [5]. При этом системы уравнений решались совместно для получения зависимостей Г(X) или a(X), которые в исходных уравнениях выражены неявно. В результате для каждой из систем находился набор параметров a1m, Δ/kT, B, для которых сумма квадратов отклонений в указанной зависимости была минимальна. Кроме того, так как в случае нелинейного варианта МНК решение может зависеть от выбора начального приближения, нами перебирались несколько вариантов с разным начальным приближением, выбираемым на сетке внутри области физически обоснованных значений параметров.
В соответствии с литературными данными расчеты проводились для микропористых активных углей, в щелевидных порах которых могли разместиться два слоя молекул адсорбатов, а в случае макропористых адсорбентов адсорбционная фаза рассматривалась как монослойная [6].
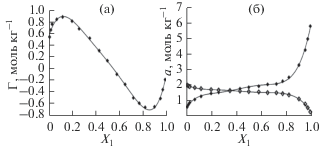
На рис. 1а представлено описание избыточной изотермы адсорбции раствора этанол–изооктан на активном угле АУ-1 при 303 K, а на рис. 1б соответствующее описание абсолютных изотерм.
Рис. 1.
Описание избыточной изотермы уравнениями (2), (3) (а) и абсолютных изотерм уравнениями (2), (4) (б) при адсорбции раствора этанол (◆)–изооктан (◇) на активном угле АУ-1 при 303 К.
На рис. 2а, 2б, рис. 3а, 3б, рис. 4а, 4б представлены аналогичные данные для адсорбции растворов бензол-этанол на АУ-1 при 338 K, бензол-четыреххлористый углерод на макропористом силикагеле КСК-2 при 338 K и этанол-этилацетат на силикагеле КСК при 338 K. Экспериментальные избыточные изотермы и рассчитанные по соотношениям (1) абсолютные изотермы – сплошные кривые, рассчитанные по уравнениям (2), (3) и (2), (4) – ромбики.
Рис. 2.
Описание избыточной изотермы уравнениями (2), (3) (а) и абсолютных изотерм уравнениями (2), (4) (б) при адсорбции раствора бензол (◆)–этанол (◇) на активном угле АУ-1 при 338 К.

Рис. 3.
Описание избыточной изотермы уравнениями (2), (3) (а) и абсолютных изотерм уравнениями (2), (4) (б) при адсорбции раствора бензол (◆)–четыреххлористый углерод (◇) на силикагеле КСК-2 при 338 К.

Рис. 4.
Описание избыточной изотермы уравнениями (2), (3) (а) и абсолютных изотерм уравнениями (2), (4) (б) при адсорбции раствора этанол (◆)–этилацетат (◇) на силикагеле КСК при 338 К.

Аналогичные данные получены и для других систем.
Видно, что избыточные и абсолютные изотермы разного вида количественно описываются уравнениями решеточной модели.
В табл. 1 приведены полученные константы уравнений для избыточных и абсолютных изотерм для систем: 1 – C2H5OH-i-C8H18–АУ-1, 303 K; 2 – С6H6–C2H5OH–АУ-1, 338 K; 3 – С6H6–CCl4–КСК-2, 338 K; 4 – C2H5OH–C2H5OCOCH3–КСК, 338 K.
Таблица 1.
Параметры уравнений избыточных (2), (3) и абсолютных (2), (4) изотерм. Для микропористых адсорбентов (1), (2) при двухслойной адсорбции приведены значения 2a1m
| Парам. | 1 изб. | 1 абс. | 2 изб. | 2 абс. | 3 изб. | 3 абс. | 4 изб. | 4 абс. |
|---|---|---|---|---|---|---|---|---|
| a1m/2a1m | 3.85 | 6.38 | 2.05 | 4.27 | 0.38 | 0.36 | 1.60 | 1.61 |
| Δ/kT | 1.49 | 1.52 | 1.30 | 1.17 | 1.92 | 1.83 | 1.92 | 1.96 |
| B | 3.87 | 3.82 | 3.80 | 3.96 | 2.58 | 2.47 | 0.88 | 0.90 |
Из приведенных данных видно, что, как и следовало ожидать, параметры для абсолютных и избыточных изотерм удовлетворительно согласуются, что свидетельствует об адекватности решеточной модели, как в случае адсорбции в микропорах активных углей, так и при монослойной адсорбции растворов на макропористых адсорбентах. При этом, как отмечено в работе [3], значения а0, рассчитанные из избыточных изотерм на микропористых адсорбентах, не соответствуют абсолютным величинам предельной адсорбции и для расчета абсолютных изотерм компонентов растворов необходимо использовать независимо найденные значения предельных адсорбций компонентов.
На основании абсолютных изотерм можно построить фазовые диаграммы соответствующих систем, т.е. зависимости Xi от Yi, и рассчитать однократные коэффициенты разделения компонентов при адсорбции для различных равновесных составов фаз
На рис. 5 и 6 приведены примеры фазовых диаграмм для адсорбции раствора бензол-этанол на микропористом угле АУ-1 при 338 K и раствора бензол–четыреххлористый углерод на макропористом силикагеле КСК-2 при 338 K, а в табл. 2 приведены значения K для всех, перечисленных выше 4-х систем для различных составов фаз.
Рис. 5.
Фазовая диаграмма для адсорбции раствора бензол (1, ◆)–этанол (2, ◇) на активном угле АУ-1 при 338 К.

Рис. 6.
Фазовая диаграмма для адсорбции раствора бензол (1, ◆)–четыреххлористый углерод (2, ◇) на макропористом силикагеле КСК-2 при 338 К.

Таблица 2.
Коэффициенты разделения для систем (1)–(4) при различных составах равновесных фаз
| Y1 | K | |||
|---|---|---|---|---|
| 1 | 2 | 3 | 4 | |
| 0.2 | 3.41 | 4.85 | 10.71 | 5.62 |
| 0.4 | 1.63 | 3.80 | 9.64 | 6.57 |
| 0.6 | 0.87 | 2.84 | 7.18 | 8.11 |
| 0.8 | 0.44 | 2.53 | 6.93 | 16.99 |
Такие данные необходимы при разработке процессов разделения компонентов растворов.
Приведенные данные показывают, что уравнения решеточной модели не только количественно описывают абсолютные изотермы адсорбции компонентов растворов, но и позволяют получать важные характеристики соответствующих адсорбционных систем.
Список литературы
Толмачев А.М. // Физикохимия поверхности и защита материалов. 2010. Т. 46. № 2. С. 136.
Толмачев А.М., Еременко Е.М., Трубников О.И., Окишева Н.А. // Журн. физич. химии. 1996. Т. 70. № 11. С. 2044.
Толмачев А.М., Бородулина М.В., Арзамасцева А.Б., Крюченкова Н.Г., Рябухова Т.О. // Вестн. Моск. ун-та. Сер. 2. Химия. 2001. Т. 42. № 4. С. 244.
Толмачев А.М. // Адсорбция газов, паров и растворов. 2012. М. Изд. “Граница”. 239 с.
Lawson C.L., Hanson R.J. Solving Least Squares Problems, Prentice–Hall, 1974.
Толмачев А.М., Трубников О.И., Бородулина М.В. // Журн. физич. химии. 2000. Т. 74. № 2. С. 357.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов


