Физикохимия поверхности и защита материалов, 2019, T. 55, № 4, стр. 396-401
Импеданс алюминиевого электрода с нанопористым оксидом
А. И. Щербаков 1, *, И. Г. Коростелева 1, И. В. Касаткина 1, В. Э. Касаткин 1, Л. П. Корниенко 1, В. Н. Дорофеева 1, В. В. Высоцкий 1, В. А. Котенев 1
1 Федеральное государственное бюджетное учреждение науки Институт физической химии и электрохимии
им. А.Н. Фрумкина Российской академии наук (ИФХЭ РАН)
119991 Москва, Ленинский проспект, 31, Россия
* E-mail: scherbakov@ips.rssi.ru
Поступила в редакцию 16.04.2018
После доработки 19.11.2018
Принята к публикации 13.12.2018
Аннотация
Методами спектроскопии электрохимического импеданса и электронной микроскопии с рентгеноспектральным микрозондом исследованы два типа оксидных пленок на алюминии: гладкой компактной и пористой (нанооксид), сформированной двухстадийным оксидированием. Выбрана эквивалентная схема, адекватно отвечающая полученным спектрам импеданса, позволяющая оценить толщины и проводимость барьерных оксидных слоев, а также площадь, занятую нанопорами для пленок различного типа.
ВВЕДЕНИЕ
К характерным особенностям алюминия относится его сравнительно высокая коррозионная стойкость, обусловленная образованием на поверхности плотной пассивирующей пленки оксида алюминия, предохраняющей металл от непосредственного взаимодействия со средой. Защитная оксидная пленка на поверхности алюминия в пассивном состоянии имеет толщину 5–100 нм [1]. Для получения оксидной пленки, имеющей регулярную ячеистую структуру, проводят процесс анодного оксидирования (анодирования) алюминия. В зависимости от условий процесса различают толстослойное и тонкослойное анодирование. Толстослойное анодирование [1–3] с различным наполнением пор широко применяется в технике, и, в зависимости от условий получения, оксид может иметь различные свойства (повышенную коррозионную стойкость, износостойкость, твердость и др.). При тонкослойном анодировании [4–8] на поверхности алюминия формируется нанопористый оксид с регулярной ячеистой структурой и диаметром пор 20–100 нм, который помимо повышения коррозионной стойкости [9], может служить подложкой для осаждения в нанопоры компонентов, придающих материалу уникальные физические и химические свойства. Так, например, для придания каталитических свойств в нанопоры оксида осаждают переходные металлы [10, 11]. Морфологические особенности и свойства получаемых композиций во многом определяются свойствами ячеистой регулярной структуры подложки [12]. В связи с этим в исследованиях много внимания уделяется изучению строения и свойств самой нанопористой подложки. Одним из эффективных методов исследования может служить метод электрохимического импеданса [13–15].
МЕТОДИКА ЭКСПЕРИМЕНТА
Оксидные пленки формировали на фольге толщиной 150 мкм из алюминия чистотой 99.99 мас. %. Фольгу предварительно отжигали при 450°С в течение 1 ч для снятия внутренних напряжений. Нанопористые оксидные пленки получали методом двухступенчатого анодирования [4] в гальваностатическом режиме при плотности тока 10 мА/см2 в 10% растворе H2SO4. Перед первым этапом анодирования образцы подвергали химическому травлению в растворе HF + + HNO3 + HCl + H2O в соотношении 1 : 10 : 20 : 69 в течение 10 мин при 20°С. Время гальваностатической обработки 2 ч. Перед вторым этапом образцы 10 мин обрабатывали в растворе, содержащем 20 г/л CrO3, 35 мл/л H3PO4 (85%) при 60–90°С. Время гальваностатической обработки 1 ч. В результате такой обработки формируется пленка нанопористого оксида с регулярной ячеистой структурой [5].
Исследования импеданса на образцах с компактным гладким, формирующемся при помещении образца алюминия в раствор, и нанопористым оксидом осуществляли на комплексе, включающем потенциостат IPC-ProMF и измеритель импеданса FRA-2 в интервале частот от 0.05 до 3000 Гц. Для того, чтобы избежать влияния электролита на процессы, которые протекают на образце и могут менять свойства оксидных пленок (проявление фарадеевского импеданса при переносе заряда вследствие электрохимического окисления алюминия в кислых и щелочных средах, взаимодействие ионов электролита с оксидной пленкой в среде ионов хлора) измерение импеданса осуществляли в достаточно “мягком” растворе 0.5 н Na2SO4. Исследования проводили при стационарном потенциале и анодной поляризации в области пассивности алюминия с амплитудой переменнотокового сигнала 20 мВ. Измерения проводили по трехэлектродной схеме. Образцы оксидированной фольги зажимали в оправке, обеспечивающей рабочую поверхность в виде круга площадью 1 см2 и надежный контакт неоксидированной поверхности металла с рабочим с электродом с обратной стороны. Вспомогательным электродом служила платиновая сетка площадью ~10 см2. Потенциалы измеряли относительно насыщенного хлорид-серебряного электрода, подключенного через солевой мостик, исключающий попадание хлоридов в рабочее пространство. Для анализа эквивалентных схем и расчета номиналов их элементов использовали программу DCS (Dummy Cell Solver), созданную автором статьи В.Э. Касаткиным (ИФХЭ РАН), позволяющую рассчитать теоретическую частотную зависимость импеданса выбранной схемы и, сравнивая ее с экспериментально полученной зависимостью, оптимизировать номиналы элементов схемы, минимизируя сумму относительных ошибок F между экспериментальными Ze и моделируемыми Zm значениями импеданса системы для каждой их частот fi в исследуемом диапазоне:
(1)
$F = \sum\limits_{i = {{f}_{{\min }}}}^{{{f}_{{\max }}}} {(Z{{e}_{i}}} - Z{{m}_{i}}){\text{/}}Z{{e}_{i}},$Для контроля морфологии поверхности использовали метод электронной микроскопии. Использовался растровый электронно-микроскопический комплекс (РЭМ) с полевым катодом Quanta 650 FEG (FEI, Нидерланды) в режиме детектирования вторичных электронов. Прибор был снабжен приставкой ретгеноспектального микроанализа элементного состава анализируемой поверхности.
ЭКСПЕРИМЕНТАЛЬНЫЕ РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
SEM-микроскопия
На рис. 1 приведены электрономикроскопические снимки поверхности алюминия с гладким оксидом (а) и нанопористым оксидом (б). Видно, что в отличие от относительно гладкой поверхности для случая (а), нанопористый оксид формируется в виде периодичной сотовой структуры, элементом которой являются шестигранники, обрамляющими круглую пору (рис. 1б). Наблюдается плотноупакованная структура заполнения поверхности сотами (поры занимают примерно 80% всей поверхности). Сотовая структура поверхности нанопористого оксида характеризуется следующими параметрами: средний диаметр пор 25 нм, шаг (период сотовой структуры) по поверхности 34 нм, средний диаметр описанной окружности шестигранника 30 нм.
Рис. 1.
Электрономикроскопическое снимки оксидированной поверхности алюминия с гладким оксидом (а), нанопористым оксидом (б), после травления электронным пучком (в) и 3-мерные после травления электронным пучком.

Структура ячеек и сот оксида может быть более четко выявлена после травления пучком электронов повышенной интенсивности за счет электрон-индуцированной кристаллизация элементов нанопористого оксида. Для этого выбранная часть анодированной поверхности выдерживалась под действием электронного пучка электронного микроскопа повышенной интенсивности (рис. 1 – прямоугольная область в центре). На рис. 1в приведен фрагмент изображения обработанной электронным пучком поверхности. На границе раздела пора-оксид выявляется переходная область толщиной 4–6 нм, видимо соответствующая двуслойной структуре оксида на стенке пор. Очевидно выявленный внешний слой стенок пор может быть сопоставлен с внедрением сульфат-ионов в материал оксида стенок поры.
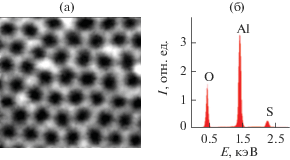
Из анализа рентгеноспектральных данных (рис. 2) следует, что на поверхности присутствуют элементы О, Al, S. Атомное соотношение между кислородом и алюминием составляет почти 1.7, что приближается к теоретическому значению (1.5 для Al2O3). Присутствие S может возникнуть от внедрения следов электролита в анодную пленку, ее поры и стенки пор. Как известно, пористые пленки, образующиеся в серной кислоте загрязнены кислотными группами ${\text{SO}}_{4}^{{ - 2}}.$
Рис. 2.
Результаты рентгеноспектрального анализа (б) поверхности образца с нанопористым оксидом (а).
На рис. 1г приведено объемное изображение нескольких соседних сот. Видно, что после кристаллизации электронным пучком топография поверхности действительно усиливается: между соседними сотами по поверхности явственно проявляется гексагональная сеть межсотовых границ, где толщина оксида максимальна. Можно предположить, что селективное “травление” остальной поверхности нанопористого оксида может быть связано с преимущественной кристаллизацией и результирующим компактированием стенок пор, где оксид был максимально дефектен благодаря внедренным при анодировании сульфат-ионам.
Спектроскопия электрохимического импеданса
На рис. 3 приведены фазовочастотные и амплитудочастотные (диаграммы Боде) характеристики образцов алюминия с гладким оксидом в исследуемом растворе при двух значениях потенциалов (потенциале коррозии, возникающем при помещении образца в раствор, и Е = +200 мВ). В обоих случаях значения логарифма модуля импеданса линейно уменьшаются с увеличением частоты. Отклонение от линейной зависимости наблюдается в области низких частот при испытаниях с поляризацией. При средних и высоких значениях частот графики зависимостей образцов без поляризации и с поляризацией практически совпадают. Фазовочастотные характеристики образцов в области средних и высоких значений частот также совпадают. При средних значениях частот отмечается независимость угла сдвига фаз от частоты. Сдвиг фаз в этом интервале частот близок к 90°. “Завал” фазовочастотной характеристики в области высоких частот можно связать с проявлением индуктивной составляющей цепи аналогично конденсаторам. В области низких частот снижение значений угла сдвига фаз можно объяснить тем, что емкостная составляющая импеданса обратно пропорциональна частоте и возрастает настолько, что существенную роль начинает играть перенос тока через оксид параллельно емкости (шунтирование емкости паразитным параллельным сопротивлением). Все перечисленные данные позволяют рассматривать систему алюминия с гладким оксидом, как неидеальный конденсатор с токами утечки через оксид, и представить в виде схемы параллельно соединенных конденсатора и сопротивления. Конденсатор в данном случае образован зарядами на поверхностях раздела металл-оксид и оксид-раствор, а в качестве диэлектрической прокладки выступает пленка оксида на поверхности металла. При поляризации электрода в анодную область (рис. 3 кривая 2) “завал” фазовочастотной характеристики с уменьшением частоты наступает раньше (при более высоких значениях частот). При отсутствии на пассивном электроде заметного переноса заряда вследствие заторможенности электрохимических процессов практически все падение напряжения (разность потенциалов разомкнутой цепи и потенциала поляризации) приходится на оксидную пленку. Это может создать в пленке оксида электрическое поле, ускоряющее миграционные явления, что фактически может снизить его сопротивление11. В результате, шунтирующий эффект сопротивления в системе с поляризацией наступает при более высоких значениях частот по сравнению с разомкнутой цепью.
Рис. 3.
Диаграммы Боде для образцов алюминия с гладким оксидом: 1 – зависимость фазового угла θ от частоты для образцов алюминия при потенциале коррозии; 2 – зависимость фазового угла θ от частоты для образцов алюминия при поляризации (Е = +200 мВ); 3 – зависимость модуля импеданса |Z| от частоты для образцов алюминия при потенциале коррозии; 4 – зависимость модуля импеданса |Z| от частоты для образцов алюминия при поляризации (Е = +200 мВ).
Диаграммы Найквиста исследованных электродов (рис. 4) представляют собой слабовыраженный полукруг. Если рассматривать только их, можно предположить разные эквивалентные схемы расчета вплоть до схемы с элементом Варбурга. Но, учитывая вышеизложенное обсуждение, выполнять расчеты по диаграмме Найквиста следует по эквивалентной схеме, включающей последовательно соединенный резистор R0 и схему из параллельно соединенных элемента постоянной фазы CPE и сопротивления R. В этой схеме R 0 отвечает за сопротивление электролита и обкладок конденсатора, сопротивление R отвечает за утечки тока через оксид, а параметры элемента СPE характеризуют емкостные свойства системы и неидеальность конденсатора. Расчетные значения параметров представлены в табл. 1.
Рис. 4.
Диаграммы Найквиста: 1 – образец алюминия с гладким оксидом при потенциале коррозии; 2 – образец алюминия с гладким оксидом при поляризации (Е = +200 мВ); 3 – образец алюминия с нанооксидом при потенциале коррозии; 4 – образец алюминия с нанооксидом при поляризации (Е = +200 мВ). Точками представлены экспериментальные данные, кривыми расчетные данные на основании эквивалентной схемы.

Таблица 1.
Таблица значений параметров, рассчитанных по эквивалентной схеме
| Образец | Потенциал, мВ | R0, Ом | R, МОм | Y, Ом с–n | n | Погреш-ность, % | Толщина оксидного слоя, нм |
|---|---|---|---|---|---|---|---|
| Al с гладким оксидом | –200 | 29 | 1.33 | 3.23 × 10–6 | 0.91 | 6.27 | 2.74 |
| –100 | 18 | 0.68 | 3.36 × 10–6 | 0.89 | 2.27 | 2.63 | |
| 0 | 23 | 0.75 | 3.14 × 10–6 | 0.90 | 3.12 | 2.82 | |
| +100 | 23 | 0.61 | 3.03 × 10–6 | 0.90 | 3.05 | 2.92 | |
| +200 | 18 | 0.52 | 3.00 × 10–6 | 0.89 | 2.56 | 2.95 | |
| +300 | 24 | 0.50 | 2.85 × 10–6 | 0.90 | 3.22 | 3.11 | |
| +400 | 2 | 0.61 | 2.85 × 10–6 | 0.88 | 6.30 | 3.11 | |
| Al с нанооксидом | –470 | 0 | 11.4 | 8.07 × 10–7 | 0.93 | 3.99 | – |
| –400 | 0 | 15.9 | 8.11 × 10–7 | 0.93 | 3.23 | – | |
| –300 | 0 | 15.5 | 8.12 × 10–7 | 0.93 | 3.67 | – | |
| –200 | 0 | 11.2 | 8.20 × 10–7 | 0.92 | 3.69 | – | |
| –100 | 4 | 48.3 | 7.92 × 10–7 | 0.94 | 3.28 | – | |
| 0 | 13 | 36.4 | 7.53 × 10–7 | 0.95 | 3.86 | – | |
| +100 | 22 | 34.7 | 7.38 × 10–7 | 0.95 | 3.46 | – | |
| +200 | 23 | 31.6 | 7.24 × 10–7 | 0.95 | 3.16 | – | |
| +300 | 18 | 30.0 | 7.16 × 10–7 | 0.95 | 3.55 | – | |
| +400 | 2294 | 2880 | 7.12 × 10–7 | 0.95 | 3.45 | – |
Из таблицы следует, что для образцов с гладким оксидом сопротивление электролита R0 невелико и в пределах ошибки эксперимента не зависит от поляризации электрода. Экспоненциальный фактор n практически не меняется. Уравнение для импеданса элемента СРЕ имеет вид ${{Z}_{{{\text{CPE}}}}} = {1 \mathord{\left/ {\vphantom {1 Y}} \right. \kern-0em} Y}{{(j2\pi f)}^{n}},$ где Y – частотно независимый предэкспоненциальный множитель, j – мнимая единица, f – частота сигнала, n – показатель степени, определяющий характер частотной зависимости (–1 ≤ n ≤ 1). Приведенное в таблице значение n имеет величину порядка 0.9, близкую к 1, что, однако, не позволяет в полной мере рассматривать элемент CPE, как конденсатор с сосредоточенными параметрами. Возможно, это связано с некоторым размытием заряда в пространстве вследствие наличия диффузионной части двойного электрического слоя в электролите. Амплитудная составляющая Y элемента CPE формально имеет размерность Ом С–n, но при n, близком к единице, может интерпретироваться в единицах емкости С (Фарады). Параметр Y линейно падает с ростом поляризации. По всей видимости, это связано с линейным приростом толщины оксида. Сопротивление R практически вдвое уменьшается с началом поляризации, а затем в пределах ошибки эксперимента остается в интервале 0.5–0.7 МОм. Можно предполагать, что уменьшение сопротивления, связанное с возникновением электрического поля в оксиде, при дальнейшей поляризации компенсируется соответствующим утолщением оксида.
Из данных, приведенных в таблице, можно оценить толщину оксидного слоя из выражения для емкости С:
где ε0 – электрическая постоянная; ε – относительная диэлектрическая проницаемость среды; S – площадь образца; d – толщина слоя.Для табличного значения относительной диэлектрической постоянной Al2O3 имеющей значение порядка 10 и емкости в интервале значений от 3.3 до 2.8 мкФ при площади образца 1 см2 можно вычислить, что толщина оксида меняется от 2.7 до 3.1 нм в зависимости от поляризации. Исходя из вычисленных значений толщины оксида, можно полагать, что речь идет о так называемом барьерном слое.
Ранее нами были тщательно проанализированы зависимости толщины барьерного слоя нанопористых и гладких оксидов алюминия от напряжения на ванне в различных электролитах. Для серной кислоты было получено, что толщина барьерного слоя увеличивается на 1.0 нм на 1 В напряжения. Для наших условий формирования нанопористых оксидов конечное напряжение на ванне порядка 15 В. Следовательно, общая толщина барьерного слоя составляет величину порядка 15 нм. Расхождение, по всей видимости, связано с шероховатостью поверхности. Сопоставление расчетной толщины и реальной может служить мерой фактора шероховатости, который в нашем случае дает значение 5. Следовательно, метод электрохимического импеданса может быть использован для расчета фактора шероховатости поверхности.
Даже в отсутствие данных о заряде обкладок и, соответственно, напряженности электрического поля в оксиде при потенциале коррозии, можно, тем не менее, оценить прирост напряженности электрического поля и заряда при наложении поляризации. Несмотря на рост толщины оксида при увеличении поляризации, прирост напряженности поля и, соответственно, заряда обкладок линейно увеличивается с ростом потенциала.
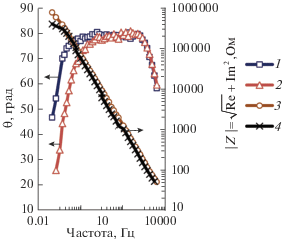
Характер частотных зависимостей угла сдвига фаз и модуля импеданса на электроде с нанооксидом алюминия (рис. 5) такой же, как и на алюминии с гладким оксидом. График зависимости модуля импеданса от логарифма частоты также линеен и его наклон соответствует наклону прямых на образцах алюминия без нанооксида. Однако, по абсолютной величине модуль импеданса выше. Область, где угол сдвига фаз независим от частоты, расположен ближе к 90° на алюминии с нанооксидом, чем на алюминии с гладким оксидом. Для наглядности на рис. 6 приведены значения угла и модуля импеданса от поляризации для обоих электродов. Следует отметить, что поляризация не влияет на эти параметры, но различия между электродами с наноструктурой на поверхности и без нее по абсолютной величине параметров достаточно заметны. В случае электрода с нанооксидом (рис. 5) низкочастотный “завал” фазовочастотной характеристики наступает при более низких частотах. Это характерно, как для разомкнутой цепи, так и для поляризованного электрода. Следовательно, эту систему также можно описать, как неидеальный конденсатор, с поправкой на то, что неидеальность конденсатора менее выражена.
Рис. 5.
Диаграммы Боде для образцов алюминия с нанооксидом: 1 – зависимость фазового угла θ от частоты для образцов алюминия при потенциале коррозии; 2 – зависимость фазового угла θ от частоты для образцов алюминия при поляризации (Е = +200 мВ); 3 – зависимость модуля импеданса |Z| от частоты для образцов алюминия при потенциале коррозии; 4 – зависимость модуля импеданса |Z| от частоты для образцов алюминия при поляризации (Е = +200 мВ).

Рис. 6.
Зависимость фазового угла и модуля импеданса образцов алюминия от поляризации при частоте 100 Гц: 1 – зависимость модуля импеданса |Z| от поляризации для образцов алюминия с нанооксидом; 2 – зависимость модуля импеданса |Z| от поляризации для образцов алюминия с гладким оксидом; 3 – зависимость фазового угла θ от поляризации для образцов алюминия с нанооксидом; 4 – зависимость фазового угла θ от поляризации для образцов алюминия с гладким оксидом.

На диаграмме Найквиста (рис. 4) кривые для образцов с нанооксидом на поверхности также имеют вид незамкнутой полуокружности. Представляя эквивалентную схему расчета в таком же виде, как и на алюминии с гладким оксидом можно рассчитать параметры составляющих элементов (табл. 1). Значения сопротивления R и амплитудной составляющей элемента CPE для образцов с нанооксидом, как и в случае гладкого оксида, снижаются с ростом поляризации. При этом сопротивление R выше, чем в первом случае, а емкость ниже. Исходя из предположения, что барьерный слой, располагающийся на дне пор, имеет такую же природу и толщину, как барьерный слой гладкого оксида, оба эффекта можно объяснить размерным фактором. Толстая часть нанооксида, в схеме расчета подключенная параллельно барьерному слою нанопор, вследствие высокого сопротивления и низкой емкости не оказывает заметного влияния на измеряемый импеданс. Следовательно, рассматривать следует только сами поры. Площадь, занятая порами, составляет лишь долю от общей поверхности. То есть, если в случае гладкого оксида в образовании конденсатора участвует вся поверхность, то в случае нанопористого оксида, только часть поверхности. Отсюда общее сопротивление образцов с нанопорами становится выше, а емкость ниже пропорционально доли поверхности, занятой нанопорами. При таком предположении можно рассчитать площадь поверхности нанооксида, занятую порами. Она составит около 0.25 от общей площади оксида. Это соответствует доле занятой порами в регулярной гексагональной структуре, в которой шестигранник поры окружен шестигранниками оксида [16].
ЗАКЛЮЧЕНИЕ
Таким образом, исследования в достаточно “мягком” растворе Na2SO4, способствующем устойчивой пассивации алюминия, показывают, что система металл-оксид может быть интерпретирована несложной эквивалентной схемой, из которой вполне надежно можно определить параметры системы. Исследования импеданса показывают, что нанооксид ведет себя также как и гладкий оксид, но с уменьшенной относительно видимой поверхности площадью. Данные измерения импеданса позволяют оценить как толщину барьерного слоя, так и относительную площадь, занятую нанопорами.
Список литературы
Томашов Н.Д., Тюкина М.Н., Заливалов Ф.П. Толстослойное анодирование алюминия и его сплавов. М.: Машиностроение, 1968. С. 156.
Анодные оксидные покрытия на металлах и анодная защита / Францевич И.Н., Пилянкевич А.Н., Лавренко В.А., Вольфсон А.И. 2-ое изд., перераб. и доп. Киев: Наук. думка, 1985. С. 280.
Diggle J.W., Downie T.C., Goulding C.W. // Chem. Rev. 1969. V. 69. № 3. P. 365.
Masuda H., Fukuda K. // Science. 1995. V. 268. P. 1466.
Щербаков А.И., Оше Е.К., Скворцова И.Б. и др. // Физикохимия поверхности и защита материалов. 2011. Т. 47. № 2. С. 176.
Щербаков А.И., Скворцова И.Б., Золотаревский В.И. и др. // Физикохимия поверхности и защита материалов. 2009. Т. 45. № 1. С. 71.
Jia Liu, Shu Liu, Haihui Zhou, Congjia Xie et al. // Thin Solid Films. 2014. № 552. P. 75.
Doman’ska M.M., Norek M., Stepniowski W.J., Budner B. // Electrochemica Acta. 2013. V. 105. P. 423.
Hossein Aghajani, Davoud Pourabbas, Mirali Seyed Shariatdoust // Protection of Metals and Physical Chemistry of Surfaces, 2017, vol. 53, Issue 6, pp. 1034–1039.
Liu Qiying, Guo Xiaohui, Chen Junli, Li Juan et al. // Nanotechnology. 2008. V. 19. № 36. 365608. 9 p.
Lu Zhou, Yu Guo, Jian Chen et al. // Fuel. 2012. V. 92. P. 373.
Лозовая О.В., Тарасевич М.Р., Богдановская В.А., Касаткина И.В., Щербаков А.И. // Физикохимия поверхности и защита материалов. 2011. Т. 47. № 1. С. 45.
Щербаков А.И., Касаткина И.В., Касаткин В.Э., Золотаревский В.И. // Физикохимия поверхности и защита материалов. 2014. Т. 50. № 2. С. 178.
De Laet J., Scheers J., Terryn H., Vereecken J. // Electrochimica Acta. 1993. V. 38. № 14. P. 2103.
Martin F.J., Cheek G.T., O’Grady W.E., Natishan P.M. // Corrosion Science. 2005. V. 47. P. 3187.
Osamu Nishinaga, Tatsuya Kikuchi, Shungo Natsui, Ryosuke O. // Suzuki Scientific Reports. 2013. V. 3. Article number: 2748.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов


