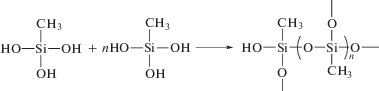Физикохимия поверхности и защита материалов, 2019, T. 55, № 4, стр. 380-390
Гибридные органокремнеземные покрытия для твердофазной микроэкстракции: высокоэффективные адсорбенты для определения следовых количеств парабенов
Б. А. Шнайдер 1, В. М. Левчик 1, М. Ф. Зуй 1, Н. Г. Кобылинская 1, *
1 Киевский национальный университет имени Тараса Шевченко, химический факультет,
кафедра аналитической химии
01601 Киев, ул. Владимирская, 64/13, Украина
* E-mail: kobilinskaya@univ.kiev.ua
Поступила в редакцию 04.07.2018
После доработки 24.10.2018
Принята к публикации 19.11.2018
Аннотация
Методом золь–гель синтеза в присутствии полиэтиленгликоля (PEG) получены новые гибридные органокремнеземные покрытия с различным содержанием алкильных функциональных групп на поверхности кварцевого волокна для твердофазной микроэкстракции (ТФМЭ). Исследованы структурно-сорбционные свойства синтезированных кремнеземных покрытий разного состава. По данным термогравиметрического анализа основной термолиз органического слоя адсорбционных покрытий наблюдается при температурах выше 350°С. Изучено влияние условий синтеза на термическую стабильность полученных покрытий. Установлено, что за счет использования различных PEG и кремнийорганических прекурсоров, соотношения компонентов в реакционной смеси, можно регулировать структурные характеристики получаемых покрытий для ТФМЭ и их адсорбционные свойства. показана перспективность использования полученных покрытий для ТФМЭ при извлечении и концентрирования парабенов в водных растворах при 24°С при рН 3.0–5.5 с их последующим газохроматографическим определением, предложенная методика характеризуется хорошей точностью и воспроизводимостью (Sr ≤ 2.3%). Проведены сравнительные исследования полученных гибридных органокремнеземных покрытий для ТФМЭ с комерческидоступным волокном с биполярным полимерным покрытием – дивинилбензол/карбоксен/полидиметилсилоксан.
1. ВВЕДЕНИЕ
Парабены – ряд сложных эфиров п-гидроксибензойной кислоты, отличающиеся радикалами эфирной группы (Схема 1 ), которые уже около ста лет используются как консерванты косметической, фармацевтической и пищевой продукции [1]. Последние исследования показали, что парабены небезопасны для здоровья человека [2, 3]. Существует мнение, что парабены вызывают рак груди, так, высокая их концентрация была обнаружена в 18 из 20 злокачественных образований. Согласно нормам ЕС содержание одного парабена в косметической продукции не должно превышать 0.4 мас. % [4]. Распространенность использования парабенов в продуктах потребления способствует попаданию их в окружающую среду и организм человека, в этой связи становится необходимым разработка высокоэффективных методик пробоподготовки и их определения не только для контроля содержания в продукции на макроуровне, но и в объектах окружающей среды, а также биообразцах, в которых они могут содержаться на уровне ppb [5, 6].
Чаще других среди ряда парабенов в промышленности используют метил- (МП), этил- (ЭП), пропилпарабены (ПП), которые являются слабыми органическими кислотами и мало отличаются между собой значениями рКа, но при этом имеют разную гидрофобность (lg PМП = 1.9 ± 0.2; lg PЭП = = 2.4 ± 0.1, lg PПП = 2.9 ± 0.2) [6], что и используется при их хроматографическом разделении [6, 7].
С целью интенсификации и минимизации пробоподготовки для определения аналитов в сложных матрицах, в последнее время активно начали применять метод микроэкстракции, в том числе волоконную твердофазную микроэкстракцию (ТФМЭ) [8]. ТФМЭ основана на равновесии раздела аналитов между жидким или газообразным образцом и тонким слоем адсорбирующего материала, которым обычно покрывается кварцевое волокно или стальная проволока. Материал адсорбционного покрытия волокна для ТФМЭ играет ключевую роль в эффективности экстракции, поскольку оказывает влияние на распределение аналитов между фазой адсорбционного покрытия и матрицей пробы, а, следовательно, влияет на селективность и степень извлечения аналита во время пробоподготвки. Идеальное адсорбционное покрытие для ТФМЭ должно обладать высокой эффективностью экстракции, высокой термической и химической устойчивостью, длительным сроком службы и прочной адгезией между покрытием волокна или проволоки.
Cхема 1. Структурные формулы метилпарабена (а), этилпарабена (б), пропилпарабена (в).
Для волоконной ТФМЭ разработаны и коммерциализированы ряд покрытий на основе, например, полиакрилата (PA), полидиметилсилоксана (PDMS), карбовакса (CW), карбоксен/полидиметилсилоксана (CAR/PDMS), полидиметилсилоксан/дивинилбензола (PDMS/DVB), карбовакс/дивинилбензола (CW/DVB), дивинилбензол/карбоксен/полидиметилсилоксана (DVB/CAR/PDMS) и карбовакс/темплатные смолы (CW/TPR) [9]. Среди недостатков существующих коммерческих полимерных покрытий для волоконной ТФМЭ можно отметить следующие:
(1) низкая термическая стойкость (обычно в диапазоне 240–280°C); однако некоторые волокна, такие как PDMS и CAR/PDMS, обладают довольно высокой термостабильнoстью (до 340°C для PDMS, в зависимости от толщины покрытия и до 320°C для CW/PDMS), тогда как, например, волокно PDMS/DVB ограничено температурами до 270°C, а волокно CW (на основе PEG без дополнительных добавок и включений) может использоваться только до 250°C;
(2) набухание в органических растворителях, что значительно ограничивает использование таких покрытий в хроматографии, особенно в жидкостной;
(3) отсутствие надежного связывания адсорбционного покрытия с неподвижной фазой волокна при относительно большой толщине адсорбционного слоя (от 7 до 100 мкм [9]). Можно предположить, что это один из основных факторов служащих причиной снижения рабочего температурного диапазона волокна и удаление адсорбционной фазы с его поверхности.
Неселективность – еще одна проблема характерная для существующих коммерческих покрытий для ТФМЭ. Для увеличения селективности к определенному классу аналитов и устойчивости в некоторых специфических средах разработаны и описаны гибридные покрытия с адсорбционными фазами на основе полипиррола [10], полианилина [11], покрытия на основе углерода [12], графен/PEG [13], ионных жидкостей [14], а также содержащие включенные в полимерную пленку частицы, например, молекулярные импринтированные полимеры [15, 16] обладающие более высокой селективностью к целевым аналитам. Гибридные адсорбционные фазы имеют более высокую cорбционную емкость, чем полимерные, к тому же и адсорбционное равновесие на них достигается быстрее [17].
Для формирования адсорбционного слоя используются разные подходы, большинство из которых основываются или на электроосаждении покрытия на металлическую проволоку или на разных вариантах золь–гель технологии. Использование золь–гель технологии при получении адсорбционных покрытий для волоконной ТФМЭ было впервые предложено в 1997 г. [18] и в последнее время приобретает все большее распространение [19–21]. Высокая термостабильность волокон для ТФМЭ полученных по золь–гель технологии позволила использовать такие волокна при высоких температурах инжекторов ГХ (т.е. более 300°С) [18, 22]. В работе [23], для экстракции полихлорированных бифенилов и полярных ароматических аминов в водной среде с последующим газохроматографическим определением протестированы три типа органокремнеземных волокон для ТФМЭ, полученные по золь–гель технологии способные выдерживать температуры до 360°С. В качестве кремнийорганического прекурсора был использован метилтриметоксисилан, а поликонденсация проводилась в водной среде путем кислотного гидролиза в присутствии трифторуксусной кислоты (ТФК) как катализатора. Использование золь–гель метода при получении органокремнеземных покрытий для ТФМЭ метода, позволяет варьируя условия синтеза (природу и соотношение реагентов в реакционной смеси (РС), режим гидролиза и обработки, позволяют вводить в адсорбционный шар ранее сформированные частицы [24] относительно легко влиять на состав, строение и свойства конечных продуктов. Следует отметить, что гибридные органокремнеземные адсорбционные покрытия для ТФМЭ полученные по золь–гель методологии показали превосходные механические, термические свойства, в первую очередь, из-за механической прочности каркасов на основе диоксида кремния, которая обусловлена их высокой степенью сшивания, и являются одними из наиболее эффективных для концентрирования и определения полярных и малополярных органических соединений [25].
Для ТФМЭ малополярных соединений (к которым относятся и парабены) предлагаются волокна с адсорбционным покрытием, содержащие на поверхности одновременно полярные и неполярные функциональные фрагменты [26], а также фазы, содержащие в одной молекуле как полярный (например, аминогруппу), так и неполярный фрагменты [27, 28]. Их применение позволяет увеличить полноту извлечения органического компонента фазы до 10%, что очень важно при рутинном анализе, особенно косметической продукции. Этот подход ограничивается высокой ценой таких покрытий, а также тем что волокна с такими покрытиями имеют тенденции к набухаемости, так как в основном они получены на основе полимеров. Одним из подходов к улучшению параметров ТФМЭ при определении парабенов является использование адсорбционных фаз, которые имеют высокую плотность закрепленного слоя, но меньшую гидрофобность, чем классические С18, например полиакрилонитрил/С18 [29]. Другим направлением улучшения характеристик адсорбционных покрытий является использование полярных фаз содержащих планарные ароматические фрагменты, такие как полианилин и его производные [30].
В данной работе предпринята попытка поиска оптимальных условий синтеза эффективных гибридных органокремнеземных покрытий на основе PEG для волоконной твердофазной микроэкстракции, которые обладают повышенной химической и термической стабильностью и содержат на поверхности алкильные функциональные группы (–CH3 и –C18H37). Исследование их термических свойств, структурных и текстурных характеристик, а также определение природы и роли дефектов в структуре адсорбционных покрытий на селективность и адсорбционные свойства по отношению к органическим молекулам. Оптимизация условий ад/десорбции и изучение возможности их регенерации. Кроме того, предполагалось провести сравнительный анализ свойств полученных органокремнеземных покрытий на основе PEG с коммерчески доступными покрытием DVB/CAR/PDMS для извлечения и определения ряда парабенов методом газовой хроматографии с пламенно-ионизационным детектированием.
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реагенты и материалы. Метилпарабен, этилпарабен, пропилпарабен производства “Реахим” (99.9%). Полиэтиленгликоль: ПЕГ-115(4000), х. ч., “Реахим”; 15 000 и 35 000 (Sigma-Aldrich).
В Sigma-Aldrich (Германия) были приобретены триметоксиметилсилан (CH3–Si(OMe)3, 95%), октадецилтриметокси силан (C18H37–Si(OMe)3, 90%). Трифторуксусная кислота (ТФК, Merck), HCl (ч. д. а.), свежеперегнанный ацетон (х. ч.).
Для получения гибридных органокремнеземных покрытий использовали промышленный держатель Supelco (США) и немодифицированное кварцевое волокно. Сравнительные экстракционные исследования проводили на DVB/CAR/PDMS-волокне той же фирмы.
Синтез и нанесение органокремнеземных покрытий на кварцевое волокно для ТФМЭ. Синтез проводили по усовершенствованной нами методике [31] следующим образом: к 400–1600 мг PEG добавляли 400 мкл ацетона и нагревали до температуры 50°С на протяжении 15 мин. Затем в РС добавляли 400 мкл метил- или октадецилтриметоксисилана и 150–600 мкл ТФК и 50–200 мкл Н2О. Полученную РС центрифугировали на протяжении 5 мин. Соотношения реагентов в РС приведены в табл. 1.
Таблица 1.
Состав РС для синтеза гибридных органокремнеземных покрытий для волоконной ТФМЭ
| Образец | PEG | Ацетон | Прекурсор | ТФК | Н2О | ||
|---|---|---|---|---|---|---|---|
| ММ*, г/моль | m(PEG), мг | V, мкл | ФГ** | V, мкл | V, мкл | V, мкл | |
| А2 | 4000 | 400 | 400 | CH3- | 800 | 300 | 100 |
| А3 | 15 000 | CH3- | 1600 | 600 | 200 | ||
| А4 | C18H37 C18H37 |
400 | 150 | 50 | |||
| А5 | 4000 | 800 | 300 | 100 | |||
| В1 | 15 000 | CH3- | 800 | 200 | |||
| В2 | CH3- | 800 | 50 | ||||
| В3 | CH3- | 800 | 100 | ||||
| С1 | 35 000 | CH3- | 800 | 200 | |||
| С3 | 35 000 | CH3- | 800 | 100 | |||
| С4 | 15 000 | CH3- | 800 | 200 | |||
Для активации кварцевого капилляра волокно длиной 1 см и диаметром 100 мкм погружали в 1 М раствор NaOH на 1 ч, промывали водой и погружали в 0.1 М HCl на 30 мин. Снова промывали водой и высушивали. Активированное волокно погружали на 30 мин в свежеприготовленный золь–гель раствор. Данную операцию повторяли трижды.
Полученное модифицированное волокно высушивали на протяжении 12 ч при комнатной температуре в эксикаторе с CaCl2. Перед использованием модифицированное волокно для ТФМЭ конденсировали в течение 1 ч при 300°С в инжекторе газового хроматографа.
Методы исследования полученных покрытий. ИК-спектры регистрировали на ИК-Фурье спектрометре “NEXUS Thermo 470 Nicolet” в диапазоне 400–4000 см–1 в режиме пропускания в таблетках из KBr (1 : 10).
Термические исследования полученных покрытий PEG/SiO2 проводили методом термогравиметрии (ТГА) на дериватографе Shimadzu DTG-60H в пределах температурного диапазона 20–550°С. Навеску образца (5–10 мг) нагревали со скоростью 10°С/мин в токе Ar. Как эталон использовали Al2O3.
Для оценки морфологии образцов использовали сканирующий электронный микроскоп JSM-6390LV (JEOL, Япония). Элементный микроанализ выполнен с помощью Microanalysis Oxford Inca Energy 200 system. Перед анализом на образцы наносилось дополнительное электропроводящее покрытие из золота.
Градуировочный график для определения метил-, этил-, пропилпарабенов c помощью ТФМЭ в водном растворе. В четырех виалах емкостью 20 мл готовили растворы с концентрациями каждого из парабенов 1.0; 2.0; 3.0; 5.0 мг/л. Для этого вносили соответствующую аликвоту стандартного водного раствора смеси парабенов с концентрацией 100 мг/л, создавали концентрацию высаливающего агента (NaCl) 100 мг/мл и оптимальное pH 6.0, добавляли дистиллированную воду до общего объема 10 мл и перемешивали раствор. Капилляр с покрытием опускали в раствор, закрепляли держатель капилляра над виалой с раствором и проводили экстракцию в течение 30 мин при комнатной температуре, перемешивая раствор на магнитной мешалке. Десорбцию проводили в течение 2 мин при 240°С в инжекторе газового хроматографа. Уравнение ГГ для определения индивидуальных образцов парабенов: МП (S = (0.4 ± 1.0) + (10.2 ± 0.3) С(мг/л), r2 = 0.99974); ЭП (S = (–32.5 ± 7.0) + (49.8 ± 2.2) С(мг/л), r2 = = 0.99902); ПП (S = (–81.1 ± 22.6) + (169.1 ± 7.2) С(мг/л), r2 = 0.99454).
Методика анализа модельных смесей парабенов с помощью волоконной ТФМЭ. В трех виалах емкостью 20 мл готовили растворы с концентрациями каждого парабена 2.5 мг/л. Для этого вносили соответствующую аликвотную часть стандартного водного раствора смеси парабенов с концентрацией 10 мг/л, затем добавляли 100 мг/мл NaCl добавляли воду до 10 мл, pH 6.0 и перемешивали раствор. Экстракцию проводили в течение 30 мин при комнатной температуре, десорбцию – в течение 2 мин при 240°С.
Методика анализа модельных смесей парабенов с помощью волоконной ТФМЭ с покрытием DVB/CAR/PDMS. В трех виалах емкостью 20 мл готовили растворы с концентрациями каждого парабена 1.0 мг/л. Для этого вносили соответствующую аликвотную часть стандартного водного раствора смеси парабенов с концентрацией 10 мг/л, добавляли NaCl до концентрации 150 мг/мл, создавали pH 6.0, доводили водой до общего объема 10.0 мл и перемешивали раствор. Капилляр с покрытием опускали в раствор и проводили экстракцию в течение 60 мин при 40°С, десорбцию – в течение 2 мин при 270°С в инжекторе газового хроматографа. Уравнение ГГ для определения индивидуальных образцов парабенов: МП (S = (–14.5 ± 3.8) + (64.8 ± 2.8) С(мг/л), r 2 = 0.99622); ЭП (S = (4.0 ± 4.8) + (361.4 ± 4.0) С(мг/л), r 2 = 0.99963); ПП (S = (16.6 ± 14.3) + (1096.2 ± ± 12.3) С(мг/л), r2 = 0.99962).
Условия газохроматографического определения парабенов. Анализ проводили на газовом хроматографе “Agilent 6890”; детектор – пламенно-ионизационный; капиллярная колонка – HP-5, 30 м × 0.32 мм × 0.25 мкм; газ-носитель – гелий (ТУ 51-40-80) расход 2.0 мл/мин. Температуру печи с 50 до 200°С увеличивали со скоростью 10°С/мин. Температура инжектора и детектора составляли 270 и 350°С, соответственно. Объем аликвотной части раствора для инжекции составлял 1 мкл.
3. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
3.1. Синтез гибридных органокремнеземных покрытий на поверхности кварцевого волокна для ТФМЭ
Раствор золя получали смешиванием соответствующих количеств силана (золь–гель-прекурсор/стационарная фаза), PEG (золь–гель-активный органический полимер), и ТФК, содержащей 5% воды (катализатор золь–гель синтеза). PEG использовали для удлинения кремнийорганической сети и для равномерного распределения стационарной органической фазы на поверхности волокна.
Получение гибридных органокремнеземных покрытий для волоконной ТФМЭ методом золь–гель синтеза можно условно описать последовательными реакциями (Схема 2 ):
(1) кислотный гидролиз прекурсора с помощью ТФК
(2) конденсация гидролизованных продуктов с PEG
(3) поликонденсация продуктов конденсации в трехмерную кремнийорганическую сетку и химическое закрепление эволюционирующего золь–гелевого полимера на поверхность волокна для создания полимерного покрытия с поверхностным связыванием
Схема 2 . Схема золь–гель синтеза гибридных органокремнеземных покрытий для ТФМЭ на основе PEG.
3.2. Структурно-сорбционные свойства полученных органокремнеземных покрытий PEG/SiO2
Применение термохимических методов, в частности термогравиметрического анализа (рис. 1), при изучении привитого слоя основан на том, что само кварцевое волокно термически устойчиво, поэтому анализ особенностей термического поведения адсорбционного слоя дает возможность делать выводы о степени связывания покрытия с поверхностью волокна и оценить его состав. Кроме того, термическая стабильность адсорбционных покрытий является одним из наиболее критических критериев применимости адсорбционных покрытий для волоконной ТФМЭ.
Рис. 1.
Кривые ТГА (а) и ДТА (б) серий полученных органокремнеземных покрытий PEG/SiO2 для ТФМЭ (обозначения см. табл. 1).

На кривых ТГА полученных покрытий PEG/SiO2 без предварительной термообработки в токе инертного газа при температурах выше 350°С наблюдается резкая потеря массы (рис. 1а) (от 40 до 78%) без ярко выраженных тепловых эффектов (рис. 1б). Вероятнее всего это связано с разрушением алкильных спейсеров органокремнеземных покрытий, высокая термическая устойчивость которых в отсутствии окислителей показана во многих исследованиях [35] и широко используется в хроматографической практике [32], а также с карбонизацией сшивающих фрагментов PEG.
Покрытия PEG/SiO2 практически не потеряли вес в диапазоне температур от 50 до 350°С, другими словами, не удалось зафиксировать какие-либо процессы, связанные с деструкцией органокремнеземного адсорбционного покрытия. Поэтому можно предположить, что алкильные группы на поверхности покрытий PEG/SiO2 в ходе термообработки не отщепляются, а введенный в РС PEG полностью взаимодействует с силанольными группами кремний-органического прекурсора с образованием прочной эфирной сетки, согласно предложенной реакции (Схема 2 ).
Повышенная термическая устойчивость полученного покрытия обусловлена сильными химическими взаимодействиями между PEG и кремнийорганическим прекурсором и большой площадью контакта между покрытием и протравленной поверхностью кварцевого волокна.
Из литературы известно [33], что с увеличением молекулярной массы термическая стабильность PEG уменьшается. Понижение термостабильности покрытия во время синтеза которого использовали PEG со средней молекулярной массой 35 000 г/моль (образец С3, табл. 1) может служить косвенным доказательством наличия не только водородных связей между взаимодействующими молекулами, но и образования ковалентной связи между силаном и PEG за счет химического взаимодействия между ними.
Незначительная потеря массы на ТГ-кривой и отсутствие теплового эффекта на ДТА-кривых для покрытий на основе PEG в среднетемпературном интервале (до 150°С) позволяет сделать вывод, что в этом температурном интервале не наблюдается дегидратация кремнийорганического слоя и в нем практически отсутствует физически связанная вода. Именно поэтому, кривая ТГА образца А3, в РС которого в четыре раза большее содержание Н2О (табл. 1), по сравнению с остальными образцами, имеет примерно 6% потерю массы в диапазоне температур от 30 до 150°С (рис. 1а), что вызвано удалением адсорбированной воды и частичным разложением избытка кислородсодержащей ТФК, которая не прореагировала во время синтеза (табл. 1). Тогда как кривые ТГА остальных покрытий PEG/SiO2 имеют плато в диапазоне между 50 и 350°C.
Таким образом, основной термолиз органического слоя образцов PEG/SiO2 начинается при температурах выше 250°С, что свидетельствует о повышении термивысокой адгезии адсорбцинного покрытия к поверхности кварцевого волокна и удовлетворяет условиям для их безопасного газохроматографического применения.
Поверхность кварцевых волокон после модифицирования у исследованных образцов однородная, немного шероховатая с незначительными дефектами согласно данным электронной микроскопии (рис. 2).
Рис. 2.
Микрофотографии СЭМ полученных гибридных органокремнеземных покрытий для ТФМЭ: a – А3; б – С1; в – В3; г – А2; д –С4; е – А5 (обозначения см. табл. 1).

Как видно из рис. 2а, диаметр волокна составляет примерно 140 мкм, а толщина адсорбционного покрытия – около 4 мкм (рис. 2в). Такая толщина покрытия для ТФМЭ способствует увеличению скорости адсорбции, особенно в случае определения низколетучих и среднелетучих аналитов [8]. Примечательно, что в большинстве исследованных образцов предложенный метод синтеза позволяет формировать алкилсодержащий адсорбционный слой плотно связанный с поверхностью кварцевого волокна (рис. 2).
Введение в РС удвоенного количества кремнийорганического прекурсора, как в случае образца А3 (табл. 1), увеличивает пористость покрытия и приводит к значительной его аморфизации (рис. 2а), что приводит к увеличению площади поверхности покрытия и к возрастанию полноты извлечения аналита, а также и к увеличению скорости установления адсорбционного равновесия на них [17], что особо важно для высоколетучих аналитов. Однако следует отметить в этом случае механическая прочность и срок службы такого покрытия для ТФМЭ снижается, что критично для регулярного применения в лабораторной практике.
Для установления полуколичественного состава полученные покрытия PEG/SiO2 были исследованы методом энергодисперсионного рентгеновского микроанализа (EDX) на примере образца B1. При проведении исследований образцы покрывали слоем золота, поэтому во всех EDX-спектрах полученных покрытий наблюдаются и пики золота, наравне с интенсивными пиками углерода, кислорода, кремния (рис. 3).
Рис. 3.
Микрофотография СЕМ (а) и соотвествующий ей EDX-спектр (б) покрытия PEG/SiO2: образец С4 (Данные микроанализа приведены в ат. %).

Пик средней интенсивности в EDX-спектре покрытия PEG/SiO2 (рис. 3а) соответствует кремнию, входящему в оболочку, которая формировалась при покрытии волокна (Схема 1 ). Действительно (рис. 3б) содержание кремния в образце около 10.30 ат. %, а углерода – 29.04 ат. %, что позволяет сделать вывод, что его содержания связано с закреплением кремнийорганических фрагментов на поверхности волокна для ТФМЭ. Таким образом, учитывая разницу содержания кремния и углерода в оболочке, а также учитывая соотношение кремния и углерода в РС, можно предположить, что они взаимодействуют в соотношении 1 : 3. Кроме того, значительный прирост углерода может быть связан еще и с углеродсодержащими алкильными спейсерами органокремнеземного прекурсора. Подтверждением этому служат результаты полученные методом ИК спектроскопии (рис. 4).
Рис. 4.
ИК-спектры полученных покрытий для волоконной ТФМЭ: C4 (1); С3 (2), A3 (3), B1 (4), B2 (5) (обозначения см. табл. 1).

В ИК-спектре PEG/SiO2 присутствие метиленовых групп проявляется в виде нескольких полос поглощения в области 2850–2960 см–1, которые, несомненно, отвечают νas(С–Н) и νs(С–Н), а наличие полосы при 3430 см–1 относится к колебаниям νs(ОН) связанных гидроксильных групп. В ИК-спектре регистрируется широкая полоса поглощения с максимумом при 3340 см–1, обусловленная νs(ОН) связанных гидроксильных групп. Кроме того, есть полоса поглощения 1647 см–1, которую можно отнести к δ(ОН) в СОН-группах, а также полосы поглощения 1424, 1364, 1335 см–1, принадлежащие к δ(СН) в СН2ОН- и СНОН-группах PEG [34]. Наличие полос при 1030 и 1096 см–1 в образцах PEG/SiO2 и уширенная полоса поглощения при 1120 см–1 для промышленного волоконного материала относятся к колебаниям νs(С–О–С) эфирных груп, подтверждающих химическое взаимодействие между PEG и кремнийорганическим прекурсором. Наличие в ИК-спектрах PEG/SiO2 полос поглощения различной интенсивности в области 1720 см–1, скорее всего обусловлены наличием в органокремнеземных покрытиях функциональных –COО- или С=О-групп. Следовательно, во время золь–гель синтеза часть растворителя (ацетона или ТФК) встраивается в получаемый каркас покрытия для волоконной ТФМЭ. Широкие полосы при 3445 см–1 проявляющиеся в ИК-спектре образцов PEG/SiO2 обусловлены характеристическими νs колебаниями OH-групп, а полосы при 1205, 1074, 961 и 803 см–1 относятся к колебаниям соответствующих силанольных (Si–O–H) и силоксановых (Si–O–Si) групп [35]. В ИК-спектре образцов А3 по сравнению со спектром С4 несколько увеличивается интенсивность полос принадлежащих валентным колебаниям С–Н связи (2850–2960 см–1) и полностью отсутствуют в спектре SiO2. Уширенные полосы поглощения образцов при 3445 см–1свидетельствует о различной степени гидратированности поверхности исследованных адсорбентов. Следует отметить наличие сорбированной воды (δ(ОН) = = 1630 см–1) в поверхностном слое всех изученных покрытий для ТФМЭ.
Таким образом, электростатический механизм закрепления полимерных фрагментов PEG и кремнийорганического прекурсора (Cхема 2) за счет конденсации прогидролизовавших метоксигрупп с концевыми гидроксильными группами PEG обеспечивает наибольшую емкость и прочность каркаса, которая усиливается образованием водородных связей между гидроксильными группами PEG и остаточными силанольными группами полученного адсорбционного покрытия, тогда как избыток PEG, также как и избыток кремнийорганического компонента, является менее эффективными РС для получения покрытий с удовлетворительными механическими и текстурными показателями. На основании полученных результатов предложены оптимальные условия получения органокремнеземных покрытий на основе PEG для ТФМЭ:
| Параметр | Значение |
|---|---|
| Прекурсор | CH3–/C18H37–Si(OMe)3 |
| Молекулярная масса PEG | 15 000 |
| Соотношение PEG : CH3–/C18H37–Si(OMe)3 | 1 : 3 |
| Продолжительность | 1 ч |
| Подготовка поверхности волокна | 1 М раствор NaOH на 1 ч |
| Температура получения | 20°С |
| Рабочий температурный диапазон | до 350°С |
Образцы с однородным механически прочным адсорбционным слоем, содержащим алкильные функциональные группы, на поверхности кварцевого волокна использовали для ТФМЭ ряда парабенов в водной среде.
3.3. Газохроматографическое определение ряда парабенов с помощью полученных органокремнеземных покрытий для волоконной ТФМЭ
При оптимизированных условиях хроматографического определения смеси парабенов аналиты выходят в виде симетричных пиков с временами удерживания 4.57, 5.24, 6.22 мин, соответственно, для метил-, этил- и пропилпарабенов (рис. 5).
pН водного раствора является решающим фактором для всех кислотно-основных аналитов, даже слабых кислот, как в случае парабенов. Для оценки оптимальных условий извлечения парабенов от кислотности среды было проведено изучение адсорбции в интервале рН от 2 до 9, поскольку известно о химической стабильности парабенов в интервале рН 4.5–7.5 [36, 37].
Площади пиков парабенов на хроматограмах незначительно увеличиваются с увеличением рН от 2 до 6.0, достигают постоянного значения при рН 4 и остаются таковыми до рН 6, а затем незначительно уменьшаются (рис. 6а). Возможным объяснением снижения эффективности экстракции при более высоких значениях рН, учитывая константы кислотности парабенов (${\text{p}}{{K}_{{\text{a}}}} = 8.2,$ ${\text{p}}{{K}_{{{{{\text{a}}}_{{{\text{Э П }}}}}}}} = 8.32$ и ${\text{p}}{{K}_{{{{{\text{a}}}_{{{\text{П П }}}}}}}} = 8.4$ [6]), есть то, что при рН ≥ 8 они находятся в ионизированной форме, что подтверждается ранее проведенными исследованиями, например [6], поэтому более эффективное извлечение наблюдается при значениях рН ≤ pKa ≈ 8, когда они находятся в молекулярной форме. С другой стороны, снижение эффективности экстракции при более кислом рН (рН < 3) обусловлено гидролизом эфирной группы парабенов (Схема 1 ). При исспользовании покрытий PEG/SiO2 наиболее полно парабены извлекаются в интервале рН 3–6. аналогичные тенденции наблюдаются и для извлечения парабенов с помощью коммерческого волокна DVB/CAR/PDMS (рис. 5б). Учитывая, что рН исходного рабочего раствора парабенов составляет около 6.0, то для их извлечения из водных растворов нет необходимости в корректировке рН.
Рис. 6.
Зависимость аналитического сигнала от pH среды при определении парабенов с помощью PEG/SiO2 (а) и DVB/CAR/PDMS (б) (С(ЭП, МП, ПП) = 1 мг/л, V = 10 мл, t = 30 мин, C(NaCl) = 100 мг/мл).

Методика определения смеси парабенов ТФМЭ с помощью полученного покрытия PEG/SiO2 при их ГХ/ПИД детектировании была проверена при анализе модельных растворов методом “введено-найдено” (табл. 2).
Таблица 2.
Результаты ГХ-ПИД анализа смеси парабенов методом “введено-найдено” с помощью коммерческого (DVB/CAR/PDMS) и полученного (PEG/SiO2, образец С4) покрытий для ТФМЭ (n = 3, P = 0.95)
| Покрытие | Введено, мг/л | МП | ЭП | ПП | |||
|---|---|---|---|---|---|---|---|
| найдено, мг/л | Sr, % | найдено, мг/л | Sr, % | найдено, мг/л | Sr, % | ||
| DVB/CAR/PDMS | 1.0 | 0.91 ± 0.08 | 3.4 | 0.97 ± 0.01 | 0.7 | 0.98 ± 0.01 | 0.3 |
| PEG/SiO2 | 2.5 | 2.42 ± 0.12 | 2.3 | 2.45 ± 0.02 | 1.8 | 2.43 ± 0.02 | 0.4 |
Полученные результаты (табл. 2) свидетельствуют о перспективности использования полученных гибридных органокремнеземных покрытий для ТФМЭ при извлечении и концентрирования парабенов из водных растворов. относительное стандартное отклонение при этом находится в пределах 0.4–2.3%.
Таким образом, в данной работе методом золь–гель синтеза были получены органокремнеземные покрытия на основе PEG для ТФМЭ с высокой степенью упорядоченности и различным содержанием алкиламинных функциональных групп на поверхности волокна, а также исследованы их структурно-сорбционные и термические характеристики. Термическая устойчивость полученных покрытий обусловлена сильными химическими взаимодействиями между PEG и кремнийорганического прекурсора и сильной адгезией между покрытием и протравленной поверхностью кварцевого волокна. Экспериментальные результаты показали, что органокремнеземные адсорбционные покрытия для ТФМЭ обладают хорошей химической и термической стабильностью, высокими адгезивными свойствами и отличными экстракционными свойствами для концентрирования парабенов в сочетании с высокой селективностью газовой хроматографии. Показано, что предложенная методика ТФМЭ при использовании синтезированного PEG/SiO2 покрытия может быть альтернативой использования существующих промышленных покрытий для извлечения парабенов из водных растворов. Разработанные методики ТФМЭ для МП, ЭП, ПП для водных образцов с последующим их ГХ-ПИД определением характеризуются достаточной правильностью и воспроизводимостью (Sr до 2.3%). Полученные результаты свидетельствуют о существенном влиянии состава реакционной смеси на сорбционные свойства получаемых покрытий и в дальнейшем позволят целенаправленно синтезировать новые органокремнеземные покрытия на основе PEG для ТФМЭ.
Список литературы
Soni M.G., Taylor S.L., Greenberg N.A., Burdock G.A. // Food Chem. Toxicol. 2002. V. 40. P. 1335–1373.
Soni M.G., Carabin I.G., Burdock G.A. // Food Chem. Toxicol. 2005. V. 43. P. 985–1015.
Elder R.L. // Int. J. Toxicol. 2008. 27 Suppl 4. P. 1–82.
http://ec.europa.eu/health/scientific_committees/consumer_safety/docs/sccs_o_132.pdf.
Frederiksen H., Jorgensen N., Andersson A-M. // J. Expos. Sci. Environ. Epidemiol. 2011. V. 21. P. 262–333.
Farajzadeh M.A., Djozan D.J., Bakhtiyari R.F. // Talanta. 2010. V. 81. P. 1360–1367.
Lokhnauth J.K., Snow N.H. // Anal. Chem. 2005. V. 77. P. 5938–5946.
Зайцев В.Н., Зуй М.Ф. // Журн. анал. химии. 2014. Т. 69. № 8. С. 787–800.
https://www.sigmaaldrich.com/technical-documents/ articles/analytical/selecting-spme-fibers.html.
Zhang Zh., Zhu L., Ma Yu., Huang Y., Li G. // Analyst. 2013. V. 138. P. 1156–1166.
Li Y., Wang Y., Zhang J., Sun C. // Environ. Monit. Assess. 2012. V. 184. P. 4345–4353.
Wong M.Y., Cheng W.R., Liu M.H., Tian W.C. et al. // Talanta. 2012. V. 101. P. 307–313.
Li Z., Ma R., Bai Sh., Wang Ch., Wang Z. // Talanta. 2014. V. 119. P. 498–504.
Wang T., Chen Y., Ma J., Hu M. et al. // Anal. Bioanal. Chem. 2014. V. 406. № 20. P. 4955–4963.
Lopez-Darias J., Anderson J.L., Pino V., Afonso A.M. Anal. Bioanal. Chem. 2011. V. 401. P. 2965–2976.
He J., Chen Si, Jiang Y., Shen Y., Zhu J., Wei H., Zhang H., Lu K. // J. Sep. Sci. 2012. V. 35. P. 308–314.
Walles M., Mullett W.M., Pawliszyn J. // J. Chrom. A. 2004. V. 1025. P. 85.
Chong S.L., Wang D., Hayes J.D., Wilhite B.W. et al. // Anal. Chem. 1997. V. 69. P. 3889.
Kumar A., Gaurav Malik A.K., Tewary D.K., Singh B. // Anal. Chim. Acta. 2008. V. 610. P. 1–14.
Piri-Moghadam H., Nazmul A.M.D., Pawliszyn J. // Anal. Chim. Acta. 2017. V. 984. P. 42–65.
Barczak M., Mcdonagh C., Wencel D. // Microchim. Acta. 2016. V. 183. № 7. Р. 2085–2109.
Sarafraz-yazdi A., Piri-Moghadam H., Es’haghi Z., Sepehr S. // Anal. Methods. 2010. V. 2. P. 746–752.
Yu J., Dong L., Wu C., Wu L., Xing J. // J. Chrom. A. 2002. V. 978. P. 37–48.
Pragst F. // Anal Bioanal Chem. 2007. V. 388. P. 1393–1414.
Ghader M., Shokoufi N., Es-haghi A., Kargosha K. // Anal. Bioanal. Chem. V. 409. № 29. P. 6739–6744.
Lopez-Darias J., Pino, V., Meng Y., Anderson J.L. et al. // J. Chrom. A. V. 1217. № 46. P. 7189–7197.
Diaz-Alvarez M., Smith S.P., Spivak D.A., Martin-Esteban A. // J. Separate. Sci. 2016. V. 39. № 3. P. 552–558.
Liu D., Song N., Cheng Y., Chen D. et al. // RSC Adv. 2014. V. 4. P. 49153–49160.
Chen Y., Sidisky L.M. // Anal. Chim. Acta. 2012. V. 743. P. 61–68.
Wu M., Zhang H., Zeng B., Zhao F. // J. Chrom. A. 2015. V. 1384. P. 22–27.
Es-haghi A., Hosseininasa V., Bagheri H. // Anal. Chim. Acta. 2014. V. 813. P. 48–55.
High Performance Liquid Chromatography in Pesticide Residue Analysis. Edited by Tuzimski T., Sherma J. CRC Press, Taylor & Francis Group. 2015. P. 582.
Bagheri H., Piri-moghadam H., Ahdi T. // Anal. Chim. Acta. 2012. V. 742. P. 45–53.
Infrared and Raman Characteristic Group Frequencies: Tables and Charts. 3rd ed By G. Socrates (The University of West London, Middlesex, U.K.). J. Wiley and Sons: Chichester. 2001. 348 p.
Лисичкин Г.В., Фадеев А.Ю., Сердан А.А., Нестеренко П.Н. Химия привитых поверхностных соединений. Под редакцией докт. хим. наук Г.В. Лисичкина. Москва: Физматлит. 2003. 592 с.
Blaug S.M., Grant D.E. // J. Soc. Cosm. Chemist. 1974. V. 25. № 9. P. 495–506.
Alexander K.S., Laprade B., Mauger J.W., Paruta A.N. // J. Pharm. Sci. 1978. V. 67. № 5. P. 624–627.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов