Физикохимия поверхности и защита материалов, 2019, T. 55, № 4, стр. 368-379
Электрохимические и структурные исследования наноалмазных композитов
В. Е. Сосенкин 1, А. Е. Алексенко 1, А. Ю. Рычагов 1, Н. А. Майорова 1, **, М. А. Овчинников-Лазарев 1, Б. В. Спицын 1, Ю. М. Вольфкович 1, *
1 Институт физической химии и электрохимии им. А.Н. Фрумкина РАН
119071 Москва, Ленинский пр., 31, Россия
** E-mail: maynat54@mail.ru
* E-mail: yuvolf40@mail.ru
Поступила в редакцию 13.12.2018
После доработки 03.02.2019
Принята к публикации 07.02.2019
Аннотация
Методом детонационного синтеза получены наноалмазные композиты (НАК) и проведены электрохимические и порометрические исследования нескольких образцов НАК, содержащих как фракцию наноалмазного порошка, так и фракцию неалмазного углерода. Исследованы образцы необработанной детонационной шихты (НАК-1) и продуктов ее газофазной очистки (НАК-2 и НАК-3), отличающиеся соотношением наноалмаза и неалмазного углерода. Содержание последнего в образцах НАК-1, НАК-2 и НАК-3 составляло 48, 24 и 1 мас. % соответственно. Показано, что интенсивность КР-полос кристаллического графита (1580 см–1) и разупорядоченной графитовой фазы (1360 см–1) выше в исходной детонационной шихте в сравнении с образцами, частично или практически полностью очищенными от неалмазного углерода. При этом удельное сопротивление образцов возрастает в ряду НАК-1 < НАК-2 < НАК-3, т.е. по мере увеличения доли фракции наноалмаза. Методом эталонной контактной порометрии установлено, что образцы обладают высокими величинами как полной удельной (1040–1290 м2 г–1), так и гидрофильной удельной поверхности, и что с увеличением концентрации наноалмаза уменьшается степень гидрофильности НАК. ЦВА кривые для образцов НАК имеют вид, характерный для заряжения двойного электрического слоя, но осложненный омическими потерями, возрастающими с увеличением доли наноалмаза. Борирование наноалмаза приводит к снижению его удельного сопротивления и к значительной гидрофилизации. Данные импедансометрии образцов НАК-1 и НАК-2 показывают, что снижение доли электропроводного углерода сопровождается существенным уменьшением емкости. Исследование электровосстановления кислорода на каталитической системе Pt/НАК-1 продемонстрировало ее устойчивость во времени, что, вероятно, обусловлено снижением степени агрегирования частиц платины вследствие меньшей скорости коррозии носителя из наноалмазного порошка по сравнению со стандартными сажами. Таким образом, некоторые из исследованных образцов НАК перспективны в качестве носителя катализатора восстановления кислорода.
ВВЕДЕНИЕ
Среди нанодисперсных углеродных материалов особое место занимают продукты детонационного синтеза, получаемые в результате масштабного производства детонационного наноалмаза (ДНА). Первые успешные работы по синтезу ДНА были выполнены в СССР в 1963 г. [1], но широкое исследование закономерностей синтеза, особенностей структуры и свойств порошков наноалмаза, а также их практическое применение были развернуты только в последние два десятилетия. Исходным строительным материалом в процессе синтеза наноалмаза является углерод, входящий в состав молекул взрывчатых веществ (ВВ). При выборе ВВ критическими являются мощность в тротиловом эквиваленте, скорость детонации и кислородный баланс (кислорододефицитность). Две первые характеристики определяют физические условия протекания синтеза алмаза во взрывной камере – давление и температуру. Под кислородным балансом понимается избыток или недостаток кислорода в веществе заряда, необходимый для полного окисления элементов, входящих в состав ВВ (С, Н и др.). Процесс детонационного синтеза наноалмазов во взрывной камере возможен только при использовании ВВ с отрицательным кислородным балансом, при этом остается неокисленным определенное количество свободного углерода, преобразуемого в ДНА. Синтез кристаллов детонационного наноалмаза обычно осуществляют путем взрыва смеси мощных кислород-дефицитных ВВ (тринитротолуол, гексоген) в условиях термодинамической стабильности алмаза (~25 ГПа, ~3000 K), длящейся на фронте детонационной волны ~1 мкс [2]. Детонационный синтез наноалмаза относится к высокопроизводительным методам получения углеродных нанокристаллических материалов, при этом, согласно данным рентгенофазового анализа, первоначальный продукт детонации смеси тринитротолуола и гексогена – детонационная шихта – содержит не менее 50% нанодисперсного алмаза с довольно узким распределением по размерам его кристаллов – от 2 до 10 нм.
Однако детонационная шихта не является фазово- и химически чистым наноматериалом, и этим обусловлена необходимость ее очистки от примесей [3]. В частности, перед практическим использованием ДНА [2] требуется удаление из нее неалмазного углерода. Промышленный способ очистки включает в себя взаимодействие с жидкой 60% азотной кислотой, перегретой до 260°С при давлении в 90 атм, обеспечивающее окисление неалмазного углерода и перевод металлических примесей в растворимые нитраты, с последующей многократной промывкой и центрифугированием. Недостатком жидкофазного метода очистки является загрязнение поверхности ДНА солевыми группами. Кроме того, при промывке водой происходит потеря наиболее мелкой фракции ДНА и образуется значительный объем жидких отходов.
Исследованиям свойств собственно алмаза посвящено большое число работ. Так, в [4, 5] были изучены его электрохимические, а в работе [6] – фотоэлектрохимические и полупроводниковые свойства. Обладающий высокой механической стойкостью, ДНА при дополнительной обработке открывает ряд возможностей в инновационных разработках топливных элементов. Как известно, существенной проблемой низкотемпературных, в частности, водород – кислородных топливных элементов является окисление (коррозия) стандартных углеродных носителей платинового катализатора (обычно в качестве таких носителей используют различные сажи, например Vulcan ХС-72) при потенциалах кислородного электрода [7]. Помимо того, что один из продуктов этой коррозии – СО – является каталитическим ядом, в результате деструкции носителя уменьшается площадь контакта между подложкой и нанесенным металлом, что приводит к десорбции наночастиц платины с носителя и уменьшению площади электрохимически активной поверхности. Кроме того, при этих потенциалах на поверхности углерода могут образовываться различные кислородсодержащие группы, что повышает сопротивление межфазной области катализатора и ослабляет взаимодействие между носителем и частицами металла, приводя к коалесценции (спеканию) последних, увеличивает гидрофильность каталитического и газодиффузионного слоев, вызывая в итоге затопление пор. За счет уменьшения толщины слоя катализатора в результате деструкции углерода увеличивается сопротивление электрода и ухудшается его контакт с токоприемником [7–10]. Введение различными методами (магнетронное напыление, гальваническое осаждение) наночастиц платиновых металлов в полупроводниковую алмазную матрицу [11] может способствовать решению этих проблем. Так, в работе [12] было установлено преимущество в стойкости к окислению у ДНА с частично графитизированной поверхностью и размером кристаллитов в единицы нм, в сравнении с традиционно используемой в ТЭ сажей типа Vulсan XC-72, а более крупные (в десятки нм) частицы алмаза обнаружили высокую стойкость к окислению при их покрытии нанокристаллитами Pt–Ru катализатора [13]. Особые возможности, при условии его производства и освоения, может обеспечить алмаз с собственной электропроводностью, получаемый легированием бором [14]. В этом случае, в отличие от обычно используемых пористых углеродных материалов, у электропроводного алмаза в электрохимических процессах будет участвовать, главным образом, более доступная внешняя поверхность. В нашем распоряжении была возможность регулировать электропроводность образцов с ДНА за счет изменения в их составе содержания неалмазного углерода. Для этого использовали альтернативный способ газофазной очистки детонационной шихты: окисление неалмазной фракции путем взаимодействия с парами концентрированной азотной кислоты при 280–350°С и 1 атм [3].
Настоящая работа была поставлена в связи c предположением, что, вследствие его кристаллической структуры, скорость окисления (коррозии) порошка наноалмаза должна быть значительно меньше, чем скорость окисления аморфных по структуре саж. Хотя у наноалмаза есть и существенный недостаток с точки зрения электрохимических применений, а именно, высокое электрическое сопротивление, в данной поисковой работе мы провели электрохимические и порометрические исследования нескольких порошков, содержащих как частицы наноалмаза, так и частицы с переходными свойствами от наноалмаза к другим формам углерода. Все эти образцы, по существу, являются наноалмазными композитами (НАК), отличающимися соотношением фракций наноалмазного порошка и неалмазного углерода. Кроме того, в работе были исследованы их емкостные и импедансные свойства.
МАТЕРИАЛЫ
Были исследованы образцы как необработанной детонационной шихты (НАК-1), так и продуктов ее газофазной очистки посредством последовательного окисления неалмазной фракции (НАК-2 и НАК-3), отличающиеся соотношением наноалмаза и неалмазного углерода. Содержание последнего, определяемого по убыли массы шихты в процессе ее очистки, в образцах НАК-1, НАК-2 и НАК-3 составило 48, 24 и 1 мас. % соответственно.
Получение борированного наноалмаза
Известно, что при введении в алмаз бора его проводимость существенно возрастает [15], поэтому была предпринята попытка введения примесного бора в образец ДНА, очищенный от неалмазного углерода (НАК-3), путем диффузионного насыщения. Для этого порошок ДНА смешивали с порошком аморфного бора дисперсностью 325 меш (размер частиц до 10 мкм) в соотношении 10 : 1. После тщательного перемешивания эту смесь прогревали в атмосфере водорода (0.5 атм) при 850°С в течение 2 ч. Непрореагировавший бор не отделяли. Отожженный порошкообразный образец приобретал электропроводность. В данной работе такой образец обозначен как НАК-4.
Поскольку исследование образцов было проведено с привлечением разных методов, условия и методика экспериментов в каждом случае приведены в начале соответствующего подраздела.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Исследование образцов методом измерения спектров комбинационного рассеяния
В рамках настоящей работы представляло интерес исследовать полученные образцы с регулируемым содержанием неалмазной фазы как электрохимическими, так и иными методами. Содержание неалмазной фазы контролировали гравиметрически, а именно, по убыли массы детонационной шихты в процессе ее селективного окисления посредством взвешивании на аналитических весах ВЛА-200 г-М. Спектры комбинационного рассеяния получали на Раман-спектрометре Senterra на ионах аргона при длине волны 532 нм, при низком уровне возбуждающего лазерного излучения.
Было показано, что интенсивность КР полос кристаллического графита (1580 см–1) и разупорядоченной графитовой фазы (1360 см–1) повышена в исходной детонационной шихте (рис. 1а) по сравнению с образцами, частично или практически полностью очищенными от неалмазного углерода. Определение в образцах соотношения sp3 (алмазного) и sp2 (высокодисперсного неалмазного и графитового) углерода во всем интервале соотношений алмазная-неалмазная фаза по спектрам комбинационного рассеяния было сопряжено с существенными затруднениями. Эти затруднения обусловлены значительным отличием интенсивности Раман-рассеяния от sp3 и sp2 углерода. Так, при длине волны возбуждающего излучения 532 нм интенсивность рассеяния для sp3 углерода в 90 раз меньше, чем соответствующая интенсивность для sp2 углерода [16]. Поэтому ‘алмазная’ полоса (частота ~1332 см–1) может быть зарегистрирована в КР спектрах только при малом (единицы %) содержании неокристаллизованного углерода (частота ~1580 см–1). КР спектр для образца с наименьшим содержанием неалмазного углерода (~1%) представлен на рис. 1б. Сдвиг алмазного пика в сторону несколько меньших частот может быть обусловлен так называемым эффектом конфайнмента от высокодисперсных кристаллов [32].
Порометрические исследования образцов наноалмазов
Для исследования пористой структуры вышеописанных порошков, содержащих частицы наноалмаза, был использован метод эталонной контактной порометрии (МЭКП) [17–19], который позволяет исследовать пористую структуру порошковых и компактных материалов в максимально широком диапазоне радиусов пор – от 1 до 105 нм, т.е. в интервале 5 порядков величины. Кроме того, МЭКП, в отличие от других порометрических методов, позволяет также исследовать гидрофильно-гидрофобные свойства образцов. Это очень важно, в частности, для углеродных материалов, к которым относятся и наноалмазы. Данный метод был признан IUPAC как корректный метод исследования пористых структур [20]. В качестве измерительных жидкостей в работе были использованы октан и вода. Октан практически идеально смачивает любые материалы (угол смачивания θ ~ 0°), а воду использовали для исследования гидрофильно-гидрофобных свойств образцов.
Как было показано в [17, 18], МЭКП позволяет определять контактный угол смачивания непосредственно в порах путем использования различных измерительных жидкостей. Для этой цели измеряется распределение объема пор по величинам их эффективного радиуса r* = r/cos θ, (где θ – угол смачивания) с использованием октана и какой-либо другой жидкости, чаще всего воды. Для материалов, плохо смачиваемых водой, θ > 0°, и порометрическая кривая, измеренная по воде, сдвинута в сторону больших величин r* по сравнению с соответствующей кривой, измеренной по октану, который смачивает материалы, в том числе углеродные, с величиной θ ~ 0°. На основании этого для данного объема пор vi и соответствующего радиуса пор ri, определяется контактный угол смачивания по формуле: cos θ = = r/r*, откуда θ = arccos r/r*.
На рис. 2 приведены интегральные (а–г) и дифференциальные (д–е) кривые распределения пор по величинам r*, измеренные для образцов НАК-1, НАК-2, НАК-3 и НАК-4 с использованием октана (кривые 1) и воды (кривые 2). Согласно вышеизложенному, порограммы 1 являются истинными, а порограммы 2 необходимы для расчета зависимостей θ от r, представленных на рис. 3. Поскольку измерения МЭКП осуществлялись в очень широком интервале радиусов пор (5 порядков), то по осям абсцисс на рисунках отложены величины lg r* и lg r.
Рис. 2.
Интегральные (а–г) и дифференциальные (д–з) кривые распределения пор по радиусам, измеренные октаном (1) и водой (2) для образцов: НАК-1 (а, д), НАК-2 (б, е), НАК-3 (в, ж), НАК-4 (г, з).

Рис. 3.
Зависимость угла смачивания водой от радиуса пор для образцов: (1) НАК-1; (2) НАК-2; (3) НАК-3; (4) НАК-4.

Из приведенных рисунков можно сделать следующие выводы:
1. На дифференциальных порограммах всех образцов в первом приближении выделяется максимум в области мезопор с lg r от 0 до 1, а также максимумы в области макропор с lg r от 3 до 5.
2. Интегральные порограммы всех образцов показывают наличие микропор с lg r < 0. В величины удельной поверхности вносят вклад как микропоры, так и мезопоры, и практически не вносят вклад макропоры.
3. Можно предположить, что микропоры и мезопоры расположены внутри частиц порошков, а макропоры – между этими частицами.
4. Макропоры являются практически гидрофобными с θ > 90°; мезопоры и микропоры обладают гидрофильно-гидрофобными свойствами с величинами θ от 0° до 90°, что хорошо видно из рис. 3. Известно, что гидрофильность углеродных материалов обусловлена наличием в них кислородсодержащих поверхностных групп (ПГ).
5. Очень сложный характер зависимостей θ от lg r обусловлен сложностью характера распределения ПГ между порами различных размеров.
6. Из рис. 3 видно, что по мере увеличения концентрации наноалмаза в образцах НАК-1, НАК-2 и НАК-3 уменьшается их гидрофильность.
В табл. 1 приведены основные характеристики пористой структуры и гидрофильно-гидрофобных свойств исследованных образцов, полученные из порометрических кривых и рассчитанные согласно [17–19].
Таблица 1.
Сводная таблица характеристик пористой структуры и гидрофильно-гидрофобных свойств образцов, где: ${{\text{v}}_{{{\text{phil}}}}}$ – гидрофильная пористость, ${{\text{v}}_{{{\text{phob}}}}}$ – гидрофобная пористость, ${{\text{v}}_{\Sigma }}$ – полная пористость, ${{v}_{{{\text{phil}}}}}$/${{v}_{\Sigma }}$ – объемная доля гидрофильных пор, Sphil – гидрофильная удельная поверхность, SΣ – полная удельная поверхность, Sphil/SΣ – доля поверхности гидрофильных пор, θav – средний угол смачивания гидрофильных пор водой
| Образец | ${{\text{v}}_{\Sigma }},$ см3 г–1 | ${{\text{v}}_{{{\text{phil}}}}},$ см3 г–1 | ${{\text{v}}_{{{\text{phob}}}}},$ см3 г–1 | ${{\text{v}}_{{{\text{phil}}}}}$/${{\text{v}}_{\Sigma }}$ | SΣ, м2 г–1 | Sphil, м2 г–1 | Sphil/SΣ | θav, град |
|---|---|---|---|---|---|---|---|---|
| НАК-1 | 2.88 | 0.97 | 1.91 | 0.336 | 1290 | 1060 | 0.82 | 45.0 |
| НАК-2 | 3.03 | 2.17 | 0.86 | 0.716 | 1223 | 1094 | 0.89 | 55.9 |
| НАК-3 | 2.79 | 1.88 | 0.91 | 0.674 | 1041 | 739 | 0.71 | 62.9 |
| НАК-4 | 1.48 | 1.35 | 0.13 | 0.91 | 520 | 400 | 0.77 | 48.4 |
Из приведенной табл. 1 и рис. 2, 3 можно сделать следующие основные выводы:
1. Все не модифицированные бором образцы (НАК-1, НАК-2 и НАК-3) обладают довольно высокими величинами как полной удельной поверхности (1041–1291 м2 г–1), так и гидрофильной удельной поверхности (739–1094 м2 г–1), что, в целом, благоприятно с точки зрения электрохимических применений.
2. Образец НАК-3 с наиболее высокой концентрацией наноалмаза характеризуется наименьшим соотношением Sphil/SΣ.
3. При переходе от образца НАК-1 к образцу НАК-3, т.е. с увеличением концентрации наноалмаза, увеличивается и значение среднего угла смачивания водой θav.
4. Из выводов 2 и 3 следует, что по мере увеличения в композите концентрации наноалмаза уменьшается его гидрофильность, что объясняется гидрофобностью поверхности алмаза.
5. Модифицирование наноалмаза бором (образец НАК-4) приводит к следующим последствиям: а) значительно уменьшается удельная поверхность (до 520 м2 г–1), вероятно, вследствие спекания при его получении (отжиг при высокой температуре); б) происходит существенная гидрофилизация, которая проявляется в уменьшении ${{v}_{{{\text{phob}}}}},$ увеличении ${{v}_{{{\text{phil}}}}}$/${{v}_{\Sigma }}$ и в уменьшении θav, по сравнению с другими образцами.
6. Из дифференциальных порограмм (рис. 2д–2з) видно, что для всех образцов, включая борированный, положение основного максимума практически одинаково – при радиусе пор 3.6 нм. Следовательно, этот максимум характеризует структурные свойства фракции наноалмаза.
7. Из рис. 3 видно, что для неборированных образцов НАК-1, НАК-2 и НАК-3 зависимости θ от r имеют минимум в интервале lg r от 0.7 до 1.6. Более крупные поры практически гидрофобны, что свойственно многим углеродным материалам [17, 18], в том числе неалмазной фракции всех образцов, при этом максимум θ в области мелких пор характеризует свойства фракции наноалмаза, что следует из вывода 6.
8. Форма зависимости θ от r для борированного образца (рис. 3, кривая 4) качественно отличается от соответствующих зависимостей для других образцов появлением третьего максимума в области средних размеров пор. Из этого же рисунка следует, что происходит борирование и неалмазной фракции НАК.
Измерение электрического сопротивления образцов наноалмаза
Измерения сопротивления образцов проводили по двухэлектродной схеме в цилиндрической тефлоновой ячейке с диаметром поршня 6 мм. В качестве контактных электродов использовали стержни из нержавеющей стали с предварительной полировкой области контакта стали с измеряемым материалом. В процессе измерения определяли массу порошка, вносимого в ячейку, и толщину его слоя, находившегося под давлением 15 кг см–2. Измерения проводили методом циклической вольтамперометрии при скоростях развертки потенциала 10 и 100 мВ с–1 в интервале напряжений от 0.1 до 4 В. С целью снижения эффектов, связанных с уплотнением порошка во времени, измерения проводили с интервалом в 1 ч до получения надежной воспроизводимости данных. Температура образцов при измерениях составляла 25°С. В табл. 2 приведены полученные величины удельного сопротивления для исследованных образцов.
Таблица 2.
Величины удельного сопротивления для исследованных образцов
| Образец | Масса, мг | Толщина, мм | Плотность, г см–3 | Сопротивление, Ом см |
|---|---|---|---|---|
| НАК-1 | 31.0 | 2.0 | 0.55 | 2 |
| НАК-2 | 15.2 | 0.5 | 1.08 | 40 × 106 |
| НАК-3 | 16.0 | 0.5 | 1.13 | 90 × 106 |
| НАК-4 | 61.0 | 2.2 | 0.98 | 17 × 106 |
Из таблицы можно сделать следующие выводы: 1) удельное сопротивление возрастает в ряду: НАК-1 < НАК-2 < НАК-3, соответственно последовательному увеличению в композите доли наноалмаза; резкое возрастание сопротивления при переходе от образца НАК-1 к образцу НАК-2 можно объяснить в рамках перколяционной модели (так называемый перколяционный скачок [21]), а также тем, что окисленные частицы углерода (образуются в процессе газофазной очистки исходной детонационной шихты при получении НАК-2 и НАК-3) являются менее электропроводными по сравнению с неокисленными (НАК-1). 2) удельное сопротивление образца НАК-4 существенно меньше, чем у соответствующего по содержанию неалмазной фракции образца НАК-3, что согласуется с литературными данными по влиянию борирования на свойства наноалмазов [14, 15].
Исследование емкостных и импедансных свойств наноалмазных композитов
Электрохимическое исследование порошков наноалмаза проводили по двухэлектродной схеме в универсальной лабораторной ячейке конденсаторного типа [22]. Рабочий электрод изготавливали методом вакуумного нафильтровывания порошка композита на пористую полипропиленовую пленку. Противоэлектрод изготавливали из высокоемкой активированной углеродной ткани (СН-900, Kuraray Co., Япония), масса которой в 50–100 раз превышала массу рабочего электрода. В этих условиях вспомогательный электрод является практически неполяризуемым и выполняет роль электрода сравнения с потенциалом, равным стационарному потенциалу активированной углеродной ткани (~600 мВ относительно обратимого водородного электрода сравнения). Электролитом являлся водный раствор KBr концентрацией 2 моль л–1. Данный электролит был выбран в качестве эталонного, поскольку обладает рядом преимуществ: широкой двойнослойной областью при отсутствии специфической адсорбции ионов, обратимой псевдоемкостной реакцией в области термодинамической устойчивости воды, низким саморазрядом и нейтральной кислотностью. Рабочий и вспомогательный электроды разделялись сепаратором из пористого полипропилена толщиной 150 мкм. На рис. 4 (см. ниже) емкостные данные, полученные из циклических вольтамперограмм (ЦВА), представлены в виде вольтфарадных кривых (получены делением величины тока на скорость развертки потенциала). Такие кривые являются простой и наглядной формой масштабирования ЦВА, построенных в координатах дифференциальная емкость (С) – потенциал (E), где: С = dQ/dЕ = Idτ/dE = I/w, I – ток, Q – количество электричества, w – скорость развертки потенциала, τ – время.
Рис. 4.
Циклические вольтфарадные кривые для образцов НАК-1 (а, б) и НАК-2 (б), измеренные относительно углеродного электрода сравнения при скоростях развертки потенциала (мВ с–1): 2 (а, б); 10 (а).

Электрохимические свойства нанесенных пленок НАК исследовали методами циклической вольтамперометрии и импедансометрии с использованием потенциостата-гальваностата Elins P-30J(M) (Россия) и импедансметра Solartron 1255 (Великобритания).
На рис. 4а приведены циклические вольтфарадные кривые для образца НАК-1. Как видно из встроенного рисунка, ЦВА кривые в интервале от –300 до +100 мВ представляют собой практически идеальный прямоугольник, характерный для заряжения двойного электрического слоя (ДЭС), не осложненного другими процессами [22, 23]. C другой стороны, известно, что для активированных углей вследствие вклада в суммарную емкость псевдоемкости редокс-реакций поверхностных групп (наличие последних показано в работе [24]) на этот прямоугольник накладываются максимумы [25]. Следовательно, можно предположить малую концентрацию поверхностных групп у наноалмазного композита, что отличает его от активированных углей. Из рис. 4 видно, что для образца НАК-1 удельная емкость в двойнослойной области потенциалов составила ~30 Ф г–1. Учитывая, что, согласно данным табл. 1, удельная гидрофильная поверхность для этого образца равна 1060 м2 г–1, то удельная емкость на единицу истинной гидрофильной поверхности составляет 2.8 мкФ см–2. Это в несколько раз меньше соответствующей величины для других высокодисперсных углеродных материалов [22], что указывает на низкую электросорбцию ионов в случае наноалмазного композита. Максимальная величина обращаемого количества электричества (около 180 Кл г–1) для этого образца наблюдалась в области окисления бромид-ионов до брома. Снижение доли электропроводного углерода, как следует из рис. 4б, приводит к резкому уменьшению емкости НАК.
Данные импедансометрии образца НАК-1 (рис. 5) показывают, что переход от двойнослойной к псевдоемкостной области потенциалов приводит к резкому росту обратимой емкости при незначительном снижении поляризационного сопротивления. Анализ спектров импеданса свидетельствует о высокой обратимости псевдоемкости соединений брома.
Оценка возможности использования наноалмазных композитов в качестве носителей катализатора для кислородного электрода топливного элемента
Исследование образцов проводили при комнатной температуре путем снятия ЦВА в диапазоне потенциалов 0.0–1.4 В со скоростями развертки от 2 до 200 мВ с–1 в растворе 0.5 М H2SO4, продутом аргоном. В качестве вспомогательного электрода использовали платиновую сетку (S ~ 10 cм2), а в качестве электрода сравнения – ртутно-сульфатный электрод (потенциалы на рис. 6–9 приведены относительно обратимого водородного электрода). Рабочим электродом служил вращающийся дисковый электрод из стеклоуглерода (СУ) диаметром 3 мм, на поверхность которого помещали исследуемый образец по нижеследующей методике.
Рис. 6.
Разностные ЦВА, полученные при скорости развертки потенциала 200 мВ с–1, для образцов: (1) НАК-1, (2) НАК-2, (3) НАК-3 и (4) НАК-4.

Рис. 7.
ЦВА для платинированных образцов наноалмазных композитов: (1) Pt/НАК-1; (2) Pt/НАК-2; (3) Pt/НАК-3; (4) Pt/НАК-4, измеренные в 0.5 М H2SO4 со скоростью развертки 50 мВ с–1. Число циклов адсорбции/восстановления (см. методику осаждения платины): 5 (1); 10 (2); 15 (3, 4).

Рис. 8.
Циклические вольтамперограммы восстановления кислорода, измеренные в растворе 0.5 М H2SO4, насыщенном кислородом при атмосферном давлении, при скорости вращения электрода 2700 об. мин–1: (а) на приготовленных образцах Pt/НАК-1 (1, 1'), Pt/НАК-2 (2), Pt/НАК-3 (3), Pt/НАК-4 (4); (б) на том же образце Pt/НАК-1 (1'–4') в течение 3-х недель после осаждения платины (электрод между измерениями хранили на воздухе).
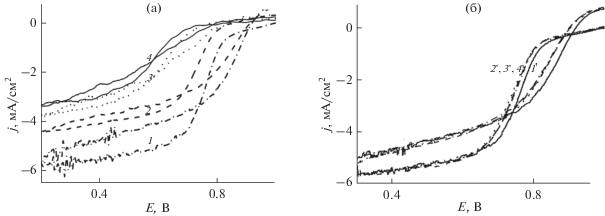
Рис. 9.
Сравнение вольтамперограмм восстановления кислорода на платине, нанесенной на Vulcan ХС-72 (1) и на образец НАК-1 (2), измеренных в растворе 0.5 М H2SO4, насыщенном кислородом при атмосферном давлении, при скорости вращения электрода 1600 об./мин.

Из каждого образца была приготовлена водная суспензия (2 мг/1 мл). Поскольку суспензия образца НАК-3 оказалась очень неустойчивой (быстро расслаивалась), в нее был добавлен Nafion (5%, Aldrich) в количестве 15 мас. %. Аликвоту суспензии образца, предварительно подвергнутой ультразвуковой обработке, с помощью микропипетки наносили на поверхность СУ и высушивали на воздухе. Масса каждого образца на электроде составляла 70 мкг см–2. Для закрепления на поверхности СУ пленок образцов НАК-1, НАК-2 и НАК-4 на них наносили тонкий слой водного раствора Nafion и также высушивали. Поскольку суспензия образца НАК-3 исходно содержала Nafion, то нанесения дополнительного слоя последнего не требовалось. ЦВА в указанном выше интервале потенциалов измеряли с разными скоростями развертки как до нанесения на электрод пленки образца, так и после этого. Затем путем математического вычитания кривой для СУ из кривой для СУ с пленкой образца получали вольтамперные зависимости, отражающие вклад непосредственно пленки образца. Для иллюстрации на рис. 6 показаны такие зависимости, полученные при одной из скоростей развертки потенциала.
Как видно из рис. 6, площадь между катодной и анодной ветвями разностной кривой последовательно уменьшается при переходе от образца НАК-1 к образцам НАК-3 и НАК-4, в соответствии с ростом концентрации наноалмаза в композите. Отсюда следует, что регистрируемые ЦВА процессы, по-видимому, протекают в основном на неалмазном углероде. Кроме того, если полученные зависимости для образца НАК-1 в первом приближении имеют вид прямоугольника, как и для других углеродных материалов, на которых протекают процессы заряжения – разряжения ДЭС [18], то для образцов НАК-2 и НАК-3 они существенно наклонены к оси абсцисс, что свидетельствует о влиянии роста электрического сопротивления наноалмазных композитов вследствие увеличения доли наноалмаза. Количественно это сопротивление можно оценить как R = ∆Е/∆i, где ∆Е – интервал потенциалов, а ∆i – величина сдвига тока, соответствующая интервалу потенциалов. Сделанные из рис. 6 по этой формуле оценки дают величину R ~ 1.0 × × 103 Ом см–2 для НАК-2 и R ~ 2.25 × 103 Ом см–2 для НАК-3. Отсюда следует, что сопротивление образца НАК-3 в 2.25 раза больше, чем НАК-2, что хорошо согласуется с данными прямого измерения сопротивления этих образцов, представленными в табл. 2. Характер зависимостей, полученных для борированного образца НАК-4, можно объяснить протеканием фарадеевских процессов с относительно небольшой емкостью, обусловленных, вероятно, наличием поверхностных групп.
Для исследования возможности использования образцов в качестве носителя катализаторов на них химическим способом осаждали платину. Методика осаждения заключалась в попеременном выдерживании электрода с пленкой НАК в растворе платинохлористоводородной кислоты (5 × 10–3 моль л–1) и в растворе боргидрида натрия (0.1 моль л–1) по 5 мин в каждом с промежуточной отмывкой электрода водой. Процедуры адсорбции иона хлорплатината и его восстановления до платины повторяли от 5 (для образца НАК-1) до 15 (для образцов НАК-3 и НАК-4) раз. О количестве (а точнее, о величине площади электрохимически активной поверхности) платины, осажденной на каждый из образцов, можно было судить по циклическим вольтамперным кривым, представленным на рис. 7.
Как видно из рисунка, наибольшее количество платины удалось осадить на образец НАК-1, для чего понадобилось 5 циклов адсорбции-восстановления. На образец НАК-2 удалось нанести значительно меньше платины даже после 10 циклов адсорбции-восстановления. И, наконец, наименьшей “емкостью” с точки зрения количества осажденной платины характеризуются образцы НАК-3 и НАК-4, вольтамперная кривая на которых практически не изменялась ни после десяти, ни после пятнадцати и более циклов адсорбции-восстановления. Такую зависимость количества осаждаемой платины от содержания частиц наноалмаза в композите можно объяснить, если предположить, что ионы хлорплатината способны адсорбироваться, главным образом, на неалмазном углероде. Поэтому снижение доли последнего приводит к сокращению площади поверхности, способной адсорбировать и “удержать” ионы хлорплатината, после восстановления которых на носителе и остается металлическая платина.
Токи восстановления кислорода на платинированных образцах НАК, измеряли в диапазоне потенциалов 0.2–1.0 В при скоростях вращения электрода от 600 до 2700 об. мин–1 в растворе 0.5 М H2SO4, насыщенном кислородом при атмосферном давлении. ЦВА, измеренные при скорости вращения 2700 об. мин–1, показаны на рис. 8а.
Как видно из рис. 8а, вследствие существенного уменьшения количества осажденной платины при переходе от образца Pt/НАК-1 к образцам Pt/НАК-3 и Pt/НАК-4 и увеличения электрического сопротивления носителя, потенциал полуволны и ток восстановления кислорода закономерно снижаются, поэтому последующие эксперименты проводили с образцом Pt/НАК-1. Было показано, что ЦВА восстановления кислорода, измеренные при разных скоростях вращения на образце Pt/НАК-1, имеют вид, характерный для платины, нанесенной на стандартный углеродный носитель [26]. Зависимость предельных токов от скорости вращения, в целом, соответствует восстановлению О2 с участием четырех электронов (до О2–), хотя величины предельных токов несколько меньше, чем в случае использования стандартного носителя Vulcan ХС-72, при тех же скоростях вращения. Это свидетельствует о наличии факторов, снижающих каталитическую активность платины, нанесенной на НАК-1, что иллюстрирует рис. 9а, на котором сопоставлены вольтамперограммы восстановления кислорода на исследуемом образце Pt/НАК-1 и на образце с платиной, нанесенной на сажу, с близкой по величине площадью электрохимически активной поверхности.
Наклоны тафелевских зависимостей для Pt/НАК-1 (рис. 9б), в целом, близки к таковым для платины на стандартном носителе, хотя их линейные участки несколько укорочены, что указывает на торможение реакции восстановлении кислорода при использовании в качестве носителя наноалмазного композита.
ЦВА восстановления кислорода на образце Pt/НАК-1 измеряли периодически в течение трех недель. Между измерениями электрод хранили на воздухе. Как видно из рис. 8б, после некоторого первоначального снижения токов восстановления (кривые 1' и 2 ' на рисунке), что, вероятно, связано с уменьшением площади электрохимически активной поверхности вследствие постепенной стабилизации структуры осадка, эти токи в дальнейшем практически не изменялись в течение всего периода измерений (кривые 2 '–4 '). Это свидетельствует о хорошей структурной стабильности каталитической системы Pt/НАК-1 и ее устойчивости во времени, что, скорее всего, обусловлено снижением степени агрегирования частиц платины, уменьшением загрязнения ее поверхности продуктами окисления носителя из-за существенно меньшей скорости коррозии носителя из наноалмазного порошка по сравнению со стандартными сажами, как это было отмечено и в случае других структурированных углеродных носителей, таких как нанотрубки, графитизированная сажа и др. [27–31].
Таким образом, можно заключить что исследованный образец НАК-1 возможно, в принципе, использовать в качестве носителя катализаторов восстановления кислорода, поскольку при близкой к стандартному катализатору активности он обладает хорошей устойчивостью с точки зрения продолжительной эксплуатации и хранения.
ЗАКЛЮЧЕНИЕ
Методом детонационного синтеза были получены наноалмазные композиты (НАК) и проведены электрохимические и порометрические исследования нескольких образцов НАК, содержащих как фракцию наноалмазного порошка, так и фракцию неалмазного углерода. Были исследованы образцы как необработанной детонационной шихты (НАК-1), так и продуктов ее газофазной очистки посредством последовательного окисления неалмазной фракции (НАК-2 и НАК-3), отличающиеся соотношением наноалмазов и неалмазного углерода. Содержание последнего в образцах НАК-1, НАК-2 и НАК-3 составляло 48, 24 и 1 мас. % соответственно. Было показано, что интенсивность КР-полос кристаллического графита (1580 см–1) и разупорядоченной графитовой фазы (1360 см–1) повышена в исходной детонационной шихте по сравнению с образцами, частично или практически полностью очищенными от неалмазного углерода. Измерения удельного сопротивления порошковых образцов показали, что оно возрастает в ряду: НАК-1 < НАК-2 < < НАК-3, т.е. по мере увеличения доли фракции наноалмаза. Методом эталонной контактной порометрии было установлено, что все не модифицированные бором образцы (НАК-1, НАК-2 и НАК-3) обладают довольно высокими величинами как полной удельной поверхности (1041–1291 м2 г–1), так и гидрофильной удельной поверхности (739–1094 м2 г–1), и что с увеличением концентрации наноалмаза уменьшается степень их гидрофильности. При этом борирование наноалмаза приводит к существенному снижению его удельного сопротивления и к значительной гидрофилизации.
ЦВА кривые для образцов НАК имеют вид, характерный для заряжения двойного электрического слоя, но осложненный омическими потерями, возрастающими с увеличением доли наноалмаза. Сравнение данных импедансометрии для образцов НАК-1 и НАК-2 показывает, что при снижении доли электропроводного углерода происходит и существенное уменьшение емкости.
Исследование электровосстановления кислорода на каталитической системе Pt/НАК-1 продемонстрировало ее устойчивость во времени, что, по всей видимости, связано с существенно меньшей скоростью коррозии носителя из наноалмазного композита, по сравнению со стандартными сажами, при потенциалах кислородного электрода, что, в свою очередь, приводит и к снижению степени агрегирования частиц катализатора. Таким образом, можно заключить, что некоторые из исследованных образцов НАК можно использовать в качестве носителя катализаторов восстановления кислорода.
Список литературы
Волков К.В., Даниленко В.В., Елин В.И. // Физика горения и взрыва. 1990. Т. 26. № 3. С. 123.
Долматов В.Ю. Детонационные наноалмазы. Санкт-Петербург: НПО Профессионал, 2011. С. 534.
Овчинников-Лазарев М.А., Королёва М.Ю., Спицын Б.В. // Успехи в химии и химической технологии. 2017. Т. 31. № 13(194). С. 48.
Плесков Ю.В. Электрохимия алмаза. М: Едиториал УРСС, 2003. 101 с.
Pleskov Yu. in: Electrochemistry of Diamond. Fujishima A., Einaga Y., Rao T.N., and Tryk D.A., Eds. Tokyo: BKC & Amsterdam: Elsevier, 2005.
Pleskov Yu.V., Sakharova A.Ya., Krotova M.D. et al. // J. Electroanal. Chem. 1987. V. 228. № 1–2. P. 19.
Bagotsky V.S. Fuel cell problems and solutions. New Jersey: John Wiley and Sons, Inc. Publication, 2009. 320 p.
Subban C., Zhou Q., Leonard B. et al. // Phil. Trans. R. Soc. A Math. Phys. Eng. Sci. 2010. V. 368. P. 3243.
Soo L.T., Loh K.S., Mohamad A.B. et al. // Appl. Catal. A General. 2015. V. 497. P. 198.
Samad S., Loh K.S., Wong W.Y. et al. // Int. J. of Hydrogen Energy. 2018. V.43. № 16. P. 7823.
Montilla F., Morallón E., Duo I. et al. // Electrochim. Acta. 2003. V. 48. № 25–26. P. 3891.
Wang Y., Zang J., Dong L. et al. // Electrochim. Acta. 2013. V. 113. P. 583.
Zhang Y., Wang Y., Bian L. et al. // Int. J. of Hydrogen Energy. 2016. V. 41. P. 4624.
Shao Y., Liu J., Wang Y., Lin Y. // J. Mater. Chem. 2009. V. 19. P. 46.
Alexenko A.E. et al. // Diam. Relat. Mat. 1992. V. 1. P. 705.
Sadezky A., Muckenhuber H., Grot H. et al. // Carbon. 2005. V. 43. P. 1731.
Вольфкович Ю.М., Сосенкин В.Е. // Успехи химии. 2012. Т. 81. С. 936.
Volfkovich Yu.M., Filippov A.N., Bagotsky V.S. Structural Properties of Porous Materials and Powders Used in Different Fields of Science and Technology. London: Springer-Verlag, 2014.
Dzyazko Yu.S., Volfkovich Yu.M., Sosenkin V.E. et al. // Nanoscale Res. Lett. 2014. V. 9. P. 271.
Rouquerol J., Baron G., Denoyel R. et al. Liquid intrusion and alternative methods for the characterization of macroporous materials (IUPAC Technical Report) // Pure Appl. Chem. 2011. V. 84. P. 107.
Хейфец Л.И., Неймарк А.В. Многофазные процессы в пористых средах. М: Химия, 1982. С. 98.
Volfkovich Yu.M., Bograchev D.A., Mikhalin A.A., Bagotsky V.S. // J. of Solid State Electrochem. 2014. V. 18. № 5. P. 1351.
Conway B.E. Electrochemical Supercapacitors. Scientific Fundamentals and Technological Applications. New York: Kluwer Academic, 1999.
Тарасевич М.Р. Электрохимия углеродных материалов. М.: Наука, 1984.
Bagotsky V.S., Skundin A.M., Volfkovich Yu.M. Electrochemical power sources. Batteries, fuel cells, and supercapacitors. Hoboken. New Jersey: Wiley, 2015.
Schmidt T.J., Paulus U.A., Gasteiger H.A., Behm R.J. // J. Electroanal. Chem. 2001. V. 508. № 1–2. P. 41.
Zhang J., Carter R.N., Yu P.T., Gu W., Gasteiger H.A. Fuel cells – proton-exchange membrane fuel cells. Catalysts: Life-Limiting Considerations. Encyclopedia of Electrochemical Power Sources. 2009. P. 626.
Wang X., Li W., Chen Z. et al. // J. Power Sources. 2006. V. 158. № 1. P. 154.
Hara M., Lee M., Liu C.-H. et al. // Electrochim. Acta. 2012. V. 70. P. 171.
Kameya Y., Hayashi T., Motosuke M. // Appl. Catalysis B: Environmental. 2016. V. 189. P. 219.
Sakthivel M., Drillet J.-F. // Appl. Catalysis B: Environmental. 2018. V. 231. P. 63.
Blaut-Blachev A.N., Averin A.A., Shapagin A.V., Spitsyn B.V. // Protection of Metals and Physical Chemistry of Surfaces, 2017, vol. 53, Issue 1, pp. 75–79.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов




