Физикохимия поверхности и защита материалов, 2019, T. 55, № 5, стр. 538-545
Формирование самоорганизующихся кремнийорганических слоев на поверхности углеродистой стали и их влияние на электрохимическое и коррозионное поведение металла
М. А. Петрунин 1, Н. А. Гладких 1, М. А. Малеева 1, Л. Б. Максаева 1, *, Ю. В. Костина 2, А. В. Шапагин 1, Т. А. Юрасова 1, В. А. Котенев 1, А. Ю. Цивадзе 1
1 Федеральное государственное бюджетное учреждение науки Институт физической химии и электрохимии
им. А.Н. Фрумкина Российской академии наук
119071 Москва, Ленинский проспект, 31, стр. 4, Россия
2 Федеральное государственное бюджетное учреждение науки Институт нефтехимического синтеза
им. А.В. Топчиева Российской академии наук
119991 Москва, Ленинский проспект, 29, Россия
* E-mail: lmaksaeva@mail.ru
Поступила в редакцию 15.03.2019
После доработки 25.03.2019
Принята к публикации 15.04.2019
Аннотация
Адсорбция на поверхности углеродистой стали винилтриметоксисилана и γ-аминопропилтриэтоксисилана из водного раствора изучена методами ИК-фурье спектроскопии, сканирующей электронной спектроскопии и энергодисперсионной рентгеновской спектроскопии. Предложен механизм формирования поверхностного слоя. Показано, что силаны при адсорбции взаимодействуют с гидроксильными группами поверхности металла с образованием связей Fe–O–Si. Исследовано влияние кремнийорганических слоев на электрохимическое поведение стали. Установлено, что в присутствии кремнийорганических слоев потенциал питтингообразования стали смещается в область положительных значений, что указывает на ингибирование локального анодного растворения металла. Проведены ускоренные коррозионные испытания стальных образцов в климатической камере и показано ингибирующее коррозию действие винил- и аминосодержащих поверхностных слоев.
ВВЕДЕНИЕ
Углеродистая сталь является одним из наиболее востребованных промышленностью конструкционных материалов. Однако, несмотря на целый ряд ценных свойств, сталь имеет низкую коррозионную устойчивость в природных средах [1, 2], поэтому стальные сооружения даже в относительно “мягких” атмосферных условиях, обычно защищают от коррозии полимерными или лакокрасочными покрытиями [3–6], а при эксплуатации в подземных и подводных условиях, дополнительно используют электрохимическую защиту [7–9]. Обычно при использовании антикоррозионных полимерных и лакокрасочных покрытий, поверхность металла подвергают предварительной химической обработке для повышения коррозионной стойкости металла и улучшения адгезии лакокрасочного (полимерного) покрытия к поверхности. До недавнего времени в химической обработке поверхности металла использовали соединения шестивалентного хрома [10, 11]. Хроматные слои эффективно защищают металл от коррозии, одновременно обеспечивая высокую адгезию покрытия [12]. Однако входящий в химический состав компонентов Cr(VI) является экологически небезопасным соединением [13], применение которого в настоящее время является крайне нежелательным и в перспективе подлежит полному запрету [14]. В последние годы предприняты усилия по поиску и замене технологий, использующих соединения Cr(VI) [15, 16], но, несмотря на большое количество проведенных исследований, экологически чистая технология предобработки металлической поверхности до настоящего времени не предложена. Поэтому разработка эффективных и экологически чистых способов предварительной обработки металлических поверхностей является важной научно-технической и практически актуальной задачей.
Органосиланы (RnSi(OC2H5)4 – n) являются экологически безопасными соединениями, которые адсорбируются на поверхности металлов с образованием поверхностных самоорганизующихся силоксановых слоев [17–22]. При этом образуются прочные гидролитически стабильные связи Me–O–Si с гидроксилированной поверхностью металла, а органический радикал R молекулы силана можно менять, вводя в него разные функциональные группы [23]. Эти группы способны взаимодействовать с компонентами широкого ряда полимерных покрытий, обеспечивая высокое сродство поверхностного слоя к широкому ряду полимерных и лакокрасочных материалов, что широко использовалось при разработке композиционных материалов для повышения адгезии полимерного связующего к поверхностям неорганических наполнителей в композитах [17, 23]. Формирование поверхностных слоев на основе экологически безопасных органосиланов способно успешно конкурировать и, в перспективе, заменить хроматную обработку металлов [24, 25].
Однако, несмотря на многолетний интерес к изучению кремнийорганических слоев на неорганических поверхностях [17–29], данных об их влиянии на коррозионные свойства конструкционных металлов недостаточно.
В связи с этим, целью настоящей работы стало изучение электрохимического и коррозионного поведения углеродистых сталей в присутствии на поверхности металла кремнийорганических самоорганизующихся слоев.
МЕТОДИКА
На поверхности стали Ст3 формировали кремнийорганические слои на основе винилтриметоксисилана (ВС) и аминоэтиламинопропилтриметоксисилан – диаминосилан (ДАС) (табл. 1).
Таблица 1.
Структурные формулы используемых силоксанов
| № | Силан | Формула |
|---|---|---|
| 1 | ВС | СН2=СН–Si(OCH3)3 |
| 2 | ДАС | NH2–(CH2)2–NH–(CH2)3–Si(OCH3)3 |
Растворы с концентрациями органосиланов 1% по массе выдерживали в течение 60 мин для гидролиза силана [25]. Нанесение органосиланов на поверхность стальных пластин проводили, погружая образцы на 10 мин в растворы при комнатной температуре. Избыток силана смывали в воде в течение 1 мин, затем пластины высушивали на воздухе при комнатной температуре в течение 2 ч и термостатировали в сушильном шкафу при температуре 110°С в течение 1.5 ч.
Коррозионные исследования проводили методом ускоренных коррозионных испытаний в климатической камере МНК_408CL (Тайвань), RH 95%, t = 60°C. Коррозию стали оценивали гравиметрически, взвешивая испытуемые образцы на аналитических весах до и после испытаний (после удаления продуктов коррозии в соответствии с [30]).
После нанесения слоев органосиланов поверхность образцов исследовали физико-химическими методами.
Инфракрасные спектры зеркального отражения регистрировали на ИК-микроскопе Hyperion 2000 (36-кратный объектив), сопряженном с вакуумным ИК-Фурье спектрометром IFS-66v/s (Bruker), разрешением 2 см–1 в диапазоне 600–4000 см–1. Обработку спектров проводили с помощью ПО “OPUS” (Bruker), коррекция с использованием преобразования Крамерса–Кронига выполнялась автоматически.
Микрофотографии поверхности получали методом сканирующей электронной микроскопии (СЭМ), а изучение распределения элементов на поверхности образцов проводили методом энергодисперсионной рентгеновской спектроскопии (ЭДС). Для этого использовали сканирующий электронный микроскоп VEGA 3 SB (Teskan, Голландия), укомплектованный энергодисперсионной приставкой – микроанализатором INCA SDD X-MAX производства Oxford Instruments и программным обеспечением INCA Energy для проведения микроанализа, построения профилей состава, карт распределения элементов.
Электрохимическое поведение углеродистой стали изучали методом снятия поляризационных кривых [30]. В электрохимических исследованиях фоновым раствором служил боратный буферный раствор (0.1 М H3BO3 + 0.4 M Na2B4O7) с pH 6.7, содержащий 0.01 М NaCl. Поляризационные кривые стали Ст3 снимали в трехэлектродной стеклянной ячейке с разделенными электродными пространствами с помощью потенциостата IPC-Pro. Потенциалы измеряли относительно хлорид-серебряного электрода и пересчитывали на нормальную водородную шкалу. В качестве вспомогательного электрода использовалась платина. Для удаления образованной на воздухе оксидной пленки, стальной электрод катодно поляризовали при Е = –0.65 В в течение 15 мин, а затем потенциостат отключали до стабилизации потенциала коррозии Ек, после чего в фоновый раствор вводили исследуемый органосилан. После установления нового значения Ек снимали анодные поляризационные кривые [31] в потенциодинамическом режиме со скоростью развертки потенциала V = 0.1 мВ/с.
Влияние поверхностных кремнийорганических слоев оценивали по изменению потенциала питтингообразования (локальной депассивации). Потенциал питтингообразования (Eпит) [31–33] определяли из анодных поляризационных кривых [32–34]. Эффективность ингибирующего действия кремнийорганического слоя оценивали по увеличению потенциала питтингообразования Епт-нс в сравнении с величиной, измеренной для немодифицированной стали в фоне Епит-ст [35] (уравнение (1)):
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Неорганические поверхности, в частности поверхности металлов, покрыты слоем оксида металла, который в растворах и в атмосфере (с естественной влажностью) гидроксилируется [36]. В ИК-спектре поверхности стальной пластины отчетливо регистрируются полосы поглощения валентных и деформационных колебаний групп –ОН (область 3600 см–1 и ниже), что далее дает возможность учитывать гидроксилированную поверхность углеродистой стали при обсуждении механизма формирования на ней кремнийорганических слоев.
После модификации поверхности стальной пластины водными растворами ВС и ДАС спектры силоксанов изменяются в сравнении со спектрами их исходных растворов. Так, в ИК-спектре ДАС, нанесенном на поверхность пластины (кривая 2, рис. 1), можно наблюдать изменение контура полос поглощения валентных колебаний νNH (3350, 3280 см–1), а также смещение максимума полос поглощения деформационных колебаний δNH в первичной аминогруппе (при 1580 см–1) в длинноволновую область. Колебания СН-групп основной цепи логично не затронуты изменениями, полосы поглощения валентных (νСН, максимумы при 2934, 2882 см–1) и основных деформационных колебаний (СН2, 1470 см–1) не меняют положения максимумов. Регистрируется и характеристичная полоса поглощения νСН в метоксигруппах (плечо при 2843 см–1). При этом метоксисилановую группу изменения затрагивают: максимумы поглощения колебаний С–О (при 1177 см–1), и Si–O (при 1038 см–1) смещены в длинноволновую область более чем на 15 см–1 по сравнению с их положением в ИК-спектре капли ДАС (кривая 3, рис. 1), но снижения их относительной интенсивности практически не происходит. Изменения относительной интенсивности полос поглощения в ИК-спектрах отражения не связаны линейно с изменением содержания функциональных групп на поверхности пластины, однако появление новых малоинтенсивных полос поглощения с максимумом при 1280 и 1226 см–1, вкупе со снижением относительной интенсивности полосы поглощения при 780 см–1, предполагает необратимые изменения в области поглощения связей C–Si (рис. 1).
Рис. 1.
ИК-спектры зеркального отражения (а) и фрагмент ИК-спектра в области 1800–600 см–1 (б) капли ДАС (кривая 3), ДАС, нанесенного на стальную пластину (кривая 2) в сравнении с ИК-спектром стали (кривая 1).
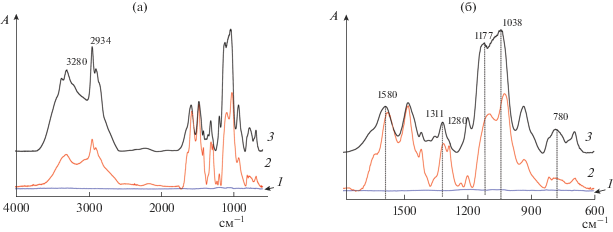
Обработка пластины ВС приводит к более кардинальным изменениям в структуре силана и, следовательно, в ИК-спектрах образцов. Наличие двойной связи в ВС значительно меняет его свойства по сравнению с ДАС. В исходном ИК-спектре жидкого ВС (кривая 2, рис. 2а) интенсивная характеристичная полоса поглощения валентных колебаний νСН от метоксигруппы (2840 см–1) имеет четкий контур, а вторая полоса (с максимумом при 2944 см–1) – неявно выраженные плечи при 2050 и 2980 см–1, что характеризует поглощение валентных колебаний СН в нескольких группах –О–СН3. Полоса поглощения гидроксильных групп имеет незначительную интенсивность, протоны при двойной связи дают малоинтенсивные полосы поглощения с максимумами при 3060 и 3022 см–1. После обработки стальной пластины в ВС в ИК-спектре ее поверхности регистрируется интенсивная широкая полоса поглощения ассоциированных ОН-групп (при 3320 см–1), при этом сохраняется полоса поглощения валентных колебаний νСН метильной группы при кислороде (при 2982 см–1), плечо при 2958 см–1 становится самостоятельной полосой поглощения, и резко снижается интенсивность характеристичной полосы поглощения валентных колебаний νСН метоксигруппы. Это может объясняться частичным сохранением метоксигрупп при Si, однако часть их необратимо отщепляется. В этом случае в области “отпечатков пальцев” должны наблюдаться как изменения, характерные для уменьшения количества метоксигрупп при Si, так и новые полосы поглощения от образовавшихся связей.
Рис. 2.
Фрагменты ИК-спектров зеркального отражения капли ВС (кривая 2), ВС, нанесенного на стальную пластину (кривая 3), в сравнении с ИК-спектром стали (кривая 1) в области 3700–3650 см–1 (а) и 1800–600 см–1 (б).

Действительно, при сохранении в ИК-спектре поверхности стали, обработанной ВС, полос поглощения винильной группы (1600, 1411, 1011, 968 см–1), и связей Si–O (1084 см–1), последняя резко падает по интенсивности, одновременно перестает регистрироваться полоса поглощения при 820 см–1, отвечающая маятниковым колебаниям метоксигрупп. В то же время интенсивные полосы поглощения при 1170, 874 и 756 см–1 свидетельствуют о наличии в образце связей С–О, и Si–C, соответственно. Другими словами, при гидролизе винилметоксисилана и модифицировании гидролизованным ВС поверхности стали происходит разрыв связи О–СН3, сопровождающийся образованием метанола и групп –Si–OH. Последние, в свою очередь, могут образовывать ковалентные связи с металлом пластины, о чем косвенно свидетельствует рост поглощения ниже 600 см–1 в ИК-спектре поверхности пластины, обработанной ВС (кривая 3, рис. 2б).
Результаты анализа ИК-спектров поверхности стали, модифицированной силанами, позволяет предложить схему (реакции (2)–(4)) формирования поверхностного самоорганизующегося кремнийорганического слоя на углеродистой стали, подтверждающую предложенные ранее механизмы формирования кремнийорганических слоев на поверхностях железа, алюминия и цинка [21, 22, 37, 38].
(2)
$\begin{gathered} {\text{RSi}}{{\left( {{\text{OC}}{{{\text{H}}}_{{\text{3}}}}} \right)}_{{{\text{3aq}}}}}{\text{ + 3}}{{{\text{H}}}_{{\text{2}}}}{\text{O}} \to \\ \to \,\,{\text{RSi}}{{\left( {{\text{OH}}} \right)}_{{\text{3}}}}{\text{ + 3C}}{{{\text{H}}}_{{\text{3}}}}{\text{OH,}} \\ \end{gathered} $На первой стадии (реакция (2)) происходит гидролиз молекул органосилана. Вторая стадия – конденсация силанольных и поверхностных гидроксильных групп с образованием поверхностных металл-силоксановых связей (реакция (3)). Третья стадия – конденсация соседних силанольных групп и образование силоксанового олигомера (реакция (4)). Степень олигомеризации n может быть от 6 до нескольких сотен, учитывая плотность гидроксильных групп на поверхности, составляющую от 6 до 20 групп/нм2 [36] и длины связи Si–O, равную 1.61 Å [39].
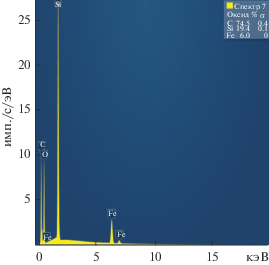
С использованием СЭМ и ЭДС было проведено исследование поверхности стали с нанесенным винилсодержащим нанослоем. На рис. 3 представлена микрофотография поверхности и картирование микрофотографии в соответствии с распределением элементов по поверхности: зеленый цвет на карте поверхности соответствует содержанию кремния, бирюзовый – кислорода, синий – углерода. Можно видеть равномерный “толстый”, хотя и дефектный слой на поверхности, элементный анализ которого (рис. 3) показал, что в изучаемом слое присутствует в основном кремний, а кроме него углерод и кислород, причем обнаруженные элементы равномерно распределены по поверхности. Это указывает на формирование равномерного кремнийорганического слоя на поверхности углеродистой стали.
Рис. 3.
Микрофотография поверхности углеродистой стали, покрытой винилсодержащим кремнийорганическим слоем (ВС).
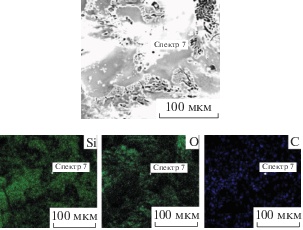
Спектр, снятый в точке (рис. 4), показал в основном наличие кремния и углерода. Небольшое количество железа, которое содержится в стальной подложке, указывает на то, что толщина кремнийорганического слоя составляет 1–2 мкм.
На рис. 5 представлена микрофотография поверхности Ст3, модифицированной ДАС. Как и в случае с ВС на поверхности образовался довольно плотный, но дефектный слой. Элементный анализ показал на стальной поверхности наличие кремния, кислорода, углерода и азота.
Спектр, снятый в точке 2 (рис. 6) показал в основном наличие кремния и углерода. Однако в случае с ДАС толщина пленки составила 2–3 мкм, поскольку такова чувствительность по глубине проникновения метода ЭДС.
Для оценки устойчивости поверхностного слоя было проведено исследование поверхности стали с винил- и аминосодержащим слоем после снятия анодных поляризационных кривых (рис. 7 и 8).
Рис. 7.
Микрофотография поверхности углеродистой стали, содержащей ДАС, после проведения электрохимических исследований.

Рис. 8.
Микрофотография поверхности углеродистой стали, содержащей ВС, после проведения электрохимических исследований.

Электронная микроскопия образцов углеродистой стали с винил- и аминосилоксановым слоем толщиной более 1 мкм, нанесенных из раствора с концентрацией 1% ВС и ДАС, показала, что после снятия анодной поляризационной кривой на поверхности стали обнаружены следы продуктов растворения и питтинги диаметром от 15 до 30 мкм, как и ожидалось, учитывая, что при снятии анодной кривой значение электродного потенциала превышало Епит на несколько сотен милливольт. ЭДС элементный анализ показал наличие на поверхности кремния, углерода и кислорода. Таким образом, установлено, что поверхностный кремнийорганический слой сохраняется на поверхности металла в условиях провоцирующих локальное анодное растворение металла, что указывает на высокую устойчивость поверхностного слоя.
В табл. 2 представлены результаты оценки ингибирующей эффективности поверхностных кремнийорганических слоев, сформированными в водных растворах органосиланов с концентрациями 1% на стали Ст3, по значению ∆Епит. Видно, что наличие на поверхности металла кремнийорганического слоя ингибирует локальное анодное растворение стали, поскольку способствуют увеличению потенциала питтингообразования [34] (потенциала локальной депассивации) (табл. 2).
Таблица 2.
Оценка ингибирующей эффективности поверхностных кремнийорганических слоев по изменению Епит
| Система | Сталь Ст3 | Ст3 + ВС | Ст3 + ДАС |
|---|---|---|---|
| ∆Епит, В | 0 | 0.1 | 0.2 |
Из табл. 2 можно видеть, что винил- (ВС) и диаминосодержащие (ДАС) слои эффективно ингибируют локальное анодное растворение углеродистой стали. Таким образом, можно ожидать, что поверхностные кремнийорганические слои будут ингибировать как равномерную, так и локальную коррозию углеродистой стали, что ранее наблюдали на алюминии, железе и цинке [21, 22, 40, 41].
Ускоренные коррозионные испытания углеродистой стали с нанесенными самоорганизующимися поверхностными кремнийорганическими слоями, проведенные в климатической камере при t = 60°C и RH 90%, показали ингибирование атмосферной коррозии металла (табл. 3).
Таблица 3.
Скорость коррозии углеродистой стали с нанесенными кремнийорганическими поверхностными слоями после 10 сут испытаний в климатической камере, t = 60°C, RH = 95%
| Система | Сталь Ст3 | Ст3 + ВС | Ст3 + ДАС |
|---|---|---|---|
| Скорость коррозии, мм/год | 0.22 | 0.11 | 0.05 |
Наиболее эффективно ингибирует равномерную коррозию диаминосодержащий слой, снижающий скорость коррозии в более, чем 4 раза. Винилсодержащий слой способен уменьшать скорость коррозии стали в 2 раза. Таким образом, показано, что винил- и диаминосодержащие поверхностные слои способны эффективно ингибировать как локальное анодное растворение, так и равномерную коррозию металла.
ВЫВОДЫ
1. Показано, что в результате адсорбции органосиланов из их водных растворов на поверхности углеродистой стали формируется равномерный самоорганизующийся ковалентно-связанный с поверхностными группами металла кремнийорганический слой. На основании результатов анализа экспериментальных данных предложена схема механизма формирования кремнийорганического слоя.
2. Установлено, что винил- и диаминосилоксановые слои эффективно ингибируют локальное анодное растворение и коррозию углеродистой стали.
3. Показано, что винилсилоксановый самоорганизующийся поверхностный слой устойчив к действию анодной поляризации, вызывающей равномерное и локальное растворение металла и сохраняется на поверхности стали, что указывает на его устойчивость к действию воды и коррозионно-активных компонентов11.
Работа выполнена при финансовой поддержке РФФИ, проект 17-03-00232, программы фундаментальных исследований президиума РАН 34П “Актуальные проблемы физикохимии поверхности и создания новых композитных материалов”, направление 4 и частично в рамках госзадания ИНХС РАН, тема № AAAA-A19-119020490054-7.
Список литературы
Коррозия. Справочник под ред Шрайера Л.Л. (или Corrosion Ed by Shreir L.L. London; Boston: Newnes-Butterworths, 1976. P. 73. 2.) М.: Металлургия. 1981. С. 17.
Кеше Г. Коррозия металлов. М.: Металлургия. 1984. С. 323.
Romanoff M. Underground Corrosion (Classic Reprint). Fb&C Limited. 2018. P. 234.
Leygraf C., Wallinder I.O., Tidblad J., Graedel T. Atmospheric Corrosion. 2nd Edition. John Wiley & Sons. Inc., New Haven. USA. 2016. P. 470.
Outdoor Atmospheric Corrosion. Herbert E. Townsend, editor. ASTM Int. West Conshohockcn, PA. USA. 2002. P. 385.
Forsgren A. Corrosion Control Through Organic Coatings. CRC Press. Taylor & Francis Group. Boca Raton. FL. USA 2006. P. 155.
ГОСТ 9.602-2016. Единая система защиты от коррозии и старения. Сооружения подземные. Общие требования к защите от коррозии. М. Стандартинформ. 2016. С. 86.
Стрижевский И.В., Белоголовский А.В., Дмитриев В.И., Петров Н.А., Филиновский В.Ю., Фрейман Л. Защита подземных металлических сооружений от коррозии. Справочник. Защита подземных металлических сооружений от коррозии. М.: Стройиздат. 1990. С. 303.
Baeckmann W.V., Schwenk W. Des katodischesKorrosionschutzes. Theorie und Praxicedes der elektrochemischer Schutzverfahren. Verlag Chemie. Weibheim, Deerfield, Florida. Basel 1980. P. 30.
Robert G. Kelly, John R. Scully, David W. Shoesmith, Rudolph G. Buchheit “Electrochemical Techniques in Corrosion Science and Engineering”. Marcel Dekker, Inc. N.Y. Basel. 2003. P. 263.
Schweitzer Ph.A. Paint and coatings: applications and corrosion resistance. CRC Press. Taylor & Francis Group. Boca Raton. FL. USA 2005. P. 71.
Kendig M.W., Davenportd A.J., Isaacs H.S. // Corrosion Science. 1993. V. 34. № l. P. 41–49.
Osborne J.H., Blohowiak K.Y., Taylor S.R. et al. // Progress in Organic Coatings. 2001. V. 41. P. 217–225.
Directive 2011/65/EU of the European Parliament and of the Council.
Buchhet R.G., Guan H., Mahajanam S., Wong F. // Progress in Organic Coatings. 2003. V. 47. P. 74–182.
Sathiyanarayanan S., Azim S.S., Venkatachari G. // Progress in Organic Coatings. 2009. V. 65. № 1. P. 152–157.
Erickson P.W., Plueddemann E.P. Historical Background of the Interface-Studies and Theories in Composite materials, edited by Bnutman L.J., Krocк R.H. V. 6. Interfaces in Polymer Matrix Composites. Edited by E.P. Plueddemann. Academic Press. N.Y.–London. 1974. P. 2329.
Ron J., Sagiv J. // J. Colloid and Interface Science. 1986. V. 112. P. 457–472.
Silanes and Other Coupling Agents, Ed. Mittal K.L. VSP. Leyden. Netherlands. Boston. USA 2009. V. 54. P. 349.
Plueddemann E.P. Silane Adhesion Promoters for Polymeric Coatings in Adhesion Aspects of Polymeric Coatings. K.L. Mittal. Ed. Plenum Press. N.Y.–London. 2011. P. 363–379.
Петрунин М.А., Максаева Л.Б., Гладких Н.А., Наркевич Е.Н., Юрасова Т.А., Рыбкин А.А., Терехова Е.В., Котенев В.А., Каблов Е.Н., Цивадзе А.Ю. // Физикохимия поверхности и защита материалов. 2018. Т. 54. № 5. С. 457–465.
Петрунин М.А., Максаева Л.Б., Юрасова Т.А., Терехова Е.В., Котенев В.А., Цивадзе А.Ю. // Физикохимия поверхности и защита материалов. 2013. Т. 49. № 6. С. 606–613.
Pluddemann E.P. Silane Coupling Agents. 2nd edition. Springer Science + Business Media. N.Y. 1991. P. 253.
Avdeev Yu.P., Karpov V.A., Maksaeva L.B., Petrunin M.A. // J. Corros. Scale Inhib. 2014. 3. № 3. P. 198–203.
Palanivel V., Zhu D.G., van Ooij W. J. // Progress in Organic Coatings 2003. V. 47. P. 384–392.
Mao Z.R., Sagiv J. // Thin Solid Films. 1985. V. 132. P. 135.
Cеменов В.В. Успехи химии. 2011. Т. 80. № 4. С. 313–416.
Peng N., Wen Y., He Y. // Progress in Organic Coatings. 2019. V. 127. P. 151–156.
Aakkula J., Jokinen J., Saarela O. // International J. Adhesion and Adhesives. 2017. V. 79. P. 83–94.
Corrosion Tests and Standards: Application and Interoretation. Robert Baboian Editor. Second Edition ASTM Int. 2005. Baltimore. MD. USA. P. 43.
Розенфедьд И.Л., Жигалова К.А. // Методы ускоренных коррозионных испытаний металлов. М.: Металлургия. 1966. С. 347.
Szklarska-Smialowska Z. Pitting and Crevice Corrosion. NACE International. 2005. P. 605.
Galvele R. // Corrosion Science. 2005. V. 47. P. 3053–3067.
Soltis J. // Corrosion Science. 2015. V. 90. P. 5–22.
Кузнецов Ю.И. // Успехи химии. 2004. Т. 73. № 1. С. 79–93.
McCafferty E. Surface Chemistry of Aqueous Corrosion Processes. 2015 Springer Heidelberg N.Y. Dordrecht London. 89 p.
Ishida H., Koenig L. // J. Colloid and Interface Sci., 1978. 64. P. 555.
Matinlinna J.P., Laajalehto K., Lassila L.V.J., Yli-Urpo A., Vallittu P.K. FT-IR and XPS surface characterization of allyltrimethoxysilane and 3-methacryIoxypropyItrimethoxysilane mixture adsorbed onto titanium substrate.in Silanes and Other Coupling Agents. Ed. K.L. Mittal/VSP. Utrecht. Netherlands. Boston. USA 2004. V. 3. P. 21–37.
Крешков А.П., Борк В.А., Бондаревская В.А., Мышляева Л.В., Сявцилло С.В., Шемятенкова В.Т. Практическое руководство по анализу мономерных и полимерных кремнийорганических соединений. Государственное научно-техническое издательство химической литературы. М.: Госхимиздат. 1962. С. 360.
Петрунин М.А., Максаева Л.Б., Юрасова Т.А., Гладких Н.А., Терехова Е.В., Котенев В.А., Каблов Е.Н., Цивадзе А.Ю. // Физикохимия поверхности и защита материалов. 2015. Т. 51. № 6. С. 656–663.
Петрунин М.А., Максаева Л.Б., Юрасова Т.А., Гладких Н.А., Терехова Е.В., Котенев В.А., Каблов Е.Н., Цивадзе А.Ю. // Физикохимия поверхности и защита материалов. 2016. Т. 52. № 6. С. 1–9.
Mehrdad Davoodi, Mojtaba Nasr-Esfahani. // Prot. Met. Phys. Chem. Surf. 2016. V. 52. № 1. P. 149.
More Aarti P., Mhaske S.T. // Prot. Met. Phys. Chem. Surf. 2017. V. 53. № 5. P. 864.
Zhan Zhang, Junsheng Wu, Yuntao He, Xuequn Cheng, Xiaogang Li. // Prot. Met. Phys. Chem. Surf. 2018. V. 54. № 4. P. 632–641.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов