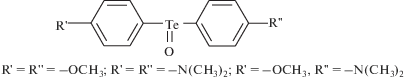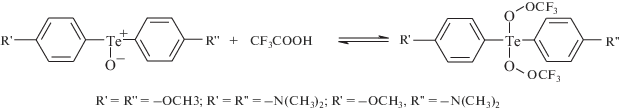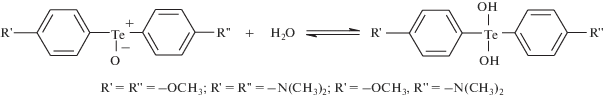Физикохимия поверхности и защита материалов, 2019, T. 55, № 6, стр. 649-656
Влияние высокой реакционной способности диарилтеллуроксидов на результаты их хромато-масс-спектрометрической идентификации
Е. В. Елисеева 1, *, Н. А. Редькин 1, В. П. Гарькин 1, И. С. Пыцкий 2, А. К. Буряк 2
1 Федеральное государственное автономное образовательное учреждение высшего образования
“Самарский национальный исследовательский университет им. академика С.П. Королева”
Самара, Россия
2 Федеральное государственное бюджетное учреждение науки Институт физической химии и электрохимии
им. А.Н. Фрумкина РАН
119071 Москва, Ленинский просп., 31, корп. 4, Россия
* E-mail: eveletskaya@gmail.com
Поступила в редакцию 28.02.2019
После доработки 05.06.2019
Принята к публикации 13.06.2019
Аннотация
В работе изучены особенности идентификации симметричных и несимметричных диарилтеллуроксидов в условиях хромато-масс-спектрометрии с электроспрей ионизацией (HPLC/MS-ESI). Показано, что для диарилтеллуроксидов при ионизации в условиях ESI характерно образование димерных ионов и ионов-ассоциатов с компонентами подвижной фазы. Кроме того, было уставлено влияние изменения концентрации аналитов в растворе и объема инжекции на вид хроматографических и масс-спектрометрических данных.
ВВЕДЕНИЕ
Одним из наиболее перспективных направлений применения диарилтеллуроксидов является препаративный органический синтез. Основой этого служит высокая реакционная способность данного класса соединений. В то же время известно, что теллурорганические соединения (ТОС) токсичны [1, 2]. Эти два фактора требуют решения целого ряда важных задач со стороны аналитической химии.
Во-первых, требуется разработка подходов к контролю синтезов с участием ТОС, который включает установление структуры целевых и побочных продуктов, прогнозирование направлений реакций, подбор условий синтеза.
Во-вторых, необходимо минимизировать риски негативного воздействия соединений теллура на окружающую среду и здоровье человека при работе и последующем применении веществ, полученных в ходе синтезов с участием ТОС. Для этого требуется обеспечить контроль примесного органических производных теллура в продуктах синтезов и других объектах техногенного характера.
Для достижения положительного решения вышеописанных задач необходимо применение современных методов анализа. Среди всего многообразия методов сочетание жидкостной хроматографии и масс-спектрометрии зарекомендовало себя, как высокочувствительный и информативный метод, позволяющий не только определять следовые количества веществ, но и устанавливать структуру соединений. Электроспрей ионизация (ESI) и химическая ионизация при атмосферном давлении (APCI), применяемые в таких анализах, позволяют переводить молекулы веществ в газовую фазу из раствора без длительного воздействия высоких температур в процессе хроматографирования. За счет этого спектры, получаемые при ионизации ESI и APCI, отличаются наличием стабильного высокоинтенсивного молекулярного иона, что облегчает идентификацию и повышает информативность результатов анализа [3]. Поэтому в данной работе была изучена специфика идентификации диарилтеллуроксидов в условиях HPLC/MS-ESI анализа.
Частично возможность использования хроматографических методов с масс-спектрометрическим детектированием в анализе диарилтеллуроксидов представлены ранее в ряде наших работ [4–6]. В них были установлены некоторые особенности и закономерности определения теллуроксидов без учета влияния их реакционной способности на результаты анализа.
Целью настоящей работы являлось изучение возможности протекания реакций в смеси диарилтеллуроксидов в зависимости от их концентрации в растворе в условиях хромато-масс-спектрометрии с электроспрей ионизацией.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе исследовали смеси трех диарилтеллуроксидов: ди(4-метоксифенил)теллуроксида, ди(4-диметиламинофенил)теллуроксида и 4-диметиламинофенил-4-метоксифенилтеллуроксида, структура которых представлена на рис. 1.
Хроматографическое разделение диарилтеллуроксидов проводили методом обращено-фазовой ВЭЖХ на жидкостном хроматографе AgilentTechnologies 1260 Infinity с масс-спектрометрическим детектором BrukerMaxisImpact с ионизацией электрораспылением.
Для исследования были использованы два хроматографических режима (табл. 1).
Таблица 1.
Хроматографические условия
| Хроматографический режим № 1 | Хроматографический режим № 2 | |
|---|---|---|
| Хроматографическая колонка |
ZORBAX SB-C18 (2.1 × 150 мм, 3.5 µм) | ZORBAX SB-C18 (2.1 × 150 мм, 3.5 µм) |
| Подвижная фаза А | Вода–метанол–ацетонитрил–ТФУ (50 : 40 : 10, 0.05%) |
Вода–метанол–ацетонитрил–ТФУ (50 : 40 : 10, 0.01%) |
| Подвижная фаза Б | Ацетонитрил с добавлением 0.05% ТФУ | Ацетонитрил с добавлением 0.01% ТФУ |
| Режим подачи элюента | Градиентный 0–3 мин: ПФ А 4–10 мин: ПФ Б 11–15 мин: ПФ А |
Градиентный 0–1 мин: ПФ А 12–13 мин: ПФ Б 14–15 мин: ПФ А |
| Скорость потока, мл/мин | 0.5 | 0.5 |
| Температура термостата колонок | 45°С | 25°С |
| Объем вводимой пробы | 1 мкл | 0.1 мкл |
| Концентрации исследуемых соединений в метаноле, мкг/мл | 5000 | 500, 250, 100, 50, 5 |
Масс-спектрометрическое детектирование проводили в режиме регистрации положительных ионов в диапазоне m/z 50–3000 при напряжении на капилляре 3500 В и напряжении на скиммере 500 В. Скорость потока и температура азота составляла 4.5 л/мин и 250°С соответственно. Скорость записи спектров – 4 спектра в секунду.
Обработку полученных хроматограмм и масс-спектров осуществляли с помощью программного обеспечения DataAnalysis 4.2. Подтверждение правильности установления брутто-формул ионов осуществляли сравнением экспериментальных значений m/z с расчетными значениями масс ионов и характеристическим изотопным распределением теллурсодержащих ионов.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
При исследовании поведения диарилтеллуроксидов в условиях хромато-масс-спектрометрического анализа были установлены некоторые особенности идентификации, связанные с высокой реакционной способностью данного класса соединений. В частности, склонность к образованию димерных ионов и ионов-ассоциатов с компонентами подвижной фазы при ионизации в масс-детекторе, а также взаимодействие с водой в процессе элюирования при уменьшении концентрации аналитов в испытуемых растворах.
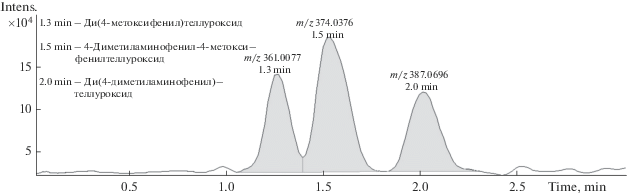
В работе в процессе подбора хроматографических условий разделения диарилтеллуроксидов первоначально использовали растворы с высокой концентрацией аналитов 5000 мкг/мл, при этом объем инжекции составлял 1 мкл. Для элюирования использовали хроматографический режим № 1. На рис. 2 представлена хроматограмма по полному ионному току (ПИТ), полученная в данных условия анализа.
По хроматографическим данным видно, что в описываемых условиях хроматографирования не достигнуто полное разделение ди(4-метоксифенил)теллуроксида и 4-дметиламинофенил-4-метоксифенилтеллуроксида. Критерий разделения составил 0.94, в то время как для большинства практических методик рекомендуется его значение не ниже 1.2.
В условиях применения масс-спектрометрического детектирования недостаточность идентификации по временам удерживания при низкой эффективности хроматографического разделения компонентов смеси дополняется возможностью идентификации по данным масс-спектров. Нами были детально изучены особенности масс-спектрометрических данных и выделены основные идентификационные признаки исследуемых диарилтеллуроксидов.
В условиях HPLC/MS-ESI анализа исследуемые диарилтеллуроксиды образуют протонированные молекулярные ионы [M + H]+, интенсивность которых максимальна в масс-спектрах ESI. Образующиеся фрагментные ионы малоинтенсивны. При отщеплении кислорода от молекулы диарилтеллуроксида образуются ионы [M–О]+, отвечающие структуре диарилтеллуридов. Также характерным для диарилтеллуроксидов является выброс атома теллура из структуры иона [M–О]+ с образованием ионов биарилов. Для диарилтеллуроксидов характерной особенностью является образование ассоциатов с компонентам подвижной фазы [M + H + CH3OH–H2O]+, [M + H + CF3COOH–H2O]+ и протонированных димеров [2M + H]+. Димеры образуют ассоциаты с трифторуксусной кислотой [2M + H + CF3COOH–H2O]+.
Рис. 3.
Масс-спектры исследуемых диарилтеллуроксидов (5000 мкг/мл) в условиях хроматографического режима № 1.
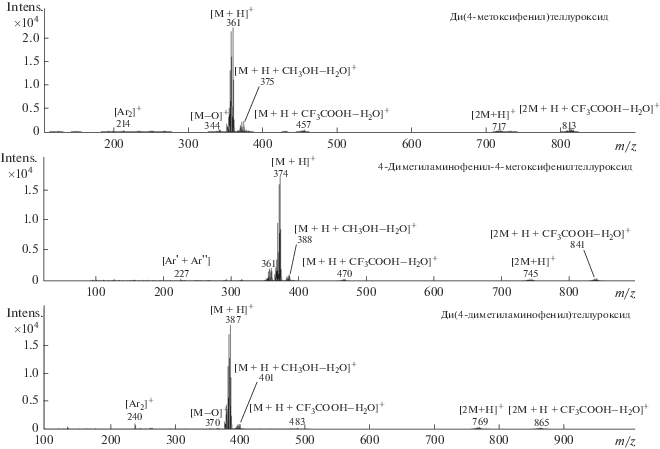
Образование ионов-ассоциатов с трифторуксусной кислотой и метанолом в масс-детекторе в процессе ионизации обусловлено способностью диарилтеллуроксидов легко взаимодействовать с данными компонентами подвижной фазы. Подтверждением этому может служить выявленная нами в работе [7] реакция взаимодействия диарилтеллуроксидов с трифторуксусной кислотой (ТФУ), протекающая в процессе элюирования в условиях обращено-фазовой тонкослойной хроматографии (рис. 4) с образованием диарилтеллурдитрифторацетатов.
Однако по сравнению с результатами работы [7] протекание этого процесса при элюировании не зафиксировано в настоящем исследовании. Объясняется этот факт тем, что при хромато-масс-спектрометрическом исследовании мы использовали подвижную фазу с концентрацией ТФУ в 10 раз меньшей. Кроме того, условия ВЭЖХ анализа подобраны таким образом, что элюирование компонентов происходит быстрее, вследствие чего время взаимодействия ТФУ и диарилтеллуроксидов значительно меньше. По этим причинам взаимодействие исследуемых соединений с трифторуксусной кислотой мы зафиксировали только в виде образования малоинтенсивных ионов-ассоциатов при ионизации ESI.
Аналогичным образом может быть объяснено и образование ионов-ассоциатов с метанолом. Следует отметить, что содержание метанола в подвижной фазе составляет 50%, но при этом взаимодействие с диарилтеллуроксидами в процессе элюирования также не наблюдается. Данное явление обусловлено значительно более низкой полярностью связи O–H по сравнению с трифторуксусной кислотой.
На основании полученных хромато-масс-спектрометрических данных и предположении о природе процессов образования ионов, связанных с реакционной способностью диарилтеллуроксидов, нами предложена обобщенная схема образования ионов (рис. 5).
Рис. 5.
Предполагаемая обобщенная схема образования ионов диарилтеллуроксидов в условиях HPLC/MS-ESI.
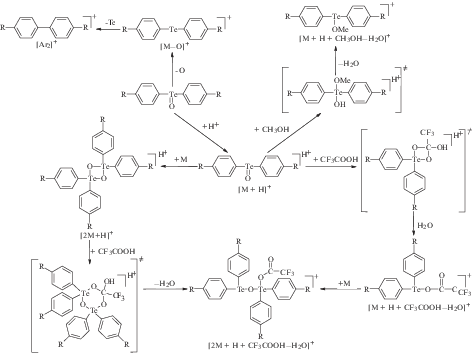
Таким образом, мы показали, что даже при недостаточной эффективности хроматографического разделения возможна идентификация диарилтеллуроксидов по данным масс-спектров. Однако при более детальном рассмотрении масс-спектров, полученных при элюировании в условиях хроматографического режима № 1 наблюдается наложение масс-спектров, вследствие которого невозможно установить наличие некоторых ионов. В частности, по причине того, что для пары 4-диметиламинофенил-4-метоксифенилтеллуроксида и ди(4-метоксифенил)теллуроксида не достигнуто достаточное хроматографическое разделение, в масс-спектре 4-диметиламинофенил-4-метоксифенилтеллуроксида присутствует молекулярный ион ди(4-метоксифенил)теллуроксида с m/z 361. За счет этого в масс-спектре несимметричного диарилтеллуроксида невозможно обнаружить ион [M–О]+m/z 368.
Для достижения наиболее эффективного разделения исследуемых теллурорганических соединений был изменен градиентный режим подачи элюента, снижена температура термостата колонок и инжектируемое количество образцов путем уменьшения концентрации растворов и объема вводимой пробы (хроматографический режим № 2). В результате было достигнуто более эффективное разделение (рис. 4).
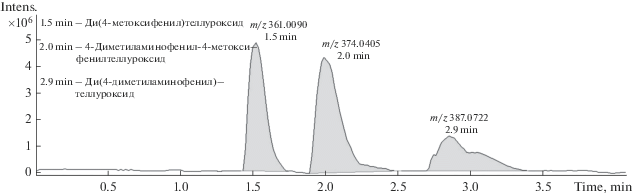
На рис. 6 представлена хроматограмма ПИТ раствора с концентрацией диарилтеллуроксидов 500 мкг/мл. В отличие от хроматограмм для растворов с концентрацией 5000 мкг/мл на хроматограмме ПИТ раствора с меньшей концентрацией наблюдается искажение формы хроматографических пиков, по виду представляющее собой наложение двух пиков и указывающее на возможность присутствия в системе двух соединений, время удерживания которых одинаково. Для объяснения данного явления были проанализированы данные соответствующих масс-спектров.
Как и в случае масс-спектров для растворов с концентрацией 5000 мкг/мл в масс-спектрах растворов с меньшими концентрациями присутствуют молекулярные ионы, димерные ионы, ионы-ассоциаты, которые имеют незначительную относительную интенсивность. Это свидетельствует о том, что присутствие данных ионов в масс-спектрах обусловлено спецификой ионизации диарилтеллуроксидов, а не процессами, которым они способны подвергаться при элюировании.
Отличительной особенностью масс-спектров при уменьшении концентрации растворов является присутствие ионов [M + H + H2O]+ и [2M + H + H2O]+. Данные ионы имеют значительную относительную интенсивность, которая возрастает при уменьшении концентрации диарилтеллуроксидов в растворе. Для ди(4-диметиламинофенил)теллуроксида и 4-диметиламинофенил-(4-метоксифенил)теллуроксида при концентрациях 5, 50 и 100 мкг/мл интенсивность иона [M + H + H2O]+ значительно превышает интенсивность молекулярного иона. Для ди(4-метоксифенил)теллуроксида при концентрациях 100 и 50 мкг/мл интенсивность ионов [M + H]+ и [M + H + H2O]+ соизмерима, и только при концентрации 5 мкг/мл ион [M + H + + H2O]+ имеет максимальную интенсивность. В табл. 2 представлено изменение соотношения интенсивностей данных ионов в зависимости от концентрации аналитов в растворе.
Таблица 2.
Соотношение интенсивностей ионов [M + H]+ и [M + H + H2O]+ (%) в масс-спектрах диарилтеллуроксидов R'–Te(O)–R" в зависимости от концентрации в растворе
| Концентрация, мкг/мл | Соотношение интенсивностей ионов [M + H]+ и [M + H + H2O]+ | |||||
|---|---|---|---|---|---|---|
| R' = R" = 4-CH3O(C6H4) | R' = 4-CH3O(C6H4), R" = 4-(CH3)2N(C6H4) | R' = R" = 4-(CH3)2N(C6H4) | ||||
| [M + H]+ | [M + H + H2O]+ | [M + H]+ | [M + H + H2O]+ | [M + H]+ | [M + H + H2O]+ | |
| 500 | 92.9 | 7.1 | 75.6 | 24.4 | 72.1 | 27.9 |
| 250 | 86.8 | 13.2 | 58.6 | 41.4 | 54.0 | 46.0 |
| 100 | 55.1 | 44.9 | 29.0 | 71.0 | 37.3 | 62.7 |
| 50 | 41.2 | 58.8 | 24.3 | 75.7 | 28.0 | 72.0 |
| 5 | 31.5 | 68.5 | 21.0 | 79.0 | 24.9 | 75.1 |
Рис. 7.
Масс-спектры исследуемых диарилтеллуроксидов (500 мкг/мл) в условиях хроматографического режима № 2.
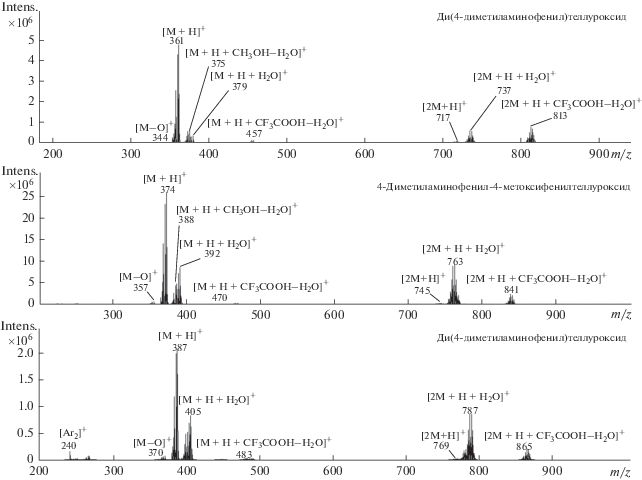
Присутствие ионов [M + H]+ и [M + H + H2O]+ в масс-спектрах свидетельствует о том, что в процессе элюирования диарилтеллуроксиды подвергаются взаимодействию с водой, являющейся компонентом подвижной фазы, с образованием соответствующих диарилтеллурдигидроксидов. Изменение соотношения интенсивностей ионов [M + H]+ и [M + H + H2O]+ указывает на то, что в системе устанавливается равновесие между двумя формами соединения, которое зависит от концентрации исследуемых соединений.
Взаимодействие с водой, содержащейся в подвижной фазе, при элюировании исследуемых соединений подтверждают также хроматографические данные. При переходе от концентрации 500 мкг/мл к концентрации 5 мкг/мл искажение формы пика наиболее выражено для растворов с концентрациями 50 мкг/мл и 100 мкг/мл (рис. 9). Это указывает на то, что в растворе присутствует два соединения, которые элюируются одновременно.
Рис. 9.
Вид хроматографических пиков диарилтеллуроксидов в зависимости от концентрации раствора (5, 50, 100, 250 и 500 мкг/мл).
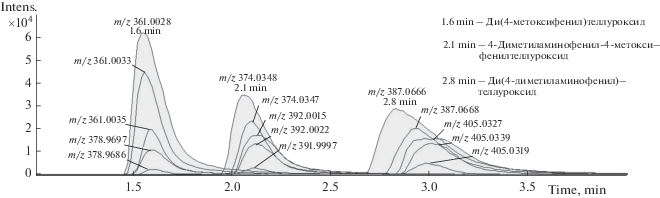
Рост интенсивности пиков [M + H + H2O]+ в масс-спектрах и искажение формы пика для исследуемых диарилтеллуроксидов неодинаково. Так, при концентрации ди(4-метоксифенил)теллуроксида 100 мкг/мл пик [M + H + H2O]+ имеет меньшую интенсивность относительно иона [M + H]+ и искажение формы хроматографического пика менее выражено, чем для 4-диметиламинофенил(4-метоксифенил)теллуроксида и ди(4-диметиламинофенил)теллуроксида при той же концентрации. Выявленная особенность указывает на то, что 4-диметиламинофенил(4-метоксифенил)теллуроксид и ди(4-диметиламинофенил)теллуроксид легче взаимодействуют с водой, чем для ди(4-метоксифенил)теллуроксид. Данный факт объясняется различным электронодонорным эффектом заместителей в ароматическом кольце диарилтеллуроксидов. По сравнению с CH3O-группой (CH3)2N-группа обладает большим электронодонорным эффектом, что усиливает полярность связи Те+–О− и способствует смещению равновесия в описываемой реакции в сторону образования диарилтеллрдигидроксидов.
Установленная особенность существования диарилтеллуроксидов в двух формах в присутствии воды может использоваться при подборе условий синтеза. В частности, путем смещения равновесия реакции гидратации возможно регулирование процессов переноса гидроксильной группы при использовании исследуемых соединений в качестве катализаторов.
ЗАКЛЮЧЕНИЕ
Выделены основные направления фрагментации и образования ионов. В условиях HPLC/MS-ESI для диарилтеллуроксиды образуют стабильные молекулярные ионы, димерные ионы и ассоциаты с компонентами подвижной фазы. Описанные ионы позволяют повысить точность идентификации теллуроксидов в присутствии других классов теллурорганических соединений.
По хромато-масс-спектрометрическим данным установлено, что в силу своей высокой реакционной способности, диарилтеллуроксиды в процессе элюирования обратимо взаимодействуют с водой с образованием органических соединений четырехвалентного теллура и другими компонентами подвижной фазы непосредственно в масс-детекторе при ионизации с образованием ионов-ассоциатов. Выявлено влияние концентрации аналитов в растворе и их структуры, соотношения компонентов подвижной фазы, полярности растворителей на процессы превращения диарилтеллуроксидов при элюировании и образования ионов-ассоциатов при ионизации. Так при элюировании равновесие смещается в сторону реакции гидратации при уменьшении концентрации исходной формы и увеличении электронодонорного эффекта заместителей в структуре диарилтеллуроксидов. Также показано, что образование ионов-ассоциатов с трифторуксусной кислотой и метанолом в масс-детекторе и отсутствие взаимодействия с данными компонентами в процессе элюирования обусловлено значительно более низким содержанием в подвижной фазе трифторуксусной кислоты и меньшей полярностью связи O–H в метаноле по сравнению с водой и ТФУ.
При идентификации диарилтеллуроксидов соединений по масс-спектрам необходимо учитывать форму существования вещества в растворе и все возможные факторы, влияющие образование ионов при ионизации, так как это оказывает непосредственное влияние на вид масс-спектров.
Список литературы
Srivastava K., Panda A., Sharma S., Singh H.B. // J. Organomet. Chem. 2018. V. 861. P. 174.
Petragnani N. Tellurium in organic synthesis. Netherlands: Academic Press, 2007. 372 p.
Bruins A.P. // Mass Spectrom. Rev. 1991. V. 10. № 1. P. 53.
Eliseeva E.V., Red’kin N.A., Gar’kin V.P., Pytskii I.S., Buryak A.K. // Protection of Metals and Physical Chemistry of Surfaces. 2015. V. 51. № 6. P. 1050.
Sorokin A.A., Gar’kin V.P., Red’kin N.S., Buryak A.K. // Russ. J. Appl. Chem. 2010. V. 83. № 12. P. 2163.
Gar’kin V.P., Rodina T.A., Solovova N.B., Buryak A.K. // Russ. J. Phys. Chem. A. 2008. V. 82. № 6. P. 881.
Елисеева Е.В., Сорокин А.А., Редькин Н.А., Гарькин В. // Сорбционные и хроматографические процессы. 2014. Т. 14. № 4. С. 621.
Irgolic K.J. Organotellurium compounds. Stuttgart: Georg ThiemeVerlag, 1990. 1004 p.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов