Физикохимия поверхности и защита материалов, 2019, T. 55, № 6, стр. 657-664
Ионные жидкости на основе цианопропильных катионов в качестве высокополярных неподвижных фаз для капиллярной газовой хроматографии
М. В. Шашков 1, *, В. Н. Сидельников 2
1 ФГБУН Институт катализа им. Г.К. Борескова Сибирского отделения Российской академии наук
Новосибирск, просп. Лаврентьева, 5, Россия
2 ФГАОУ ВПО Национальный исследовательский Новосибирский государственный университет
Новосибирск, ул. Пирогова, 2, Россия
* E-mail: shashkov@catalysis.ru
Поступила в редакцию 28.02.2019
После доработки 05.06.2019
Принята к публикации 11.06.2019
Аннотация
Работа посвящена исследованию высокополярных капиллярных колонок с неподвижными фазами на основе ионных жидкостей (ИЖ) с цианопропилсодержащими катионами. Исследовано пять имидазолевых и хинолиниевых цианопропилсдержащих ИЖ. Показана их высокая полярность. Измеренная селективность по Абрахаму показала повышение специфических типов взаимодействия по сравнению с нецианопропильными аналогами. Показана высокая термостабильность до 300°С в особенности для дикатионных ИЖ. Продемонстрированы примеры разделения для одномерной и двумерной газовой хроматографии.
ВВЕДЕНИЕ
Среди методов анализа летучих органических соединений газовая хроматография (ГХ) является наиболее значимым и информативным. Для достижения наилучшего разделения существует набор неподвижных жидких фаз (НЖФ) различной селективности [1]. Благодаря ряду преимуществ наиболее распространенными фазами являются полисилоксановые полимеры. Их селективность зависит от природы бокового заместителя в полисилоксановой цепи. Таким образом, весь спектр хроматографических полярностей (и селективностей) определяется наличием в боковой цепи метильных, фенильных, а также трифторпропилильных и цианопропильных заместителей [1]. Наиболее полярными из этих неподвижных фаз являются те, что содержат цианопропильную группу. Благодаря своей высокой полярности колонки с такими фазами широко применяются для анализа гетеропримесей в неполярных матрицах, для детального анализа ароматических, а также сложных смесей кислородсодержащих, в особенности метиловых эфиров жирных кислот, включая цис/транс изомеры. Большим недостатком и ограничением цианопропилсилоксановых НЖФ является их невысокая термическая стабильность, которая ограничивается пределом 260°С [1–3]. Это существенно ограничивает область их применения и препятствует их использованию при анализе высококипящих продуктов. Другим их недостатком является невозможность изменения типов взаимодействий с разделяемыми веществами, что не позволяет регулировать селективность этих фаз в широком диапазоне. Связано это с тем, что в данном случае селективность определена лишь одним типом групп – цианопропильных. Введение других по природе групп, например фенильных, автоматически снижает полярность таких НЖФ [4]. Поэтому возникает задача поиска новых неподвижных фаз с одновременно высокой полярностью и термической стабильностью, а также с широким доступным набором селективностей.
Недавно было обнаружено, что на роль таких НЖФ подходят ионные жидкости (ИЖ). Среди множества классов ИЖ, когда-либо исследованных в хроматографии [5, 6], наиболее подходящими в качестве НЖФ оказались ИЖ с имидазолевыми, пиридиниевыми, фосфониевыми катионами и (NTf2–)-анионом (бистрифторметилсульфонилимид) [6–8]. НЖФ на основе данных ИЖ имеют термостабильность до 300°С, в то же время их хроматографическая полярность превосходит все традиционные полярные фазы [9, 10]. Другим важным преимуществом этих ИЖ является возможность варьирования структуры путем изменения природы заместителей в катионе. Это позволяет регулировать селективность НЖФ в широких пределах, что дает возможность синтезировать ИЖ наиболее подходящие для решения конкретных аналитических задач [11, 12]. Представляет интерес поиск ИЖ, которые могли быть еще более полярными по сравнению с уже существующими, а также имели новые свойства селективности по отношению к ряду аналитов.
Учитывая, что наличие цианопропильного заместителя приводит к созданию максимально-полярных полисилоксановых НЖФ, возможным путем модификации ИЖ для увеличения их полярности является введение цианопропильного заместителя в структуру катиона. Ранее на примере имидазолевой ИЖ нами было показано, что введение цианопропильной группы действительно позволяет увеличить полярность по сравнению с алкилированными аналогами [13].
В настоящей работе исследованы разделительные возможности имидазолевых и хинолиниевых ИЖ с цианопропильными заместителями, проведено их сравнение с другими типами НЖФ. Показаны возможности капиллярных колонок с цианопропильными ИЖ для решения практических задач одномерной и двумерной газовой хроматографии.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез ИЖ и приготовление колонок
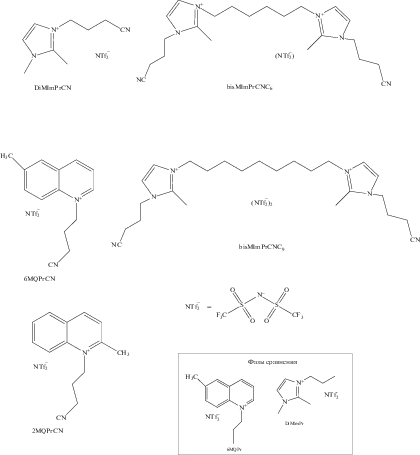
В данной работе были исследованы капиллярные колонки на основе 5 имидазолевых и хинолиниевых ИЖ, структурные формулы которых представлены на рис. 1. В качестве аниона использовали бистрифтор-метилсульфонилимид (NTf2–). Синтез ИЖ проводили по методикам, аналогичным описанных в [13]. Структуру ИЖ и чистоту подтверждали методом Н1-ЯМР.
Приготовление колонок проводили статическим методом низкого давления по методике, описанной в [14]. Для приготовления использовали кварцевый капилляр с полиимидным покрытием диаметром 0.25 мм и длиной 10 м, расчетная толщина пленки готовых колонок составляла 0.2 мкм.
Измерение полярности и селективности
Для измерений индекса полярности по Мак-Рейнольдсу (P.N.) проводили хроматографирование смеси тестовых веществ Мак-Рейнольдса при температуре 120°С: бензол, бутанол, пентанон-2, нитропропан-1, пиридин. Репером мертвого времени служил н-пентан, для вычисления индексов Ковача измеряли удерживание нормальных углеводородов С10–С16. Значения полярности определяли в соответствии со шкалой полярности, использованной в [10], где за нулевое значение полярности принимается сквалан, за 100 – фаза SPB-IL100 (Supelco).
Для расчета параметров модели Абрахама получали данные удерживания для 21 тестового вещества – тех, что использованы в работе [13], дескрипторы (E, S, A, B, L) для которых взяты из [15]. Температура измерений 120°С. Для расчета параметров модели (e, s, a, b, l) применялся метод множественной линейной регрессии с использованием ПО STATISTICA-10.0.228.8.
Измерения полярности и характеристик удерживания, проводили на хроматографе Agilent 7890A c пламенно-ионизационным детектором. Температура детектора и испарителя – 250°С, газ-носитель гелий. Температура термостата – 120°С.
Получение разделений и исследование термостабильности
Исследование термостабильности и получение хроматограмм тестовых смесей и метиловых эфиров жирных кислот проводили на хроматомасс-спектрометре Agilent 7000В c детектором на основе тройного квадруполя. Условия разделения были следующие. Для разделения тестовых смесей: изотермический режим 140°С, скорость потока 0.9 мл/мин (гелий). Для разделения метиловых эфиров жирных кислот: температурная программа термостата колонок: 80°С (3мин), далее программирование со скоростью 7°С/мин до конечной температуры 200°С, скорость потока 1 мл/мин (гелий). Температура испарителя и детектора (ПИД) выставлялась равной конечной температуре анализа.
Для исследования термостабильности термостат колонок нагревали по программе 200°С (30 мин) – далее 10°С/мин до 300°С (15 мин). Для колонки ZB-WAX конечная температура была 250°С.
ГХ/ГХ разделение продуктов газойля каталитического крекинга были выполнены c использованием хроматографа Agilent 7890А и автосамплером G4513A. Был использован потоковый модулятор Agilent и программное обеспечение ZOEX (для визуализации двумерных образов). При получении всех разделений в работе в качестве первой колонки использовали колонку НP-5 длиной 25 м, диаметром 0.25 мм, толщина пленки НЖФ 0.25 µм. В качестве второй колонки использовали колонку ИЖ bisMImPrCNC6 длиной 5 м, диаметром 0.25 мм, толщина пленки НЖФ 0.2 µм. Условия разделения: температурная программа термостата колонок: 70°С (3 мин), далее программирование со скоростью 10°С/мин до конечной температуры 280°С. Температура испарителя и детектора (ПИД) 280°С. Скорость потока газа носителя: для первой колонки (гелий) 1 мл/мин, для второй колонки (водород) 25 мл/мин. Период модуляции составлял 1.5 с.
Оценка полярности и селективности
Наиболее важной характеристикой НЖФ, которая определяет область применения колонок на их основе, является разделительная способность. Разделительная способность в хроматографии связана с двумя факторами: селективностью неподвижной фазы и эффективностью хроматографической колонки [2]. Эффективность в значительной мере зависит от технологий приготовления колонок и в меньшей степени от природы фазы. Что касается селективности, то она напрямую связана с химической природой НЖФ. Объективная численная оценка селективности полярных НЖФ не является простой задачей. Дело в том, что удерживание на полярных фазах определено несколькими различными по природе типами межмолекулярных взаимодействий между фазой и аналитом. Поэтому, для оценки селективности НЖФ требуется модель, которая бы в явном виде учитывала вклад различных межмолекулярных взаимодействий в хроматографическое удерживание.
Существующие ранее способы оценки селективности фаз, основанные на шкале Мак-Рейнольдса [16] и Роршнайдера [17] основаны на удерживании фазой нескольких тестовых соединений. Такой подход даёт возможность сравнить фазы между собой путем и сделать предварительный вывод о селективности колонок. В нашей работе были определены полярности исследуемых колонок по Мак-Рейнольдсу, которые приведены в табл. 1 (последний столбец). Для сравнения здесь же приведены значения полярности для некоторых алкилимидазолевых ИЖ и традиционной полярной фазы на основе полиэтиленгликоля (ZB-WAX) [13]. Видно, что все исследуемые в работе ИЖ являются высокополярными, причем почти все (за исключением bisMPrCNImC9) имеют полярность свыше 90 единиц. Если сравнить их с аналогичными алкилзамещенными ИЖ, то видно, что они являются заметно более полярными. Причем в случае сравнения пропилимидазолевой DiMPrCNIm и цианопропилимидазолевой DiMPrCN разница составляет несколько единиц, то в случае хинолиниевых ИЖ, пара пропилхинолиниевая 6MQPr и цианопропилхинолиниевая 6MQPrCN составляет 20 единиц. Сравнение полярности дикатионных bisMPrCNImC6 и bisMPrCNImC9 указывает на то, что длина алкильного мостика между катионами сильно влияет на полярность, что объясняется увеличением вклада дисперсионных взаимодействий.
Таблица 1.
Параметры модели Абрахама (e, s, a, b, l) и полярность по Мак-Рейнольдсу (P.N.) для колонок на основе цианопропильных ИЖ и фаз сравнения
| e | s | a | b | l | r2 | P.N. | |
|---|---|---|---|---|---|---|---|
| Цианопропильные ИЖ | |||||||
| DiMPrCNIm | 0.25 | 1.81 | 1.25 | 0.3 | 0.35 | 0.999 | 94 |
| bisMPrCNImC9 | 0.35 | 1.57 | 1.22 | 0.29 | 0.41 | 0.999 | 81 |
| bisMPrCNImC6 | 0.31 | 1.63 | 1.23 | 0.35 | 0.31 | 0.999 | 99 |
| 6MQPrCN | 0.27 | 1.70 | 1.28 | 0.59 | 0.37 | 0.999 | 99 |
| 2MQPrCN | 0.23 | 1.65 | 1.39 | 0.15 | 0.35 | 0.999 | 99 |
| Колонки сравнения | |||||||
| DiMPrIm [12] | 0.01 | 1.67 | 1.21 | 0.12 | 0.31 | 0.999 | 88 |
| 6MQPr | 0.22 | 1.58 | 1.20 | 0.52 | 0.41 | 0.999 | 79 |
| ZB-WAX [12] | 0.29 | 1.53 | 2.39 | 0.00 | 0.49 | 0.998 | 51 |
Сравнительно недавно Михаэлем Абрахамом была предложена модель линейной зависимости свободной энергии (ЛЗСЭ), которая учитывает индивидуальные вклады всех типов взаимодействий для каждого из анализируемых веществ [4]. Основой модели является предположение, что свободная энергия взаимодействия между веществом и фазой зависит линейно от каждого из индивидуальных типов взаимодействий. При заданной температуре вместо энергии используют логарифм константы распределения (KL), в итоге базовое уравнение модели выглядит следующим образом [18]:
(1)
$lg{{K}_{L}} = {\text{c}} + {\text{eE}} + {\text{sS}} + {\text{aA}} + {\text{bB}} + {\text{lL}},$Используя данный подход мы провели оценку и вычислили параметры модели, соответствующие различным межмолекулярным взаимодействиям для изучаемых в работе цианопропильных ИЖ. Для сравнения приведены также данные для некоторых алкилимидазолевых ИЖ и традиционной полярной фазы на основе полиэтиленгликоля (ZB-WAX) [13].
Из табл. 1 видно, что для всех цианопропильных ИЖ наблюдаются высокие значения диполь-дипольных взаимодействий (s). Если сравнить их с аналогичными алкилзамещенными ИЖ, то есть сравнить пары DiMPrCNIm–DiMPrIm и 6MQPr– 6MQPrCN, оказывается, что для цианопропилзамещенных они оказываются ощутимо выше. Такая же картина наблюдается и для показателей водородного связывания (a, b). Причем для показателя (а), где фаза выступает как акцептор протона, разница несущественная, в то время как для пары DiMPrCNIm – DiMPrIm показатель (b) отличается более чем в два раза. По показателю ароматических взаимодействий (e) в этой паре также наблюдается разница в селективности – если для DiMPrCNIm показатель (e) имеет значение 0.25, то для DiMPrIm он практически равен нулю 0. По показателю дисперсионных взаимодействий (l) все цианопропильные ИЖ имеют немного большие показатели по сравнению с алкильными аналогами. Однако это несущественно, если учесть что по остальным показателям (e, s, a, b) цианопропильные фазы характеризуются большими значениями межмолекулярных взаимодействий – именно эти взаимодействия отвечают за удерживания полярных аналитов. Если сравнить все исследуемые ИЖ с традиционной полярной колонкой на основе полиэтиленгликоля – ZB-WAX, то можно отметить большую разницу по всем типам взаимодействий как в меньшую (например, l и a), так и в большую (s, b) сторону.
ИЗУЧЕНИЕ ТЕРМИЧЕСКОЙ СТАБИЛЬНОСТИ
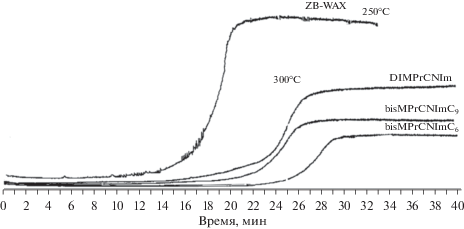
Важным эксплуатационным параметром любой неподвижной фазы является ее максимально допустимая рабочая температура [1]. Дело в том, что при длительном воздействии высокой температурой на НЖФ может происходить ее деструкция и постепенный унос из колонки с потоком газа-носителя. Для оценки термостабильности ИЖ был измерен уровень фонового тока при нагреве колонки в диапазоне 200–300°С. На рис. 2 приведено сравнение подъема уровня фонового тока для колонок с цианопропильными ИЖ и ZB-WAX от температуры.
Из рис. 2 видно, что фазы на основе ИЖ проявляют различную термическую стабильность. Большинство исследуемых НЖФ обладают достаточно хорошей термоустойчивостью, которая выше коммерческой фазы на основе полиэтиленгликоля ZB-WAX, даже несмотря на более высокую температуру. Таким образом, все они позволяют работать при температурах до 300°С. Наиболее низкий фоновый ток показали дикатионные ИЖ bisMPrCNImC9 и bisMPrCNImC6, которые оказались термостабильнее однокатионной ИЖ DiMPrCNIm. Таким образом, как и в случае с алкилзамещенными ИЖ дикатионные оказываются более термостабильны по сравнению со своими однокатиоными аналогами [9].
ПРИМЕРЫ РАЗДЕЛЕНИЙ
Как видно, цианопропильные ИЖ обладают как высокими значениями полярности по Мак-Рейнольдсу, так и проявляют высокие значения специфических взаимодействий. Чтобы наглядно показать как это влияет на разделительную способность колонок с данными фазами, рассмотрим примеры разделения некоторых тестовых и реальных смесей.
Первым примером является тестовая смесь содержащая углеводороды, метиловые эфиры кислот, спирты, а также 2,6-диметилфенол. Примеры хроматограмм для некоторых из изучаемых НЖФ представлены на рис. 3.
Рис. 3.
Разделение тестовой смеси на колонках с цианопропильными ионными жидкостями. 1 – С14, 2 – С15, 3 – нонаналь, 4 – октанол-1, 5 – метилундеканоат, 6 – деканол-1, 7 – метилдодеканоат, 8 – 2,6-диметилфенол. Температура 140°С.
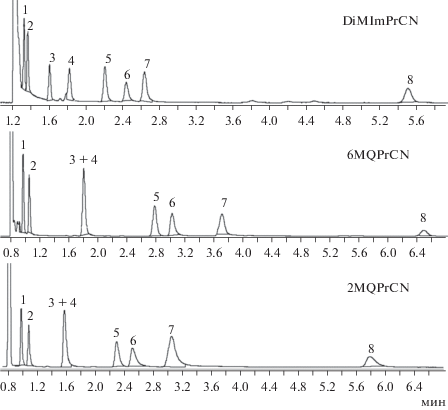
Из рис. 3 видно, что все ИЖ характеризуются плохим удерживанием углеводородов С15–С16 по равнению с полярными соединениями. Они выходят намного раньше чем полярные соединения, находящиеся в тестовой смеси. Например, нонаналь и октанол-1 выходят после них, хотя имеют на 6–7 атомов углерода меньше чем углеводороды С15–С16. Это говорит о высокой полярности рассматриваемых НЖФ. Также можно отметить сильное удерживание 2,6-диметилфенола относительно всех остальных компонентов смеси. При сравнении различных ИЖ между собой можно отметить различную селективность по отношению к паре октанол-1 – нонаналь. На хинолиниевых ИЖ они не делятся, а вот на имидазолевой ИЖ DiMimPrCN хорошо разделены. Это объясняется тем, что для этой ИЖ характерно более высокое значение коэффициента (a), отвечающего за образование водородной связи (см. табл. 1) по сравнению с остальными рассматриваемыми ИЖ.
Рассмотрим примеры разделения реальных смесей. Как известно, одним из важных приложений высокополярных фаз является разделение метиловых эфиров жирных кислот [20]. Это имеет значение для оценки качества и состава пищевых продуктов, а также для исследований метаболических профилей живых организмов [21, 22]. На рис. 4 представлена хроматограмма эфиров жирных кислот, полученных из одноклеточных водорослей.
Рис. 4.
Разделение метиловых эфиров жирных кислот микроводорослей Chlorella Sorokiniana на колонке с bisMImPrCNC6. Условия: программирование 80–200°С со скоростью 7°/мин колонка 20 м × 0.25 мм × 0.25 мкм.
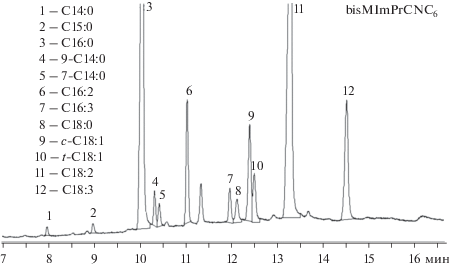
На рис. 4 видно хорошее разделение эфиров, включая позиционные изомеры пальмитолеиновой кислоты (пики 4, 5) и цис/транс изомеры олеиновой кислоты (пики 9, 10). Это показывает преимущества данной колонки, так как обычно разделение цис/транс изомеров метиловых эфиров требует не только наиболее полярных цианопропилсилоксановых НЖФ, но и использование колонок большой длины (до 100 м) [23]. В то время как в нашем случае разделение получено на колонке 20 м, что позволяет провести разделение за существенно меньшие времена.
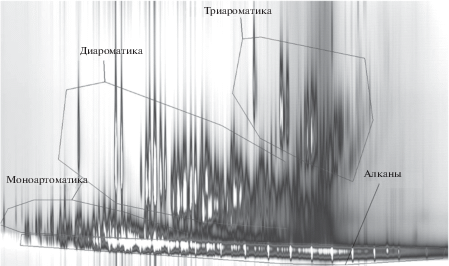
Еще одной областью применения колонок на основе ИЖ является двумерная хроматография (ГХ/ГХ). Данный метод позволяет объединить разделительные возможности двух колонок различной селективности [24]. Процедура разделения в двумерной хроматографии заключается в следующем. На первой, длинной колонке, происходит разделение пробы с максимально возможной эффективностью. В течение процесса разделения на первой колонке, небольшие порции элюента прошедшие первую колонку попадают в устройство, называемое модулятором. В модуляторе эти порции накапливаются в течение короткого времени (около 2 с) и затем поступают во вторую колонку, где происходит их быстрое разделение в течение этих 2 с. Полученные результаты представляют в виде двумерного образа, пример которого приведен на рис. 5. Для достижения наилучшего разделения необходимо использовать две колонки с наиболее отличными характеристиками полярности и селективности. Идеальной ситуацией является использование пары – неполярная/высокополярная колонка. Однако выбор высокополярных колонок ограничивается недостаточной их термической стабильностью. С этой точки зрения ИЖ являются идеальным вариантом как с точки зрения высокой селективности, так и с точки зрения возможности использовать их при высокой температуре и разделять высококипящие нефтепродукты, к примеру, газойль каталитического крекинга нефти. Пример разделения такого образца при использовании высокополярной ИЖ bisDiMPrCNImC6 в качестве второй колонки представлен на рис. 5. Можно видеть не только хорошее разделение между группами ароматики, но и также то, что разделение возможно до высокой температуры 280°С, при этом проявляется подъема уровня фонового тока.
ЗАКЛЮЧЕНИЕ
Известно, что полисилоксановые НЖФ и многие описанные в литературе ИЖ, не содержащие цианогруппу, обладают высокими значениями хроматографической полярности. Показано, что цианопропилимидазолевые ионные жидкости обладают не только более высокой полярностью как по сравнению с известными ИЖ, так и с цианопропилсилоксановыми НЖФ. Кроме того, изученные в работе ИЖ обладают другими типами взаимодействий с разделяемыми веществами. Помимо высокой полярности и уникальной селективности колонки с изученными фазами на основе ИЖ обладают высокими значениями термостабильности по сравнению с цианопропильными полисилоксанами. В том случае, если цианопропильный заместитель введен в катион дикатионных ИЖ, то это приводит к дальнейшему увеличению термостабильности колонок что позволяет проводить высокотемпературные разделения методом двумерной хроматографии вплоть до температуры 300°С.
Работа выполнена в рамках государственного задания института катализа СО РАН.
Список литературы
Rotzsche H. Stationary Phases in Gas Chromatography. Elsevier Science, 1991.
Scott R.P.W. Principles and Practice of Chromatography. 2002.
Gu Q. et al. // J. Chromatogr. A. 2011. V. 1218. № 20. P. 3056–3063.
Abraham M.H., Poole C.F., Poole S.K. // J. Chromatogr. A. 1999. V. 842. № 1–2. P. 79–114.
Shashkov M.V., Sidel’nikov V.N. // Russ. J. Phys. Chem. A. 2011. V. 86. № 1. P. 138–141.
Yao C., Anderson J.L. // J. Chromatogr. A. 2009. V. 1216. № 10. P. 1658–1712.
Anderson J.L., Armstrong D.W. // Anal. Chem. 2005. V. 77. № 19. P. 6453–6462.
Shashkov M.V., Sidelnikov V.N. // J. Struct. Chem. 2014. V. 55. № 5. P. 980–985.
Shashkov M.V., Sidelnikov V.N. // Anal. Bioanal. Chem. 2012. V. 403. № 9.
Supelco; Sigma-Aldrich. Supelco Ionic Liquid GC Columns: Introduction to the Technology // Supelco Ion. Liq. GC Columns. 2014. P. 42.
Shashkov M.V., Sidelnikov V.N. // J. Sep. Sci. 2016. V. 39. № 19.
Twu P. et al. // J. Chromatogr. A. 2011. V. 1218. № 31. P. 5311–5318.
Shashkov M.V., Sidelnikov V.N. // J. Chromatogr. A. 2013. V. 1309. P. 56–63.
Anderson J.L., Armstrong D.W. // Anal. Chem. 2003. V. 75. № 18. P. 4851–4858.
Ulrich S., Brown T.N., Watanabe N., Bronner G., Abraham M.H., Goss K.-U.N.E. UFZ-LSER database v 3.2 [Internet]. Leipzig, Deutschland, Helmholtz Zentrum für Umweltforschung – UFZ, 2017.
McReynolds W.O. // J. Chromatogr. Sci. 1970. V. 8. № 12. P. 685–691.
Rohrschneider L. // Anal. Chem. 1973. V. 45. № 7. P. 1241–1247.
Poole C.F., Poole S.K. // J. Chromatogr. A. 2008. V. 1184. № 1–2. P. 254–280.
Callihan B.K., Ballantine D.S. // J. Chromatogr. A. 2000. V. 893. № 2. P. 339–346.
Ragonese C. et al. // Anal. Chem. 2009. V. 81. № 13. P. 5561–5568.
Piligaev A.V. et al. // Bioresour. Technol. 2018. V. 250.
Delmonte P. et al. // J. Chromatogr. A. 2012. V. 1233. P. 37–146.
Ratnayake W.M.N., Hansen S.L., Kennedy M.P. // JAOCS. 2006. № 3. P. 475–488.
Shashkov M.V., Sidel’nikov V.N. // Prot. Met. Phys. Chem. Surf. 2015. V. 51. № 6.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов