Физикохимия поверхности и защита материалов, 2020, T. 56, № 4, стр. 428-434
Морфологические и структурные изменения диоксида титана в процессе фрагментации
Ю. В. Кузьмич 1, Л. Г. Герасимова 1, *, М. В. Маслова 1, Е. С. Щукина 1
1 Институт химии и технологии редких элементов и минерального сырья им. И.В. Тананаева – обособленное подразделение Федерального государственного бюджетного учреждения науки Федерального
исследовательского центра “Кольский научный центр Российской академии наук”
184209 Мурманская область, Апатиты, Россия
* E-mail: gerasimova@chemy.kolasc.net.ru
Поступила в редакцию 24.06.2019
После доработки 22.10.2019
Принята к публикации 29.10.2019
Аннотация
С помощью рентгеновского дифракционного анализа и метода БЭТ, основанного на адсорбции–десорбции N2, изучены структурные и морфологические изменения частиц диоксида титана в процессе ультратонкой фрагментации. По уширению дифракционных рефлексов методом аппроксимации с применением функции псевдо-Фойгта рассчитаны размеры кристаллитов и микродеформаций, свидетельствующие о нарушении их структурного порядка с образованием фрагментов новой фазы, схожей с брукитом. При изучении морфологии частиц титановых фаз, установлено, что после механической активации в присутствии ПАВ адсорбция азота описывается изотермой типа IVa в области значений р/р0 0.1–0.95 и изотермой типа II при р/р0 выше 0.95. Петля гистерезиса изотерм образцов относится к типу Н3, что характерно для частиц с пластинчатой морфологией. Пористая система частиц представлена мезопорами с диаметром, изменяющимися в пределах 20–50 нм. Общий объем микропор не превышает 10% от их общего объема. Из активированного образца при обжиге формируется монофазный продукт со структурой рутила с увеличением размера кристаллитов. Удельная поверхность диоксида титана после обжига изменяется в пределах 6.5–7.5 м2/г, что примерно в 3 раза превышает этот показатель для традиционных марок рутила.
1. ВВЕДЕНИЕ
Свойства твердых веществ в значительной степени определяются их структурой, ее стабильностью, а также морфологией поверхности частиц. В частности, четырехзарядный диоксид титана существует в виде трех структурных разновидностей – стабильного рутила и метастабильных анатаза и брукита [1–3]. Основой структур этих модификаций являются октаэдры TiO6, которые расположены так, что каждый ион кислорода принадлежит трем октаэдрам. Однако на один октаэдр в рутиле приходится – 2 общих ребра, в анатазе – 4, в бруките – 8. Этот факт влияет на прочность связи кислорода с титаном в кристаллической решетке. У рутила она сильнее, чем у анатаза и брукита. Поэтому рутил устойчив к атмосферным воздействиям и повышенной температуре, что позволяет использовать его в качестве базового наполнителя при изготовлении специальных лакокрасочных материалов для ответственных покрытий, эксплуатируемых в экстремальных условиях, в том числе Арктики, косметики, высококачественной бумаги, а также в составе терморегулируемых клеев и герметиков, используемых в аэрокосмической отрасли [2]. Метастабильный анатаз является хорошим фотокатализатором. Каждая область использования диоксида титана предъявляет требования не только к его структуре, но и к поверхностным характеристикам, которые обеспечивают максимальный эффект при внесении его в состав изделий.
В последние десятилетия интерес к изучению структурных и морфологических особенностей диоксида титана значительно возрос, что связано с его уникальными свойствами. Как правило, свойства TiO2 формируются при проведении его синтеза. Многие из известных методов синтеза (золь–гель, микроволновые, гидротермальные, гидрохимические) сопряжены с определенными трудностями в их реализации, поскольку основаны на процессах, протекающих в жидкофазном режиме, что сопровождается образованием значительного количества стоков, требующих затрат на их утилизацию. Способы, основанные на фрагментации частиц при высокоэнергетическом воздействии, позволяют устранить недостатки “мокрой” химии [4]. Энергетический импульс, приобретенный при фрагментации частиц диоксида титана, может компенсироваться химической реакцией, например, при нанесении на поверхность частиц функциональных покрытий.
Целью настоящих исследований является изучение твердофазных процессов, основанных на механоактивации и термолизе метастабильных оксотитановых фаз, изучение их структурных и морфологических характеристик.
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Метастабильное состояние системы (структуры) – благоприятная основа для направленного воздействия с формированием новых фаз заданного размера частиц с новыми свойствами поверхности и соответственно новым набором свойств. В качестве эффективных факторов воздействия выбрана комбинация из двух последовательных операций обработки: механоактивация и обжиг порошков. В результате высокоэнергетического воздействия достигается уменьшение размера частиц до нанометрового масштаба с образованием новой поверхности и одновременным ростом микродеформации кристаллической решетки с искажением связи между титаном и кислородом. При последующем обжиге удается упорядочить активированную механическим воздействием структуру частиц порошка.
Исходным объектом исследования служил порошок диоксида титана анатазной модификации, который получали из титановой соли – (NH4)2TiO(SO4)2 ⋅ H2O [5]. Соль прокаливали в электрической муфельной печи при температуре 700°С в течение 4 ч. Скорость нагревания до заданной температуры – 10 град/мин [6]. Полученный порошок помещали в планетарную мельницу Pulverisette-7 c емкостями, футерованными титаном, объемом 45 мл. Измельчающие элементы – титановые шары диаметром 10 мм. Скорость вращения рабочих емкостей – 750 об./мин. Массовое отношение шары : порошок = 10 : 1. Продолжительность обработки – 1 ч. Для устранения налипания порошка на стенки и шары добавляли поверхностно-активное вещество (ПАВ) – олеиновая кислота, количество которой варьировали в пределах от 0.5 до 5 мас. %. Активированный порошок подвергали обжигу при 830°С в течение 2 ч.
Исходные, механоактивированные и прокаленные образцы изучались с помощью физико-химических методов. В частности, фазовый состав устанавливали с помощью дифрактометра Shimadzu XRD 6000 с программным обеспечением, разработанном на основе метода Rietveld [7, 8], что позволяет идентифицировать фазы и осуществить оценку размеров частиц по показателю области когерентного рассеяния (ОКР), микронапряжений (ε) и проследить ход трансформационной эволюции фаз нанокристаллических частиц TiO2. Для математического представления отдельных рефлексов дифрактограмм использовали функцию псевдо-Фойгта.
Приведенное уширение находили по выражению β*(2θ) = β(2θ)cos θ/λ [7]. Авторы данной работы по величине экспериментального уширения определяют суперпозицию двух уширений – размерного βs и деформационного βd. Построением зависимости приведенного уширения от вектора рассеяния (s = 2 sin θ/λ) и экстраполяцией уширения на нулевое значение вектора рассеяния определяется размер кристаллита D = 1/β*(2θ = 0). Микродеформацию ε устанавливается по значению наклона зависимости приведенного уширения βd(2θ) = 4ε tg θ, ε = Δd/d, где Δd – изменение межплоскостного расстояния, d – межплоскостное расстояние.
Морфологические характеристики порошков (удельная поверхность, объем и размер пор) определяли на приборе TriStar 3020 Micromeritics (США) по показателям сорбции-десорбции азота.
3. РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
По результатам рентгеновского дифракционного анализа (дифрактограммы на рис. 1, 2) удалось пронаблюдать структурный генезис диоксида титана при его ультратонкой фрагментации и при последующем обжиге полученного порошка.
Рис. 1.
Дифрактограммы исходного анатаза и образцов после его механической активации при скорости 750 об./мин и продолжительности – 2 ч, добавка ПАВ, мас. %; 1 – исходный анатаз; 2 – 0.5; 3 – 2.5; 4 – 5. ⚪ – анатаз; + – брукит.
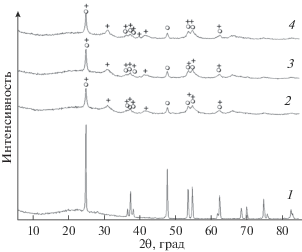
Рис. 2.
Дифрактограммы образцов после механоактивации и прокаливания при 830°С в течение 3 ч. Добавка ПАВ, мас. %; 1 – 0.5; 2 –2.5; 3 - 5; ⚪ – анатаз; ⬜ – рутил.
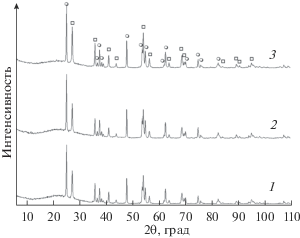
Влияние механического воздействия на частицы анатаза с заданной добавкой ПАВ (0.5–5 мас. %) проявляется в снижении интенсивности дифракционных рефлексов на дифрактограммах, а также в появлении рефлексов новой фазы подобной брукиту. Уширения рефлексов, их смещение и перекрытие несколько затрудняют идентификацию фаз диоксида титана. Например, рефлексы анатаза (101) и брукита (120), (111) взаимно перекрываются. Однако некоторые рефлексы (002) указывают на структурную конверсию кристаллитов анатаза в фазу брукита.
Обжиг порошков после механоактивации при 830°С приводит к повышению кристалличности порошков с параллельным преобразованием нестабильной фазы по схеме: брукит–анатаз–рутил (рис. 2).
Результаты расчета размера кристаллитов и величины микронапряжений, приведенные в табл. 1, свидетельствуют о том, что после механоактивации кристаллиты диоксида титана приобретают достаточно высокую степень деформационных изменений (ε до 1.14%). Повышение расхода ПАВ до 2.5 и 5 мас. % сопровождается снижением этого показателя в 2 раза. При этом степень деформации анатаза изменяется незначительно ε – 0.22–0.3%. Размер частиц кристаллитов анатаза и брукита изменяется от 18 до 27 нм. В образце после обжига превалирующей (более 90%) является фаза рутила. Перестройку структуры с ее уплотнением и увеличением размера кристаллитов претерпевают активированные фаза брукита и анатаза. По-видимому, увеличение продолжительности прокаливания будет способствовать снижению количества примеси анатаза в образце.
Таблица 1.
Размер области когерентного рассеяния и величины микронапряжений
| Скорость 750 об./мин, без обжига | ||||||
|---|---|---|---|---|---|---|
| Добавка ПАВ, мас. % | 1 | 2.5 | 5 | |||
| Показатели | ОКР, нм | ε, % | ОКР, нм | ε, % | ОКР, нм | ε, % |
| Анатаз | 27 | 0.30 | 25 | 0.22 | 21 | 0.24 |
| Брукит | 21 | 1.14 | 21 | 0.58 | 18 | 0.52 |
| Скорость 750 об./мин, обжиг при 830°С, продолжительность – 3 ч | ||||||
| Добавка ПАВ, мас. % | 1 | 2.5 | 5 | |||
| Показатели | ОКР, нм | ε, % | ОКР, нм | ε, % | ОКР, нм | ε, % |
| Рутил | 33 | 0.03 | 37 | 0.015 | 41 | 0.045 |
| Анатаз | 51 | 0.01 | 56 | 0.02 | 54 | 0.035 |
Влияние механоактивации на морфологию частиц диоксида титана (показатели удельной поверхности и общего объема пор) устанавливали по результатам адсорбции-десорбции азота по методам BET [9, 10], BJH [9, 11] и t-метод (Harkins-Jura) [12, 13].
Показано, что изучаемые объекты содержат весь спектр нанопор: микропоры (<2 нм), мезопоры (2–50 нм) и макропоры (>50 нм) [14]. Изотермы адсорбции-десорбции азота для образцов диоксида титана (рис. 3), построенные с использованием метода BET, позволяют охарактеризовать их на основании классификации IUPAC как тип IVa в области значений р/р0 от 0.1 до 0.95, а при р/р0 выше 0.95 изотермы относятся к типу II.
Рис. 3.
Изотермы адсорбции-десорбции частиц диоксида титана после фрагментации. Условия – 750 об./мин, 2 ч. Прокаливание при 830°С, время – 3 ч. Пунктирная линия при добавке ПАВ – 5 мас. %, сплошная линия – 0.5 мас. %.

Согласно теории BET, для описания изотермы используют линейное уравнение [14]:
Как видно из рис. 3 у обоих образцов в начале изотермы отсутствует выраженное “колено” (точка В), что объясняется процессом многослойной адсорбции, маскирующей начальный однослойный процесс. Такое поведение изотермы на начальном участке происходит при низком параметре С, что и препятствует точной интерпретации удельной емкости монослоя. Характерное отличие от традиционных изотерм [15] – это линейность графика, которое соблюдается в интервале от 0.05 до 0.55 р/р0. В области относительных давлений выше диапазона линейности изотерма приобретает резкую крутизну, что является признаком узкого распределения мезопор по размеру.
Петля гистерезиса на изотермах обеих образцов относится к типу Н3. Петли подобного типа отличаются следующими особенностями: ветвь адсорбции напоминает изотерму типа II; нижний предел ветви десорбции находится в кавитационно-индуцированном интервале значений относительного давления, что характерно для пластинчатых частиц с мезо- и макропорами. Характер петли гистерезиса позволяет утверждать, что исследуемые частицы диоксида титана после механической активации имеют пластинчатую структуру, что подтверждает данные полученные нами ранее [16].
Резкий рост изотермы в области петли гистерезиса (0.8 < р/р0 < 1.0) объясняется большой внешней поверхностью и наличием значительной мезопористости, началом поровой конденсации в крупных порах. Если отсутствует влияние стенок пор и краевые эффекты (мезопоры близкие к размеру 50 нм и макропоры) на частицы адсорбата (азот), то сорбция происходит по типу многослойного покрытия площади. На это также указывает отсутствие плато после верхнего края петли гистерезиса. Поры заполняются без образования полусферического мениска и продолжается многослойная конденсация на поверхности, как на беспористой поверхности.
При всех прочих равных параметрах процесса механической активации (рис. 3) количество введенного ПАВ оказывает следующее влияние на сорбционную емкость продукта: при добавке 0.5 мас. % удельная адсорбция при р/р0 = 1 достигает 25.5 см3/г, а при 5 мас. % – 31.9 см3/г.
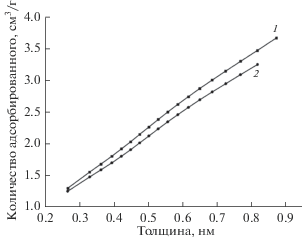
График ВЕТ (рис. 4) линеен в диапазоне относительных давлений от 0.05 до 0.30 р/р0, это позволяет утверждать, в данном случае расчет удельной поверхности образцов после механической активации проведен с достаточной достоверностью (табл. 2).
Рис. 4.
Линии ВЕТ для образцов после механической активации. Условия – 750 об./мин, 2 ч. Прокаливание при 830°С, время – 3 ч. 1 – 0.5 мас. % ПАВ, 2 – 5 мас. % ПАВ.

Таблица 2.
Результаты исследования морфологии частиц исследуемых образцов различными методами
| Метод | Параметр | Образец TiO2, количество ПАВ, мас. % | ||
|---|---|---|---|---|
| 1 | 2.5 | 5 | ||
| Метод ВЕТ | Удельная площадь поверхности (Одноточечный метод) при р/р0 = 0.297, м2/г | 6.5414 | 7.5971 | 6.975 |
| Удельная площадь поверхности (Многоточечный метод) при р/р0 = 0.05–0.3, м2/г | 6.6317 | 7.7233 | 7.0925 | |
| Средняя ширина пор адсорбции, нм | 7.84 | 7.71 | 8.06 | |
| Общий объем адсорбирующих пор с диаметром пор менее 40 нм, при р/р0 = 0.297 (Одноточечный метод), см3/г | 0.013 | 0.015 | 0.014 | |
| Метод BJH, с поправкой Halsey | Адсорбционный совокупный объем пор частиц диаметром (Vads ) – 1.7 нм – 300 нм, см3/г | 0.039452 | 0.042407 | 0.049339 |
| Десорбционный совокупный объем пор частиц диаметром(Vdes) – 1.7 нм – 300 нм, см3/г | 0.039463 | 0.042435 | 0.049354 | |
| Средний диаметр пор (по адсорбции) Dads, нм | 23.6336 | 21.8616 | 26.9504 | |
| Средний диаметр пор (по десорбции) Ddes, нм | 22.84 | 21.3439 | 26.1151 | |
| Корректирующее уравнение Halsey: t = 3.54[–5/ln(p/p0)]0/333 [20] | ||||
| Метод t-графика, с уравнением Harkins–Jura | Точка пересечения с ординатой (Y0), см3/г | 0.210606 | ||
| Объем микропор (V), см3/г | 0.000326 | 0.000268 | 0.000266 | |
| Наклон t-графика (f), см3/г нм | 3.846004 | |||
| Внешняя площадь поверхности (S), м2/г | 5.949 | 7.1318 | 6.5143 | |
| Площадь микропор (Sмикр), м2/г | 0.6827 | 0.5915 | 0.5782 | |
| Количество адсорбированного N2, при р/р0 = 0.665, см3/г | 3.2626 | 3.8017 | 3.4839 | |
| Уравнение Harkins–Jura для определения толщины слоя: t = [13.99/(0.034–lg(p/p0))]0/5 [10] | ||||
Используя t-метод Harkins-Jura [16, 17] были определены площади поверхности образцов после фрагментации частиц диоксида титана и сделана оценка объема микропор. На рис. 5 приведены графики для двух образцов полученных при расходе ПАВ 0.5 и 5 мас. %. Для расчета стандартного t-графика использовано уравнение Harkins-Jura преобразованное De Boer J.H. [11, 18]: t = [13.99/(0.034 – lg(p/p0))]0/5. Объем микропор определяется по выражению [13]: V = Y0 × × 0.001547, см3/г, где Y0– точка пересечения с ординатой t-графика, эквивалентная объему микропор; коэффициент 0.001547 – появляется при пересчете объема газа в объем жидкости. Используя значение наклона t-графика можно определить внешнюю поверхность адсорбента: S = f × × 1.547, м2/г, где f – наклон t-графика, см3/г нм.
Рис. 5.
Вид t-графика для двух образцов после механической активации диоксида титана с добавкой ПАВ 1 – 5 мас. %; 2 – 0.5 мас. %.
Полученные данные по площади внешней поверхности позволяют оценить площадь микропор, используя значение общей поверхности адсорбции:
Метод, разработанный Barrett-Joyner-Halenda (BJH) [15] для определения объема и площади мезопор в результате модифицирования уравнения Kelvin’а, обладает определенными достоинствами и широко используется. Однако при этом следует отметить, что по данным Di Renzo [12, 19] кривая распределения пор по размерам BJH смещена в сторону меньших диаметров пор по сравнению с результатами метода основанного на современной теории нелокального функционала плотности (nonlocal density functional theory – NLDFT) примерно на 25% в широком диапазоне изменения диаметра пор.
В работе мы пользовались методом BJH. Для расчета размера пор использовали выражение, предложенное авторами [15]: D = 4 × 103 × Vcum/Scum, где Vcum и Scum – кумулятивные объем и площадь пор, соответственно.
Как видно, в обоих случаях (1 и 5 мас. % ПАВ) зависимость объема пор от среднего размера пор имеет два максимума – первый в области 3 нм, второй в области 30 нм. Однако характер хода зависимости позволяет высказать предположение о том, что в исследуемых объектах имеются как микропоры (менее 2 нм), так и макропоры (более 50 нм). Количественная оценка пор в данных диапазонах ограничена техническими характеристиками прибора TriStar 3020 Micromeritics (США).
Рис. 6.
Зависимость объема пор от диаметра пор. Десорбция азота на частицах диоксида титана после механической активации в присутствии: (а) 0.5 мас. %; (б) 5 мас. % ПАВ.

В табл. 2 сведены результаты, полученные при изучении различными способами поверхностных свойств образцов диоксида титана после фрагментации с различной добавкой ПАВ и их последующего обжига.
ВЫВОДЫ
С помощью РФА показано, что в условиях механоактивации анатаза формируются фрагменты новой фазы схожей с брукитом. При обжиге активированных образцов удается упорядочить структуру кристаллитов. При этом примерно в 2 раза увеличивается их размер, и диоксид титана приобретает структуру рутила. При обжиге неактивированного анатаза такая конверсия достигается лишь при длительном прокаливании при 900°С.
По уширению дифракционных рефлексов методом аппроксимации с применением функции псевдо-Фойгта найдены величины размера кристаллитов (ОКР) и микродеформаций (ε). После механоактивации без обжига размер кристаллитов не превышает 20 нм, после обжига – 40 нм. Аналогичная зависимость характерна и для величины микронапряжения.
При изучении поверхностных свойств титановых фаз, установлено, что после механической активации в присутствии ПАВ адсорбция азота описывается изотермой типа IVa в области значений р/р0 0.1–0.95, при р/р0 выше 0.95 изотермы относятся к типу II. Петля гистерезиса изотерм образцов относится к типу Н3, что характерно для частиц с пластинчатой морфологией. Пористая система частиц представлена мезопорами с диаметром, изменяющимся в пределах 20–50 нм. Общий объем микропор не превышает 10% от общего объема.
Удельная поверхность диоксида титана после обжига изменяется в пределах 6.5–7.5 м2/г, что примерно в 3 раза превышает этот показатель для диоксида титана, полученного по традиционной технологии.
Список литературы
Guoma P.I., Mills M.J. // J. Am. Ceram. Soc. 2001. V. 84. Is. 3. P. 619–622.
Salari M., Rezaee M., Mousavikoie S.M., Marashi P., Aboutalebi H. // International J. Modern Physics B. 2008. V. 22. № 18n19. P. 2955–2961.
Muscat J., Swamy V., Harrison N.M. // Physical Review B. 2002. V. 65. 224112. P. 224112-1–224112-15.
Raiender G., Giri P.K. // J. Alloys and Compounds. 2016. V. 676. P. 591–600.
Герасимова Л.Г., Маслова М.В., Щукина Е.С. // Химическая технология. 2008. № 6. С. 241–244.
Патент 2613509 РФ, МПК С01G 23/047, B82B 3/00 (2006.01). Способ получения диоксида титана / Герасимова Л.Г., Кузьмич Ю.В., Николаев А.И., Щукина Е.С., Киселев Ю.Г.; Ин-т химии и технологии редких элементов и минер. сырья Кол. науч. центра РАН. № 2015151982/05; заявл. 03.12.15; опубл. 16.03.17. Бюл. № 8.
Кожевников Н.С., Курлов А.С., Урицкая А.А., Ремпель А.А. // Журн. структурной химии. 2004. № 45. С. 156–161.
Курлов А.С., Гусев А.И. // Физика и химия стекла. 2007. Т. 33. № 3 С. 383–392.
Mingming Wei, Li Zhang, Yongqiang Xiong, Jinhua Li, Ping’an Peng // Microporous and Mesoporous Materials. 2016. V. 227. P. 88–94.
Harkins W.D., Jura G. Surfaces of Solids. XIII // J. American Chemical Society. 1944. V. 66. Is. 8. P. 1366–1373.
De Boer J.H., Lippens B.C., Linsen B.G. et al. // J. Colloid and Interface Science. 1966. V. 21. Is. 4. P. 405–414.
Di Renzo F., Galarneau A., Trens P., Tanchoux N., Fajula F. // Studies in Surface Science and Catalysis. 2002. V. 142. P. 1057–1066.
Neimark A.V., Ravikovitch P.I., Vishnyakov A. // J. Physics: Condensed Matter. 2003. V. 15. № 3. 1. 347. P. 347–367.
Brunauer S., Emmett P.H., Teller E. // J. Am. Chem. Soc. 1938. 60(2). P. 309–319.
Barrett E.P., Joyner L.G., Halenda P.P. // J. American Chemical Society. 1951. V. 73. № 1. P. 373–380.
Thommes M., Kaneko K., Neimark A.V., Olivier J.P., Rodriguez-Reinoso F., Rouquerol J., Sing K.S.W. // Pure Appl. Chem. 2015. V. 87. Is. 9–10. P. 1051–1069.
Вячеславов А.С., Ефремова М. Определение площади поверхности и пористости материалов методом сорбции газов (Методическая разработка) Московский государственный университет имени М.В. Ломоносова, Факультет наук о материалах. М., 2011. 65 с.
Валеева А.А., Петровых К.А., Шретнер Х., Ремпель А.А. // Неорганические материалы. 2015. Т. 51. № 11. С. 1221–1227.
Lu H.M., Zhang W.X., Jiang Q. // Advanced Engineering Materials. 2003. V. 5. Is. 11. P. 787–788.
Zhang H., Banfield J.F. // The J. Physical Chemistry B. 2000. V. 104. Is. 15. P. 3481–3487.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов


