Физикохимия поверхности и защита материалов, 2022, T. 58, № 4, стр. 350-360
Динамика изменения скорости и механизма разрушения композиционного материала на основе углерода и керамики
Н. И. Сидняев *
Московский государственный технический университет им. Н.Э. Баумана
105005 Москва, 2-я Бауманская, 5, стр. 1, Россия
* E-mail: Sidnyaev@yandex.ru
Поступила в редакцию 22.09.2021
После доработки 14.03.2022
Принята к публикации 05.04.2022
- EDN: TWYFOU
- DOI: 10.31857/S0044185622040210
Аннотация
Представлены результаты исследований разрушения композиционных материалов, где основное внимание уделяется окрестности точки торможения, так как максимум теплового потока приходится на ее окрестность. Показана сильная зависимость вязкости расплава от температуры, которая приводит к необходимости совместного решения уравнения движения пленки и уравнения сохранения энергии. Постулируется, что учет нестационарности прогрева для полимерных материалов имеет принципиальное значение прежде всего потому, что при равных с другими теплозащитными материалами скоростях уноса массы оплавляющие покрытия имеют большее время установления квазистационарного режима. Сдвигающие силы (трение и градиент давления) в целом слабее возрастают с изменением режима течения в пограничном слое, чем коэффициент теплообмена. Проведен анализ основных закономерностей разрушения полимерных материалов. Показано, что скорость уноса существенно зависит от энтальпии торможения газового потока. Результаты численных расчетов, показывают, что процесс неравновесного уноса массы может быть рассчитан инженерными методами.
1. ВВЕДЕНИЕ
Последние исследования теплозащитных материалов четко разделяют понятия теплостойкости и термостойкости. Теплостойкость – это та предельная температура, по достижении которой, например, полимер теряет свою прочность под действием той или иной нагрузки [1–3]. Под термостойкостью понимается предельная температура, при которой начинаются химические изменения в полимере, отражающиеся на его свойствах, т.е. происходит термическая или термохимическая деструкция полимера [4–7].
Структура полимера во многом определяет его свойства. Полимеры с линейной структурой, как, например, полиэтилен, полистирол, политетрафторэтилен, полиметилметакрилат и др., при нагревании до температуры плавления не теряют своих пластических свойств [3]. При дальнейшем повышении температуры они плавятся и затем цепь макромолекулы постепенно распадается на отдельные звенья. Ввиду того что молекулярная масса конечных продуктов разложения много меньше массы полимера, они в отличие от полимера находятся при температуре разложения в газовой фазе [8–10]. Примером реакции деполимеризации может служить разложение фторопласта-4, начиная с 670 К: ${{\left( {{{{\text{C}}}_{2}}{{{\text{F}}}_{4}}} \right)}_{n}}$(фторопласт-4) $ \to n{{{\text{C}}}_{2}}{{{\text{F}}}_{4}}$ (тетрафторэтилен), а термодеструкция – разложение полиэтилена начиная с 570 К: ${{{\text{(C}}{{{\text{H}}}_{2}})}_{n}} \to {{({\text{C}}{{{\text{H}}}_{2}})}_{{{{n}_{1}}}}} + {{({\text{C}}{{{\text{H}}}_{2}})}_{{{{n}_{2}}}}} + ...$, где ${{n}_{1}}$, ${{n}_{2}}$ и т. д. в среднем равны 50, т. е. средняя молекулярная масса продуктов распада близка к 700.
Процесс термической деструкции полимеров представляет собой совокупность гомогенных и гетерогенных химических реакции и фазовых превращений, сопровождающихся обычно поглощением тепла и потерей массы за счет выделения летучих продуктов разложения [11–14]. Как известно, все химические реакции делятся на гомогенные, протекающие в объеме, и гетерогенные, протекающие на поверхности раздела между фазами [15–18 ]. Оба типа реакций характеризуются своей скоростью, зависимость которой от концентрации веществ описывается степенным законом (закон действующих масс):
(1)
$ - \frac{{\partial {{\rho }_{A}}}}{{\partial \tau }} = K\rho _{A}^{\alpha }\rho _{B}^{\beta } \ldots .$Здесь α, β стехиометрические коэффициенты веществ А и В. Скорость реакции пропорциональна произведению концентрации реагирующих веществ в соответствующих степенях. Константа скорости реакции K зависит от температуры в соответствии с законом Аррениуса:
где L – предэкспонентный множитель, моль/с; R – универсальная газовая постоянная, кДж/моль К; T – температура реагирующих веществ, K; E – энергия активации реакции, кДж/моль, определяемая обычно из эксперимента. В химической кинетике показатели при концентрациях могут не соответствовать стехиометрическим коэффициентам, т.е. числу молекул данного вещества, участвующих в реакции. При гетерогенной деструкции, протекающей с выделением газообразных продуктов, которые диффундируют из зоны реакции к внешней поверхности материала, а затем десорбируют во внешнюю среду, скорость разложения будет определяться скоростями трех процессов: скоростью химической реакции; скоростью отвода газообразных продуктов из зоны реакции и скоростью их десорбции с внешней поверхности [14–17]. Скорость процесса в целом всегда определяется наиболее медленными его стадиями, при невысоких давлениях десорбция газа происходит гораздо быстрее, чем два первых процесса, т.е. скорость разложения будет определяться скоростью собственно химической реакции и скоростью диффузии газообразных продуктов внутри материала. В том случае, если лимитирующей стадией процесса является диффузия, кажущаяся кинетика реакции будет описываться уравнениями диффузии и, следовательно, не будет отражать скорости собственно химической реакции. В этом случае говорят, что процесс протекает в диффузионной области. Чаще всего он описывается уравнением реакции первого порядка, так как скорость диффузии прямо пропорциональна концентрации вещества в объеме [3]. В диффузионной области кинетика процесса не имеет ничего общего с истинной кинетикой гетерогенных химических реакций. Если скорость химической реакции значительно меньше скорости диффузии, то скорость процесса в целом будет определяться скоростью собственно химической реакции. В этом случае говорят, что процесс протекает в кинетической области и описывается уравнением химической кинетики той реакции, которая протекает на поверхности. Для полимеров скорость деструкции в общем случае определяется только кинетикой процесса разложения, которая зависит от интенсивности теплового воздействия. Обычно полагают, что во всем температурном диапазоне деструкции зависимость скорости разложения от температуры и массы материала описывается уравнением такого же вида, что и уравнение для скорости гомогенной химической реакции:Функция $f(\rho )$ характеризует механизм разложения вещества и чаще всего задается в виде простой степенной зависимости: $f(\rho ) = \rho n$, где n – порядок реакции. Учитывая это выражение и соотношение (1), (2), получаем кинетическое уравнение процесса термического разложения в виде
(4)
$g = - \frac{{\partial \rho }}{{\partial \tau }} = K\exp \left( {\frac{E}{{RT}}} \right){{\rho }^{n}}.$Согласно кинетическому уравнению плотность материала ρ на внешней поверхности уменьшается за счет термодеструкции, при этом соответственно уменьшается и g. В пределе ρ должно стремиться к нулю. На практике этого не наблюдается, что связано, вероятно, с резким уменьшением вязкости расплава термопластов с температурой $\mu = K{{(T)}^{{ - n}}}$, где п = 15–30, и заполнением пустот полимера, находящегося в вязкотекучем состоянии. Продукты деструкции покидают материал путем диффузии, но плотность вещества в зоне разложения в результате подтекания расплавленного полимера остается примерно постоянной. Нетрудно показать, что чем выше температура, тем сильнее зависимость концентрации реагирующего вещества от времени, т.е. продолжительность реакции уменьшается с ростом температуры.
2. ПОСТАНОВКА ЗАДАЧИ
Физическим прототипом данной расчетной модели является процесс оплавления кристаллических материалов при интенсивном нагреве высокоскоростным потоком [1–5]. В самом характере нагрева четко различаются два периода. В первом температура поверхности монотонно возрастает, пока не достигнет температуры разрушения. На этом отрезке задача ничем не отличается от рассмотренных в работах [6–9]. В частности, с их помощью легко рассчитать время достижения начала разрушения поверхности, а также профиль температуры в теле, который сформируется к этому моменту. Достигнув температуры разрушения, кристаллические вещества плавятся и практически мгновенно сносятся в виде тончайшей жидкой пленки набегающим потоком газа. Небольшие толщины пленки расплава на кристаллических телах обусловлены низкой вязкостью расплава. Предполагается, что температура внешней поверхности пленки практически не отличается от температуры разрушения поверхности, соответствующей внутренней границе пленки расплава. Как температура разрушения, так и сопровождающий его тепловой эффект остаются постоянными во всем интересующем практику диапазоне тепловых потоков. В работах [10–12] установлено, что при уносе массы с образованием жидкой фазы для достижения высокой эффективности охлаждения вязкость жидкости должна быть большой. Гидродинамическое поведение таких высоковязких жидкостей часто является неньютоновским, что означает, что коэффициент вязкости зависит от касательного напряжения. Ньтоновская жидкость – вязкая жидкость, подчиняющаяся в своем течении закону вязкого трения Ньютона, то есть касательное напряжение и градиент скорости в такой жидкости линейно зависимы. Коэффициент пропорциональности между этими величинами известен как вязкость. Течение неньютоновских жидкостей не подчиняется закону Ньютона и ее вязкость зависит от градиента скорости. Обычно такие жидкости сильно неоднородны и состоят из крупных молекул, образующих сложные пространственные структуры. Чем быстрее происходит внешнее воздействие на взвешенные в жидкости макромолекулы связующего вещества, тем выше ее вязкость. Из-за наличия большого градиента температуры внутри слоя жидкости, образующегося на поверхности разрушающегося материала, решение данной задачи в изотермической постановке может привести к большим неточностям [12], поэтому необходимо одновременно интегрировать всю систему уравнений жидкого слоя, состоящую из уравнений неразрывности, движения и энергии, с учетом зависимости коэффициента вязкости от температуры и касательного напряжения.
Существующие в настоящее время теории уноса массы пренебрегают неньютоновскими эффектами [2, 14, 15]; поэтому цель настоящего исследования состоит в том, чтобы изучить условия, при которых упрощенная теория остается справедливой, а также исследовать отклонения от обычных характеристик процесса уноса массы в тех случаях, когда неньютоновские эффекты становятся значительными [16]. Ради простоты, расчеты процесса уноса массы проводятся в окрестности критической точки, где неньютоновское поведение жидкости обусловлено как поверхностным трением, так и градиентом давления [13]. Поведение оплавленной жидкости связано со структурными изменениями, происходящими при ее движении. Так, например, в случае полимера при больших касательных напряжениях происходит временная предпочтительная ориентация длинных молекул в направлении, параллельном направлению набегающего потока. Под воздействием приложенных касательных напряжений могут разорваться макромолекулы в стеклокерамике, такие, как комплексы ${\text{Si}}{{{\text{O}}}_{4}}$ в кремнеземистых керамических материалах.
3. ВЛИЯНИЕ СОСТАВА МАТЕРИАЛА НА ТЕПЛОФИЗИЧЕСКИЕ СВОЙСТВА И МЕХАНИЗМ ПРОГРЕВА И РАЗРУШЕНИЯ
Существуют два наиболее распространенных, способа построения композиционных теплозащитных материалов. В первом несущий каркас образуется переплетенными тугоплавкими волокнами, а связующая компонента не позволяет волокнам наполнителя скользить друг относительно друга. Во втором случае конструкционной основой являются соты из стеклопластика или металла, а их внутренний объем заполняется смесью органической смолы, пористых микрошариков и микроволокон.
Второй тип теплозащитных систем хорошо работает в условиях длительного нагрева с умеренным силовым воздействием потока. Поэтому его целесообразно использовать, например, в пилотируемых спускаемых космических аппаратах. Напротив, первый тин композиционных теплозащитных материалов хорошо противостоит сверхвысоким тепловым и динамическим нагрузкам, но обладает меньшей эффективностью при длительном нагреве умеренной интенсивности. Учитывая огромное разнообразие композиционных теплозащитных материалов, не представляется возможным описать процесс их нестационарного нагрева и разрушения какой-то одной схематической моделью. В связи с этим мы ограничимся иллюстрацией общего подхода к исследованию этих процессов, а для определенности в процессе изложения будем ориентироваться на стеклопластики на фенолформальдегидной смоле как на типичного и наиболее распространенного представителя армированных композиционных теплозащитных материалов.
Что касается второго типа композиционных теплозащитных материалов (па основе сотовых конструкции), то механизм их разрушения, как правило, подобен разрушению материалов разлагающегося типа и ниже анализироваться не будет.
Сначала рассмотрим теплофизические свойства композиционных теплозащитных материалов. При комнатной температуре их можно рассчитать, если известны теплофизические свойства и массовые доли составляющих. Так, для стеклопластиков с массовым содержанием смолы ${{\varphi }_{{{\text{см}}}}}$ плотность ${{\rho }_{0}}$ связана с плотностями наполнителя ${{\rho }_{{\text{н}}}}$ и связующего ${{\rho }_{{{\text{см}}}}}$ соотношением:
(5)
${1 \mathord{\left/ {\vphantom {1 {{{\rho }_{0}}}}} \right. \kern-0em} {{{\rho }_{0}}}} = \left( {{{{{\varphi }_{{{\text{см}}}}}} \mathord{\left/ {\vphantom {{{{\varphi }_{{{\text{см}}}}}} {{{\rho }_{{{\text{см}}}}}}}} \right. \kern-0em} {{{\rho }_{{{\text{см}}}}}}}} \right) + \left( {{{{{\varphi }_{{\text{н}}}}} \mathord{\left/ {\vphantom {{{{\varphi }_{{\text{н}}}}} {{{\rho }_{{\text{н}}}}}}} \right. \kern-0em} {{{\rho }_{{\text{н}}}}}}} \right);\,\,\,\,{{\varphi }_{{\text{н}}}} = 1 - {{\varphi }_{{{\text{см}}}}}.$Аналогично теплоемкость ${{с}_{0}}$ описывается уравнением:
(6)
${{с}_{0}} = {{\varphi }_{{{\text{см}}}}}{{с}_{{{\text{см}}}}} + \left( {1 - {{\varphi }_{{{\text{см}}}}}} \right){{с}_{{\text{н}}}}.$Если материал имеет начальную пористость, то при расчете результирующих теплофизических свойств ее можно учесть, если соответствующим образом изменить теплофизические характеристики одной из компонент, например, связующего. При расчете коэффициента теплопроводности ${{\lambda }_{0}}$ определяющим параметром является не массовая доля компонент, а их объемное содержание, которое связано с массовой долей через отношение плотности смеси к плотности данной компоненты ${{Х}_{{{\text{см}}}}} = {{\left( {{{\varphi }_{{{\text{см}}}}}{{\rho }_{0}}} \right)} \mathord{\left/ {\vphantom {{\left( {{{\varphi }_{{{\text{см}}}}}{{\rho }_{0}}} \right)} {{{\rho }_{{{\text{см}}}}}}}} \right. \kern-0em} {{{\rho }_{{{\text{см}}}}}}},$ ${{Х}_{{\text{н}}}} = {{\left( {{{\varphi }_{{\text{н}}}}{{\rho }_{0}}} \right)} \mathord{\left/ {\vphantom {{\left( {{{\varphi }_{{\text{н}}}}{{\rho }_{0}}} \right)} {{{\rho }_{{\text{н}}}}}}} \right. \kern-0em} {{{\rho }_{{\text{н}}}}}}$. В первом приближении коэффициент теплопроводности композиционного материала можно представить в виде суммы: ${{\lambda }_{0}} = {{\lambda }_{{{\text{см}}}}}{{Х}_{{{\text{см}}}}} + {{\lambda }_{{\text{н}}}}{{Х}_{{\text{н}}}}.$
Однако в действительности особенности структуры композиционного материала могут привести к значительным отличиям в величине коэффициента теплопроводности. На основании обработки экспериментальных данных для расчета теплопроводности стеклопластиков рекомендуется следующая формула:
(7)
${{\lambda }_{0}} = {{\lambda }_{{{\text{см}}}}}\left[ {\frac{{(1 - {{Х}_{{\text{н}}}}){{{{\lambda }_{{{\text{см}}}}}} \mathord{\left/ {\vphantom {{{{\lambda }_{{{\text{см}}}}}} {{{\lambda }_{{\text{н}}}}}}} \right. \kern-0em} {{{\lambda }_{{\text{н}}}}}} + (1 + {{Х}_{{\text{н}}}})}}{{(1 + {{Х}_{{\text{н}}}}){{{{\lambda }_{{{\text{см}}}}}} \mathord{\left/ {\vphantom {{{{\lambda }_{{{\text{см}}}}}} {{{\lambda }_{{\text{н}}}}}}} \right. \kern-0em} {{{\lambda }_{{\text{н}}}}}} + (1 - {{Х}_{{\text{н}}}})}}} \right].$Соответствующим образом могут быть рассчитаны и другие тепло-физические свойства. Так, вязкость расплавленного стекла, в котором находятся твердые частички примесей (например, углерода), будет тем сильнее отличаться от вязкости чистого стекла ${{\mu }_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}$, чем больше объемное содержание примесей ${{X}_{{\text{н}}}}$:
(8)
${\mu \mathord{\left/ {\vphantom {\mu {{{\mu }_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{\mu }_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}} = \exp \left[ {\frac{{2.5{{X}_{{\text{н}}}}}}{{1 - 1.35{{X}_{{\text{н}}}}}}} \right].$При малых ${{X}_{{\text{н}}}}$ формула (8) переходит в известное соотношение Эйнштейна для вязкости суспензии.
С ростом температуры не только изменяются теплофизические свойства материала, в нем начинают протекать определенные физико-химические процессы, для расчета которых необходимы соответствующие методы расчета. Так, в условиях интенсивного нагрева стеклопластик нагревается как однородный материал всего лишь до 400 К, после чего в нем происходит первое физико-химическое превращение – испарение влаги. По степени влияния на механизм разрушения этот процесс не может конкурировать с большинством других физико-химических превращений, среди которых особое место занимает термическое разложение связующего. Начинаясь при температурах порядка 550 К, разложение органического связующего не только сопровождается поглощением тепла, но, главное, приводит к образованию значительных масс газообразных продуктов. При этом в материале появляется большое число полостей и каналов, через которые летучие компоненты из зоны разложения просачиваются (фильтруются) к внешней нагреваемой поверхности. Стенки пор или внутренних каналов состоят из спеченных и частично разрушенных волокон наполнителя, между которыми распределены твердые частички кокса – второго конечного продукта термического разложения органического связующего.
Газообразные продукты разложения в процессе их фильтрации через вышележащий нагретый слой подвергаются дальнейшему разложению до низкомолекулярных, устойчивых компонент типа СО или Н2, причем возможно осаждение на стенках пор тонкого налета пиролитического углерода. При высоких температурах (выше 1700 К) молекулы стекла и углерода (как пиролитического, так и кокса) могут вступать в химическое взаимодействие друг с другом непосредственно в твердой фазе, продуктом этой реакции являются как газообразные, так и новые твердые компоненты [13–15].
Для построения модели нестационарного прогрева композиционного материала необходимо знать температурные интервалы, в которых протекают важнейшие физико-химические превращения твердой фазы (термическое разложение связующего, гетерогенное взаимодействие компонент и т.д.). Температурный интервал реакции можно установить, располагая данными по ее кинетике или уравнением, описывающим скорость изменения плотности материала. Допустим, что для всех реакций в твердой фазе внутри композиционного материала можно использовать уравнение аррениусовского типа:
(9)
$\frac{{dh}}{{d\tau }} = {{\left( {\Gamma - h} \right)}^{n}}B\exp \left( { - \frac{E}{{RT}}} \right);\,\,\,\,h = 1 - \frac{\rho }{{{{\rho }_{0}}}}.$Здесь через $h(T,\tau )$ обозначена доля газообразных продуктов реакции, а через Γ – максимально возможное содержание этих продуктов в общей массе прореагировавшего вещества. Если говорить о процессе коксования, то величина Γ непосредственно связана с коксовым числом К и является функцией температуры $\Gamma \left( T \right) = 1 - K$.
Параметры n (порядок реакции), B (предэкспонентный множитель) и Е (энергия активации) определяются экспериментально.
Интеграл кинетического уравнения (3) при постоянной температуре записывается в следующем виде (для n = 1):
(10)
$h = \Gamma \left( T \right)\left\{ {1 - \exp \left[ { - B\tau \exp \left( { - \frac{E}{{RT}}} \right)} \right]} \right\}.$Отсюда следует, что время достижения заданной начальной концентрации быстро уменьшается с ростом температуры Т:
(11)
$\begin{gathered} {{\tau }_{{{\text{инд}}}}} = \left( {\ln \frac{{\Gamma \left( T \right)}}{{\Gamma \left( T \right) - {{h}_{{\text{н}}}}}}} \right){{B}^{{ - 1}}}\exp \left( { - \frac{E}{{RT}}} \right); \\ {{h}_{{\text{н}}}} \leqslant \Gamma \left( T \right). \\ \end{gathered} $Это время принято называть индукционным периодом реакции. Если принять в первом приближении, что зависимость ${{\tau }_{{{\text{инд}}}}}\left( T \right)$ не зависит от характера изменения температуры во времени $T(\tau )$, то мы получаем возможность связать температуру начала реакции ${{T}_{{\text{н}}}}$, при которой концентрация газообразных продуктов $h = {{h}_{{\text{н}}}}$, с темпом нагрева $b = \left( {{{\partial T} \mathord{\left/ {\vphantom {{\partial T} {\partial \tau }}} \right. \kern-0em} {\partial \tau }}} \right)$. В частности, если внутри температурного интервала протекания реакции принять темп изменения температуры постоянным $b = {\text{const}}$, то интересующие нас величины связаны соотношением:
(12)
$b = \frac{{B\left( {{{T}_{{\text{н}}}} - {{T}_{{{\text{нач}}}}}} \right)}}{{\ln \left[ {{{\Gamma \left( {{{T}_{{\text{н}}}}} \right)} \mathord{\left/ {\vphantom {{\Gamma \left( {{{T}_{{\text{н}}}}} \right)} {\left( {\Gamma \left( {{{T}_{{\text{н}}}}} \right) - {{h}_{{\text{н}}}}} \right)}}} \right. \kern-0em} {\left( {\Gamma \left( {{{T}_{{\text{н}}}}} \right) - {{h}_{{\text{н}}}}} \right)}}} \right]}}\exp \left( { - \frac{E}{{R{{T}_{{\text{н}}}}}}} \right).$Здесь ${{T}_{{{\text{нач}}}}}$ – значение температуры, при котором индукционное время реакции (11) равно бесконечности или, другими словами, это нижний температурный предел начала реакции.
Интересно отметить, что при реакции взаимодействия окислов с углеродом ${{T}_{{{\text{нач}}}}}$ оказывается определенным образом связанным с температурой плавления окисла (рис. 1). Следовательно, начало восстановления окисла углеродом обусловлено прежде всего термической устойчивостью окисла [1–3]. Известно, что реакции в твердой фазе обычно носят сложный, многостадийный характер, вследствие чего кинетические константы реакции в разных условиях нагрева могут отличаться. Однако экспериментальные данные ограничены случаем нагрева при постоянной температуре внешней среды и притом весьма противоречивы [4–6]. Наиболее полное исследование процесса восстановления молекулы двуокиси кремния ${\text{Si}}{{{\text{O}}}_{2}}$ углеродом проведено в работе [1]. При этом показано, что процесс протекает по следующей схеме:
(13)
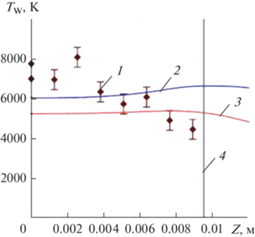
${\text{Si}}{{{\text{O}}}_{2}}\left( {{\text{тв}}} \right) + С\left( {{\text{тв}}} \right) \rightleftarrows {\text{SiO}}\left( {{\text{газ}}} \right) + СО\left( {{\text{газ}}} \right).$Рис. 1.
Сравнение температуры вдоль критической линии каталитической стенки с расчетными результатами: 1 – экспериментальные данные; 2 – равновесное течение; 3 – неравновесного течения; 4 – расстояние от критической точки.
Хотя при меньших температурах в качестве промежуточного продукта может образовываться карбид кремния. При стехиометрическом соотношении компонент скорость взаимодействия зависит от величины поверхности соприкосновения углерода и стекла, вследствие чего в реальных стеклопластиках она может в несколько раз снизиться. Экспериментальные данные [4] дают два набора кинетических констант соответственно для максимальной и минимальной скоростей взаимодействия:
(14)
$\begin{gathered} {{\left( {{E \mathord{\left/ {\vphantom {E R}} \right. \kern-0em} R}} \right)}_{1}} = 32720\,\,{\text{К}};\,\,\,\,{{B}_{1}} = 5 \times {{10}^{6}}\,\,{{{\text{c}}}^{{ - 1}}}; \\ {{\left( {{E \mathord{\left/ {\vphantom {E R}} \right. \kern-0em} R}} \right)}_{2}} = 27750\,\,{\text{К}};\,\,\,\,{{B}_{2}} = 9 \times {{10}^{3}}\,\,{{{\text{c}}}^{{ - 1}}}. \\ \end{gathered} $Исходя из этих данных, с помощью уравнения (12) нетрудно показать, что реакция восстановления стекла, (13) при увеличении темпа нагрева быстро смещается и область высоких температур. В случае квазистационарного разрушения темп нагрева можно связать со скоростью линейного перемещения поверхности разрушения ${{v}_{\infty }}$. Используя для этой цели первое уравнение (7) и решая его совместно с уравнением кинетики реакции (9), можно определить температуру Т* = ТW и скорость при которых концентрация углерода, перешедшего в газообразную окись СО, достигнет 0.1 (рис. 2).
Рис. 2.
Зависимость квазистационарных значений температуры поверхности и скорости уноса массы от теплофизических свойств композиционного материала (влияние $\lambda $, где индекс 0 соответствует основному варианту).
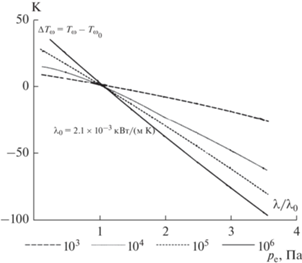
Видно, что уменьшение коэффициента темплопроводности $a = {\lambda \mathord{\left/ {\vphantom {\lambda {\rho c}}} \right. \kern-0em} {\rho c}}$ или увеличение скорости разрушения ${{v}_{\infty }}$, приводит к смещению температурного интервала реакции в область более высоких температур Т*. При заданной скорости разрушения ${{v}_{\infty }}$ замена первого набора кинетических параметров, соотношение (8)–(14), вторым приводит к смещению температуры начала реакции на 300–1000 К.
За счет частичного протекания реакции гетерогенного восстановления стеклокерамики углеродом состав поверхностного слоя стеклопластика может несколько отличаться от исходного. Кроме того, при взаимодействии с набегающим газовым потоком различные составляющие материала могут разрушаться с неодинаковыми скоростями. Поэтому при рассмотрении композиционных теплозащитных материалов важно выделить так называемый определяющий механизм разрушения, понимаем такую последовательность протекания взаимосвязанных физико-химических процессов, которая в итоге приводит к выходу всех компонент – продуктов разрушения с единой скоростью.
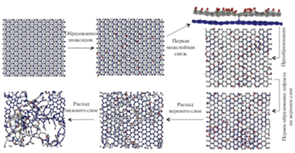
У композиционных материалов такой определяющий механизм, как правило, связан с поведением какой-либо одной компоненты, массовое содержание которой в материале достаточно велико и которая в состоянии образовать механически прочный каркас в условиях интенсивного внешнего теплового воздействия. Скорости разрушения всех остальных компонент оказываются зависящими от скорости уноса массы определяющей компоненты, хотя в свою очередь через химические и тепловые связи они могут известным образом повлиять на величину последней [16]. Проследим это на примере гипотетической композиции – механической смеси кварцевого стекла и углерода: ${\text{Si}}{{{\text{O}}}_{2}} + {\text{C}}$. Очевидно, что при малом содержании углерода определяющей компонентой будет стекло, которое, оплавляясь, будет уносить с собой твердые частички углерода. Возможность гетерогенного взаимодействия компонент или поверхностного выгорания углерода будет тем меньше, чем меньше доля химически активной поверхности по отношению к полной поверхности частичек стекла. Вязкость расплава композиционного материала в соответствии с формулой (8) будет непрерывно возрастать по мере увеличения доли примесей, соответственно скорость уноса массы должна уменьшаться. Схематически это положение иллюстрируется на рис. 3. Однако при уменьшении доли расплава и с ростом температуры поверхности одновременно должна возрастать роль химических процессов и прежде всего прямого восстановления двуокиси кремния углеродом. Это увеличит скорость уноса массы.
Рис. 3.
Характер изменении скорости и механизма разрушения композиционного материала на основе углерода и стекла от весового содержания углерода ${{\varphi }_{c}}$.

Рассмотрим другой предельный вариант – смесь углерода с небольшими добавками ${\text{Si}}{{{\text{O}}}_{2}}$. В диффузионном режиме окисления скорость уноса массы такой композиции должна определяться соотношением: ${{\varphi }_{c}}{{G}_{\Sigma }} = {{12} \mathord{\left/ {\vphantom {{12} {16}}} \right. \kern-0em} {16}}{{\left( {{\alpha \mathord{\left/ {\vphantom {\alpha {{{c}_{p}}}}} \right. \kern-0em} {{{c}_{p}}}}} \right)}_{\omega }}{{\tilde {c}}_{{O,e}}}$.
Необходимо отметить, что уменьшение доли углерода приводит к резкому возрастанию ${{G}_{\Sigma }}$. При добавлении в углерод стекла, вероятно, нельзя считать, что оно по мере выгорания частиц углерода беспрепятственно сносится потоком. Очевидно, что при некоторой минимальной концентрации ${{\varphi }_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}$ наличие стекла приведет к замедлению горения, так как поверхность углерода будет обволакиваться пленкой расплава. Можно предположить, что переход от одного определяющего механизма разрушения (плавления стекла) к другому (горение углерода) происходит не скачком, а через некоторую последовательность промежуточных состояний, причем начало перехода, вероятно, зависит от режима внешнего обтекания. Многочисленные экспериментальные исследования, как тепловые, гак и прочностные, показали, что оптимальная массовая концентрация стекла в армированных композиционных материалах на органическом связующем составляет ${{\varphi }_{{{\text{Si}}{{{\text{O}}}_{2}}}}} \approx $ 0.6–0.8. С точки зрения механизма разрушения такое соотношение компонент указывает на определяющую роль стекла, однако процессы химического взаимодействия компонент могут в определенных случаях внести свои коррективы.
4. НЕСТАЦИОНАРНЫЙ ПРОГРЕВ КОМПОЗИЦИОННОГО ТЕПЛОЗАЩИТНОГО МАТЕРИАЛА
Схематический разрез разрушающегося стеклопластика проведен на рис. 4. На поверхности покрытия может существовать пленка расплавленного стекла с распределенными в ней твердыми частицами разрушенного коксового остатка. Далее лежит сравнительно толстый пористый слой обугленной (прококсованной) смолы, поддерживаемой стеклянными волокнами. Еще глубже в материале находится зона разложения, в которой происходит пиролиз органической связки до смеси летучей g и твердой s компонент. Наконец, подложку теплозащитного слоя составляет однородный материал, в котором еще не начались физико-химические превращения. В зависимости от условий обтекания расход жидкой фазы в пленке расплава может быть весьма значительным, с другой стороны, возможны случаи, когда расплав будет полностью испаряться. В любом случае будем предполагать, что пленка расплава достаточно тонкая и не препятствует просачиванию через нее пузырьков газообразных продуктов разрушения.
Частички кокса практически являются чистым углеродом, поэтому при температуре плавления стекла они остаются твердыми. Растекающаяся пленка стекла “взламывает” пористую структуру прококсованного слоя и уносит частички кокса с собой. В свою очередь последние влияют на течение расплава, балластируя пленку и увеличивая ее эффективную вязкость в соответствии с уравнением (8).
Исходя из этого, математическое описание задачи об оплавлении стеклопластика практически не отличается от описания аналогичной задачи для однородного стекла. Основную трудность представляет расчет нестационарного прогрева, поскольку заранее неизвестно, на какой глубине внутри покрытия находится источник образования газов, которые затем фильтруются по пористым каналам в направлении к внешней поверхности [17].
Неопределенность размеров и формы пор затрудняет расчет внутреннего теплообмена между газообразными продуктами разложения и твердой фазой. Однако, учитывая высокие температуры, можно допустить, что радиационный и конвективный теплообмен в порах настолько интенсивны, что можно принять гипотезу о местном температурном равновесии. Предположим также, что физико-химические свойства всех компонент газообразных продуктов разложения одинаковы и что гидравлическим сопротивлением пористой среды можно пренебречь. Тогда в окрестности точки торможения затупленного тела уравнение сохранения; энергии можно представить следующим образом:
(15)
${{\left( {pc} \right)}_{\Sigma }}\left( {\frac{{\partial T}}{{\partial \tau }} + v\frac{{\partial T}}{{\partial y}}} \right) = \frac{\partial }{{\partial y}}\left( {{{\lambda }_{\Sigma }}\frac{{\partial T}}{{\partial y}}} \right) - {{c}_{g}}{{G}_{g}}\frac{{\partial T}}{{\partial y}} - Q{\text{*}}.$Это уравнение отличается членом, учитывающим наличие пленки расплава, тем самым нормальная компонента скорости $v = v\left( {y,\tau } \right)$ оказывается переменной. С другой стороны, в отличие от уравнения сохранения энергии в однородных оплавляющихся материалах в рассматриваемом случае учтены термическое разложение связующего с тепловым эффектом Q* и фильтрация с расходом ${{G}_{g}}$ газообразных продуктов разложения, имеющих коэффициент теплоемкости ${{G}_{g}}$.
Особенностью композиционных материалов является переменная пористость по толщине прогретого слоя. Если определить пористость Π как отношение свободного объема, занятого газом, к полному объему материала, а массовую пористость ${{\Pi }_{m}}$ как отношение массы образовавшегося газа к полной массе материала (стеклопластика), то эффективные значения теплопроводности и теплоемкости можно представить следующими приближенными соотношениями:
(16)
$\begin{gathered} {{\lambda }_{\Sigma }} = \left( {1 - \Pi } \right){{\lambda }_{s}} + \Pi {{\lambda }_{g}}; \\ {{\left( {\rho c} \right)}_{\Sigma }} = \left( {1 - {{\Pi }_{m}}} \right){{\left( {\rho c} \right)}_{s}} + {{\Pi }_{m}}{{\left( {\rho c} \right)}_{g}}, \\ \end{gathered} $причем каждое слагаемое – теплопроводность твердой фазы ${{\lambda }_{s}}$ и газа ${{\lambda }_{g}}$, а также произведения плотности на теплоемкость твердой фазы ${{\left( {\rho c} \right)}_{s}}$ и газа ${{\left( {\rho c} \right)}_{g}}$ могут изменяться с температурой. Поскольку плотность газа ${{\rho }_{g}}$ много меньше плотности твердого вещества, а их теплоемкости сравнимы по величине, то вторым слагаемым в выражении для ${{\left( {\rho c} \right)}_{\Sigma }}$ можно пренебречь. Исходя из общей схемы твердофазных реакций, формула (9), уравнение сохранения массы в зоне термического разложения записывается в следующем виде:
(17)
$\frac{{\partial h}}{{\partial \tau }} + {{v}_{\infty }}\frac{{\partial h}}{{\partial y}} = B{{\left( {\Gamma - h} \right)}^{n}}\exp \left( {\frac{E}{{RT}}} \right);\,\,\,\,0 \leqslant h \leqslant \Gamma .$Следует обратить внимание на то, что в данном уравнении используется линейная скорость разрушения ${{v}_{\infty }}$, поскольку зоны плавления и коксования связующего никогда не совпадают, так как эти процессы протекают в разных температурных интервалах. Уравнения массового расхода газообразных продуктов разложения согласно принятой схеме разрушения записываются в следующем виде:
внутри зоны термического разложения
(18)
${{G}_{g}}\left( {\tau ,y} \right) = {{\varphi }_{{{\text{см}}}}}{{\rho }_{o}}\int\limits_\infty ^y {\frac{{\partial h}}{{\partial \tau }}} ,\,\,\,\,\Pi = \frac{{{{\varphi }_{{{\text{см}}}}}{{\rho }_{o}}}}{{{{\rho }_{с}}}}\left[ {1 - \left( {1 - h} \right)\frac{{{{\rho }_{{{\text{см}}}}}}}{{{{\rho }_{с}}}}} \right]$Поглощение тепла при разложении связующего определяется как
(19)
$Q{\kern 1pt} * = \frac{{{{\varphi }_{{{\text{ст}}}}}{{\rho }_{о}}\Delta H{\text{*}}}}{\Gamma }В{{\left( {\Gamma - h} \right)}^{n}}\exp \left( { - \frac{E}{{RT}}} \right).$Соответственно объемная пористость Π, массовая пористость ${{\Pi }_{т}}$ и плотность твердой фазы ${{\rho }_{с}}$ связаны с массовой долей газообразных продуктов реакции h следующими соотношениями:
(20)
$\begin{gathered} \Pi = \frac{{{{\varphi }_{{{\text{см}}}}}{{\rho }_{0}}}}{{{{\rho }_{{{\text{см}}}}}}}\left[ {1 - (1 - h)\frac{{{{\rho }_{{{\text{см}}}}}}}{{{{\rho }_{с}}}}} \right]; \\ {{П}_{{\text{м}}}} \approx {{\varphi }_{{{\text{см}}}}}h;\,\,\,{{\rho }_{c}} = {{\rho }_{0}}\left( {1 - {{\varphi }_{{{\text{см}}}}}h} \right), \\ \end{gathered} $Полезно детально анализировать процессы, протекающие и топком слое, прилегающем к поверхности, и определяющие скорость линейного разрушения стеклопластика (разрушение в данном случае включает в себя плавление и гетерогенное взаимодействие углерода со стеклом), в данной работе ограничимся рассмотрением связи между распространением тепла и термическим разложением связующего. Численное интегрирование уравнений (15)–(17) совместно с уравнениями течения пленки расплава позволяет установить влияние кинетических констант реакции разложения смолы на параметры разрушения. В качестве граничных условий, характеризующих внешнее обтекание, приняты постоянные значения температуры и давления торможения, что соответствует условиям сравнительных стендовых испытаний теплозащитных материалов. Прежде всего следует отметить, что в условиях нестационарного прогреве изменение доли газообразных продуктов термического разложения h(у) в основном определяется предэкспонентным множителем В. Действительно, как видно из рис. 5, при изменении отношения E/R от 11 575 до 23 150 К форма и протяженность профиля h(y) остаются практически неизменными. Увеличение В приводит к интенсификации разложения в узкой зоне коксования. Оба кинетических параметра оказывают существенное влияние на расположение зоны разложения относительно профиля температуры (рис. 6).
Рис. 5.
Изменение доли газообразных продуктов термического разложении смолы. $1 - E = {{{{E}_{0}}} \mathord{\left/ {\vphantom {{{{E}_{0}}} 2}} \right. \kern-0em} 2},$ $B = {{B}_{0}},$ ${\text{ }}2 - E = {{E}_{0}},$ $B = {{B}_{0}},$ $3 - E = {{E}_{0}},$ $B = 100{{B}_{0}}$, $\frac{{{{E}_{0}}}}{R} = 23\,150\,\,{\text{K;}}$ ${{B}_{0}} = {{10}^{6}}\,\,{{{\text{c}}}^{{ - 1}}}$; ${{\delta }_{T}}$ – глубина прогрева.
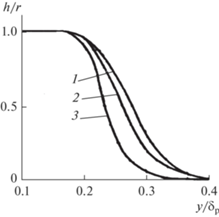
Рис. 6.
Относительное положение профиля температуры и профили содержания газообразных продуктов h при нестационарном разрушении стеклопластиков. $1 - E = {{{{E}_{0}}} \mathord{\left/ {\vphantom {{{{E}_{0}}} 2}} \right. \kern-0em} 2},$ $B = {{B}_{0}},$ $2 - E = {{E}_{0}},$ $B = 100{{B}_{0}},$ $3 - E = 0.8{{E}_{0}},$ $B = {{B}_{0}},$ $4 - E = {{E}_{0}},$ $B = {{B}_{0}},$ $5 - E = {{E}_{0}},$ $B = 0.01{{B}_{0}},$ $\frac{{{{E}_{0}}}}{R} = 23\,150\,\,{\text{K}};$ ${{B}_{0}} = {{10}^{6}}\,\,{{{\text{c}}}^{{ - 1}}}.$
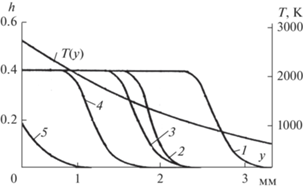
Определим температуру коксования Т* как температуру, при которой доля газообразных продуктов разложения h(Т) составит половину своего максимального значения Γ. Можно установить наглядную зависимость этой температуры от заданных кинетических констант и времени. Здесь ${{\tau }_{{v,q}}}$ – время установления постоянной скорости перемещения поверхности разрушения однородного стеклообразного материала.
Анализ численных результатов показывает, что температура коксования Т* не является постоянной, она несколько уменьшается со временем до своего стационарного значения, определяемого константами кинетики разложения. Интересно отметить, что одно и то же значение Т* соответствует двум парам значений (E/R) и В, причем отклонение энергии активации примерно па 20% (варианты 1 и 2) равносильно изменению предэкспонентного множителя на два порядка (варианты 1 и 4). При постоянном множителе В температура коксования Т* почти пропорциональна заданному значению E/R (строки 1 и 2).
Специальные расчеты показали, что при прочих равных параметрах изменение теплового потока и теплофизических свойств материала достаточно слабо отразилось на величине температуры коксования Т*.
Рисунок 7 иллюстрирует характер изменения скорости термического разложения во времени. Результаты численных расчетов нестационарного оплавления стеклообразных материалов показали, что из всех физических параметров, входящих в дифференциальные уравнения и граничные условия, на ход зависимости скорости уноса массы от времени ${{G}_{\sum }}\left( \tau \right)~$ влияют лишь теплопроводность материала и его плотность. Изменение всех остальных параметров приводит лишь к отличиям в установившихся значениях скорости оплавления ${{G}_{\sum }}$ и температуре поверхности ${{T}_{\omega }}$. Представленные на рис. 7 величины с индексом 0 приняты в качестве “эталонных” и соответствуют параметрам и результатам основного варианта расчета, а диапазон изменения теплофизических свойств выбран с учетом их реальных отклонений.
Рис. 7.
Неравномерная скорость разложения композиционных материалов с различной теплопроводностью. 1 – λ = 2λ0; 2 – переменная теплопроводность; 3 – λ = 1.2λ0; 4 – основной расчетный вариант; 5 – λ = 0.8λ0.
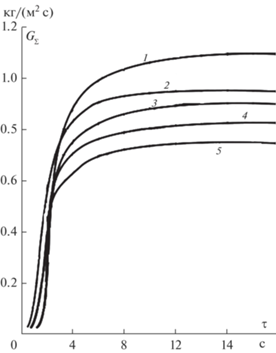
Полимерные материалы отличаются от других покрытий большим разнообразием физических свойств (вязкости, плотности, теплопроводности и т.д.). Поэтому представляет интерес вопрос о влиянии этих свойств или их отклонения от заданных “эталонных” значений па основные параметры оплавления: суммарную скорость уноса массы ${{G}_{\sum }}$ и температуру разрушающейся поверхности ${{T}_{\omega }}$.В расчетах предполагалось, что теплоемкость и плотность разных рецептур может отличаться в 2–2.5 раза: 1000 ≤ ρ ≤ 2250 кг/м3; 1.00 ≤ с ≤ 2.5 кДж/ (кг К). Несколько сильнее может отличаться коэффициент теплопроводности. С ростом температуры он начинает резко увеличиваться, причем тем сильнее, чем прозрачнее материал для теплового излучения. Например, у кварцевого стекла величина эффективного коэффициента теплопроводности может увеличиться по сравнению с табличным при 273 К в 5–7 раз. Еще сильнее может изменяться вязкость расплава μ(T). Известно, что добавление в кварцевое стекло даже 10–20% примесей (Al2O3,ВаО и т.д.) может на несколько порядков изменить абсолютное значение вязкости расплава, а также характер зависимости вязкости от температуры. Результаты численных расчетов нестационарного оплавления стеклообразных материалов показали, что из всех физических параметров, входящих в дифференциальные уравнения и граничные условия, на ход зависимости скорости уноса массы от времени ${{G}_{\sum }}\left( \tau \right)~$влияют лишь теплопроводность материала (рис. 6, 7) и его плотность. Изменение всех остальных параметров приводит лишь к отличиям в установившихся значениях скорости оплавления ${{G}_{\sum }}$ и температуре поверхности ${{T}_{\omega }}$. Расчетами показано, что при определении скорости оплавления можно пренебречь зависимостью теплоемкости от температуры, а использовать ее среднеинтегральное значение $\bar {c}$, которое вычисляется как
Это обстоятельство намного упрощает анализ, поскольку при температурах поверхности выше 2300 К теплоемкости $\bar {c}$ почти всех стеклообразных материалов отличаются не более чем на 25%. Хотя скорость уноса массы ${{G}_{\sum }}$ и температура поверхности ${{T}_{\omega }}$ слабо зависят отплотности материала р, для толщины унесенного слоя, определяемой интегральным соотношением:
С началом разрушения внешней поверхности на этот процесс накладывается перемещение внутренних изотерм вместе с поверхностью, в результате чего расход газообразных продуктов разложения стремится к своему квазистацнонарному значению
(21)
${{\left. {{{G}_{g}}} \right|}_{{\tau \to \infty }}} = {{\varphi }_{{ст}}}{{p}_{0}}\Gamma {{v}_{\infty }},$ЗАКЛЮЧЕНИЕ
Необходимо отметить, что полная модель разрушения полимерных материалов достаточно сложна. Сильная зависимость вязкости расплава от температуры приводит к необходимости совместного решения уравнения движения пленки и уравнения сохранения энергии. При этом последнее приходится интегрировать по всей глубине прогрева конденсированной фазы, ибо у стеклообразных материалов нет фиксированной температуры плавления. Температурный профиль в пленке расплава определяет такие чисто внутренние процессы в теплозащитном материале, как термическое разложение смолы, фильтрация газообразных продуктов коксования, гетерогенное взаимодействие наполнителя и связующего. Учет нестационарности прогрева для полимерных материалов имеет принципиальное значение прежде всего потому, что при равных с другими теплозащитными материалами скоростях уноса массы оплавляющиеся покрытия имеют большее время установления квазистационарного режима. Кроме того, внутри пленки расплава и в прогретом слое у стеклопластиков возможно резкое увеличение эффективного коэффициента теплопроводности за счет переноса тепла излучением поверхности. Необходимо отметить что, экспериментальные исследования разрушающихся материалов в основном ограничены условиями обтекания с постоянными параметрами газовых потоков. Результаты расчетов нестационарного оплавления стеклообразных материалов показали, что из всех физических параметров, входящих в уравнения и граничные условия, на ход зависимости скорости уноса массы от времени влияют лишь теплопроводность материала и его плотность. Поэтому дополнительно изучен вопрос о влиянии этих свойств или их отклонения от заданных “эталонных” значений на основные параметры оплавления: суммарную скорость уноса массы и температуру разрушающейся поверхности. В расчетах предполагалось, что теплоемкость и плотность разных концентраций может отличаться в 2–3 раза. Коэффициент теплопроводности с ростом температуры начинает резко увеличиваться, причем тем сильнее, чем прозрачнее материал для теплового излучения. У кварцевого стекла величина эффективного коэффициента теплопроводности может увеличиться по сравнению с табличным при 273 К в 5–7 раз.
Еще сильнее может изменяться вязкость расплава. Результаты расчетов оплавления стеклообразных материалов показали, что из всех физических параметров, входящих в дифференциальные уравнения и граничные условия, на ход зависимости скорости уноса массы от времени влияют лишь теплопроводность материала и его плотность. Изменение всех остальных параметров приводит лишь к отличиям в установившихся значениях скорости оплавления и температуре поверхности.
Список литературы
Сидняев Н.И. Обзор методик исследования обтекания гиперзвуковым потоком газа тел с разрушающимся покрытием // Теплофизика и аэромеханика. 2004. Т. 11. № 4. С. 501–522.
Каданов Л.П. Распространение лучистой энергии внутри аблирующеготела // Теплопередача. 1961. Т. 83. № 2. С. 147–160.
Сидняев Н.И. Обтекание гиперзвуковых летательных аппаратов в условиях поверхностного разрушения. М.: Физматлит, 2017. 302 с.
Сидняев Н.И., Белкина Э.В. О влиянии гиперзвукового потока на скорость оплавления теплозащитной поверхности в условиях разрушения // Новые огнеупоры. 2020. № 1. С. 20–27. https://doi.org/10.17073/1683-4518-2020-1-20-27
Горский В.В., Полежаев Ю.В. Тепло- и массобмен на поверхности стеклографитовых материалов в высокотемпературном газовом потоке // Механика жидкости и газа. 1972. № 6. С. 71–87.
Сидняев Н.И. Исследование аэродинамических характеристик тел вращения с проницаемым наконечником при обтекании гиперзвуковым потоком // Прикладная механика и техническая физика. 2007. Т. 48. № 2. С. 12–20.
Горский В.В., Запривода А.В. О применении полной термохимической модели разрушения углерода к задаче разрушения углепластика в условиях нестационарного нагрева // ТВТ. 2014. Т. 52. № 2. С. 240.
Гришин А.М., Парашин А.Д., Якимов А.С. Термохимическое разрушение углепластика при многократном импульсном нагружении // ФГВ. 1993. Т. 29. № 1. С. 87.
Sidnyaev N.I. Numerical solution of the problem of gas efflux from a closed volume into atmosphere // Technical physics letters. 2005. V. 31. № 1. P. 17–24.
Гофман А.Г., Гришин А.М. Теоретическое исследование термохимического разрушения графита в высокоэнтальпийном воздухе // ПМТФ. 1984. № 4. С. 107.
Бейкер Р.Л. Влияние неравновесных химических процессов на сублимацию графита // РТК. 1977. Т. 15. № 10. С. 21.
Gubta R.N., Yoss J.M., Thompson R.A., Lee K.P. A review of reaction rates and thermodynamic and transport properties for an 11- species air model for chemical and thermal non-equilibrium calculations to 30е000 K. NASA-RP-1232, 1990.
Anna A., Boyd I. D., Colombo V., Ghedini E., Sanibondi P., Boselli M., Gherardi M. Computational Modeling of Surface Catalysis for Graphite Exposed to High-Enthalpy Nitrogen Flow. NATOAVT-199/RSM-0029, 2012.
Сидняев Н.И. Исследование теплообмена в пограничном слое при обтекании азотом каталитической графитовой стенки // Теплофизика и аэромеханика. 2020. Т. 27. № 2(122). С. 201–212.
Основы теории полета космических аппаратов / В.С. Авдуевский, Б.М. Антонов, Н.А. Анфимов и др.; под ред. Нариманова Г.С. и Тихонравова М.К. М.: Машиностроение, 1972. 607 с.
Андрейчук О.Б., Малахов Н.Н. Тепловые испытания космических аппаратов. М., Машиностроение, 1982. 143 с.
Sidnyaev N.I. Studi of heat and mass transfer for hypersonic flow past a complex body of revolution // Thermophysics and Aeromechanics. 2006. V. 13. № 1. P. 2–12.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов