Физикохимия поверхности и защита материалов, 2022, T. 58, № 4, стр. 361-367
Исследование адсорбции паров ацетона на микропористом углеродном адсорбенте методом кварцекристаллического микровзвешивания
В. Н. Симонов 1, 2, *, С. Д. Артамонова 1, А. А. Фомкин 1, А. В. Школин 1, И. Е. Меньщиков 1
1 Федеральное государственное бюджетное учреждение науки Институт физической химии и электрохимии
им. А.Н. Фрумкина РАН (ИФХЭ)
119071 Москва, Ленинский проспект, 31, корп. 4, Россия
2 Национальный исследовательский ядерный университет “Московский инженерно-физический институт”
115409 Москва, Каширское ш., 31, Россия
* E-mail: simonov.valer@yandex.ru
Поступила в редакцию 15.03.2022
После доработки 30.03.2022
Принята к публикации 05.04.2022
- EDN: GQYXWV
- DOI: 10.31857/S0044185622040222
Аннотация
Разработаны требования к микропористой структуре углеродного адсорбента для селективной адсорбции паров ацетона – газового маркера сахарного диабета. Показано, что наиболее перспективными являются адсорбенты с шириной микропор 0.8–1.2 нм. Изготовлен адсорбционный кварцекристаллический сенсор паров ацетона с концентрацией до 150 ppm на основе активированного угля марки АР-1, способный стать приборной основой неинвазивной идентификации сахарного диабета. Минимальный порог чувствительности сенсора в рабочем диапазоне паров ацетона в выдыхаемом воздухе 0–20 ppm при времени регистрации 3 мин составляет 0.19 ppm.
ВВЕДЕНИЕ
Разработка неинвазивных методов контроля уровня глюкозы в крови, позволяющих отслеживать состояние больного сахарным диабетом, является чрезвычайно важной областью исследований [1]. Одним из таких возможных методов является анализ содержания паров ацетона в выдыхаемом воздухе [2]. Известно довольно много подобных устройств. Однако в подавляющем большинстве случаев они имеют те или иные недостатки. Среди этих недостатков можно выделить невысокую надежность, большой разброс показаний и длительное время измерений [3]. В некоторых случаях на подготовку пробы может затрачиваться от 10 до 20 мин [4].
Критическое значение объемной концентрации паров ацетона, соответствующее опасному содержанию сахара в крови, лежит в зависимости от индивидуальных показаний больного в пределах 2–5 ppm, а диапазон значений концентрации практически не превышает 15 ppm. Указанные характеристики являлись отправными для данной работы, направленной на возможность разработки сенсора уровня глюкозы в крови человека по содержанию паров ацетона в выдыхаемом воздухе. При этом рассматривается простейший конструктивный вариант, когда анализируется замкнутый объем ацетоноазотной смеси, имитирующей выдыхаемый воздух. В качестве сенсоров выделяются адсорбционные кварцекристаллические сенсоры (АКС), содержащие пьезоэлемент (ПЭ) в форме пластины, к которой прикреплен активный к ацетону адсорбент [5–8].
Подавляющее большинство АКС работают на ПЭ, использующих сдвиговую по толщине пластины моду колебаний. При этом в качестве адсорбента, как правило, используется полимерная пленка, технология нанесения которой проста и хорошо отработана [7, 8]. Чувствительность таких сенсоров зачастую недостаточна для определения критической концентрации паров ацетона в выдыхаемом воздухе. Другой существенный недостаток ПС на полимерных пленочных адсорбентах заключается в их низкой селективности по отношению к другим газообразным компонентам, присутствующим в выдыхаемом воздухе. В особенности это актуально в отношении паров воды.
В то же время существует целый класс адсорбентов, выпускаемых промышленностью в значительных объемах, хорошо изученных и имеющих высокоселективные адсорбционные свойства. Например, изотермы активных углей обладают высокой крутизной в области микроконцентраций летучих органических соединений (ЛОС), а активность таких адсорбентов по отношению к парам воды при концентрациях ниже ~40% пренебрежимо мала [9, 10].
Задачей данной работы являлось определение условий применимости активных углей в качестве чувствительных элементов АКС паров ацетона в выдыхаемом воздухе больных сахарным диабетом. Она решается путем определения параметров адсорбента, обеспечивающих достаточно высокую адсорбционную способность, и применением оригинальной конструкции сенсора [11].
ТЕОРЕТИЧЕСКИЙ АНАЛИЗ
Для селективного улавливания паров ацетона из воздуха необходимо выполнение условия превышения дифференциальной мольной теплоты адсорбции целевого компонента (ацетона) над теплотой адсорбции основных компонентов выдыхаемого воздуха на активных углях: азота (~8.3 кДж/моль) и кислорода (~8.0 кДж/моль) [12, 13]. Теплота адсорбции ацетона С3Н6О (~40 кДж/моль) [14] значительно превосходит теплоту адсорбции азота и кислорода. В связи с этим для оптимизации пористой структуры адсорбента с целью повышения избирательной адсорбции ацетона провели моделирование на основе теории объемного заполнения микропор (ТОЗМ) адсорбции ацетона на ряде модельных пористых углеродных адсорбентов со щелевидной микропористой структурой. В расчетах использовали термическое уравнение адсорбции Дубинина–Радушкевича (ДР) [15].
(1)
$~а = ~\,\,{{а}_{0}}\left( Т \right)\exp \left[ { - {{{\left( {{А \mathord{\left/ {\vphantom {А Е}} \right. \kern-0em} Е}} \right)}}^{2}}} \right],$В ТОЗМ связь между эффективной полушириной микропор х0 (нм) и характеристической энергией адсорбции стандартного пара бензола Е0 (кДж/моль) для щелевидной модели микропор определяется уравнением связи [16]:
(2)
${{x}_{0}} = {{12} \mathord{\left/ {\vphantom {{12} {{{E}_{0}}}}} \right. \kern-0em} {{{E}_{0}}}}.$Для реальных адсорбентов с ростом объема микропор W0 поры становятся более широкими, х0 – растет, а характеристическая энергия адсорбции Е падает. Таким образом, на изобарных кривых зависимости адсорбции ацетона от ширины микропор в изотермических условиях должен быть максимум адсорбционной активности, определяющий оптимальную пористую структуру адсорбента при адсорбции ацетона. В работе в качестве модельной структуры использовали кристалл графита, в котором последовательное выгорание слоев гексагонального углерода при активации углеродного адсорбента приводит к образованию щелевидных микропор разной ширины [17]. В качестве объекта исследования выбрана наиболее технологически возможная микропористая структура адсорбента, поры в которой разделены двухслойными углеродными стенками. В модели микропор для анализа выбраны структуры с выгоранием последовательно одного из пяти (АУ1:5), двух из шести (АУ2:6) и так далее до семи (АУ7:11) выгоревших слоев углерода.
Ограничение количества выгоревших слоев связано с предельной шириной микропор по классификации М.М. Дубинина – не более 3.0–3.2 нм [16]. В таких микропорах процесс адсорбции осуществляется по механизму объемного заполнения. Структурно-энергетические характеристики (СЭХ) таких адсорбентов, рассчитанные по ТОЗМ, представлены в табл. 1.
Таблица 1.
Характеристики пористой структуры модельных адсорбентов со щелевидными микропорами, разделенными двухслойными углеродными стенками (АУ), рассчитанные по ТОЗМ
| Структура | АУ 1:5 | АУ 2:6 | АУ 3:7 | АУ 4:8 | АУ 5:9 | АУ 6:10 | АУ 7:11 |
|---|---|---|---|---|---|---|---|
| Удельный объем микропор W0, см3 г–1 | 0.35 | 0.57 | 0.79 | 1.01 | 1.23 | 1.45 | 1.67 |
| Эффективная ширина микропор X0, Å | 5.3 | 8.6 | 12.0 | 15.3 | 18.7 | 22.0 | 25.4 |
| Характеристическая энергия адсорбции бензола E0, кДж моль–1 | 45.5 | 27.8 | 20.0 | 15.7 | 12.8 | 10.9 | 9.5 |
| Характеристическая энергия адсорбции ацетона E, кДж моль–1 | 35.3 | 21.7 | 15.6 | 12.2 | 10.0 | 8.5 | 7.3 |
| Плотность адсорбента с микропорами ρad, г см–3 | 1.51 | 1.14 | 0.91 | 0.76 | 0.649 | 0.568 | 0.50 |
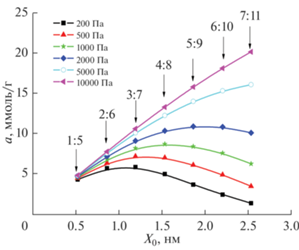
Используя СЭХ модельных адсорбентов (табл. 1), на основе ТОЗМ по уравнению ДР (1) рассчитали адсорбцию ацетона в изобарных условиях. Результаты проиллюстрированы на рис. 1, на котором можно видеть рост адсорбции ацетона с увеличением давления. При малых давлениях (p < 2000 Па) с ростом ширины микропор Х0 на изобарах наблюдается максимум адсорбции, обусловленный антибатным влиянием на адсорбцию двух факторов: рост адсорбции вследствие увеличения объема микропор и ослабление адсорбции за счет уменьшения характеристической энергии адсорбции ацетона. Такой подход был использован при анализе адсорбции метана на микропористых активных углях [18].
Рис. 1.
Зависимость адсорбции ацетона (С3Н6О) на модельных углеродных адсорбентах с микропорами, разделенными двухслойными углеродными стенками, от ширины микропор Х0 при температуре Т = 298 К в изобарных условиях.
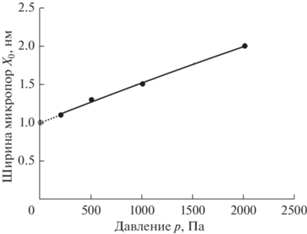
Как следует из рис. 1, в изотермических условиях максимум адсорбционной активности с ростом давления сдвигается в область более широких пор. На рис. 2 представлена зависимость положения этого максимума от давления. Экстраполяция зависимости (рис. 2) в область рабочих значений давления 0–150 ppm (0–3.8 Па) показывает, что адсорбционная активность адсорбента максимальна при ширине микропор вблизи (0.8–1.2) нм или в среднем ~1.0 нм. Адсорбент с такими порами обеспечивает максимальную адсорбцию ацетона и может быть эффективно использован в адсорбционных сенсорах ацетона в выдыхаемом воздухе.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Адсорбент
В данной работе в качестве микропористого углеродного адсорбента для АКС использовали микропористый углеродный адсорбент АР-1 производства АО “Сорбент” (г. Пермь, Россия). СЭХ адсорбента АР-1 определяли по изотерме адсорбции паров бензола при температуре 293 К на оригинальной адсорбционной вакуумной установке весового типа, изготовленной в ИФХЭ РАН [19, 20]. В табл. 2 представлены результаты расчета СЭХ адсорбента АР-1. На основании полученных данных (табл. 2, рис. 1) можно сделать заключение, что адсорбент АР-1 с эффективной шириной микропор X0 = 0.98 нм отвечает условию максимальной селективной адсорбции ацетона в модельной структуре АУ2-6 и может быть использован для обнаружения ацетона в выдыхаемом воздухе.
Таблица 2.
Структурно-энергетические характеристики микропористого углеродного адсорбента АР-1
| Удельный объем микропор, W0, см3/г | 0.59 |
| Стандартная характеристическая энергия адсорбции бензола, Е0, кДж/моль | 24.30 |
| Средняя эффективная полуширина микропор: x0, нм | 0.49 |
| Удельная поверхность, SБЭТ, м2/г | 1147 |
Адсорбат
В работе использовали ацетон (С3Н6О) марки ЧДА с чистотой по паспорту 99.9%. По данным [21] ацетон обладает следующими физико- химическими характеристиками: молекулярная масса М = 58.079 г/моль; нормальная температура кипения Т0 = 329.22 К; температура тройной точки 178.5 К; критическая температура Тс = 508 К; критическое давление рс = 4.76 МПа; критическая плотность ρс = 273 кг/м3.
Методика исследования
Частицу активного угля с размерами 3 × 0.5 × 0.8 мм наклеивали на торец кварцевого резонатора с номинальной частотой 200 кГц, изготовленный в ООО “Пьезо” (Россия). ПЭ резонатора имел форму прямоугольной пластины размерами 23 × 3.5 × × 0.7 мм (рис. 3). Присоединение адсорбента к ПЭ осуществлялось 2-компонентным эпоксидным клеем “Секунда” (Россия). Внешний вид АКС представлен на рис. 3, где 1 – ПЭ; 2 – гранула углеродного адсорбента, приклеенная к ПЭ 1; 3 – держатель ПЭ.
Рис. 3.
Адсорбционный кварцекристаллический сенсор ацетона. 1 – ПЭ, 2 – адсорбент, 3 – держатель ПЭ.

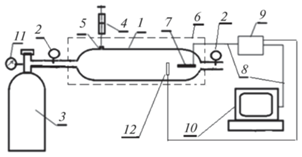
Экспериментальные исследования характеристик сенсоров проводили на стенде, схема которого представлена на рис. 4. В качестве анализируемого газа использовали ацетоноазотную смесь. Диапазон концентраций смеси задавали в пределах от 1 до 150 ppm. Необходимую концентрацию смеси формировали в баллоне 1 для подготовки газовой смеси (рис. 4) объемом ~3 л, который при открытых кранах 2 сначала продували азотом из баллона 3. Затем краны закрывали, и в баллон 1 микрошприцем 4 через мембрану 5 впрыскивали необходимый объем насыщенных паров ацетона или жидкий ацетон, который, испаряясь, образовывал смесь нужной концентрации. Для пассивного термостатирования сенсора баллон 1 был обернут в тепловую изоляцию 6. Сенсор 7 был соединен линией связи 8 с микропроцессором 9 и компьютером 10. Контролирование давления в баллоне 3 проводили с помощью манометра редуктора 11, а температуру в баллоне 1 – с использованием кварцевого датчика температуры (КДТ) 12, расположенного вблизи АКС.
Рис. 4.
Стенд для испытания сенсоров. 1 – баллон для подготовки газовой смеси, 2 – краны, 3 – баллон с сухим азотом, 4 – микрошприц, 5 – мембрана, 6 – тепловая изоляция, 7 – сенсор, 8 – линия связи, 9 – микропроцессор, 10 – компьютер, 11 – редуктор, 12 – кварцевый датчик температуры.
Измерение частоты, динамического сопротивления и добротности сенсора осуществлялось непрерывно до и после подачи ацетона в баллон процессором 5, а затем записывалось и выводилось на монитор компьютера через равные промежутки времени. Система измерения на основе микропроцессора 9 была описана в работах [22, 23]. В качестве КДТ использовали кварцевый преобразователь температуры ПТК-3МЦ с порогом чувствительности ±0.005 К и погрешностью ±0.05 К (СКТБ ЭлПА, г. Углич, Россия).
Результаты и их обсуждение
При исследовании характеристик АКС исходили из того, что его использование в приборе, измеряющем концентрацию паров ацетона в выдыхаемом воздухе, может проходить в режиме, когда в момент начала процесса измерения в память процессора записывается начальное “нулевое” значение частоты АКС, соответствующее отсутствию паров ацетона. Это снижает до нуля погрешности, связанные с нестабильностью нулевых показаний из-за временного дрейфа (старения сенсора) или температуры. Погрешность АКС при подобном режиме работы состояла в основном из погрешности, вызванной флуктуациями частоты (порог чувствительности), а также под воздействием изменения окружающей температуры за время измерения концентрации паров ацетона. Очевидно, что старением за время измерения (несколько минут) можно пренебречь.
Для определения порога чувствительности сенсора его выдерживали в условиях температурного режима с дрейфом температуры со скоростью не более ±0.1 К/мин, используя показания КДТ. На первом этапе измеряли флуктуацию частоты δfs в среде азота в течение 10 мин путем нескольких (10–12) последовательных замеров с интервалом 10–15 с, продолжая контролировать температуру в баллоне с сенсором. Затем вычисляли отклонения частоты от среднего значения (за вычетом обусловленного влиянием измеренного посредством КДТ дрейфа температуры). Величина отклонения по модулю не превышала 0.015 Гц.
На втором этапе было проведено исследование степени влияния клея на характеристики сенсоров. Для этого на один из торцов сенсора наносили клей и измеряли адсорбцию клеем паров ацетона. Величина адсорбции оказалась примерно в 100 раз меньше адсорбции активированным углем, т.е. влияние клея на характеристики сенсоров оказалось пренебрежимо малым. Далее исследовали такие параметры сенсоров, как коэффициент преобразования, статическую и динамическую характеристики процессов адсорбции.
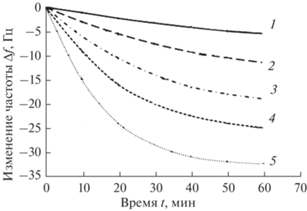
Известно, что переходные процессы адсорбции паров ацетона при концентрациях в единицы и десятки ppm занимают время от нескольких часов до нескольких суток [14]. В то же время, в связи с тем, что время получения информации о содержании сахара в крови в данный момент должно быть достаточно коротким, практический интерес представляют процессы измерения длительностью не более нескольких минут. Тем не менее, для более глубокого представления о кинетике процессов исследовано изменение частоты сенсора ∆f от времени t в течение 60 мин. с момента впрыска паров ацетона в баллон с сенсором. На рис. 5 представлены зависимости изменения частоты сенсора ∆f от времени t для концентраций паров ацетона от 3.3 до 150 ppm. Ход кривых (рис. 5) близок к экспоненциальному характеру. Но скорость адсорбции зависит от концентрации С паров ацетона. Поэтому при малых С изменение частоты ∆f, будучи относительно невелико и находясь на начальном участке экспоненты, практически пропорционально времени. С возрастанием С изменение частоты увеличивается, но скорость изменения снижается. Происходит отклонение от линейной зависимости и в дальнейшем изменение частоты практически прекращается.
Рис. 5.
Изменение частоты сенсора ∆f от времени t для различных концентраций паров ацетона: 1 – 3.3 ppm, 2 – 11 ppm, 3 – 27.5 ppm, 4 – 55 ppm, 5 – 150 ppm.
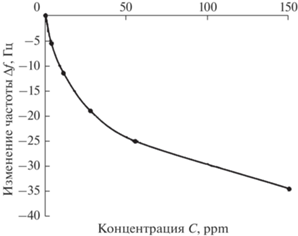
Зависимость ∆f от С для различных значений времени регистрации t приведены на рис. 6 (t = 60 мин) и рис. 7 (t = 1, 2, 3 мин).
Рис. 7.
Зависимость изменения частоты ∆f сенсора от концентрации паров ацетона С при различных t: 1 – 1 мин, 2 – 2 мин, 3 – 3 мин.
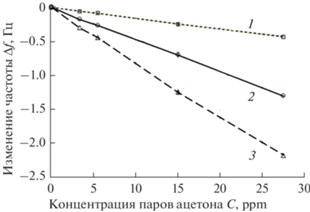
Зависимости при малых t представляют особый интерес, поскольку именно такие t приемлемы для медицинских приборов, особенно индивидуального пользования.
Порог чувствительности сенсора δС = δfs/S для t = 1 мин составил δС = 0.94 ppm, для 2 и 3 мин соответственно 0.3 и 0.2 ppm.
Для надежного контроля порогового значения концентрации в 2 ppm наиболее подходят режимы длительностью 2–3 мин. Им соответствует порог чувствительности соответственно 0.32 и 0.19 ppm.
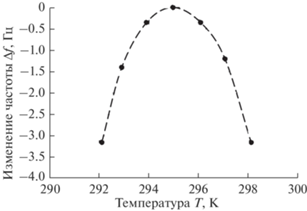
Поскольку в течение времени измерения могут происходить изменения окружающей температуры, мы проанализировали влияние температуры на изменение Δf частоты сенсора. Для этого сенсор, находящийся в баллоне с азотом, помещали в термокамеру, температуру в которой медленно (со скоростью не более 0.05 К/мин) изменяли в диапазоне от 292 до 298 К. Результаты измерений представлены на рис. 8.
Зависимость изменения частоты от температуры (рис. 8) с погрешностью ±0.05 Гц описывается полиномом 2-ой степени, что совпадает с температурно-частотной характеристикой кварцевых резонаторов продольных колебаний, на одном из типов которых реализован сенсор:
где Kt = 0.35 (Гц/К2) – коэффициент 2-го порядка температурной чувствительности сенсора.В соответствии с (3) температурную погрешность δС(T) сенсора рассчитывали по формуле
(4)
$\delta С(T){\text{ }} = {{\Delta f(T)} \mathord{\left/ {\vphantom {{\Delta f(T)} {{{S}_{k}}}}} \right. \kern-0em} {{{S}_{k}}}} = {{ - {{K}_{t}}{{{(T--295)}}^{2}}} \mathord{\left/ {\vphantom {{ - {{K}_{t}}{{{(T--295)}}^{2}}} {{{S}_{k}}}}} \right. \kern-0em} {{{S}_{k}}}},$Используя зависимость (4), можно рассчитать требования к режиму изменения температуры сенсора, чтобы δС(T) не превысило значение, соответствующие допустимой погрешности. Для выполнения требования δС(T) < 0.2 ppm ограничения по нестабильности температуры сенсора составят для t = 2 и t = 3 мин соответственно 0.2 и 0.16 К. Такие условия могут быть реализованы посредством пассивного термостатирования.
Таким образом, суммарная погрешность из-за основных источников нестабильности сенсора – фазовой и температурной – составит величину на уровне менее 0.5 ppm.
ЗАКЛЮЧЕНИЕ
Разработаны требования к микропористой структуре углеродного адсорбента для селективной адсорбции ацетона – газового маркера сахарного диабета из ацетоноазотной смеси. На основе ТОЗМ показано, что наиболее активными адсорбентами для адсорбции паров ацетона являются адсорбенты с шириной микропор 0.8–1.2 нм, в частности, активированный уголь АР-1. Разработан и изготовлен кварцекристаллический сенсор паров ацетона на основе этого угля. Проведены испытания сенсора в диапазоне 0–150 ppm, которые показали, что максимальное значение порога чувствительности сенсора при закончившихся адсорбционных процессах может достигать значений менее сотых долей ppm. Однако практической реализации этих исключительных возможностей препятствует большая инерционность адсорбции при малых концентрациях (менее 100 ppm).
Для определения концентрации паров ацетона в выдыхаемом воздухе для идентификации сахарного диабета предлагается использовать изменение частоты АКС через 2–3 мин после введения анализируемой смеси, что в сочетании с пассивным термостатированием обеспечивает измерение паров ацетона с погрешностью не более ±0.5 ppm.
Работа выполнена в ИФХЭ им. А.Н. Фрумкина РАН в соответствии с государственным заданием. Проект № 122011300053-8; планом Научного совета РАН по физической химии, тема № 20-03-460–01, а также в Национальном исследовательском ядерном университете “МИФИ” в соответствии с инициативным планом исследовательской работы.
Список литературы
Мезенцева М.А., Букрина Т.А. Неинвазивные методы измерения сахара в крови. Труды VI Научно-практической конференции “Информационно-измерительная техника и технологии”. Томск. 2015.
Атутов С.Н., Данилина Н.А., Микерин С.Л. и др. // Автометрия. 2014. Т. 50. № 4. С. 107.
Roberts K., Jaffe A., Verge Ch. et al // J. Diabetes Sci. and Technol. 2012. V. 6. Issue 3. P. 659.
Horváth I., Hunt J., Barnes P.J. // Eur. Respir. J. 2005. V. 26. P. 523.
Малов В.В. Пьезорезонансные датчики. М.: Энергоатомиздат, 1989.
Lucklum R., Hauptmann P. // Anal Bioanal Chem. 2006. V. 384. P. 667.
Cao1 Z., Murayama K., Aoki K. // Anal. Chim. Acta. 2001. V. 448. P. 47.
Russell S.P., Weinkauf D.H. // Polymer. 2001. V. 42. P. 2827.
Ramirez D., Qi Sh., Rood M. et al. // Environ. Sci. Technol. 2005. V. 39. P. 5864.
Cal M.P. // Dis. of D. Ph.: http://hdl.handle.net/2142/22021
Фомкин А.А., Симонов В.Н. // Пьезорезонансный сенсор микроконцентрации веществ // Патент РФ № 2722975. Госреестр изобретений РФ, 05.06.2020.
Потапов С.В., Фомкин А.А., Синицын В.А. и др. // Физикохимия поверхности и защита материалов. 2010. Т. 46. № 5. С. 445.
Кузнецова Т.А., Толмачев А.М., Крюченкова Н.Г. и др. // Физикохимия поверхности и защита материалов. 2013. Т. 49. № 4. 339.
Кельцев Н.В. Основы адсорбционной техники. М.: Химия, 1984.
Дубинин М.М. Адсорбция и пористость. М.: ВАХЗ, 1972.
Dubinin M.M. Carbon, 23(4): 373–380, 1985.
Яковлев В.Ю. Фомкин А.А. // Коллоидный журн. 2009. Т. 71. № 6. 860.
Меньщиков И.Е., Фомкин А.А., Школин А.В. и др. // Известия АН. Сер. Хим. 2018. Т. 67. № 10. С. 1814.
Фомкин А.А., Регент Н.И., Синицын В.А // Изв. АН. Сер. хим. 2000. № 6. 1018.
Shkolin A.V., Fomkin A.A. // Measurement Techniques. 2018. V. 61. № 4. P. 3951.
Варгафтик Н.Б. Справочник по теплофизическим свойствам газов и жидкостей. М.: Наука, 1972.
Симонов В.Н., Фомкин А.А., Власов Д.А. // Измерительная техника. 2016. № 10. С. 65.
Симонов В.Н., Власов Д.А. // Измерительная техника. 2019. № 3. С. 71.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов