Журнал аналитической химии, 2019, T. 74, № 6, стр. 445-454
Ионселективные электроды на основе поливинилхлорида, модифицированного п-трифторацетилбензоатными группами
Ю. В. Матвейчук 1, *, Е. М. Рахманько 1
1 Белорусский государственный университет, химический факультет
220030 Минск, ул. Ленинградская, 14, Беларусь
* E-mail: Yu_Matveychuk@mail.ru
Поступила в редакцию 31.10.2017
После доработки 11.04.2018
Принята к публикации 11.04.2018
Аннотация
Разработаны ионоселективные электроды (ИСЭ), обратимые к гидрофильным сульфат-, гидрофосфат- и сульфид-ионам, на основе модифицированного поливинилхлорида (МПВХ), сочетающего в себе функцию полимерной матрицы и нейтрального переносчика. Описана методика синтеза МПВХ, заключающаяся в прививке к ПВХ n-трифторацетилбензоатных групп. Ранее ИСЭ такого типа содержали в качестве основы ПВХ и гептиловый эфир n-трифторацетилбензойной кислоты (ГЭ n-ТФАБК). Использование МПВХ позволило значительно увеличить время жизни указанных ИСЭ за счет предотвращения изменений, связанных как с растворением ГЭ n-ТФАБК (для ${\text{Н Р О }}_{4}^{{2 - }}$-СЭ, S2–-СЭ, работающих в щелочных средах), так и с кристаллизацией гидратной формы ГЭ n-ТФАБК на поверхности мембран ${\text{SО }}_{4}^{{2 - }}$-СЭ, работающих в кислой среде.
Использование нейтральных переносчиков для разработки ионселективных электродов остается актуальным направлением в ионометрии [1–4]. Гептиловый эфир n-трифторацетилбензойной кислоты широко известен как карбонатный ионофор I [5–7], который также нашел применение в качестве нейтрального переносчика в мембранах ИСЭ, обратимых не только к ${\text{С O}}_{3}^{{2 - }},$ но и к ${\text{SО }}_{4}^{{2 - }},$ ${\text{М о О }}_{4}^{{2 - }},$ ${\text{WО }}_{4}^{{2 - }},$ ${{{\text{C}}}_{{\text{2}}}}{\text{O}}_{4}^{{2 - }}$ и др. [8–10].
Отмечено [11, 12], что пленочные ИСЭ на основе высших четвертичных аммониевых солей (ЧАС), содержащие в составе мембран нейтральный переносчик ГЭ n-ТФАБК, имеют малое время жизни (обратимые к ионам ${\text{SО }}_{4}^{{2 - }},$ ${\text{SeО }}_{4}^{{2 - }}$ – 2–3 недели, к ионам ${\text{Н Р О }}_{4}^{{2 - }},$ ${\text{М о О }}_{4}^{{2 - }}$ – 10 дней, к ионам S2– – 3–4 дня). Малые сроки эксплуатации можно объяснить следующим образом: в случае ИСЭ, работающих в кислой среде (${\text{SО }}_{4}^{{2 - }},$ ${\text{SeО }}_{4}^{{2 - }}$-СЭ, рН 3–3.5), происходит постепенная гидратация ГЭ n‑ТФАБК и выход на поверхность мембраны гем-диольной формы ГЭ n-ТФАБК с последующей ее кристаллизацией (рис. 1); в случае ИСЭ, работающих в щелочной среде (${\text{Н Р О }}_{4}^{{2 - }}$-СЭ, рН 10; S2–-СЭ, рН 12.8–13.0), происходит ионизация сольватирующей добавки и ее постепенное растворение.
Рис. 1.
Изображения, полученные с помощью сканирующего электронного микроскопа LEO-1420 кристаллов ГЭ n-ТФАБК (а), мембраны ${\text{SО }}_{4}^{{2 - }}$-СЭ на основе ГЭ n-ТФАБК после 3 нед. эксплуатации (б); мембраны ${\text{SО }}_{4}^{{2 - }}$-СЭ без ГЭ n-ТФАБК после 3 нед. эксплуатации (в).

Как первый, так и второй процессы приводят к уменьшению концентрации карбонильной формы ГЭ n-ТФАБК с течением времени до значений, сопоставимых с концентрацией ЧАС и, как следствие, к заметному ухудшению аналитических характеристик. Для проявления высокой селективности к потенциалопределяющим ионам содержание сольватирующей добавки в мембране должно быть больше содержания (ЧАС+)2An2−, чтобы в системе могло образоваться достаточное количество комплексов An2− с ГЭ n-ТФАБК. Кроме того, при хранении мембран, содержащих ГЭ n-ТФАБК, наблюдается экссудация (“выпотевание”) сольватирующей добавки.
Одна из важных тенденций, связанных с новыми мембранными материалами, – замена традиционных компонентов мембран (пластификатора, полимера, ионофора) модифицированными материалами. Иммобилизация ионофоров на полимерной матрице – один из путей увеличения времени жизни ИСЭ, а также повышения устойчивости по отношению к анализируемому раствору [4].
В данной работе апробирован новый электродный материал – трифторацетилбензоатный поливинилхлорид (ТФАБ-ПВХ) – для изготовления ИСЭ на основе высших ЧАС, обратимых к ионам S2–, ${\text{SО }}_{4}^{{2 - }}$ и ${\text{Н Р О }}_{4}^{{2 - }}.$ Это позволило предотвратить негативные изменения, связанные с поведением ГЭ n-ТФАБК в мембранах и существенно увеличить время жизни ИСЭ. Предложенные ИСЭ функционируют при различных рН (S2−-СЭ при рН 12.9; ${\text{SО }}_{4}^{{2 - }}$-СЭ при рН 3.2; ${\text{Н Р О }}_{4}^{{2 - }}$-СЭ при рН 10), что дает возможность изучить химическую стабильность ТФАБ-ПВХ.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез трифторацетилбензоатного поливинилхлорида. Реагенты: хлорид 1-бутил-3-метилимидазолия (БМИМ+Cl–) ч. (BASF), n-трифторацетилбензойная кислота (синтезирована по методике [13]), диметилсульфоксид (ДМСО) х. ч., тетрагидрофуран (ТГФ) (Fluka AG), поливинилхлорид (Fluka AG).
Хлорид 1-бутил-3-метилимидазолия (0.60 г) смешивают с n-трифторацетилбензойной кислотой (0.40 г) и нагревают при 90°С в вакууме водоструйного насоса до образования гомогенной системы и прекращения выделения газа. Полученную ионную жидкость растворяют в 7 мл диметилсульфоксида. Отдельно в 10.0 мл ТГФ растворяют при нагревании 1.00 г ПВХ. Растворы смешивают и нагревают с обратным холодильником при перемешивании магнитной мешалкой в течение 3 ч, поддерживая равномерное кипение ТГФ, после чего реакционную смесь охлаждают до комнатной температуры и по каплям при интенсивном перемешивании прибавляют к 200 мл дистиллированной воды. Выпавший осадок отфильтровывают, промывают несколько раз дистиллированной водой и сушат на воздухе при комнатной температуре. Схема синтеза представлена на схеме 1 .
Схема 1 . Схема синтеза трифторацетилбензоатного поливинилхлорида (ТФАБ-ПВХ).
Содержание n-трифторацетилбензоатных фрагментов в ТФАБ-ПВХ оценивали методом ИК-спектроскопии с использованием метода градуировочного графика в координатах интенсивность поглощения карбонильной группы–содержание n-трифторацетилбензоатных фрагментов. В качестве стандартных образцов использовали пленки ПВХ с различным содержанием n-ТФАБК. Содержание трифторацетилбензоатных фрагментов в ТФАБ-ПВХ составляло 16%.
ИК-спектры регистрировали на спектрометре Bruker ALPHA с приставкой нарушенного полного внутреннего отражения ATR Di в диапазоне волновых чисел от 4000 до 400 см–1. Запись спектров проводили через 4 см–1.
Мембраны ионселективных электродов на основе поливинилхлорида изготавливали по стандартной методике [14]. Они содержали следующие компоненты: ПВХ (Fluka AG) – 33 мас. %, ионообменник − 5 мас. %, сольватирующая добавка (ГЭ n-ТФАБК) – от 0 до 20 мас. %, пластификатор − остальное. Растворитель мембранной композиции – ТГФ (Fluka AG).
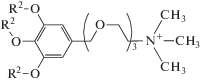
Мембраны ИСЭ на основе ТФАБ-ПВХ содержали следующие компоненты: ТФАБ-ПВХ – 50 мас. %, ионообменник – 5 или 2 мас. %, пластификатор − остальное. В качестве ионообменника использовали хлорид 3,4,5-трисдодецилоксибензил(оксиэтил)3триметиламмония ((оксиэтил)3ТМ, схема 2 ), синтез которого описан в работе [15]; в качестве пластификаторов мембран – 1-бромнафталин ч. д. а. (1-БН), о-нитрофенилдециловый эфир (о-НФДЭ). Состав мембран ИСЭ по ионообменнику и пластификатору был оптимизирован в работах [11, 12].
Схема 2 . Структурная формула хлорида 3,4,5-трисдодецилоксибензил(оксиэтил)3триметиламмония.
Для приготовления растворов использовали K2SO4 ч., KCl ч. д. а., NaBr ч., KNO3 ч. д. а., Н3РО4 ч., Ва(ОН)2 · 8Н2О ч. д. а., Na2HPO4 · 2H2O ч., аммиак водный х. ч., Na2S · 9Н2О ч. д. а.
После изготовления мембраны всех ИСЭ вымачивали в течение 2 сут в 0.1 М растворах соответствующих солей. В качестве внутреннего раствора для всех ИСЭ использовали смесь 1 × 10−2 М соответствующей соли и 1 × 10−3 М KCl.
В растворе сульфида натрия рН поддерживали на уровне 12.9 ± 0.1 с помощью раствора Ва(ОН)2, который связывает СО2 из воздуха, тем самым устраняя мешающее влияние карбонат-ионов и подкисление раствора; в растворе сульфата калия на уровне 3.2 ± 0.1 с помощью ортофосфорной кислоты; в растворе гидрофосфата натрия на уровне 10 ± 0.2 с помощью разбавителя, представляющего собой дистиллированную воду, подщелоченную раствором аммиака. Соответствующие значения рН поддерживали и в растворах мешающих ионов при изучении селективности разработанных ИСЭ.
Ионселективные электроды калибровали как методом последовательного, так и двукратного разбавления. Коэффициенты потенциометрической селективности (lg KPot(i, j)) определяли методом отдельных растворов в варианте равных потенциалов основного и мешающего ионов (SSM) [15]; все остальные характеристики – в соответствии с рекомендациями [14].
Активности ионов в градуировочных растворах рассчитывали согласно теории Дебая–Хюккеля [16].
Потенциал исследуемой электрохимической ячейки измеряли иономером И-160.1МП при 22 ± 1°С. В качестве электрода сравнения использовали хлоридсеребряный электрод ЭВЛ-1М3.1, для определения рН – стеклянный электрод ЭСЛ-43-07СР.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
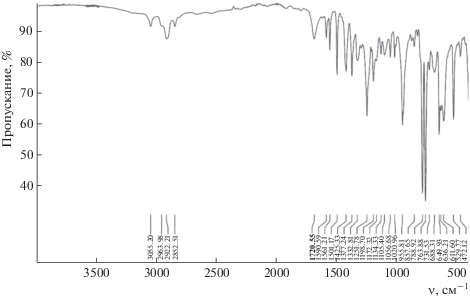
На рис. 2 представлен ИК-спектр используемого ТФАБ-ПВХ. Высокоинтенсивная полоса при 1689 см–1 относится к валентным колебаниям карбонильной группы ν(СО) сложноэфирного фрагмента. Карбонильная группа трифторацетильной группировки в спектре ТФАБ-ПВХ не проявляется, так как она находится в гидратной форме (валентные колебания ОН-групп в виде уширенных полос поглощения при >3100 см–1) [17].
На рис. 3 представлен ИК-спектр мембраны на основе ТФАБ-ПВХ. Видно, что в спектре присутствует только полоса 1720 см–1, относящаяся к ν(С=О) как карбонильной группы трифторацетилбензоатных фрагментов, так и карбонильной группы [17]. Дегидратация исходного ТФАБ-ПВХ протекает в процессе испарения тетрагидрофурана при изготовлении мембран ИСЭ.
Рис. 3.
ИК-спектр мембраны на основе трифторацетилбензоатного поливинилхлорида (пластификатор – 1-бромнафталин).
Изменение аналитических характеристик ${\mathbf{S}}О _{{\mathbf{4}}}^{{{\mathbf{2}}--}}$-СЭ, $HPO_{{\mathbf{4}}}^{{{\mathbf{2}}--}}$-СЭ, S2–-СЭ в зависимости от времени эксплуатации. На рис. 4 представлены электродные функции ${\text{SО }}_{4}^{{2 - }}$-СЭ, ${\text{Н Р О }}_{4}^{{2 - }}$-СЭ, S2–-СЭ на основе ПВХ и ГЭ n-ТФАБК. В табл. 1–3 приведены данные по изменению аналитических характеристик ${\text{SО }}_{4}^{{2 - }}$-СЭ, ${\text{Н Р О }}_{4}^{{2 - }}$-СЭ, S2–-СЭ в зависимости от времени эксплуатации. Видно, что все три ИСЭ обладают достаточно хорошими исходными аналитическими характеристиками, которые сохраняются непродолжительное время.
Рис. 4.
Электродные функции ионселективных электродов на основе ПВХ, (оксиэтил)3ТМ (5 мас. %.): 1 – ${\text{Н Р О }}_{4}^{{2 - }}$-СЭ (пластификатор –о-нитрофенилдециловый эфир), 2 – ${\text{SО }}_{4}^{{2 - }}$-CЭ (пластификатор – 1-бромнафталин), 3 – S2–-CЭ (пластификатор – 1-бромнафталин).
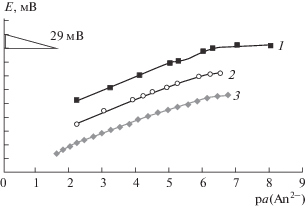
Таблица 1.
Изменение аналитических характеристик ${\text{SО }}_{4}^{{2 - }}$-СЭ (на основе (оксиэтил)3TM, 1-БН, ГЭ n-ТФАБК)
| Характеристика | Время, сут | |||||
|---|---|---|---|---|---|---|
| 1 | 5 | 10 | 15 | 20 | 25 | |
| ПО*, M | 6.3 × 10–7 | 6.5 × 10–7 | 6.5 × 10–7 | 7.0 × 10–7 | 1.0 × 10–6 | 2.0 × 10–6 |
| Наклон, мВ/декада | 27.5 ± 0.3 | 27.5 ± 0.3 | 27.5 ± 0.3 | 27.0 ± 0.3 | 26.5 ± 0.5 | 26.0 ± 0.6 |
| lg КPot(${\text{SО }}_{4}^{{2 - }}$/Cl─) | –2.2 ± 0.2 | –2.2 ± 0.2 | –2.2 ± 0.2 | –2.1 ± 0.2 | –1.8 ± 0.2 | –1.3 ± 0.2 |
| Дрейф, мВ/ч; с(${\text{SО }}_{4}^{{2 - }}$) = 1 × 10−3 M | 0.3 | 0.4 | 0.4 | 0.8 | 2.9 | 7.0 |
| Время отклика, с; с(${\text{SО }}_{4}^{{2 - }}$) = 1 × 10−3−1 × 10−4 M | 30 | 30 | 35 | 65 | 240 | 380 |
| Воспроизводимость, мВ; с(${\text{SО }}_{4}^{{2 - }}$) = 1 × 10−3 M | 0.3 | 0.3 | 0.4 | 0.8 | 3.5 | 7.2 |
Таблица 2.
Изменение аналитических характеристик ${\text{Н Р О }}_{4}^{{2 - }}$-СЭ (на основе (оксиэтил)3TM, о-НФДЭ, ГЭ n-ТФАБК)
| Характеристика | Время, сут | |||||
|---|---|---|---|---|---|---|
| 1 | 5 | 7 | 10 | 13 | 15 | |
| ПО, M | 7.1 × 10–7 | 7.5 × 10–7 | 7.7 × 10–7 | 9.5 × 10–7 | 2.0 × 10–6 | 3.5 × 10–6 |
| Наклон, мВ/декада | 27.3 | 27.3 | 26.9 | 26.0 | 26.0 | 26.0 |
| lg КPot(${\text{Н Р О }}_{4}^{{2 - }}$/Cl─) | –2.4 ± 0.1 | –2.4 ± 0.1 | –2.4 ± 0.1 | –2.1 ± 0.1 | –1.8 ± 0.1 | –1.5 ± 0.1 |
| Дрейф, мВ/ч; с(${\text{Н Р О }}_{4}^{{2 - }}$) = 1 × 10−3 M | 1.3 | 1.3 | 1.5 | 1.9 | 3.0 | 4.8 |
| Время отклика, с; с(${\text{Н Р О }}_{4}^{{2 - }}$) = 1 × 10−3−1 × 10−4 M | 35 | 35 | 35 | 80 | 120 | 160 |
| Воспроизводимость, мВ; с(${\text{Н Р О }}_{4}^{{2 - }}$) = 1 × 10−3 M | 0.7 | 0.8 | 0.8 | 1.2 | 2.4 | 4.8 |
Таблица 3.
Динамика изменения аналитических характеристик S2–-СЭ (на основе (оксиэтил)3TM, 1-БН, ГЭ n-ТФАБК)
| Характеристика | Время, сут | |||||
|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | |
| ПО, M | 5.0 × 10–7 | 5.0 × 10–7 | 6.0 × 10–7 | 7.3 × 10–7 | 1.0 × 10–6 | 3.0 × 10–6 |
| Наклон, мВ/декада | 27.1 | 27.1 | 26.8 | 26.5 | 26.0 | 26.0 |
| lgКPot(S2–/Cl–) | –1.3 ± 0.1 | –1.3 ± 0.1 | –1.1 ± 0.1 | –1.0 ± 0.1 | –0.8 ± 0.1 | –0.6 ± 0.1 |
| Дрейф, мВ/ч; с(S2–) = 1 × 10−3 M | 1.8 | 1.8 | 2.3 | 2.8 | 3.5 | 6.7 |
| Время отклика, с; с(S2─) = 1 × 10−3−1 × 10−4 M | 40 | 40 | 60 | 75 | 100 | 220 |
| Воспроизводимость, мВ; с(S2─) = 1 × 10−3 M | 0.8 | 0.8 | 1.0 | 1.4 | 5.5 | 9.7 |
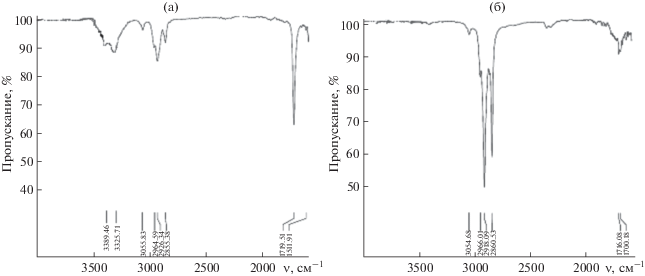
На рис. 5а представлен ИК-спектр мембраны после 2 нед. эксплуатации, на рис. 5б – после 4 нед. эксплуатации. Видно, что после 4 нед. эксплуатации в спектре появляется высокоинтенсивная полоса 1689 см−1, относящаяся к сложноэфирной группе (пластификатор 1-бромнафталин не имеет полос поглощения в области 1650–1750 см–1). При этом полоса 1721 см–1 полностью не исчезает, т.е. гидратная и карбонильная формы ГЭ n-ТФАБК находятся в равновесии. Появляются также полосы 3324, 3386 см–1, относящиеся к ν(ОН). По мере накопления гидратной формы ГЭ n-ТФАБК электродные характеристики ${\text{SО }}_{4}^{{2 - }}$-СЭ значительно ухудшаются.
Рис. 5.
Фрагменты ИК-спектров мембраны на основе ГЭ n-ТФАБК: (а) – 2 нед. эксплуатации, (б) – 4 нед. эксплуатации.

На рис. 6 показаны ИК-спектры мембраны S2–-СЭ на первые (а) и на шестые сутки от начала эксплуатации (б). В спектре мембраны (рис. 6а) наблюдается интенсивная полоса при 1719 см−1, относящаяся к ν(С=О) карбонильной группы как трифторацетильной группировки, так и карбоксильной группы. На шестые сутки эксплуатации происходят заметные изменения в спектре: практически исчезают полосы 1719, 3389, 3325 см−1, что указывает на растворение нейтрального переносчика.
Рис. 6.
Фрагменты ИК-спектров мембраны на основе гептилового эфира n-трифторацетилбензойной кислоты: (а) – 1-е сут эксплуатации, (б) – 6-е сут эксплуатации.
Ионселективные электроды на основе трифторацетилбензоатного поливинилхлорида (ТФАБ-ПВХ). На рис. 7 представлены электродные функции ${\text{SО }}_{4}^{{2 - }}$-СЭ, ${\text{Н Р О }}_{4}^{{2 - }}$-СЭ, S2–-СЭ на основе ТФАБ-ПВХ. В табл. 4 приведены выборочные аналитические характеристики ${\text{SО }}_{4}^{{2 - }}$-СЭ, в табл. 5 – ${\text{Н Р О }}_{4}^{{2 - }}$-СЭ, в табл. 6 – S2–-СЭ в сравнении с результатами, полученными для ИСЭ, изготовленных на основе ПВХ с добавлением и в отсутствие сольватирующей добавки (20 мас. %). Видно, что при сопоставимых концентрациях ГЭ n-ТФАБК в мембранах из обычного ПВХ и n-трифторацетильных групп в ТФАБ-ПВХ электродные характеристики ${\text{SО }}_{4}^{{2 - }}$-СЭ, ${\text{Н Р О }}_{4}^{{2 - }}$-СЭ и S2–-СЭ имеют достаточно близкие значения, особенно при содержании ЧАС в мембранах 2 мас. %. Уменьшением содержания ЧАС достигается увеличение мольного соотношения n(ГЭ n-ТФАБК) : n(ЧАС).
Рис. 7.
Электродные функции ионселективных электродов на основе трифторацетилбензоатного поливинилхлорида (50 мас. %), (оксиэтил)3ТМ (5 мас. %): 1 – ${\text{Н Р О }}_{4}^{{2 - }}$-СЭ (пластификатор – о-нитрофенилдециловый эфир), 2 – ${\text{SО }}_{4}^{{2 - }}$-CЭ (пластификатор – 1-бромнафталин), 3 – S2–-CЭ (пластификатор – 1-бромнафталин).
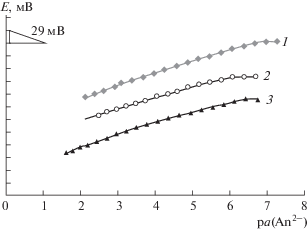
Таблица 4.
Сравнение аналитических характеристик ${\text{SО }}_{4}^{{2 - }}$-СЭ
| Характеристика | Серия ИСЭ | Состав ИСЭ | |
|---|---|---|---|
| (оксиэтил)3ТМ 5 мас. %, 1-БН |
(оксиэтил)3ТМ 2 мас. %, 1-БН |
||
| ПО, М | А | 1.0 × 10–6 | 7.9 × 10–7 |
| Б | 7.0 × 10–7 | 6.3 × 10–7 | |
| В | 1.3 × 10–6 | – | |
| lg КPot(${\text{SО }}_{4}^{{2 - }},$ Cl─) | А | –1.4 | –1.7 |
| Б | –2.1 | –2.25 | |
| В | 0.2 | – | |
| lg КPot(${\text{SО }}_{4}^{{2 - }},$ Br─) | А | –0.95 | –1.25 |
| Б | –1.8 | –1.9 | |
| В | 1.0 | – | |
| lg КPot(${\text{SО }}_{4}^{{2 - }},$${\text{NО }}_{3}^{ - }$) | А | 0.3 | 0.2 |
| Б | –0.3 | –0.45 | |
| В | 1.2 | – | |
| Наклон, мВ/декада | А | 25.7 | 26.5 |
| Б | 26.5 | 27.2 | |
| В | 28.1 | – | |
| Время жизни, сут | А | 70 | |
| Б | 20 | ||
| В | 80 | ||
Таблица 5.
Сравнение аналитических характеристик ${\text{Н Р О }}_{4}^{{2 - }}$-СЭ
| Характеристика | Серия ИСЭ | Состав ИСЭ | |
|---|---|---|---|
| (оксиэтил)3ТМ 5 мас. %, о-НФДЭ |
(оксиэтил)3ТМ 2 мас. %, о-НФДЭ |
||
| ПО, М | А | 7 × 10–7 | 5.0 × 10–7 |
| Б | 5.0 × 10–7 | 4.5 × 10–7 | |
| В | 1.0 × 10–6 | 1.0 × 10–6 | |
| lg КPot(${\text{Н Р О }}_{4}^{{2 - }},$${\text{SО }}_{4}^{{2 - }}$) | А | –0.8 | –1.0 |
| Б | –1.1 | –1.3 | |
| В | –0.05 | –0.1 | |
| lg КPot(${\text{Н Р О }}_{4}^{{2 - }},$ Cl–) | А | –1.6 | –2.0 |
| Б | –2.2 | –2.65 | |
| В | 0.4 | 0.4 | |
| lg КPot(${\text{Н Р О }}_{4}^{{2 - }},$${\text{NО }}_{3}^{ - }$) | А | 0.9 | 0.5 |
| Б | 0.3 | 0.0 | |
| В | 3.0 | 2.9 | |
| Наклон, мВ/декада | А | 27.5 | 28.4 |
| Б | 28.7 | 28.5 | |
| В | 27.3 | 26.8 | |
| Время жизни, сут | А | 50 | |
| Б | 10 | ||
| В | 70 | ||
Примечание: А, Б, В – см. в примечании к табл. 4.
Таблица 6.
Сравнительный анализ S2–-СЭ
| Характеристика | Серия ИСЭ | Состав ИСЭ: (оксиэтил)3ТМ 5 мас. %, 1-БН |
|---|---|---|
| ПО, М | А | 6.0 × 10–7 |
| Б | 3.8 × 10–7 | |
| В | 7.6 × 10–7 | |
| lg КPot(S2–, Br─) | А | –0.9 |
| Б | –1.35 | |
| В | –0.35 | |
| lg КPot(S2–, Cl─) | А | –1.3 |
| Б | –1.55 | |
| В | –0.9 | |
| lg КPot(S2–, ${\text{NO}}_{3}^{ - }$) | А | –0.4 |
| Б | –0.75 | |
| В | 0.35 | |
| Наклон, мВ/декада | А | 27.1 |
| Б | 27.1 | |
| В | 27.4 | |
| Время жизни, сут | А | 10 |
| Б | 3–4 | |
| В | 20 |
Примечание: А, Б, В – см. в примечании к табл. 4.
Главный результат проведенного исследования – существенное увеличение времени жизни ИСЭ, так как за счет ковалентного связывания n-ТФАБК удается, во-первых, предотвратить быстрое растворение нейтрального переносчика и увеличить время жизни даже S2–-СЭ, работающего при рН ~ 13, с 3–4 до 10 дней, во-вторых, предотвратить выход на поверхность гидратной формы ГЭ n-ТФАБК для ${\text{SО }}_{4}^{{2 - }}$-СЭ, работающего при рН ~ 3, и тем самым увеличить его время жизни с 20 до 70 дней. Таким образом, ТФАБ-ПВХ – это материал, проявляющий повышенную по сравнению с традиционными композициями химическую устойчивость даже в сильнощелочной среде.
* * *
Таким образом, синтезирован и исследован электродный материал – поливинилхлорид, содержащий n-трифторацетилбензоатные группы, сочетающий функции полимерной матрицы и нейтрального переносчика. Использование этого материала позволяет существенно увеличить время жизни ИСЭ, обратимых к гидрофильным сульфат-, гидрофосфат- и сульфид-ионам, которые работают как в кислых, так и в щелочных средах. Электродные характеристики ИСЭ на основе МПВХ и ИСЭ на основе обычного ПВХ с добавкой ГЭ n-ТФАБК близки.
Список литературы
Umezawa Yo., Umezawa K., Bühlmann Ph., Hamada N., Aoki H., Nakanishi J., Sato M., Xiao K.P., Nishimura Yu. Potentiometric selectivity coefficients of ion-selective electrodes Part II. Inorganic anions (Technical report) // Pure Appl. Chem. 2002. V. 74. № 6. P. 923.
Bühlmann Ph., Chen L.D. Ion-selective electrodes with ionophore-doped sensing membranes / Supramolecular chemistry from molecules to nanomaterials / Eds. Gale P.A., Steed J.W. N.Y.: John Wiley & Sons, Ltd, 2012. V. 5. P. 2539.
Bühlmann Ph., Pretsch E., Bakker E. Carrier-based ion-selective electrodes and bulk optodes. 2. Ionophores for potentiometric and optical sensors // Chem. Rev. 1998. V. 98. P. 1593.
Михельсон К.Н., Печенкина И.А. Материалы мембран ионоселективных электродов на основе ионофоров: проблемы и достижения (обзор) // Электрохимия. 2015. Т. 51. № 2. С. 115.
Beer D., Bissett A., Wit R., Jonkers H., Köhler-Rink S., Nam H., Kim B.H., Eickert G., Grinstain M. A microsensor for carbonate ions suitable for microprofiling in freshwater and saline environments // Limnol. Oceanogr.: Methods 6. 2008. P. 532.
Abramova N., Levichev S., Bratov A. The influence of CO2 on ISFETs with polymer membranes and characterization of a carbonate ion sensor // Talanta. 2010. V. 81. P. 1750.
Behringer Ch., Lehmann B., Haug J.-P., Seiler K., Morf W.E., Hartman K., Simon W. Anion selectivities of trifluoroacetophenone derivatives as neutral ionophores in solvent-polymeric membranes // Anal. Chim. Acta. 1990. V. 233. P. 41.
Lomako S.V., Astapovich R.I., Nozdrin-Plotnitskaya O.V., Pavlova T.E., Shi Lei, Nazarov V.A., Okaev E.B., Rakhman’ko E.M., Egorov V.V. Sulfate-selective electrode and its application for sulfate determination in aqueous solutions // Anal. Chim. Acta. 2006. V. 562. P. 216.
Матвейчук Ю.В., Рахманько Е.М., Жилко В.В. Новые пленочные молибдат- и вольфрамат-селективные электроды на основе высших ЧАС с различной стерической доступностью обменного центра // Методы и объекты хим. анализа. 2017. Т. 12. № 1. С. 240.
Рахманько Е.М., Матвейчук Ю.В., Станишевский Л.С., Ясинецкий В.В. Оксалатселективный электрод и его применение в анализе // Журн. аналит. химии. 2015. Т. 70. № 7. С. 758. (Rakhman’ko E.M., Matveichuk Yu.V., Stanishevskii L.S., Yasinetskii V.V. An oxalate-selective electrode and its application to analysis // J. Analyt. Chem. 2015. V. 70. № 7. Р. 873.)
Матвейчук Ю.В. Влияние гептилового эфира n-трифторацетилбензойной кислоты на аналитические характеристики сульфат-селективных электродов / “Аналитика РБ–2017” Тез. докл. Пятой респ. конф. по аналит. химии с межд. участием, Минск, 19–20 мая 2017 г. Минск: Изд. центр БГУ, 2017. С. 16.
Матвейчук Ю.В., Рахманько Е.М., Окаев Е.Б., Рассадина Д.С. Гидрофосфат-селективные электроды на основе высших четвертичных аммониевых солей со стерически доступным обменным центром / “Аналитика РБ–2017” Тез. докл. Пятой респ. конф. по аналит. химии с межд. участием, Минск, 19–20 мая 2017 г. Минск: Изд. центр БГУ, 2017. С. 18.
Синтезы фторорганических соединений (мономеры и промежуточные продукты) / Под ред. Кнунянца И.Л., Якобсона Г.Г. М.: Химия, 1977. С. 252.
Камман К. Работа с ионоселективными электродами. М.: Мир, 1980. 288 с.
Bakker E., Pretsch E., Bühlmann Ph. Selectivity of potentiometric ion sensors // Anal. Chem. 2000. V. 72. P. 1127.
Dean J.A. Lange’s handbook of chemistry. McGRAW-HILL, INC., 1999. 1291 p.
Stuart B.H. Infrared spectroscopy: Fundamentals and applications. N.Y.: Wiley, 2004.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии