Доклады Российской академии наук. Химия, науки о материалах , 2021, T. 501, № 1, стр. 20-26
Синтез, свойства и применение гомополиимидов на основе 3,5-диаминобензойной кислоты
А. В. Чучалов 1, 2, *, Б. А. Байминов 1, Ю. В. Биличенко 2, А. Ф. Косолапов 3, С. Л. Семенов 3, Е. Г. Кононова 1, М. И. Бузин 1, Е. М. Чайка 1, Е. С. Афанасьев 1, Д. А. Сапожников 1, Я. С. Выгодский 1
1 Институт элементоорганических соединений
им. А.Н. Несмеянова Российской академии наук
119991 Москва, Россия
2 Российский химико-технологический университет
им. Д.И. Менделеева
125047 Москва, Россия
3 Научный центр волоконной оптики
им. Е.М. Дианова РАН – обособленное подразделение Федерального исследовательского центра “Институт общей физики им. А.М. Прохорова Российской академии наук
119333 Москва, Россия
* E-mail: soul551@rambler.ru
Поступила в редакцию 30.09.2021
После доработки 12.11.2021
Принята к публикации 15.11.2021
Аннотация
Методом одностадийной высокотемпературной поликонденсации в N-метил-2-пирролидоне получены карбоксилсодержащие гомополиимиды на основе 3,5-диаминобензойной кислоты и диангидридов различных тетракарбоновых кислот. Изучено влияние строения диангидрида на свойства формируемых полимеров и показана возможность их применения in situ при изготовлении высокотермостабильных первичных покрытий кварцевых световодов.
ВВЕДЕНИЕ
Ароматические полиимиды (ПИ) обладают качествами, востребованными в современных высокотехнологичных областях: термостойкостью, высокими механическими характеристиками при повышенных и пониженных температурах (вплоть до криогенных), радиационной стойкостью, а доступность сырьевой базы делает их одними из наиболее перспективных термостойких полимеров. На основе полиимидов изготавливают лаки и пленки электроизоляционного назначения (пазовая изоляция, изоляция проводов и кабелей, ленточные провода и кабели и т.п.). Они используются также в качестве мембран, пен, связующих в производстве стекло- и углепластиков, высокомодульных композиционных материалов и т.д. ПИ также находят все большее применение и в роли защитных покрытий световодов [1–6].
Ранее была показана возможность применения органорастворимых ПИ в качестве защитных покрытий световодов [4, 5, 7, 8]. Для достижения необходимой адгезии ПИ-покрытия к поверхности световода и его стабильности во время термических и механических испытаний в раствор ПИ добавляют аппрет, однако раствор с аппретом нестабилен и образует гель через непродолжительное время [9].
Другим известным способом улучшения адгезии является введение в полимер дополнительных функциональных групп, формирующих, например, водородные связи с субстратом. Показано [8–10], что использование 3,5-диаминобензойной кислоты (ДАБК) позволяет добиться удовлетворительной адгезии ПИ к поверхности кварцевого световода без добавления аппрета. Однако в данных работах описываются, как правило, сополиимиды на основе дорогостоящих кардовых и других мономеров, а ДАБК используется как сомономер.
Перспективность карбоксилсодержащих полиимидов (КПИ) не ограничивается их применением в роли защитных покрытий. Они представляют значительный интерес для газоразделения [11, 12], электрохимических устройств [13, 14], аэрогелей [15] и создания композиционных материалов различного назначения [16–18]. Основным способом синтеза КПИ в указанных публикациях является двухстадийный метод, имеющий ряд существенных недостатков [7].
Настоящая работа посвящена одностадийному синтезу гомополиимидов на основе 3,5-диаминобензойной кислоты и диангидридов различных тетракарбоновых кислот, в том числе недорогих и многотоннажных, в N‑метил-2-пирролидоне, изучению их свойств и исследованию возможности применения полученных растворов КПИ in situ в изготовлении защитных покрытий кварцевых световодов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Исходные соединения очищали сублимацией в вакууме (20 Па) при температуре, близкой к температуре плавления (в скобках приведены значения Тпл по данным каталога Aldrich): 3,5-диаминобензойная кислота Тпл = 235–238°C (235–238°C); диангидриды 2,2-бис-(3,4-дикарбоксифенил)-1,1,1,3,3,3-гексафторпропана Тпл = 244–245°C (244–247°C), бензофенон-3,3',4,4'-тетракарбоновой кислоты Тпл = 218–221°C (218–222°C), бензол-1,2,4,5-тетракарбоновой кислоты Тпл = = 218–221°C (218–222°C), 3,3',4,4'-тетракарбокcидифенилоксида Тпл = 229–230°C (225–229°C) и 3,3-бис-(3,4-дикарбоксифенил)фталида Тпл = 259–260°C (260–261°C).
N-метил-2-пирролидон (N-МП) перегоняли над CaH2 в вакууме. N,N-Диметилформамид (ДМФА), диметилсульфоксид (ДМСО), хлороформ (ХЛФ) и циклогексанон (ЦГН) использовали без предварительной очистки.
Синтез полиимидов. (Со)полиимиды синтезировали высокотемпературной поликонденсацией эквимольных количеств диангидридов тетракарбоновых кислот и 3,5-диаминобензойной кислоты в N-МП. Концентрация полимера в растворе 0.25 г мл–1. Реакцию проводили при 180°С в течение 5–6 ч в среде аргона. Полимеры выделяли осаждением из полученных после синтеза растворов в метанол. Образцы полимеров промывали метанолом в приборе Сокслета в течение двух дней, после чего сушили в вакууме при 200°С до постоянной массы. Выход ПИ близок к количественному.
Изготовление пленок и покрытий. Пленки полимеров получали поливом растворов в N-МП на стеклянную подложку и нагревании при 50–70°C. Полученные образцы толщиной 20–30 мкм сушили в вакууме при 200°С.
Полиимидные покрытия световодов формовали из растворов полимеров в N-МП (С = 0.25 г мл–1) на 9 м вытяжной башне по описанной ранее методике [4, 5].
Методы исследования. Логарифмическую вязкость ηln растворов 0.05 г полимера в 10.0 мл N-МП определяли в вискозиметре Оствальда при 25°С.
ИК-спектры снимали на спектрометре BRUKER “Tensor 37” (Германия), образцы прессовали с KBr.
Термостойкость полимеров определяли методом динамического термогравиметрического анализа на воздухе при скорости нагревания 5°С мин–1 на дериватографе Q1500 (фирма МОМ, Венгрия) на образцах массой ~15 мг.
Термомеханические кривые снимали на приборе TA Instruments TMA Q400 (США): диаметр зонда 2.54 мм, сила нагружения 1Н (100 г), скорость нагревания 5°С мин–1.
Деформационно-прочностные испытания пленок проводили на динамометре типа “Поляни” (Венгрия). Форма образцов – полоски. Размер рабочего участка: 10 × 2.2 мм, толщина 30–50 мкм. Скорость растяжения 0.0186 мм сек–1.
Прочность кварцевых световодов с полиимидным покрытием измеряли методом двухточечного изгиба [19].
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
С целью установления влияния природы диангидрида тетракарбоновой кислоты на свойства КПИ методом одностадийной высокотемпературной поликонденсации синтезированы полимеры различного строения (рис. 1).
Выбор исходного диангидрида был обусловлен стремлением придать полимеру повышенную тепло- и термостойкость, гибкость или жесткость, органорастворимость, коммерческую доступность и т.д. Синтез КПИ проводили в N-метил-2-пирролидоне без традиционно используемого при одностадийном способе катализатора кислотного или основного типа с целью дальнейшего применения раствора ПИ in situ, минуя энерго- и трудозатратные стадии выделения и очистки полимера. Строение синтезированных полимеров подтверждали методом ИК-спектроскопии. В ИК-спектрах полученных КПИ присутствуют характерные для полиимидов полосы поглощения в области 1760 и 1710 см–1, отвечающие анти- и симметричным колебаниям карбонильной группы имидного цикла, а также полосы в области 720 и 1380 см–1, соответствующие валентным колебаниям связи N–C имидного цикла.
КПИ-1 и КПИ-2 на основе наиболее коммерчески доступных диангидридов бензол-1,2,4,5-тетракарбоновой кислоты и бензофенон-3,3',4,4'-тетракарбоновой кислоты выпадали в осадок на начальной стадии синтеза и нерастворимы в N-МП, м-крезоле, диметилсульфоксиде, диметилформамиде, циклогексаноне и хлороформе (табл. 1).
Одним из способов улучшения растворимости ПИ является введение мостиковых “шарнирных” групп в основную цепь макромолекул. Так, включение простой эфирной связи в КПИ-3 придает полимеру растворимость в N-МП. Однако при хранении раствор КПИ-3 склонен к гелеобразованию (рис. 2а), что, по-видимому, связано с ориентацией макромолекул и созданием физической сетки зацеплений. При этом образующийся гель не разрушается при продолжительном нагревании или охлаждении. Выделенный после синтеза КПИ-3 сохраняет растворимость в N-МП (табл. 1). Полученный КПИ‑3 обладает логарифмической вязкостью ηln = 1.0 дл г–1 и характеризуется высокими значениями температуры стеклования и температуры 10%-й потери массы (Тс = 330°С, Т10% = 520°С), а также образует прочные пленки с весьма высокой деформируемостью (σ = 140 МПа, E = 1.2 ГПа, ε = 15%), что важно при изготовлении покрытий световодов.
На основе 4,4'-(4,4'-изопропилидендифенокси)-бис-(фталевого ангидрида) синтезирован КПИ-4. Такой полимер растворим уже в широком круге органических растворителей: N-МП, N,N-диметилформамиде, диметилсульфоксиде, циклогексаноне и хлороформе. Однако полученный высокомолекулярный КПИ-4 (ηln = 0.6 дл г–1) характеризуется меньшими значениями тепло- и термостойкости (Тс = 270°С, Т10% = 470°С), по сравнению с КПИ-3, что, очевидно, обусловлено наличием в основной цепи макромолекул значительной доли алифатических фрагментов и простых эфирных связей. При этом относительно невысокая Tс и хорошая растворимость позволяют существенно облегчить его переработку.
Таблица 2.
Свойства ПИ
| Полимер | ηln, дл г–1 (N-МП) | Tс, °C | T10%, °C (на воздухе) | Свойства пленок | ||
|---|---|---|---|---|---|---|
| σ, МПа | E, ГПа | ε, % | ||||
| КПИ-3 | 1.0 | 330 | 520 | 140 | 1.2 | 15 |
| КПИ-4 | 0.6 | 270 | 470 | 100 | 0.9 | 14 |
| КПИ-5 | 0.4 | 340 | 470 | хрупкая | ||
| КПИ-5 (м-крезол)а | 0.6 | 340 | 470 | 60 | 0.9 | 7 |
| КПИ-6 | 0.4 | 370 | 520 | 70 | 0.9 | 7 |
Для улучшения термических характеристик и сохранения растворимости синтезирован КПИ-5 на основе диангидрида 2,2-бис-(3,4-дикарбоксифенил)-1,1,1,3,3,3-гексафторпропана. Полиимид имеет более высокую теплостойкость (Тс = 340°С, Т10% = 470°С), чем КПИ-4, а благодаря объемным гексафторизопропилиденовым группам, растворим в широком круге органических растворителей (табл. 1). Механические свойства формируемых КПИ-5 пленок оказались ниже, чем у других карбоксилсодержащих полиимидов. Вероятно, это является следствием невысокого значения логарифмической вязкости полученного КПИ-5, которая составила 0.4 дл г–1. Отметим, что более высокомолекулярный КПИ-5 можно получить в среде м-крезола (ηln = 0.6 дл г–1). Однако такой полимер все равно формирует пленки с невысоким разрывным удлинением (σ = 60 МПа, E = 0.9 ГПа, ε = 7%), что исключает его использование в качестве покрытий.
Синтезирован КПИ-6, который растворим в органических растворителях (табл. 1) за счет объемной фталидной группы в ангидридном фрагменте и, как и КПИ-5, обладает высокой теплостойкостью (Тс = 340°С), а также термостойкостью, превышающей другие исследованные КПИ (Т10% = 520°С). Однако невысокая прочность и хрупкость формируемых им пленок препятствуют его применению.
Согласно данным табл. 1, КПИ-3 и КПИ-4 с гибкой простой эфирной связью формируют более деформируемые и прочные пленки. Поэтому полученные после синтеза растворы КПИ-3 и КПИ-4 использовали для нанесения покрытий на кварцевые световоды (рис. 3) [4, 5, 8]. Результаты измерений прочности световодов до и после испытаний представлены в виде графиков Вейбулла на рис. 4. Каждая точка на графике соответствует прочности на изгиб отдельного участка световода, а количество точек отвечает числу проведенных испытаний для каждого образца [19]. Термические испытания световодов с первичными защитными покрытиями необходимы для оценки возможности изготовления вторичного высокотемпературного кожуха и прогнозирования срока службы световода [20].
Рис. 4.
Прочность образцов световодов с покрытием из КПИ-4 до и после термических испытаний при 300°С (а) и 350°С (б), а также до и после гидролитических испытаний (в) в виде графиков Вейбулла. F – накопленная вероятность разрушения световода.
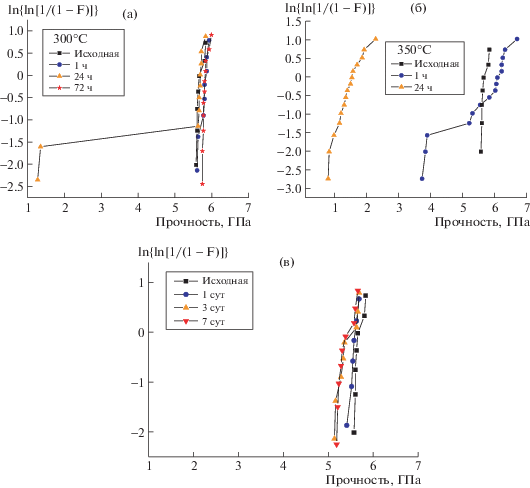
Наилучшие результаты были достигнуты для световода с покрытием из КПИ-4 (рис. 3, 4): усредненная исходная прочность световода равна 5.6 ± 0.1 ГПа, после выдержки при 300°C в течение 72 ч прочность световода возросла на 5% (рис. 4а), что обусловлено удалением остаточного растворителя [4].
Несмотря на невысокую ТсКПИ-4, равную 270°С, световод с покрытием из него способен длительно (72 ч) выдерживать температуру 300°С (рис. 4а). Появление дефектов в покрытии, приводящее к значительному снижению прочности световода, зафиксировано после 1 ч выдержки при 350°С (рис. 4б). Кроме того, покрытие на основе данного КПИ проявляет гидролитическую устойчивость и сохраняет высокую прочность после 7 сут выдержки в воде (рис. 4в).
ЗАКЛЮЧЕНИЕ
Таким образом, показано, что гомополиимиды на основе 3,5-диаминобензойной кислоты могут быть как нерастворимыми при применении диангидридов тетракарбоновых кислот, формирующих жесткоцепную структуру полимера, так и растворимыми в различных органических растворителях при использовании диангидридов тетракарбоновых кислот, содержащих мостиковые “шарнирные” или объемные “кардовые” фрагменты. Исследовано влияние строения КПИ на их свойства и свойства получаемых из них покрытий. Установлена значительная термическая устойчивость покрытия световода, изготовленного из карбоксилированного полиимида на основе 3,5-диаминобензойной кислоты и 4,4'-(4,4'-изопропилидендифенокси)-бис-(фталевого ангидрида) (72 ч при 300°С без потери прочности световодом). Полученные покрытия имеют сопоставимую с коммерческим аналогом CeramOptecTM (Латвия) термостабильность и превосходят его по гидролитической устойчивости [4, 7].
Список литературы
Chang K.-C., Hsu C., Lu H., Ji W., Chang C., Li W., Chuang T., Yeh J., Liu W., Tsai M. // Express Polym. Lett. 2014. V. 8. № 4. P. 243–255. https://doi.org/10.3144/expresspolymlett.2014.28
Yu Y.-H., Yeh J.-M., Liou S.-J., Chang Y.-P. // Acta Mater. 2004. V. 52. № 2. P. 475–486. https://doi.org/10.1016/j.actamat.2003.09.031
Chang C.-C., Chen W.-C. // Chem. Mater. 2002. V. 14. № 10. P. 4242–4248. https://doi.org/10.1021/cm0202310
Косолапов А., Пластинин Е., Семенов С., Байминов Б., Сапожников Д., Алексеева Д., Выгодский Я. // Краткие сообщения по физике физического института им. П.Н. Лебедева РАН. 2017. V. 44. № 6.
Семенов С.Л., Сапожников Д.А., Ерин Д.Ю., Забегаева О.Н., Куштавкина И.А., Нищев К.Н., Выгод-ский Я.С., Дианов Е.М. // Квантовая электроника. 2015. V. 45. № 4. P. 330–332.
Zhang Y., Qu L., Liu J., Wu X., Zhang Y., Zhang R., Qi H., Zhang X. // J. Coat. Technol. Res. 2019. V. 16. № 2. P. 511–520. https://doi.org/10.1007/s11998-018-0129-5
Сапожников Д., Байминов Б., Чучалов А., Семенов С., Косолапов А., Забегаева О., Выгодский Я. // Высокомолек. соед. Сер. Б. 2020. V. 62. № 1. P. 44–52. https://doi.org/10.31857/S2308113920010076
Сапожников Д., Байминов Б., Выгодский Я. // Высокомолек. соед. Сер. С. 2020. V. 62. № 2. P. 166–173. https://doi.org/10.31857/S2308114720020132
Sapozhnikov D.A., Bayminov B.A., Zabegaeva O.N., Alexeeva D.D., Semjonov S.L., Kosolapov A.F., Plasti-nin E.A., Buzin M.I., Vygodskii Y.S. // High Perform. Polym. 2017. V. 29. № 6. P. 663–669. https://doi.org/10.1177/0954008317696567
Сапожников Д., Чучалов А., Байминов Б., Шибаева П., Чайка Е., Бузин М., Косолапов А., Семенов С., Выгодский Я. // Изв. АН. Сер. хим. 2020. № 8. P. 1486–1491.
Liu Z., Liu Y., Qiu W., Koros W.J. // Angew. Chem. Int. Ed. 2020. V. 59. № 35. P. 14877–14883. https://doi.org/10.1002/anie.202003910
Liu Y., Liu Z., Liu G., Qiu W., Bhuwania N., Chinn D., Koros W.J. // J. Membr. Sci. 2020. V. 593. P. 117430. https://doi.org/10.1016/j.memsci.2019.117430
Panangala S.D., Karunaweera C., Jayawickramage R., Balkus K.J. Jr., Ferraris J.P. // ACS Appl. Polym. Mater. 2019. V. 1. № 11. P. 3203–3209. https://doi.org/10.1021/acsapm.9b00873
Pham H.Q., Kim G., Jung H.M., Song S.W. // Adv. Funct. Mater. 2018. V. 28. № 2. P. 1704690. https://doi.org/10.1002/adfm.201704690
Pei X., Zhai W., Zheng W. // Langmuir. 2014. V. 30. № 44. P. 13375–13383. https://doi.org/10.1021/la5026735
Zheng X., Liu J., Wang K., Liu R., Yuan Y., Liu X. // Prog. Org. Coat. 2018. V. 124. P. 122–128. https://doi.org/10.1016/j.porgcoat.2018.08.002
Huang F., Rad A.T., Zheng W., Nieh M.-P., Corne-lius C.J. // Polymer. 2017. V. 108. P. 105–120. https://doi.org/10.1016/j.polymer.2016.11.046
Huang F., Cornelius C.J. // J. Membr. Sci. 2017. V. 542. P. 110–122. https://doi.org/10.1016/j.memsci.2017.08.003
Matthewson M.J., Kurkjian C.R., Gulati S.T. // J. Am. Ceram. Soc. 1986. V. 69. № 11. P. 815–821. https://doi.org/10.1111/j.1151-2916.1986.tb07366.x
Stolov A.A., Simoff D.A. // J. Therm. Anal. Calorim. 2020. P. 1–17. https://doi.org/10.1007/s10973-020-10146-7
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Химия, науки о материалах





