Электрохимия, 2021, T. 57, № 10, стр. 613-622
Микротрубчатые мембраны для селективного получения кислорода и водорода
И. В. Ковалев a, b, И. А. Мальбахова a, А. М. Воробьев a, Т. А. Борисенко a, М. П. Попов a, *, А. А. Матвиенко a, А. И. Титков a, А. П. Немудрый a
a Институт химии твердого тела и механохимии СО РАН
Новосибирск, Россия
b Новосибирский государственный технический университет
Новосибирск, Россия
* E-mail: popov@solid.nsc.ru
Поступила в редакцию 29.12.2020
После доработки 01.04.2021
Принята к публикации 05.04.2021
Аннотация
В настоящей работе приведены результаты исследования газовой проницаемости микротрубчатых кислород- и водород-проницаемых мембран. Для микротрубчатых кислород-проницаемых мембран состава Ba0.5Sr0.5Co0.75Fe0.2Mo0.05O3 – δ впервые изучено влияние серебряного катализатора при использовании нового метода нагрева. Альтернативные водород-проницаемые мембраны на основе металлического никеля изготовлены из оксида никеля методом фазовой инверсии с последующим восстановлением в водороде.
ВВЕДЕНИЕ
Эффект газовой проницаемости был обнаружен более сотни лет назад [1], однако его исследование до сих пор представляет интерес. В классическом варианте [2] процесс диффузионной газовой проницаемости через мембрану описывается согласно следующей схеме: физадсорбция → хемосорбция → абсорбция → твердофазная диффузия и зеркальные процессы на обратной стороне мембраны. В зависимости от природы газа и материала мембраны газовая диффузия может протекать с аномальной для твердых тел скоростью, что находит применение в различных отраслях инженерной мысли. Одними из наиболее интересных, с прикладной точки зрения, являются (1) кислород- и (2) водород-проницаемые мембраны.
(1) Материалами для кислород-проницаемых (КП) мембран, как правило, являются перовскитоподобные оксиды со смешанной кислород-электронной проводимостью (СКЭП). КП-мембраны находят применение в различных инновационных технологиях [3–5], например, сепарации кислорода из воздуха с помощью ион-транспортных мембран, которые легко интегрируются в высокотемпературные процессы: каталитической конверсии природного газа в синтез-газ [6]; окислительного пиролиза метана с получением ацетилена [7]; эффективного сжигания топлива с утилизацией углекислого газа [8], а также конверсии химической энергии топлива в электрическую энергию с помощью твердооксидных топливных элементов (ТОТЭ) [9].
(2) Традиционным материалом для водород-проницаемых (ВП) мембран является палладий. ВП-мембраны используют в процессах, где требуется водород исключительной чистоты без наличия серосодержащих соединений и оксида углерода(II) [10]. Ввиду высокой стоимости палладия в настоящее время ведутся разработки по созданию альтернативных ВП-мембран. Одним из наиболее перспективных материалов для данных целей является никель. Преимуществом никелевых мембран является не только значительно низкая стоимость материала, но и высокая устойчивость к воздействию отравляющих веществ [11]. Однако водородная проницаемость никелевых мембран намного ниже, чем у мембран на основе палладия при аналогичных рабочих температурах, поскольку растворимость водорода и коэффициент диффузии твердой фазы в никеле намного ниже, чем палладия [11].
Для увеличения газовой проницаемости мембран применяют различные стратегии, основанные на:
– создании мембраны с определенной микро- и макроструктурой [12]. Для формирования архитектуры мембраны применяют метод фазовой инверсии для получения мембран в виде микротрубок с высокой пористостью (вплоть до 50 об. %) и тонким газоплотным слоем (до десятков микрон). Как правило, формование мембран в микротрубчатой (МТ) форме приводит к заметному повышению удельных функциональных характеристик [12, 13];
– модификации мембраны при помощи катализатора. Известно, что нанесение на поверхность кислород-проницаемой мембраны серебряного катализатора приводит к увеличению кислородных потоков [14].
В данной работе проведен синтез кислород- и водород-проницаемых мембран в форме микротрубок. Проведено исследование влияния модификации поверхности КП-мембраны каталитически активным материалом на кислородную проницаемость.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Изготовление мембран
Порошки состава Ba0.5Sr0.5Co0.75Fe0.2Mo0.05O3 – δ (BSCFM5) для КП-мембраны были получены керамическим методом при смешении реагентов в стехиометрических соотношениях в планетарной шаровой мельнице АГО-2 в течение 1.5 мин в этиловом спирте, из расчета 1 мл спирта на 1 г конечного продукта. В качестве реагентов использовали нитрат бария, оксиды железа, молибдена, кобальта и карбонат стронция. Все порошки были предварительно просушены в печи при 600°C в течение 5 ч. После смешения полученный порошок традиционно прокаливали в печи при температуре 900°C в течение 6 ч для частичного удаления побочных продуктов и увеличения удельной площади реакции, затем снова помещали в АГО‑2 для измельчения и гомогенизации в течение 10 мин.
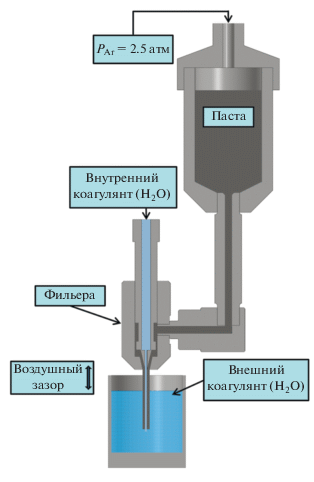
Микротрубчатые мембраны были получены методом фазовой инверсии. Для приготовления пасты смешивали порошок-прекурсор (BSCFM5 – для КП-мембран, NiO – для ВП мембран), растворитель (N-метил-2-пирролидон) и связующее (полисульфон) в массовом соотношении 10 : 4 : 1 соответственно, а затем диспергировали с помощью вакуумного диссольвера DISPERMAT LC-55 (VMA-Getzmann, Германия) со скоростью 1500 об/мин в течение 1 ч с дальнейшей дегазацией при 300 об/мин в течение 1 ч. Полученную пасту выдавливали через фильеру в емкость с водой, воздушный зазор ≈1 см. Схема процесса получения представлена на рис. 1. Полученные заготовки выдерживали в дистиллированной воде сутки для удаления остатков растворителя, после высушивали при 120°C в течение 1 ч.
После сушки трубки для КП-мембран спекали в печи в воздушной атмосфере при 1160–1170°C в течение 6 ч, с температурной полкой на 450°C длительностью 2 ч для выгорания остаточного органического связующего; скорость нагрева Vн = = 250°C/ч; скорость охлаждения выбирали равной скорости нагрева.
Для восстановления заготовок из оксида никеля(II), полученных методом фазовой инверсии, до никелевых микротрубчатых мембран, использовали программируемое спекание при температурах 600–1100°С со скоростью нагрева 50–300°С/ч и скоростью охлаждения 300°С/ч в восстановительной среде 5% водорода–95% аргона.
Для проведения синтеза никелевых мембран методом частичного окисления–восстановления использовали никелевые капилляры из полуфабрикатного никеля марки НП2. Капилляры частично окисляли в высокотемпературной печи ПВК-1,6 при температуре 1200°С, а затем полученные заготовки восстанавливали в трубчатой печи в восстановительной среде 5% водорода–95% аргона при температуре 600°С в течение 1 ч, со скоростями нагрева и охлаждения 200°С/ч.
Приготовление серебряных чернил
Наночастицы серебра для получения серебряного катализатора на поверхности КП-мембран были синтезированы восстановлением в высококипящих спиртах по методике, описанной в [15]. Затем полученные частицы суспендировали в ацетоне с образованием коллоидного раствора [16]. Приготовленные серебряные чернила различной концентрации наносили аддитивно-экструзионным методом с последующим термическим отжигом.
Характеризация образцов
Морфологию полученных мембран исследовали с помощью сканирующего электронного микроскопа (СЭМ) TM-1000 (Hitachi, Япония).
Газоплотность мембран была определена при помощи коммерческого люминесцентного пенетранта NORD-TEST ROT 3000 (Helling, Германия).
Структуру соединений исследовали методом рентгенофазового анализа (РФА) с помощью дифрактометра D8 Advance (Bruker, Германия), используя высокоскоростной детектор LynxEye (СuKα-излучение). Данные были получены в диапазоне 2θ от 20° до 60° с шагом 0.02°.
Измерение кислородной проницаемости
Установка для измерения кислородной проницаемости изображена на рис. 2. Для проведения экспериментов по изучению кислородной проницаемости использовали мембраны без модификации поверхности и мембраны, на внутреннюю поверхность которых наносили серебряные чернила с концентрацией 10 мас. % по серебру, выбранной как оптимальная. Для измерений мембраны герметизировали полимерными патрубками с двух сторон, на некотором отдалении от краев мембраны наносили токопроводящее покрытие и закрепляли контакты из серебряной проволоки (Rзоны нагрева ≈ 15 кОм), после этого помещали в герметичный кварцевый реактор (4). Внутрь мембраны на протяжении эксперимента подавали аргон, с внешней стороны азот и кислород в различных соотношениях в режиме противотока, скорости потоков Jin = 90 мл/мин и Jout = = 150 мл/мин были подобраны ранее экспериментально. Газы подавали с помощью смесителя UFPGS-4 (3) (SoLO, Россия). Реактор располагали вертикально, продувочный газ подавали через нижний патрубок для сглаживания градиента температуры по длине реактора. Нагрев осуществляли пропусканием через мембрану переменного электрического тока с помощью источника (1), более подробно описание метода представлено в нашей прошлой работе [17]. Контроль температуры осуществляли с помощью пирометра с обратной связью IGA 300 (2) (IMPAC, Германия). Скорость нагрева Vнагр = 350°C/ч. Концентрацию прошедшего через мембрану кислорода отслеживали с помощью квадрупольного масс-спектрометра QMS 200 (5) (SRS, США). Эксперимент проводили в диапазоне температур 650–800°C с шагом 50°C. На каждой температуре измеряли концентрацию кислорода в аргоне в диапазоне парциальных давлений кислорода с питающей стороны 0.1–0.7 с шагом 0.1 и выдержкой по времени не менее 5 мин на каждом значении, после каждого шага по температуре проводили калибровку масс-спектрометра по воздуху для повышения точности измерений.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Кислород-проницаемые мембраны
Для определения структурных параметров порошка оксида BSCFM5 и сравнения с литературными данными использовали метод порошковой дифрактометрии. Согласно полученным данным (рис. 3), структура BSCFM5 описывается пространственной группой Pm$\bar {3}$m. Полученные данные совпадают с литературными [18] и свидетельствуют о полном протекании твердофазной реакции.
Из характеризованного порошка BSCFM5 методом фазовой инверсии были изготовлены микротрубчатые мембраны (внешний диаметр 3 мм, внутренний диаметр 2.5 мм). Данные СЭМ слома микротрубчатых мембран состава BSCFM5 приведены на рис. 4, где видна развитая микроструктура с наличием finger-like пор и газоплотного слоя, толщину которого можно оценить в ~50 мкм.
На основе изготовленных мембран было получено четыре образца с различной концентрацией нанесенного серебряного катализатора. Сравнительные микрофотографии внутренней поверхности микротрубчатых BSCFM5 мембран с различной концентрацией серебра представлены на рис. 5.
Рис. 5.
СЭМ поверхности мембраны: (а) без серебряного покрытия; (б) с нанесенными чернилами концентрации 2; (в) 5; (г) 10 мас. %.

Из сравнительных данных видно, что серебряное покрытие на поверхности мембраны является неравномерным вплоть до использования чернил с 10 мас. % серебра. Таким образом, в дальнейшей работе были изучены МТ-мембраны двух типов: без модификации поверхности и с серебряным катализатором, полученным с использованием наиболее концентрированных чернил.
Эксперимент по изучению кислородной проницаемости показал, что в среднем величина удельных кислородных потоков на модифицированной мембране в 1.3 меньше, чем на мембране без нанесения серебряного покрытия (рис. 6). Рассчитанная на основании анализа кислородных потоков энергия активации составила 96 ± 1 кДж/моль для модифицированной мембраны, тогда как энергия активации на немодифицированной мембране того же состава 84 ± 3 кДж/моль (рис. 7).
Рис. 6.
Линеаризация данных кислородных потоков, полученных на (а) немодифицированной мембране и (б) мембране с серебряным покрытием.

Рис. 7.
Аррениусовские графики для: (а) немодифицированной мембраны; (б) мембраны с серебряным покрытием.

Чтобы разобраться в причинах полученных результатов, нами были проведены элементный и рентгеноструктурный анализы рабочей области модифицированной мембраны после эксперимента, по результатам которых наличие серебра не было установлено, однако незначительное его количество было обнаружено качественным химическим анализом, что говорит о существенном снижении концентрации серебра в сравнении с начальным состоянием поверхности. Такое изменение мы связываем с экстремальными условиями проведения эксперимента: высокие значения температуры, потока продувочного газа, а также плохая адгезия серебра к керамике. Наши предположения подтверждаются экспериментально, что наблюдается из представленных СЭМ микрофотографий, сделанных после экспериментов с изменением таких параметров, как подача продувочного газа и температура. На представленных снимках по длине мембраны наблюдается предсказанный унос серебра, что выражается в изменении концентрации частиц серебра по длине рабочей поверхности в направлении подачи продувочного газа (рис. 8).
Различие в величине удельных кислородных потоков, на наш взгляд, обусловлено тем, что серебро, концентрируясь по границам зерен, снижает количество активных центров, препятствуя переносу кислорода. Различия в энергиях активаций незначительны и могут быть обусловлены множеством факторов, в том числе различием в длине рабочей области исследуемых мембран, прямое влияние на эффективную энергию активации которого было обнаружено ранее [19].
Водород-проницаемые мембраны
При получении никелевых водород-проницаемых мембран методом фазовой инверсии использовали два подхода – восстановление мембран с использованием предварительного отжига при температуре 1400°С и без него. Данные сканирующей электронной микроскопии показывают, что при восстановлении предварительно отожженных заготовок из оксида никеля(II) в диапазоне температур 600–1100°С (скорость нагрева 50°С/ч) не достигается газоплотность образцов (рис. 9). Это связано с тем, что при восстановлении оксида никеля(II) до металлического никеля теряется около 40% объема с образованием высокой пористости [20]. При достаточно высоких скоростях нагрева пористость не успевает трансформироваться из открытой в закрытую.
Рис. 9.
Микроснимки никелевых мембран, полученных методом фазовой инверсии с предварительным отжигом при разных температурах восстановления (скорость нагрева 50°С/ч): 600 (а), 800 (б), 1000°С (в).

Для предотвращения повышенной пористости было решено уменьшить скорость нагрева заготовки из оксида никеля(II) при восстановлении. Результаты электронной микроскопии (рис. 10) и тест на газоплотность при помощи пенетранта определили, что снижение скорости нагрева позволяет достичь полной газоплотности никелевой мембраны.
Рис. 10.
Микроснимки никелевой мембраны, полученной методом фазовой инверсии без предварительного отжига при температуре восстановления 1100°С (скорость нагрева 50°С/ч).

При разработке метода получения никелевых ВП-мембран методом частичного окисления–восстановления промышленных капилляров предполагалось, что два фронта окисления капилляра идут параллельно и навстречу друг другу. При дальнейшем восстановлении частично окисленного никелевого капилляра ввиду потери объема при переходе из NiO в Ni будет образовываться пористый слой на поверхности, который будет способствовать повышенной диффузии водорода через мембрану. При проведении эксперимента по получению мембраны данным методом было показано, что итоговый продукт представляет из себя трубчатую трехслойную структуру, у которой внешние слои более пористые, чем сердцевина мембраны (рис. 11). При этом тест на газоплотность показывает, что данные мембраны не являются газоплотными.
Рис. 11.
Микроснимки никелевой мембраны, полученной методом частичного окисления–восстановления при температуре окисления 1150°С и температуре восстановления 600°С.

Механизм окисления никеля хорошо установлен [21, 22]. Рост слоя оксида происходит преимущественно за счет диффузии катионов никеля и переноса электронов через слой оксида. Взаимодействие кислорода на внешней поверхности оксида приводит к образованию вакансий никеля. Вакансии никеля диффундируют к границе раздела металл/оксид, что соответствует диффузии никеля в обратном направлении. В результате оксид растет на внешней поверхности (оксид–газ), а вакансии накапливаются в металле, что и является причиной образования пор в продукте реакции. После стадии окисления образуется два слоя оксида и слой недоокисленного металла между ними. Толщина слоев контролируется временем реакции. Наблюдается характерная для диффузионных процессов корневая зависимость толщины оксида от времени реакции [22]. На стадии восстановления в водороде оксид превращается в пористый металл. Уменьшение объема при реакции реализуется в виде лабиринта пор. Размер пор сильно зависит от температуры и концентрации водорода [23]. Пористые слои металла являются газопроницаемыми и в результате образуется мембрана, состоящая из двух пористых слоев и сплошного слоя исходного металла между ними. Однако в данной работе было обнаружено, что в слое оставшегося, недоокисленного металла поры расположены преимущественно вдоль границ зерен. Также на границах зерен в этом слое наблюдаются небольшие выделения фазы оксида. Можно предположить, что нарушение газоплотности мембраны связано с образованием сквозных каналов или трещин вдоль границ зерен в слое недоокисленного металла после цикла окисление–восстановление.
ЗАКЛЮЧЕНИЕ
В настоящей работе показано, что использование серебра в качестве поверхностного катализатора кислородной проницаемости микротрубчатых мембран на основе оксидов со смешанной кислород-электронной проводимостью приводит к снижению удельных кислородных потоков, а также не влияет на энергию активацию процесса. Ко всему прочему, серебряное покрытие является крайне нестабильным в рабочих условиях эксплуатации данных мембран, что также является аргументом против использования серебра как катализатора.
Показано, что метод обратной фазовой инверсии с контролируемым спеканием позволяет получать газоплотную никелевую водородселективную мембрану. Полная газоплотность достигается при спекании заготовки из оксида никеля(II) при температуре 1100°С со скоростью нагрева 50°С/ч. Установлено, что метод частичного окисления–восстановления промышленных капилляров не позволяет синтезировать никелевые мембраны, удовлетворяющие необходимым условиям для водородселективных мембран.
Список литературы
Cailletet, L., First report of H embrittlement of metals, 1864, Compt. Rend, vol. 58, p. 327.
Wang, J., On the Diffusion of Gases through Metals, Proc. Cambridge Philos. Soc., 1936, vol. 32, p. 657.
Pena, M.A. and Fierro, J.L.G., Chemical structure and performance of perovskite oxides, Chem. Rev., 2001, vol. 101, p. 1981.
Sunarso, J., Baumann, S., Serra, J.M., Meulenberg, W.A., Liu, S., and Lin, Y.S., Mixed ionic-electronic conducting (MIEC) ceramic-based membranes for oxygen separation, J. Membr. Sci., 2008, vol. 320, p. 13.
Marques, F.M.B., Kharton, V.V., Naumovich, E.N., Shaula, A.L., Kovalevsky, A.V., and Yaremchenko, A.A., Oxygen ion conductors for fuel cells and membranes: selected developments, Solid State Ionics, 2006, vol. 177, p. 1697.
Pei, S., Kleefisch, M., Kobylinski, T.P., Faber, J., Udovich, C.A., Zhang-McCoy, V., Dabrowski, B., Balachandran, U., Mieville, R.L., and Poeppel R.B., Failure mechanisms of ceramic membrane reactors in partial oxidation of methane to synthesis gas, Catal. Lett., 1994, vol. 30, p. 201.
Ten Elshof, J.E., van Hassel, B.A., and Bouwmeester, H.J.M., Activation of methane using solid oxide membranes, Catal. Today, 1995, vol. 25, p. 397.
Leo, A., Liu, Sh., and Diniz da Costa, J.C., Development of mixed conducting membranes for clean coal energy delivery, Int. J. Greenh. Gas Con., 2009, vol. 3, p. 357.
Mahato, N., Banerjee, A., Gupta, A., Omar, S., and Balani K., Progress in material selection for solid oxide fuel cell technology: a review, Prog. Mater. Sci., 2015, vol. 72, p. 141.
Tarasov, B.P., Hydrogen energetics: Past, present, prospects, Russ. J. Gen. Chem., 2007, vol. 77, p. 660.
Li, Y., Zhang, M., Chu, Y., Tan, X., Gao, J., Wang, S., and Liu, S., Design of Metallic Nickel Hollow Fiber Membrane Modules for Pure Hydrogen Separation, AIChE J., 2018, vol. 64, no. 1, p. 1.
Popov, M.P., Bychkov, S.F., and Nemudry, A.P., Direct AC heating of oxygen transport membranes, Solid State Ion., 2017, vol. 312, p. 73.
Popov, M.P., Bychkov, S.F., Bulina, N.V., and Nemudry, A.P., In situ high-temperature X-Ray diffraction of hollow fiber membranes under operating conditions, J. Eur. Ceram. Soc., 2019, vol. 39, p. 1717.
Sunarso, J., Baumann, S., Serra, J.M., Meulenberg, W.A., Liu, S., Lin, Y., and Diniz da Costa, J.C., Mixed ionic-electronic conducting ceramic-based membranes for oxygen separation, J. Membrane. Sci., 2009, vol. 340, p. 148.
Titkov, A.I., Logutenko, O.A., Gerasimov, E.Yu., Shundrina, I.K., Karpova, E.V., and Lyakhov, N.Z., Synthesis of silver nanoparticles stabilized by carboxylated methoxypolyethylene glycols: The role of carboxyl terminal groups in the particle size and morphology, J. Incl. Phenom. Macro., 2019, vol. 94, p. 287.
Malbakhova, I.A., Titkov, A.I., Uvarov, N.F., and Ulihin, A.S., Synthesis of graphite/Ag/AgCl nanocomposite electrode materials, Mater. Today: Proceedings, 2019, vol. 25, p. 398.
Popov, M.P., Bychkov, S.F., and Nemudry, A.P., Direct AC heating of oxygen transport membranes, Solid State Ion., 2017, vol. 312, p. 73.
Shubnikova, E.V., Bragina, O.A., and Nemudry, A.P., Mixed conducting molybdenum doped BSCF materials, Ind. Eng. Chem. Res., 2018, vol. 59, p. 242.
Shubnikova, E.V., Popov, M.P., Chizhik, S.A., Bychkov, S.F., and Nemudry, A.P., The modeling of oxygen transport in MIEC oxide hollow fiber membranes, Chem. Eng. J., 2019, vol. 372, p. 251.
Manukyan, K.V., Avetisyan, A.G., Shuck, C.E., Cha-tilyan, H.A., Rouvimov, S., Kharatyan, S.L., and Mukasyan, A.S., Nickel Oxide Reduction by Hydrogen: Kinetics and Structural Transformations, J. Phys. Chem. C, 2015, vol. 119, no. 28, p. 16131.
Jeangros, Q., Hansen, T.W., Wagner, J.B., Dunin-Borkowski, R.E., Hébert, C., Vanherle, C.J., and Hessler-Wyser, A., Oxidation mechanism of nickel particles studied in an environmental transmission electron microscope, Acta Mater., 2014, vol. 67, p. 362.
Mrowec, S. and Grzesik, Z., Oxidation of nickel and transport properties of nickel oxide, J. Phys. Chem. Solids, 2004, vol. 65, p. 1651.
Hidayat, T., Rhamdhani, M.A., Jak, E., and Hayes, P.C. Investigation of Nickel Product Structures Developed during the Gaseous Reduction of Solid Nickel Oxide, Metall. Mater. Trans. B, 2009, vol. 40B, p. 462.
Дополнительные материалы отсутствуют.