Электрохимия, 2021, T. 57, № 8, стр. 457-464
Получение и электропроводность молибдатов висмута, замещенных сурьмой и оловом
А. В. Климова a, b, *, З. А. Михайловская a, Е. С. Буянова a, b, С. А. Петрова c
a Институт геологии и геохимии им. академика А.Н. Заварицкого УрО РАН
Екатеринбург, Россия
b Уральский федеральный университет им. первого Президента России Б.Н. Ельцина, Химический факультет
Екатеринбург, Россия
c Институт металлургии УрО РАН
Екатеринбург, Россия
* E-mail: bbgiyongchy@gmail.com
Поступила в редакцию 30.11.2020
После доработки 06.02.2021
Принята к публикации 12.03.2021
Аннотация
Статья посвящена исследованию возможности получения, установлению специфики структуры и свойств кислородно-ионных проводников на основе молибдата висмута, замещенного сурьмой и оловом в подрешетке молибдена. Для полученных составов были установлены области гомогенности и изучены структурные особенности. Определены параметры элементарной ячейки и объемная плотность образцов. Методом ИК-спектроскопии определены характеристические частоты связей металл-кислород. Общая электропроводность составов исследована методом импедансной спектроскопии в диапазоне температур 200–825°С. Построены температурные и проанализированы концентрационные зависимости проводимости.
ВВЕДЕНИЕ
Кислород-ионные проводники являются перспективными материалами мембран кислородных датчиков, каталитических систем, газоразделительных устройств, топливных элементов. По совокупности электрофизических характеристик, термической и структурной устойчивости, молибдаты висмута с колончатой структурой относятся к этой категории соединений.
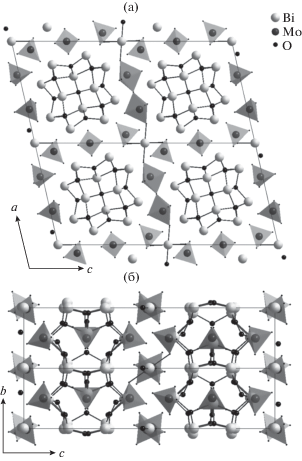
В структуре колончатых молибдатов висмута имеются, с одной стороны, колончатые фрагменты [Bi12O14]n, обеспечивающие анизотропный перенос ионов кислорода, а с другой стороны, квазижидкая подрешетка, состоящая из полиэдров MoOn и изолированных ионов висмута (рис. 1) [1–3].
При комнатной температуре Bi13Mo5O34.5 – δ кристаллизуется в триклинной симметрии, выше 310°С переходит в моноклинную модификацию, что приводит к повышению его электропроводящих характеристик. Обратный переход в триклинную модификацию сопровождается резким снижением электропроводности. Замещение позиций висмута или молибдена в Bi13Mo5O34.5 – δ другими атомами может привести к стабилизации моноклинной модификации и оптимизации проводящих свойств. Высокая подвижность молибден-кислородной подрешетки нивелирует размерный фактор иона-заместителя, что определяет чрезвычайное разнообразие возможных допантов. Теоретически допустимо замещение висмута в колонках [Bi12O14]n; замещение “изолированных” позиций висмута; замещение молибдена в молибден-кислородных полиэдрах [4–6].
Как было отмечено выше, группировка MoOn в колончатых молибдатах висмута не связана жестко с другими структурными элементами, что позволяет ей не только совершать необходимые для ионного транспорта ротационные движения, но и допускает внедрение в структуру подобных по координации, но совершенно отличных по размерам ионов, например фосфора [7, 8]. Настоящая работа посвящена исследованию возможности замещения позиций молибдена в колончатых молибдатах висмута оловом и сурьмой, которые ранее в качестве допантов не рассматривались, а сурьма, в силу своей природы (полуметалл), в принципе используется довольно редко. Для оценки возможных эффектов за счет применения указанных элементов, как ионов-заместителей, рассмотрим примеры иных оксидных соединений.
При 580°С для молибдата лантана La2Mo2O9 (LM) наблюдается фазовый переход первого рода [9]. Калориметрические исследования образцов показали, что введение легирующей примеси Sb в LM приводит к снижению температуры фазового перехода α → β с 570 до 520°С и к существенному подавлению этого перехода. В области высоких температур проводимость полученных твердых растворов также увеличивается, авторы объясняют это образованием дополнительных кислородных вакансий после введения пятивалентной сурьмы на позиции шестивалентного молибдена.
При синтезе сложных оксидов в восстановительных условиях сурьма проявляет степень окисления +3 и легко занимает позиции трехвалентных металлов с большими координационными числами (6–8), например железа или висмута. Авторами [10] был проведен синтез твердых растворов с общими формулами Bi2 –xSbxMoO6, где 0 ≤ x ≤ 2. Отмечена хорошая проводимость полученных соединений. При введении сурьмы в молибдаты железа происходит искажение структуры FeMoO4 и, за счет этого, модификация его каталитических характеристик: повышение селективности в процессах окисления изобутана и уменьшение скорости разрушения катализатора [11].
Возможность замещения оловом проанализирована для широкого круга самых разных по свойствам и составу оксидов. Например, аналогично системам с сурьмой, исследованы составы LM с оловом. Олово может находиться в степени окисления Sn2+ и Sn4+ и, следовательно, при введении в структуру может создавать дополнительные кислородные вакансии, приводящие к увеличению проводимости. Авторами [12] по стандартной твердофазной методике был синтезирован ряд соединений состава La2Mo2 –xSnxO9 – δ (x = 0–0.3). Они обнаружили, что фазовый переход α → β между 550–570°С сдвигается в сторону более низких температур при повышении концентрации допанта. Отмечено увеличение энергии активации электропроводности с возрастанием концентрации вводимого иона, что мешает миграции ионов кислорода. Только в температурном диапазоне 520–590°С образцы с концентрацией Sn x ≤ 0.05 имеют проводимость выше, чем для LM. С увеличением концентрации допанта при температурах выше 590°С проводимость твердых растворов последовательно снижается.
Таким образом, введение сурьмы и олова на позиции молибдена в колончатых молибдатах висмута перспективно для возможной стабилизации полиморфных модификаций и повышения электропроводящих свойств подобных соединений.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Исследуемые твердые растворы с общими формулами Bi13Mo5 –xSnxO34.5 – δ (x ≤ 0.7, Δx = 0.1), Bi13Mo5 –xSbxO34.5 – δ (x ≤ 1.0, Δx = 0.1) синтезированы по стандартной керамической технологии при использовании следующих исходных оксидов: Bi2O3 (ос. ч.), MoO3 (ос. ч.), SnO2 (ос. ч.) и Sb2O3. Оксид сурьмы получен гидролизом SbCl3 (ос. ч.) в горячей подкисленной воде с последующим отмыванием и сушкой осадка. Аттестация полученного Sb2O3 проведена методами химического и рентгенофазового анализов. Исходные оксиды предварительно прокаливали для удаления влаги и получения устойчивых модификаций. Сурьма в оксиде Sb2O3 при отжиге на воздухе выше 683–723 K, согласно [13], повышает степень окисления до +4…+5, что позволяет предположить ее максимальное значение в конечном продукте. Смеси тщательно гомогенизировали и прессовали в брикеты. Брикеты помещали в тигли на прослойку из порошка этого же состава (для минимизации взаимодействия с тиглем) и подвергали отжигу в две стадии. Первая стадия – отжиг при 823 K (24 ч), затем закаливание брикета помещением его в воду комнатной температуры. Вторая стадия – отжиг при 1163 K, затем медленное охлаждение вместе с печью. Границы области гомогенности и существования структурных модификаций, структурные параметры полученных твердых растворов определены методом порошковой рентгеновской дифракции с использованием дифрактометра D8 ADVANCE Bruker AXS (ЦКП “Урал-М” ИМЕТ УрО РАН, детектор VÅNTEC, CuKα-излучение, Ni-фильтр, θ/θ геометрия) в интервале углов 2θ = 5°–125° с шагом 0.02°. Частотные характеристики связей металл–кислород устанавливали методом ИК-фурье-спектроскопии путем снятия ИК-спектров отражения (спектрометр Nicolet 6700 с приставкой нарушенного полного внутреннего отражения (НПВО) Smart Orbit, средняя и дальняя ИК-области).
Анализ распределения частиц порошков по размерам методом дифракции лазерного излучения был выполнен на анализаторе дисперсности SALD-7101 Shimadzu (источник света – фиолетовый полупроводниковый лазер, длина волны 375 нм). Анализ микроструктуры спеченных образцов проведен с использованием растрового электронного микроскопа JEOL JSM 6390LA, оснащенного рентгеновским энергодисперсионным микроанализатором INCA Energy 450 X-Max 80.
Денситометрические измерения осуществляли пикнометрически (порошок) и гидростатическим взвешиванием плотно спеченных керамических брикетов, покрытых тонким слоем гидроизолирующего лака. Пористость образцов определяли как результат соотношения полученных экспериментальных и теоретических рентгенографических плотностей.
Оценку величины общей электропроводности полученных молибдатов висмута проводили методом импедансной спектроскопии в двухконтактной ячейке с платиновыми электродами и интервале температур 200–825°C в режиме охлаждения на импедансметре Elins Z-3000 (интервал частот 3 MГц–10 Гц). Для анализа годографов импеданса был использован метод эквивалентных схем (Zview software, Version 2.6b, Scribner Associates, Inc.).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Согласно результатам аттестации порошков методом РФА для всех серий образцов Bi13Mo5 –xSnxO34.5 – δ (x ≤ 0.7, Δx = 0.1) и Bi13Mo5 –xSbxO34.5 – δ (x ≤ 1.0, Δx = 0.1) граница области гомогенности твердых растворов ограничена значением x = 0.3. В случае серии Bi13Mo5 –xSnxO34.5 – δ триклинная модификация твердых растворов существует до x ≤ 0.2, в случае Bi13Mo5 –xSbxO34.5 – δ – до x ≤ 0.1 (Пр. гр. P-1). При увеличении концентрации допанта происходит стабилизация моноклинной модификации молибдата висмута (Пр. гр. P2/c). На рис. 2 в качестве примера приведена рентгеновская дифрактограмма образца Bi13Mo5 –xSbxO34.5 – δ для x = 0.3. С использованием метода Ритвельда (пакет Fullprof [14]) проведено уточнение структуры и рассчитаны параметры элементарной ячейки. В качестве стартовых были выбраны модели, описанные в работе [15].
Рис. 2.
Рентгеновская порошковая дифрактограмма образца Bi13Mo5 –xSbxO34.5 – δ, x = 0.3. Точки – экспериментальные данные, сплошная линия – расчетная кривая, штрихи – положение рефлексов, в нижней части – разностная кривая. На вставке представлен фрагмент в больших углах, показывающий сходимость экспериментальных и модельных кривых при малых значениях интенсивностей рефлексов (RBragg = 4.98, RF = 3.40, Rexp = 8.56, Rp = 11.3, Rwp = 10.5, χ2 = 1.93).

Методом лазерного светорассеяния установлено, что размер частиц полученных порошков отвечает средним значениям для твердофазного метода синтеза и составляет для серии Bi13Mo5 –xSbxO34.5 – δ 0.3–50 мкм, для серии Bi13Mo5 –xSnxO34.5 – δ – 0.3–30 мкм, частицы склонны к агломерации. Максимум распределения приходится на интервал 5–12 мкм.
Согласно денситометрическому анализу, полученные из исследуемых порошков керамические брикеты хорошо спекаются, среднее значение общей пористости брикетов составляет от 2 до 5%.
Микроструктура и состав брикетированных образцов из области гомогенности исследованы методом электронной микроскопии с энергодисперсионным микроанализом (ЭДА). На рис. 3 приведены микрофотографии сколов брикетов некоторых образцов, иллюстрирующие их однородность и отсутствие посторонних включений. Согласно результатам ЭДА, для спеченных брикетов характерно равномерное распределение элементов в соответствии с номинальным составом.
Рис. 3.
СЭМ-изображения сколов образцов Bi13Mo5 –xSbxO34.5 – δ (a) и Bi13Mo5 –xSnxO34.5 – δ (б), x = 0.2.

Как следует из табл. 1 и 2 с рассчитанными параметрами элементарной ячейки замещенных сурьмой и оловом молибдатов висмута, в рамках триклинной симметрии для всех составов наблюдается возрастание объема ячейки по сравнению с матричным соединением, что связано с замещением молибдена допантами большего ионного радиуса (rMo6+ = 0.41 Å, rSb3+ = 0.76 Å, rSb5+ = = 0.60 Å, rSn4+= 0.55 Å, КЧ = 4) [17]. При этом параметр b практически не изменяется, так как жесткость элементарной ячейки в данном направлении определяется висмут-кислородными слоями, а основной вклад в увеличение объема вносит антибатное изменение параметров a и c. С ростом концентрации допанта при переходе в моноклинную модификацию происходит уменьшение объема элементарной ячейки, вероятно связанное с локальной перестройкой кислородной подрешетки, что описано в более ранних работах [15, 16]. В частности, для образцов чистого и допированного Bi13Mo5O34.5 – δ было показано, что при нахождении молибдата висмута в триклинной модификации, молибден проявляет смешанную координацию по кислороду (координационные числа 4 и 5). Если сложный оксид находится в моноклинной модификации − исключительно тетраэдрическую координацию. Таким образом, при повышении симметрии элементарной ячейки в ходе допирования или повышения температуры происходит уменьшение эффективного размера полиэдра MoOn и сжатие элементарной ячейки.
Таблица 1.
Значения параметров элементарной ячейки для составов Bi13Mo5 –xSnxO34.5 – δ
| Sn, x | Пр. гр. | Параметры элементарной ячейки | ||||||
|---|---|---|---|---|---|---|---|---|
| a ± 0.002, Å | b ± 0.001, Å | c ± 0.005, Å | α ± 0.01, град | β ± 0.01, град | γ ± 0.01, град | V ± 0.01, Å3 | ||
| 0 | P-1 | 11.799 | 5.803 | 24.744 | 89.87 | 102.75 | 89.90 | 1652.42 |
| 0.1 | P-1 | 11.800 | 5.805 | 24.756 | 89.87 | 102.852 | 89.94 | 1653.27 |
| 0.2 | P-1 | 11.786 | 5.805 | 24.780 | 89.95 | 102.892 | 89.93 | 1652.64 |
| 0.3 | P2/c | 11.749 | 5.803 | 24.785 | 90 | 102.84 | 90 | 1647.57 |
Таблица 2.
Значения параметров элементарной ячейки для составов Bi13Mo5 –xSbxO34.5 – δ
| Sb, x | Пр. гр. | Параметры элементарной ячейки | ||||||
|---|---|---|---|---|---|---|---|---|
| a ± 0.002, Å | b ± 0.001, Å | c ± 0.005, Å | α ± 0.01, град | β ± 0.01, град | γ ± 0.01, град | V ± 0.01, Å3 | ||
| 0 | P-1 | 11.799 | 5.803 | 24.744 | 89.87 | 102.75 | 89.90 | 1652.42 |
| 0.1 | P-1 | 11.800 | 5.805 | 24.750 | 89.85 | 102.83 | 89.90 | 1653.01 |
| 0.2 | P2/c | 11.795 | 5.804 | 24.762 | 90 | 102.88 | 90 | 1652.50 |
| 0.3 | P2/c | 11.783 | 5.804 | 24.775 | 90 | 102.89 | 90 | 1651.63 |
В ИК-спектрах твердых растворов (рис. 4) для составов Bi13Mo5 –xSnxO34.5 – δ, как и в матричном соединении, наблюдаются характеристические полосы, отвечающие колебаниям типичных для молибдатов висмута связей висмут – кислород, молибден – кислород [18]. Полосы поглощения в области 560–400 см–1 относятся к валентным и деформационным колебаниям связей Bi–O [19], в области 680–900 см–1 наблюдаются полосы, отвечающие валентным колебаниям связи Mo–O, симметричным и асимметричным колебаниям тетраэдров MoO4. При увеличении концентрации допантов сдвига характеристических полос связи Bi–O не происходит. Колебания связи Sn–O обычно наблюдаются в диапазоне 670–560 см–1 [20], и в настоящей работе в ИК-спектре зафиксированы небольшие по интенсивности полосы поглощения при 665 и 643 см–1, что подтверждает присутствие олова в пробах.
Аналогично для составов Bi13Mo5 –xSbxO34.5 – δ теоретически в области 900–400 см–1 могут наблюдаться полосы поглощения, относящиеся к валентным и деформационным колебаниям связей Sb–O [21, 22] (768–718 см–1 – симметричные валентные колебания связи Sb–O, полосы в интервале 595–508 см–1 – ассиметричные колебания), однако из-за наложения характеристических полос, отвечающих колебаниям связей висмут – кислород, молибден – кислород отдельно колебания связи Sb–O обнаружить не удалось.
Общая электропроводность серий Bi13Mo5 ‒ xSnxO34.5 – δ и Bi13Mo5 –xSbxO34.5 – δ исследована методом импедансной спектроскопии в интервале температур 825–200°С в режиме охлаждения. Характерные для всех исследуемых соединений типичные годографы импеданса и описывающие их эквивалентные схемы приведены на рис. 5 для высокотемпературной (650–890°С) и низкотемпературной области (300–550°С).
Рис. 5.
Годографы импеданса составов Bi13Mo4.8Sn0.2O34.3 и Bi13Mo4.8Sb0.2O34.2 при 1023 (а) и 573°С (б).

Импедансная диаграмма при температурах выше 650°С представляет асимметричный полукруг, который может быть описан (рис. 5а) эквивалентной схемой, состоящей из последовательно соединенных сопротивления R0 и двух элементов Войта R1–CPE1 и R2–CPE2. Значение CPE–T составляет величину 10–5–10–6 Ф, что позволяет отнести параметр R0 к общему сопротивлению образца, а элементы Войта – к описанию электродного процесса [23].
В низкотемпературной области импедансная диаграмма имеет вид незавершенного (часто сложенного из двух плохо разделяемых) полукруга с “хвостом”, что позволяет предположить эквивалентную схему (рис. 5б) из двух цепочек R1 + + CPE1 и R2 + CPE2 и элемента Варбурга Ws. Соединение R1 + CPE1 относится к общему сопротивлению образца (емкостной параметр CPE1–T около 10–11 Ф) и описывает малый полукруг, R2 + + CPE2 относится к электродному процессу (CPE2 составляет 10–6 Ф). Элемент Варбурга характеризует затрудненный с понижением температуры диффузионный процесс и вносит основной вклад в сопротивление системы.
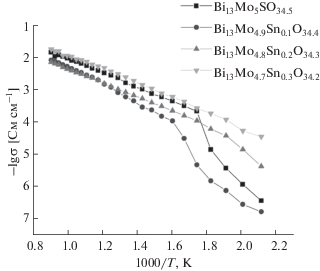
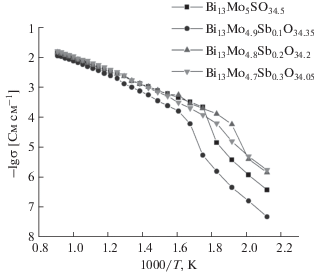
На основе кривых импеданса построены температурные зависимости электропроводности в аррениусовских координатах, представленные на рис. 6 и 7. На температурных кривых для обеих серий образцов заметны перегибы, по всей видимости отвечающие фазовому переходу из триклинной в моноклинную модификацию с ростом температуры, причем температура перехода падает с ростом концентрации допанта от 300 до 200°C и ниже (для состава с x = 0.3 в серии с оловом), что аналогично другим молибдатам [8, 15], и в целом находится в согласии с рентгеновскими исследованиями структуры образцов. Однако стоит отметить, что несмотря на стабилизацию моноклинной модификации при определенных значениях x, у некоторых составов все-таки происходят обратимые изменения в циклах нагревание-охлаждение. Например, составы Bi13Mo5 –xSbxO34.5 – δ (x = 0.2, 0.3), согласно РФА, после синтеза находятся в моноклинной модификации, однако на зависимостях lg σ–1000/Т, снятых в режиме охлаждения, можно заметить небольшие перегибы в области 200–240°C. Существенного влияния на величину электропроводности родоначальника серий при температурах выше 650°C (т.е., моноклинной модификации) введение сурьмы и олова не оказывает, величина энергии активации высокотемпературного участка зависимости lg σ–1000/T практически не изменяется и находится в диапазоне 0.42–0.48 эВ. Этот факт также находится в согласии с литературными данными по другим молибдатам, следовательно, сложная колончатая структура исходного соединения не оказывает существенного влияния на электроперенос в подобных материалах. Гораздо более значимый разброс наблюдается в низкотемпературной части, где максимальными значениями электропроводности обладают составы, кристаллизующиеся при этих температурах в моноклинной форме.
Значения для электропроводности твердых растворов приведены в табл. 3. Таким образом, в исследованной области температур все составы имеют величину общей электропроводности в интервале 4.95 × 10–8–1.79 × 10–2 Ом–1 см–1. Электропроводность Bi13Mo5O34.5 – δ, допированного Sb, будет несколько ниже во всей области температур, чем электропроводность при допировании Sn (рис. 8).
Таблица 3.
Удельная электропроводность соединений составов Bi13Mo5 –xSnxO34.5 – δ и Bi13Mo5 –xSbxO34.5 – δ при 350 и 750°C
| Состав | σ350°C, См см–1 | σ750°C, См см–1 |
|---|---|---|
| Bi13Mo5O34.5 | 4.48 × 10–4 | 1.07 × 10–2 |
| Bi13Mo4.9Sn0.1O34.4 | 1.11 × 10–4 | 5.98 × 10–3 |
| Bi13Mo4.8Sn0.2O34.3 | 2.28 × 10–4 | 4.94 × 10–3 |
| Bi13Mo4.7Sn0.3O34.2 | 6.06 × 10–4 | 1.79 × 10–2 |
| Bi13Mo4.9Sb0.1O34.35 | 1.60 × 10–4 | 8.38 × 10–3 |
| Bi13Mo4.8Sb0.2O34.2 | 5.50 × 10–4 | 1.04 × 10–2 |
| Bi13Mo4.7Sb0.3O34.05 | 3.06 × 10–4 | 1.17 × 10–2 |
ЗАКЛЮЧЕНИЕ
По стандартной твердофазной технологии синтезированы сложные оксиды составов Bi13Mo5 – xSnxO34.5 – δ (y ≤ 0.7, Δy = 0.1) и Bi13Mo5 ‒ xSbxO34.5 – δ (y ≤ 1.0, Δy = 0.1), определены их области гомогенности и границы существования триклинной и моноклинной модификаций. Определены рентгеноструктурные характеристики замещенных молибдатов висмута (группа симметрии, параметры элементарных ячеек). Проведено исследование образцов методом ИК-спектроскопии для уточнения положения атомов в структуре. Методом импедансной спектроскопии выявлены характер и особенности импедансных спектров и температурных зависимостей электропроводности исследуемых составов. Наибольшую электропроводность показывают молибдаты висмута, допированные оловом и сурьмой c концентрацией допанта x = 0.3. По совокупности электрофизических характеристик, термической и структурной устойчивости, замещенные молибдаты висмута с колончатой структурой можно считать перспективными материалами для использования в электрохимических устройствах.
Список литературы
Buttrey, J.D., Compositional and structural trends among the bismuth molybdates, Top. Catalysis, 2001, vol. 15, p. 235.
Vannier, R.N., Mairesse, G., Abraham, F., and Nowogrocki, G., Bi26Mo10Oδ Solid Solution Type in the Bi2O3–MoO3–V2O5 Ternary Diagram, J. Solid State Chem., 1996, vol. 122, p. 394.
Ling, C.D., Miller, W., Johnson, M.R., and Richard, D., Local Structure, Dynamics, and the Mechanisms of Oxide Ionic Conduction in Bi26Mo10O69, Chem. Mater., 2012, vol. 24, p. 4607.
Castro, A., Enjalbert, R., Baules, P., and Galy, G., Synthesis and Structural Evolution of the Solid Solution Bi(Bi12 –xTexO14)Mo4– xV1+ xO20 (0 ≤ x < 2.5), J. Solid State Chem., 1998, vol. 139, p. 185.
Galy, J., Enjalbert, R., Rozier, P., and Millet, P., Lone pair stereoactivity versus anionic conductivity. Columnar structures in the Bi2O3–MoO3 system, Solid State Sci., 2003, vol. 5, p. 165.
Enjalbert, R., Hasselmann, G., and Galy, J., [Bi12O14E12]n Columns and Lone Pairs E in Bi13Mo4VO34E13: Synthesis, Crystal Structure, and Chemistry of the Bi2O3–MoO3–V2O5 System, J. Solid State Chem., 1997, vol. 131, p. 236.
Vannier, R.N., Danzé, S., Nowogrocki, G., Marielle, H., and Mairesse, G., A new class of mono-dimensional bismuth-based oxide anion conductors with a structure based on [Bi12O14]∞ columns, Solid State Ionics, 2000, vol. 136, p. 51.
Михайловская, З.А., Буянова, Е.С., Петрова, С.А., Морозова, М.В., Еремина, К.С. Одномерные кислородно-ионные проводники на основе замещенных фосфором молибдатов висмута: получение и характеристики. Журн. неорг. химии. 2017. Т. 62. С. 1555. [Mikhaylovskaya, Z.A., Buyanova, E.S., Petrova, S.A., Morozova, M.V., and Eremina, K.S., One-dimensional oxygen-ion conductors based on phosphorus-substituted bismuth molybdates: Preparation and characterization, Russ. J. Inorg. Chem., 2017, vol. 62, p. 1549.]
Alekseeva, O.A., Verina, I.A., Sorokina, N.I., Kharitonova, E.P., and Voronkova, V.I., Structure and Properties of Antimony–Doped Lanthanum Molybdate La2Mo2O9, Crystallogr. Rep., 2011, vol. 56, p. 435.
Bégué, P., Enjalbert, R., Galy, J., and Castro, A., Single-crystal X-ray investigations of the structures of γ(H)Bi2MoO6 and its partially substituted As3+ and Sb3+ homologues, Solid State Sci., 2000, vol. 2, p. 637.
Graziani, M. and Rao, C.N.R., Advances in Catalyst Design: Proceedings of the 2nd Workshop on Catalyst Design, Singapore: World Scientific, 1993, vol. 2, p. 412
Borah, L.N. and Pandey, A., Impedance studies of La2Mo2 –xSnxO9 – δ oxide ion conductors, Acta Metall Sin-Engl., 2013, vol. 26, p. 425.
Лидин, Р.А., Молочко, В.А, Андреева, Л.Л. Химические свойства неорганических веществ, М.: Химия, 2000, 480 с. [Lidin, R.A., Molochko, V.A., and Andreeva, L.L., Chemical properties of inorganic substances (in Russian), Moscow: Khimiya, 2000, 480 p.]
Rodriguez-Carvajal, J., Recent developments of the program FULLPROF, CPD Newsletter, 2001, vol. 26, p. 12.
Mikhaylovskaya, Z.A., Petrova, S.A., Abrahams, I., Buyanova, E.S., Morozova, M.V., and Kellerman, D.G., Structure and conductivity in iron-doped Bi26Mo10O69 – δ, Ionics, 2018, vol. 24, p. 3983. https://doi.org/10.1007/s11581-018-2543-1
Mikhaylovskaya, Z.A., Petrova, S.A., Buyanova, E.S., and Abrahams, A., High-Temperature Studies of the Structure of Complex Oxides Based on Bi26Mo10O69 –d, J. Struct. Chem., 2018, vol. 59, p. 2001.
Shannon, R.D., Revised effective ionic radii and systematic studies of interatomic distances in halides and chalcogenides, Acta Crystallogr., Sect. A., 1976, vol. 32, p. 751.
Li, H.H., Li, K.W., and Wang, H., Hydrothermal synthesis and photocatalytic properties of bismuth molybdate materials, Mat. Chem. Phys., 2009, vol. 116, p. 134.
Paul, T. and Ghosh, A., Structure and vibrational properties of La2 –xBixMo2O9 (0.05 ≤ x ≤ 0.4) oxygen ion conductors, J. Alloy Compd., 2014, vol. 613, p. 146.
Ayeshamariam, A., Ramalingam, S., Bououdina, M., and Jayachandran, M., Preparation and characterizations of SnO2 nanopowder and spectroscopic (FT-IR, FT-Raman, UV–Visible and NMR) analysis using HF and DFT calculations, Spectrochim. Acta A, 2014, vol. 118, p. 1135.
Geng, L., Meng, C.Y., Lin, C.S., and Cheng, W.D., A new strontium antimonateIII Sr5Sb22O38: Synthesis, crystal structure and characterizations, J. Solid State Chem., 2013, vol. 203, p. 74.
Deng, Z., Chen, D., Tang, F., Ren, J., and Muscat, A.J., Synthesis and purple-blue emission of antimony trioxide single-crystalline nanobelts with elliptical cross section, Nano Res., 2009, vol. 2, p. 151.
Irvine, J.T.S., Sinclair, D.C., and West, A.R., Electroceramics: Characterization by Impedance Spectroscopy, Advanced Materials, 1990, vol. 2, p. 132.
Дополнительные материалы отсутствуют.