Журнал физической химии, 2020, T. 94, № 2, стр. 238-244
Раскрытие циклов нафтеновых углеводородов на цеолитных катализаторах
Л. М. Кустов a, b, *, А. Л. Кустов a, b
a Российская академия наук, Институт органической химии им. Н.Д. Зелинского
119991 Москва, Россия
b Московский государственный университет им. М.В. Ломоносова, Химический факультет
119992 Москва, Россия
* E-mail: lmk@ioc.ac.ru
Поступила в редакцию 12.05.2019
После доработки 12.05.2019
Принята к публикации 14.05.2019
Аннотация
Проведена оценка каталитической активности цеолитных катализаторов, содержащих нанесенные наночастицы металлов в раскрытии циклов модельных циклических соединений. Установлено, что наилучшие результаты – селективность в раскрытии метилциклопентана до 58% и выход н-гексана до 23.4% достигаются при использовании цеолита 1%Pt/NaX.
Одна из основных проблем переработки топлив – удаление полициклических ароматических и нафтеновых углеводородов, присутствие которых вызывает образование продуктов уплотнения на катализаторах или сажи в выхлопных газах двигателя в случае дизельного топлива, а также приводит к снижению цетанового числа. Присутствие полициклических нафтенов и ароматических углеводородов нежелательно и в бензиновых топливах. Наличие тяжелых полициклических соединений в дизельном топливе приводит также к повышению точки замерзания и снижению качества зимних топлив. Улучшение качественных характеристик моторных топлив тесно связано с ужесточением требований к содержанию в них ароматических углеводородов, в частности бензола. Одним из направлений решения данной проблемы может быть селективное раскрытие циклов ароматических и нафтеновых углеводородов с образованием алканов с тем же числом атомов углерода, что и в исходном углеводороде [1]. В случае раскрытия полициклических соединений положительным эффектом может считаться и образование моноциклических соединений, которые менее склонны к образованию сажи и имеют более низкую температуру замерзания. Процессы раскрытия циклов, безусловно, более актуальны для конверсии тяжелого углеводородного сырья, содержащего полициклические нафтеновые и ароматические углеводороды, чем для конверсии легких моноциклических соединений бензинового ряда. Раскрытие циклов наряду с получением бензил-алкилата (алкилированием изобутана бутенами), скелетной изомеризацией алканов и риформингом составляют группу методов, направленных на повышение октанового числа бензинов.
Литературные данные о раскрытии циклов нафтенов, содержащих циклы С6, и тем более полициклические углеводороды, весьма ограничены. Имеется несколько ключевых публикаций в этой области [1–8], тогда как упоминания реакции раскрытия циклов в других работах связаны скорее с побочно протекающими процессами, в которых во многих случаях образуются, в основном, легкие газообразные продукты (скорее продукты крекинга или гидрокрекинга, чем раскрытия циклов). Следует отметить, однако, что реакции гидрокрекинга и раскрытия циклов очень близки, так как требуют присутствия водорода, и раскрытие циклов, по-видимому, протекает на части активных центров, ответственных за гидрокрекинг. По сути дела, раскрытие циклов – это мягкий гидрокрекинг применительно к циклическим структурам. Реакции раскрытия циклов протекают при сравнительно невысоких температурах: от 220–240°С для рутениевых нанесенных катализаторов до 380–400°С для платиновых систем, а большинство из известных систем активны при 280–320°С (Ir, Rh, многие биметаллические системы). Диапазон давлений, наиболее благоприятных для этой реакции, – 20–50 атм. При этом более низкие давления способствуют преобладанию процессов крекинга (образования легких газообразных продуктов), тогда как более высокие давления приводят к снижению активности благодаря конкуренции за адсорбционные центры между углеводородом и водородом. Что касается характерных объемных скоростей, использующихся в раскрытии циклов, то они достаточно велики (1–4 ч–1). Мольное соотношение водород : углеводород варьируется от 10 до 2–3, причем в случае ароматических субстратов требуется дополнительное избыточное количество водорода для гидрирования ароматического кольца в нафтеновую структуру.
Наиболее полный анализ активности нанесенных металлов в реакциях с участием водорода (раскрытие циклов, гидрирование, гидрогенолиз) дан в книге Соморджаи [9]. Однако подавляющее большинство данных приведено для реакций раскрытия циклов циклопропана и циклобутана, имеется несколько примеров конверсии циклопентана и бензола. Приведена лишь небольшая таблица, в которой сведены результаты по гидрогенолизу (раскрытию циклов) циклогексана. Известно, что раскрытие молекул циклопропана и циклобутана протекает достаточно легко при низких температурах, часто на катализаторах, не содержащих металлов [10]. Тем не менее, анализ данных для С3- и С4-циклов показывает, что для катализаторов на основе оксида алюминия активность в раскрытии этих циклов уменьшается в ряду Ru > Rh > Pt. Введение меди в катализатор (биметаллические композиции Pt–Cu, Ni–Cu) подавляет процесс раскрытия циклов [11, 12], тогда как модифицирование этих металлов рением оказывает благоприятный эффект [13].
Одна из первых работ по раскрытию циклов на примере циклогексана и метилциклопентана опубликована в 1977 г. японскими учеными, которые использовали катализатор Ni/Al2O3 [14]. Из циклогексана была получена смесь состава н-гексан : 2-метилпентан : 3-метилпентан = 2–6 : 1 : 1, состав которой сильно зависел от температуры реакции. В случае метилциклопентана была получена смесь н-гексан : 2-метилпентан : 3-метилпентан = 1 : 5 : 5, и ее состав не изменялся существенным образом с повышением температуры в достаточно широком диапазоне. Краткий обзор некоторых оксидных систем, активных в раскрытии циклов дан в [15].
Задача настоящего исследования – оценка каталитической активности цеолитных катализаторов, содержащих нанесенные наночастицы металлов в раскрытии циклов модельных циклических соединений.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали цеолиты NaX (Si/Al = = 1.25), NaY (Si/Al = 3.0), K-LTL (Si/Al = 3.5), LaY, LaCaNaY, LaNaY, H-BEA (Si/Al = 13), H-ZSM-5 (Si/Al = 30) в качестве носителей наночастиц платины, родия, палладия или рутения. Металлы наносили пропиткой высушенного при 150°С носителя водным раствором H2PtCl6, [(Rh(NH3)6]Cl3, PdCl2, RuCl3 c последующим прокаливанием при 300–400°С и восстановлением в токе водорода при 300–400°С. Содержание металла составляло 0.5–1 мас. %.
Реакцию гидрогенолиза проводили в импульсной или непрерывной проточной установке с варьированием температуры реакции от 200 до 400оС. Состав продуктов определяли методом газовой хроматографии на хроматографе ЛХМ-8МД с пламенно-ионизационным детектором, колонка SE-30 (1 мм × 50 м).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
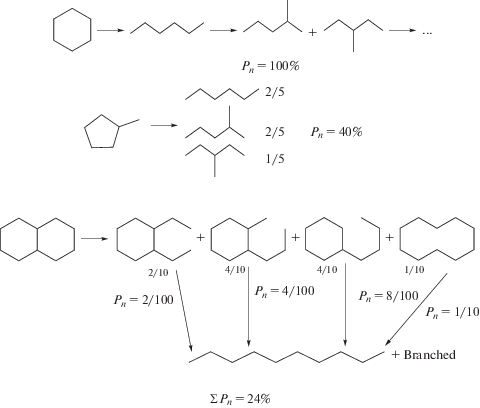
Рассмотрим чисто теоретически вероятности раскрытия различных циклических углеводородов с целью получения линейных алканов, наиболее ценных с точки зрения повышения цетанового числа, без учета термодинамических и кинетических факторов. Лишь в случае моноциклических структур (рис. 1) вероятность такого процесса (Pn) достаточно велика, тогда как в случае декалина и других полициклических соединений эта вероятность существенно снижается (24%). Очевидно, что наиболее сложно разорвать внутреннюю связь в молекуле декалина, поэтому реальная возможность получения линейных алифатических структур еще ниже приведенных оценок.
Термодинамические данные для модельной реакции гидрогенолиза циклогексана в н-гексан представлены в табл. 1. Приведенные данные свидетельствуют о том, что достаточно высокие выходы целевых продуктов могут быть достигнуты при относительно невысоких температурах. На основании этих оценок в качестве модельных субстратов были выбраны циклогексан и метилциклопентан. Предварительные исследования показали, что механизм процесса достаточно сложен и включает ряд реакций, таких как крекинг, скелетная изомеризация, раскрытие цикла, сужение цикла (получение циклопентановых структур из циклогексана), дегидрирование и гидрогенолиз. Активность цеолитных катализаторов в значительной степени определяется составом катализатора, содержанием нанесенного металла, соотношением кислотных центров различной природы, а также условиями реакции, в частности, температурой, давлением, соотношением углеводород : водород.
Таблица 1.
Равновесный состав (мас.%) реакционной смеси для раскрытия циклогексана
| T, °C | Циклогексан | H2 | н-C6H14 |
|---|---|---|---|
| 100 | 1.0 | 0.02 | 98.98 |
| 200 | 3.9 | 0.1 | 96.0 |
| 300 | 10.7 | 0.3 | 89.0 |
| 400 | 20.6 | 0.5 | 78.9 |
| 500 | 33.3 | 0.8 | 65.9 |
| Циклогексан | H2 | 2-Метилпентан | |
| 100 | 0.5 | 0.01 | 99.49 |
| 200 | 2.9 | 0.1 | 97 |
| 300 | 7.8 | 0.2 | 92 |
| 400 | 16.6 | 0.4 | 83 |
| 500 | 29.3 | 0.7 | 70 |
Условия реакции для проточной системы выбрали следующими: температуру варьировали от 180 до 450°С с оптимальным интервалом 200–300°С, объемная скорость составляла 0.4–0.5 ч–1, разбавление (соотношение углеводород : водород) – 1 : 11; загрузка катализатора – 0.5 г. Эксперименты в импульсной установке проводили в тех же режимах, что и для проточной установки, за исключением подачи углеводорода, который подавали через петлю объемом 1 мл, загрузка катализатора составляла 0.2 г.
Каталитические данные для конверсии циклогексана и метилциклогексана в импульсной и проточной установке представлены в табл. 2–4. Из состава продуктов видно, что в случае цеолитов вместо целевой реакции раскрытия циклов преобладают реакции дегидрирования и крекинга, особенно при высоких температурах. Эти реакции приводят к образованию бензола и легких продуктов С1–С3. Также идут реакции изомеризации циклогексана в метилциклопентан и н-гексана в метилпентаны. Наилучшие результаты в раскрытии циклогексана показал цеолит 0.5Pt/LaNaX. При конверсии циклогексана около 86% содержание гексанов в смеси составило несколько более 4%. На основных формах цеолитов основным процессом является дегидрирование с образованием бензола, а на кислотных формах (Н- и La-формы) преобладают реакции крекинга и изомеризации в метилциклопентан. Отметим, что рутениевые системы катализируют реакцию гидрогенолиза с получением легких газов С1–С4. Для кислотных форм цеолитов отмечено также образование некоторого количества более тяжелых продуктов С6+, видимо, за счет вторичных реакций олигомеризации продуктов крекинга (олефинов) и алкилирования циклических углеводородов ненасыщенными продуктами крекинга.
Таблица 2.
Конверсия циклогексана на цеолитных катализаторах в импульсном режиме при атмосферном давлении (C6H12 : H2 = 1 : 11 (об.); загрузка катализатора – 200 мг; He –газ-носитель, 1.2 л/ч; объем импульса смеси 1 мл)
| Катализатор | T, °C | Состав смеси углеводородов, мас. % | |||||
|---|---|---|---|---|---|---|---|
| C1–C5 | C6 | MЦП | ЦГ | C6H6 | C6+ | ||
| 0.5Pt/NaY | 210 | 1.9 | – | – | 98.1 | – | |
| 265 | 0.2 | – | – | – | 99.8 | ||
| 315 | 0.7 | – | – | – | 99.3 | ||
| 1Pt/NaX | 265–320 | – | – | – | – | ≈100 | |
| 1Rh/KL | 210 | 0.8 | – | 0.2 | 86.7 | 12.3 | |
| 265 | 3.0 | 0.05 | 0.05 | 39.9 | 57.0 | ||
| 320 | 11.3 | – | – | 0.2 | 87.6 | ||
| 1Rh/NaY | 210 | 3.0 | – | 4.4 | 83.6 | 9.0 | |
| 265 | 3.6 | – | – | – | 96.4 | ||
| 315 | 4.3 | – | – | – | 94.3 | 0.9 | |
| 1Ru/KL | 210 | 0.8 | – | 0.1 | 99.1 | – | |
| 265 | 5.5 | – | 0.1 | 92.7 | 1.7 | ||
| 315 | 22.5 | – | 0.1 | 72.0 | 5.3 | 0.1 | |
| 1Ru/NaY | 210 | 0.5 | – | 1.1 | 98.2 | 0.2 | |
| 265 | 2.1 | – | 0.9 | 96.4 | 0.4 | 0.2 | |
| 315 | 11.1 | – | 0.7 | 86.8 | 1.4 | ||
| 0.5Pt/LaY, FAU | 210 | 0.1 | – | 20.1 | 26.3 | 53.5 | – |
| 230 | 3.4 | – | 16.9 | 12.0 | 65.3 | 2.4 | |
| 265 | 6.0 | 0.7 | 4.5 | 0.9 | 84.1 | 3.8 | |
| 315 | 6.8 | 0.75 | 0.05 | – | 91.3 | 1.1 | |
| 0.5Pt/H-β | 210 | – | 1.4 | 35.9 | 54.0 | 8.7 | – |
| 265 | 10.6 | 1.4 | 16.0 | 10.6 | 58.5 | 2.9 | |
| 315 | 13.0 | – | – | – | 79.0 | 8.0 | |
| 0.5Pt/0.65La 0.33Ca0.02NaY |
210 | – | 0.2 | 26.2 | 68.2 | 5.4 | – |
| 265 | 8.6 | 0.9 | 13.4 | 16.7 | 60.4 | – | |
| 315 | 9.5 | 0.9 | 0.5 | 0.1 | 88.0 | 1.0 | |
| 0.5Pt/LaNaX | 210 | – | – | 19.0 | 80.7 | 0.3 | |
| 265 | 15.4 | 2.1 | 23.4 | 58.5 | 0.6 | ||
| 315 | 71.4 | 4.1 | 10.5 | 14.0 | |||
| 1Rh/LaNaX | 210 | 1.9 | – | 8.3 | 89.6 | 0.2 | |
| 265 | 21.2 | 2.1 | 8.3 | 67.3 | 1.1 | ||
| 315 | 99.6 | – | – | 0.4 | |||
| 1Ru/LaNaX | 210 | 0.7 | – | 0.5 | 98.8 | ||
| 265 | 4.4 | – | 2.8 | 92.8 | – | ||
| 315 | 20.1 | 0.8 | 7.8 | 71.2 | 0.1 | ||
| 350 | 30.0 | 2.2 | 11.5 | 56.1 | 0.2 | ||
Таблица 3.
Конверсия метилциклопентана на цеолитных катализаторах в импульсном режиме при атмосферном давлении (S – cелективность в раскрытии цикла, C6H12 : H2 = 1 : 11 (об.); загрузка катализатора – 200 мг; He –газ-носитель, 1.2 л/ч; объем импульса смеси 1 мл)
| Катализатор | Т, °С | S, % | Состав смеси углеводородов, мас. % | |||||
|---|---|---|---|---|---|---|---|---|
| C1–C5 | C6H14 | MЦП | ЦГ | С6H6 | С6+ | |||
| 0.5Pt/NaY | 265 | 12.4 | 0.05 | 1.6 | 87.1 | 8.2 | 3.0 | 0.05 |
| 1Pt/NaX | 320 | 50.6 | 1.1 | 13.2* | 73.9 | 5.3 | 6.1 | 0.4 |
| 350 | 58.2 | 3.2 | 23.5* | 59.6 | 4.6 | 7.4 | 1.7 | |
| 1Rh/KL | 265 | 33.1 | 4.6 | 4.6 | 86.1 | 3.8 | 0.9 | – |
| 315 | 14.0 | 16.4 | 3.8 | 72.9 | 2.1 | 3.9 | 0.9 | |
| 1Rh/NaY | 265 | 23.1 | 11.3 | 4.3 | 81.4 | 2.7 | – | 0.3 |
| 1Ru/KL | 265 | 7.8 | 4.2 | 0.7 | 91.0 | 4.1 | – | |
| 315 | 4.3 | 14.3 | 0.7 | 83.9 | 1.1 | – | ||
| 1Ru/NaY | 315 | 4.5 | 8.2 | 0.7 | 84.4 | 6.7 | – | |
| 0.5Pt/H-β | 210 | 7.2 | – | 1.3 | 81.9 | 14.0 | 2.8 | – |
| 265 | 1.8 | 17.9 | 1.8 | 1.9 | 0.3 | 27.5 | 50.6 | |
| 315 | – | 33.2 | – | – | – | 55.6 | 11.2 | |
| 0.5Pt/0.65La | 210 | – | 3.6 | – | 86.1 | 8.7 | 1.6 | |
| 0.33Ca0.02NaY | 265 | 17.1 | 15.4 | 6.3 | 63.2 | 7.2 | 7.9 | |
| 0.5Pt/LaNaX | 265 | 16.7 | 23.3 | 7.3 | 56.4 | 10.5 | 2.3 | 0.2 |
| 1Rh/LaNaX | 265 | 26.0 | 11.0 | 6.9 | 73.5 | 7.8 | 0.7 | 0.1 |
| 280 | 24.9 | 21.9 | 9.7 | 61.0 | 6.7 | 0.7 | ||
| 315 | 14.3 | 50.8 | 9.4 | 34.4 | 4.6 | 0.8 | ||
| 1Ru/LaNaX | 265 | 14.2 | 7.2 | 2.0 | 85.9 | 4.7 | 0.2 | |
| 315 | 16.0 | 26.5 | 6.2 | 61.2 | 5.4 | 0.7 | ||
| 350 | 12.9 | 57.2 | 9.5 | 26.4 | 6.4 | 0.5 | ||
Таблица 4.
Конверсия циклогексана в непрерывной проточной установке при атмосферном давлении. C6H12:H2 = 1:11 (об.); VHSV = 0.3 ч–1; загрузка катализатора 0.8 г.
| Катализатор | t, мин | T, °C | Состав продуктов, мас. % | |||||
|---|---|---|---|---|---|---|---|---|
| C1–C5 | MЦП | C6Н14 | ЦГ | C6H6 | C6+ | |||
| 0.5Pt/NaX | 10 | 265 | – | – | – | 85 | 15 | – |
| 20 | 265 | – | – | – | 84 | 16 | – | |
| 30 | 315 | – | – | – | 24 | 76 | – | |
| 60 | 210 | – | – | – | 98 | 2 | – | |
| 70 | 265 | – | – | – | 83 | 17 | – | |
| 0.5Pd/NaY | 5 | 265 | – | – | – | 74 | 26 | – |
| 40 | 315 | – | 1 | – | 64 | 35 | – | |
| 0.5Pt/NaY | 10 | 265 | – | – | – | 96 | 4 | – |
| 25 | 315 | – | 2 | – | 77 | 21 | – | |
| 40 | 335 | – | 3 | – | 67 | 30 | – | |
| 0.5Pt/KL | 5 | 330 | – | 5 | – | 66 | 6 | – |
| 20 | 315 | – | 2 | – | 89 | 9 | – | |
| 30 | 280 | – | 1 | – | 94 | 5 | – | |
| 40 | 265 | – | – | – | 97 | 3 | – | |
| 100 | 210 | – | – | – | 100 | – | – | |
| 0.5Pt/NaLaX | 5 | 265 | 10 | 46 | – | 36 | 8 | – |
| 20 | 265 | 21 | 34 | 1 | 37 | 8 | – | |
| 30 | 315 | 29 | 27 | 2 | 28 | 24 | – | |
| 0.5Pt/H–β | 5 | 265 | 31 | 40 | 5 | 9 | 15 | – |
| 20 | 265 | 25 | 45 | 4 | 10 | 16 | – | |
| 40 | 265 | 18 | 51 | 3 | 10 | 18 | – | |
| 70 | 315 | 9 | 3 | 2 | – | 79 | – | |
| 140 | 265 | 2 | 50 | 1 | 13 | 34 | – | |
| 0.5Pt/HZSM–5 | 10 | 340 | 48 | 1 | 1 | 7 | 2 | 2 |
| 25 | 315 | 43.5 | 5 | 2.5 | 45 | 2 | 2 | |
| 60 | 280 | 22 | 6 | 2 | 69 | 1 | – | |
| 70 | 265 | 8 | 5 | 1 | 86 | – | – | |
Обращает на себя внимание различие в поведении катализаторов в конверсии циклогексана и метилциклопентана (табл. 2 и 3). В отличие от циклогексана конверсия метилциклопентана протекает с образованием значительного количества гексанов (до 23.5%), в том числе н-гексана (до 6–7% в реакционной смеси), причем это более характерно для щелочных форм цеолитов, тогда как на кислотных формах, как и в случае циклогексана идут процессы крекинга. Для цеолита 1%Pt/NaX селективность в образовании гексанов (продуктов прямого раскрытия цикла) достигает 50–60% в отличие от конверсии циклогексана на том же катализаторе. С другой стороны, образование бензола незначительно, поскольку оно должно протекать через образование циклогексана и его последующего дегидрирования. Отметим, что и содержание циклогексана в смеси невелико, даже при использовании в качестве катализаторов кислотных форм цеолитов, в отличие от содержания метилциклопентана при конверсии циклогексана.
Все эти данные свидетельствуют о том, что конверсия этих двух углеводородов протекает по различным маршрутам на цеолитных катализаторах. Обычно полагают, что раскрытие циклогексановых структур происходит через образование метилциклопентановых структур, однако полученные результаты свидетельствуют о том, что это не совсем так.
Проведение процесса в проточной непрерывной системе показало, что конверсия циклогексана на щелочных формах цеолитов, содержащих благородные металлы, приводит, в основном, к продуктам дегидрирования. Выход метилциклопентана на этих системах невелик (<3–5%). Напротив, на кислотных формах цеолитов (H- или La-формы) кроме бензола образуются метилциклопентан, С6-парафины и продукты крекинга. Выход метилциклопентана увеличивается с понижением температуры реакции в отличие от продуктов крекинга. Наибольшие выходы метилциклопентана (~20–23%) наблюдаются для 0.5%Pt/LaNaX и 1%Pt/LaY. Максимальная активность в раскрытии циклогексана установлена для 0.5%Pt/LaNaX (4.1% алканов C6), 1%Rh/LaNaX (2.1%), и 1%Ru/LaNaX (2.2%). На этих катализаторах ароматические продукты не образуются, а доля продуктов крекинга значительна. Однако селективность по продуктам раскрытия циклов остается низкой (4–5%). Отметим цеолит Pt/H-BЕА, который проявляет умеренную активность в раскрытии циклов.
Таким образом, полученные результаты могут быть объяснены схемой, которая включает реакции изомеризации метилциклопентана в циклогексан и наоборот, крекинг, дегидрирование циклогексана, раскрытие обоих циклов:

Очевидно, что присутствие сильных кислотных центров в высокой концентрации (Н-формы) приводит к образованию значительного количества продуктов крекинга. Однако некоторое количество кислотных центров (желательно средней силы) все же необходимо для осуществления процесса.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (код проекта № 19-03-00808).
Список литературы
Tailleur R.G. // Fuel Proc. Technol. 2006. V. 87. № 9. P. 759.
Cusher N.A. // In: Handbook of Petroleum Refining Processes, McGraw-Hill, New York, 1986.
McVicker G.B., Daage M., Touvelle M.S. et al. // J. Catal. 2002. V. 210. № 1. P. 137.
Vaarkamp M., Dijkstra P., van Grondelle J. et al. // Ibid. 1995. V. 151. P. 330.
Martens J.A. // Thesis, Univ. Leuven, 1985.
Lam Y.L., Sinfelt J.H. // J. Catal. 1976. V. 42. P. 319.
Anderson J.B.F., Burch R. // J. Chem. Soc., Faraday Trans. 1987. V. 83. P. 913.
Sinfelt J.H. // J. Catal. 1973. V. 29. P. 308.
Somorjai G.A. // Introduction to Surface Chemistry and Catalysis. New York: Wiley, 1994.
Torok B., Pálinkó I., Bartók M. // Catal. Lett. 1995. V. 31. P. 421.
Schepers F.J., van Senden J.G., van Broekhoven E.H., Ponec V.J. // J. Catal. 1985. V. 94. P. 400.
Roberti A., Ponec V., Sachtler W.M.H. // Ibid. 1973. V. 28. P. 381.
Bolivar C., Leclercq G., Maurelet R. et al. // Ibid. 1976. V. 45. P. 179.
Miki Y., Yamadaya S., Oba M. // Ibid.1977. V. 49. № 3. P. 278.
Kustov L.M., Finashina E.D., Avaev V.I., Ershov B.G. // Fuel Process. Technol. 2018. V. 173. P. 270.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии