Журнал физической химии, 2020, T. 94, № 2, стр. 245-248
Термохимическое исследование реакций кислотно-основного взаимодействия в водном растворе β-аминомасляной кислоты
А. И. Лыткин a, В. В. Черников a, О. Н. Крутова a, *, Г. Ньягоя a
a Ивановский государственный химико-технологический университет
Иваново, Россия
* E-mail: kdvkonkpd@yandex.ru
Поступила в редакцию 25.04.2019
После доработки 02.07.2019
Принята к публикации 15.07.2019
Аннотация
Калориметрическим методом измерены тепловые эффекты взаимодействия раствора β-аминомасляной кислоты с растворами HNO3 и КОН в различных интервалах рН при температуре 298.15 К и значениях ионной силы 0.25; 0.5 и 0.75 (КNO3). Определены тепловые эффекты ступенчатой диссоциации аминокислоты. Рассчитаны стандартные термодинамические характеристики (ΔrH°, ΔrG°, ΔrS°) реакций кислотно-основного взаимодействия в водных растворах β-аминомасляной кислоты. Рассмотрена связь термодинамических характеристик диссоциации аминокислоты со структурой данного соединения.
Диссоциацию β-аминомасляной кислоты (C4H9NO2) в водном растворе можно представить схемой:
(1)
${{{\text{Н}}}_{2}}{{{\text{L}}}^{{ + ~}}} \leftrightarrow {{{\text{Н}}}^{{ + ~}}} + {\text{Н}}{{{\text{L}}}^{ + }},$(2)
${\text{Н}}{{{\text{L}}}^{ \pm }}^{~} \leftrightarrow {{{\text{Н}}}^{{ + ~}}} + {{{\text{L}}}^{ - }}.$В литературе имеются надежные данные по константам ионизации β-аминомасляной кислоты [1–5]. Эти работы выполнены при различных значениях ионной силы, на фоне отличающихся по своей природе поддерживающих электролитов. Для того, чтобы можно было сравнивать значения констант ступенчатой диссоциации β-аминомасляной кислоты, полученные разными авторами, мы пересчитали величины рK1 и рK2 на нулевую ионную силу. Термодинамические константы ступенчатой диссоциации β-аминомасляной кислоты определяли также графическим методом по уравнению [6]:
(3)
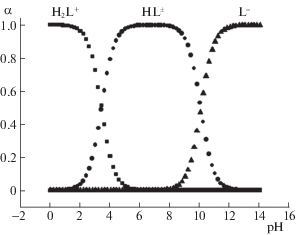
${\text{p}}{{K}^{c}} = {\text{p}}{{K}^{{^{ \circ }}}} - \Delta {{Z}^{2}}A\frac{{\sqrt I }}{{1 + 1.6\sqrt I }} + \delta I.$После графической обработки литературных данных [1–5], в качестве наиболее вероятных значений термодинамических констант диссоциации β-аминомасляной кислоты можно принять при 298.15 К: ${\text{р}}K_{1}^{0}$ = 3.53 ± 0.02, ${\text{р}}K_{2}^{0}$ = 10.11 ± 0.03. На рис. 1 представлена диаграмма равновесий в водном растворе β-аминомасляной кислоты, построенная на основании расчетов равновесного состава растворов аминокислоты при различных значениях рН с использованием программы KEV [7].
Рис. 1.
Диаграмма равновесий в водном растворе D,L-3 аминомасляной кислоты при 298.15 К и ионной силе I = 0.0.
Данные по теплотам реакций кислотно-основного взаимодействия с участием β-аминомасляной кислоты в литературе отсутствуют.
Целью настоящей работы является изучение влияния концентрации фонового электролита на тепловые эффекты диссоциации β-аминомасляной кислоты методом прямой калориметрии, расчет стандартных термодинамических характеристик реакций кислотно-основного взаимодействия в растворах аминокислоты; обсуждение полученных результатов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Выбор концентрационных условий проведения калориметрических опытов проводился на основании диаграммы равновесий в водном растворе D,L-3 аминомасляной кислоты (рис. 1). Долевое распределение частиц H2L+, HL± и L– при различных значениях рН среды (рис. 1) указывает на возможность независимого определения теплот диссоциации катиона и цвиттер-иона D,L-3 аминомасляной кислоты.
Были измерены теплоты смешения растворов D,L-3 аминомасляной кислоты с растворами HNO3 и KOH в различных интервалах pH на калориметре с изотермической оболочкой и автоматической записью кривой температура-время [8]. Работа калориметрической установки была проверена по общепринятому калориметрическому стандарту – теплоте растворения кристаллического хлорида калия в воде. Препарат KCl очищали двукратной перекристаллизацией реактива марки “x.ч.” из бидистиллята. Перед взятием навесок хлорид калия высушивали в сушильном шкафу при 393.15 К до постоянной массы. Согласование экспериментально полученных энтальпий растворения КСl(кр.) в воде ΔsolН(∞Н2О) = = 17.25 ± 0.06 кДж/моль с наиболее надежными литературными данными [9] свидетельствует об отсутствии заметной систематической погрешности в работе калориметрической установки. Навески растворов взвешивали на весах марки ВЛР-200 с точностью 2 × 10–4 г.
В работе использован препарат D,L-3 аминомасляной кислоты фирмы “TCI” (Япония), без дополнительной очистки содержание основного вещества в препарате составляло 98.0%. Растворы аминокислоты готовили растворением навесок препарата в свежеприготовленном бидистилляте непосредственно перед проведением опыта. Перед взятием навесок кристаллические препараты высушивали до постоянной массы при температуре 343.15 К. Бескарбонатный раствор КOH и раствор HNO3 приготавливали из реактива марки “х.ч.” по обычной методике [10].
При определении теплового эффекта присоединения протона к карбоксильной группе D,L-3 аминомасляной кислоты в качестве калориметрической жидкости использовался 0.02 М раствор аминокислоты (рНисх = 3.8), а в ампулу соответственно помещали точную навеску раствора НNO3 (с концентрацией 0.8814 моль/кг раствора). После смешения растворов величина рН была близка к 2.2. Экспериментальные данные по теплотам смешения и разведения приведены в табл. 1.
Таблица 1.
Тепловые эффекты (Дж/моль) взаимодействия 0.02 М раствора β-аминомасляной кислоты с раствором НNO3 (рНисх 3.8 – рНкон 2.2 ), Т = 298.15 К
| I | m, г | –ΔmixH, Дж/моль | m, г | –ΔdilH, Дж/моль | α | –ΔdisH(H2L+) Дж/моль |
|---|---|---|---|---|---|---|
| 0.25 | 0.5011 | 1662 | 0.5001 | 1052 | 0.8248 | 2011 ± 200 |
| 0.5011 | 1660 | 0.5005 | 1089 | 0.8247 | ||
| 0.5011 | 1656 | 0.5006 | 1076 | 0.8248 | ||
| (1659 ± 170) | (1072 ± 150) | |||||
| 0.5 | 0.5022 | 912 | 0.5006 | 890 | 0.8249 | 2392 ± 200 |
| 0.5022 | 915 | 0.5002 | 896 | 0.8248 | ||
| 0.5023 | 910 | 0.5001 | 894 | 0.8248 | ||
| (913 ± 180) | (893 ± 150) | |||||
| 0.75 | 0.5011 | 2706 | 0.5002 | 394 | 0.8245 | 2834 ± 200 |
| 0.5012 | 2699 | 0.5003 | 383 | 0.8242 | ||
| 0.5012 | 2703 | 0.5006 | 362 | 0.8243 | ||
| (2702 ± 180) | (379 ± 150) |
При определении тепловых эффектов процесса (2), были измерены теплоты взаимодействия водного раствора аминокислоты (концентрация раствора 0.8927 моль/кг раствора) с 0.1 М раствором КОН, а также теплоты разведения раствора D,L-3 аминомасляной кислоты в растворах фонового электролита (КNO3). Полученные величины теплот смешения и разведения D,L-3 аминомасляной кислоты представлены в табл. 2.
Таблица 2.
Тепловые эффекты (Дж/моль) взаимодействия раствора β-аминомасляной кислоты с 0.02 М растворами КОН при Т = 298.15 К
| I | m, г | –ΔmixH1, Дж/моль | –ΔdilH1, Дж/моль | –ΔneutH, Дж/моль | ΔdisH(HL±), Дж/моль |
|---|---|---|---|---|---|
| 0.25 | 0.5005 | 18 003 | 7896 | 10 154 | 47 165 ± 340 |
| 0.4991 | 18 120 | 7832 | 10 145 | ||
| 0.5003 | 17 899 | 7796 | 10 200 | ||
| (18 007 ± 260) | (7841 ± 150) | (10166 ± 260) | |||
| 0.5 | 0.5002 | 14 500 | 5804 | 8684 | 48 269 ± 300 |
| 0.4993 | 14 460 | 5771 | 8659 | ||
| 0.4998 | 14 529 | 5815 | 8756 | ||
| (14 496 ± 210) | (5797 ± 150) | (8699 ± 220) | |||
| 0.75 | 0.57003 | 11 081 | 3256 | 7849 | 48 920 ± 310 |
| 0.5000 | 10 958 | 3225 | 7835 | ||
| 0.4997 | 11 001 | 3143 | 7822 | ||
| (11 013 ± 200) | (3174 ± 120) | (7839 ± 220) |
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Тепловой эффект диссоциации частицы H2L+ (${{\Delta }_{{{\text{dis}}}}}H_{{{{{\text{H}}}_{{\text{2}}}}{\text{L}}}}^{ + }$) рассчитывали по уравнению:
(4)
${{\Delta }_{{{\text{dis}}}}}H_{{{{{\text{H}}}_{2}}{\text{L}}}}^{ + } = - ({{\Delta }_{{{\text{mix}}}}}H - {{\Delta }_{{{\text{dil}}}}}H){\text{/}}{{\alpha }_{1}},$Процесс нейтрализации водного раствора β‑аминомасляной кислоты можно представить уравнением:
(5)
${\text{H}}{{{\text{L}}}^{{ \pm ~}}} + {\text{O}}{{{\text{H}}}^{--}} \leftrightarrow {{{\text{L}}}^{ - }} + {{{\text{H}}}_{2}}{\text{О}}.$Тепловой эффект диссоциации бетаинового протона β-аминомасляной кислоты (${{\Delta }_{{{\text{dis}}}}}H_{{{\text{HL}}}}^{ \pm }$) рассчитывали по уравнению:
(6)
${{\Delta }_{{{\text{neut}}}}}H = ({{\Delta }_{{{\text{mix}}}}}{{H}^{1}} - {{\Delta }_{{{\text{dil}}}}}{{H}^{1}}){\text{/}}{{\alpha }_{2}}$(7)
${{\Delta }_{{{\text{dis}}}}}H_{{HL}}^{ \pm } = {{\Delta }_{{{\text{neut}}}}}H - \Delta {{H}_{w}},$Величина ΔHw была взята из работы [11] для фонового электролита, использовавшегося в нашей работе. Найденные тепловые эффекты диссоциации аминокислоты приведены в табл. 2. Погрешность определена как стандартное отклонение средней величины из трех–четырех параллельных опытов.
Тепловые эффекты диссоциации β-аминомасляной кислоты в стандартном растворе найдены экстраполяцией теплот ступенчатой диссоциации при фиксированных значениях ионной силы на нулевую ионную силу по уравнению, предложенному в [6]:
где ΔrHi, ${{\Delta }_{{\text{r}}}}H_{i}^{0}$ – изменение энтальпии при конечном значении ионной силы и при I = 0, соответственно, Ψ(I) – функция ионной силы, вычисленная теоретически, Δz2 – разность квадратов зарядов продуктов реакции и исходных компонентов, b – эмпирический коэффициент.Точки в координатах (ΔН – ΔZ2Ψ(I) от I), удовлетворительно укладывались на прямую. При обработке по МНК получили энтальпии диссоциации β-аминомасляной кислоты при нулевой ионной силе: ΔdisH(H2L±) = –1.56 ± 0.20 кДж/моль и ΔdisH(HL±) = 46.99 ± 0.30 кДж/моль.
Стандартные термодинамические характеристики процессов ступенчатой диссоциации β-аминомасляной кислоты представлены в табл. 3.
Таблица 3.
Стандартные термодинамические характеристики (кДж/моль) кислотной диссоциации β-аминомасляной кислоты (Т = 298.15 К)
| Процесс | рК0 | ΔrН0, | ΔrG0, | А | –Δr$H_{{\text{з}}}^{0}$ | Δr$H_{{{\text{нз}}}}^{0}$ | ΔrS0, Дж/(мольK) |
|---|---|---|---|---|---|---|---|
| H2L+ = HL± + H+ | 3.53 ± 0.03 | –1.56 ± 0.20 | 20.15 ± 0.35 | 1301 | 12.88 | 11.32 | –72.8 ± 1.1 |
| HL± = L– + H+ | 10.11 ± 0.05 | 46.99 ± 0.30 | 57.71 ± 0.35 | 943 | 2.52 | 49.51 | –35.9 ± 1.4 |
Для анализа данных по термодинамике реакций кислотно-основного взаимодействия и комплексообразования с биолигандами оказывается полезным подход, основанный на представлениях Герни, подробно описанный в работе [12]. Изменение энтальпии можно представить в виде суммы температрно-зависимого (ΔrНз) и температурно-независимого (ΔrНнз) слагаемых
В работе [12] было предложено разделить протоноакцепторные частицы на две группы в зависимости от величины вклада $\left| {{{\Delta }_{{\text{r}}}}{{Н}_{{{\text{нз}}}}}} \right| = \left| {{{\Delta }_{{\text{r}}}}{{G}_{{{\text{нз}}}}}} \right|$. Первая группа характеризуется высоким значением данного вклада. Сюда относятся все частицы, содержащие аминогруппу. Численные значения вклада $\left| {{{\Delta }_{{\text{r}}}}{{Н}_{{{\text{нз}}}}}} \right| = \left| {{{\Delta }_{{\text{r}}}}{{G}_{{{\text{нз}}}}}} \right|$ при протонировании частиц этого типа составляют, как правило 30–40 кДж/моль и больше. Эту группу называют неэлектростатической. Значение зависящего от температуры вклада при протонировании частиц этого типа невелико.
У частиц второй группы, протонирование которых происходит через кислород, величина независящего от температуры вклада много меньше и лишь в редких случаях превышает 12 кДж/моль. Примерно ту же величину составляет у частиц этой группы и зависящий от температуры вклад ΔrНз.
В нашем случае молекула аминокислоты содержит обе эти функциональные группы; протонирование R-NH2 происходит очевидно, как у частиц первой группы (ΔrНнз для β-аминомасляной кислоты составляет 49.51 кДж/моль), а протонирование кислород содержащего фрагмента – как у частиц второй группы (ΔrНнз для β-аминомасляной кислоты равняется 11.32 кДж/моль) (табл. 3).
В литературе имеются данные по термодинамическим характеристикам 2-аминомасляной кислоты и 4-аминомасляной кислоты [13, 14]. Аминогруппа 3-аминомасляная кислоты проявляет более сильные основные свойства (более высокое значение ${\text{р}}K_{2}^{{^{ \circ }}} = 10.11$), чем аминогруппа 2‑аминомасляная кислота (${\text{р}}K_{2}^{{^{ \circ }}} = 9.18$) и менее сильные чем аминогруппа 4-аминомасляная кислота (${\text{р}}K_{2}^{{^{ \circ }}} = 10.48$). Единичный отрицательный заряд карбоксильной группы, приводит к повышению электронной плотности на аминогруппе и электростатическое притяжение (эффект поля) между аммоний-катионом и карбоксилат-анионом затрудняет отрыв протона от аммонийной группы. При переходе от 2-аминомасляная кислоты к 4-аминомасляная кислоте ослабевает действие индукционного эффекта, так как аминогруппа отделена от карбоксильной группы большим количеством углеродных атомов. Ослабление действия индукционного эффекта ведет к ослаблению азот-водордной связи и, как следствие, заряженные амино группы 4-аминомасляная кислоты могут связывать больше воды, чем ${\text{NH}}_{{\text{3}}}^{{\text{ + }}}$-группа в 2-аминомасляная кислоте. Это проявляется, в частности в том, что $\left| {\Delta S_{1}^{0}} \right|$ при диссоциации 4-аминомасляная кислота больше по абсолютной величине, чем $\left| {\Delta S_{1}^{0}} \right|$ при диссоциации 2-аминомасляная кислота и 3-аминомасляная кислоты.
Работа выполнена в рамках НИИ Термодинамики и кинетики химических процессов Ивановского государственного химико-технологического университета в рамках Государственного задания (базовая часть), проект № 4.7104.2017/89 с использованием оборудования Центра коллективного пользования ИГХТУ (ЦКП ИГХТУ).
Список литературы
Sharma V., Mathur H., Kilarni P. et al. // Indian J. Chem. 1965. V. 3. P. 475.
Letter J., Bauman J. // J. Am. Chem. Soc. 1970. V. 92. № 3. P. 437.
Sostaric I., Simeom V. // Monatsh. Chem. 1975. V. 106. P. 169.
Bottari E. // Ann. Chim. (Rome). 1976. V. 66. P. 193.
Brandariz I., Fiol S., Sastre de Vicente M. // J. Chem. Eng. Data. 1993. V. 38. № 4. P. 531.
Васильев В.П. Термодинамические свойства растворов электролитов, М.: Высш. школа, 1982. 313 с.
Meshkov A.N., Gamov G.A. // Talanta. 2019. V. 198. P. 200.
Lytkin A.I., Chernikov V.V., Krutova O.N., Skvortsov I.A. // J. Thermal Analysis and Calorimetry. 2017. V. 130 (1). P. 457.
Parcker W.B. Thermal Properties of Aqueous Uni-Univalent Electrolytes.Washington: NSRDS-NBS, 1965. B. 2. P. 342.
Коростелев П.П. Приготовление растворов для химико-аналитических работ, М.: Изд-во АН СССР, 1962. С. 398.
Лобанов Г.А., Васильев В.П. // Изв. вузов. Химия и хим. технология. 1969. Т. 12. № 6. С. 740.
Васильев В.П. // Журн. неорган. химии. 1984. Т. 29. № 11. С. 2785.
Lin H.-K., Gu Z.-Z., Chen X.-M. // Thermochim. Acta. 1988. V. 123. P. 201.
Лыткин А.И., Крутова О.Н., Черников В.В. и др. // Журн. физ. химии. 2017. Том 91. № 1. С. 5.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии


