Журнал физической химии, 2020, T. 94, № 3, стр. 467-473
Влияние природы газа-носителя на характеристики удерживания сорбатов
В. Е. Ширяева a, Т. П. Попова a, А. Ю. Канатьева a, А. А. Королев a, А. А. Курганов a, *
a Российская академия наук, Федеральное государственное бюджетное учреждение науки
Институт нефтехимического синтеза им. А.В. Топчиева
119991 Москва, Россия
* E-mail: kurganov@ips.ac.ru
Поступила в редакцию 16.04.2019
После доработки 14.05.2019
Принята к публикации 07.08.2019
Аннотация
Проверена возможность определения фазового соотношения хроматографической колонки хроматографическим методом исходя из полуэмпирической зависимости времени удерживания гомологов от числа атомов углерода в его структуре. Рассмотрено влияние природы и давления газа-носителя на величину фазового отношения. Показано, что независимо от природы газа-носителя среднее значение для полярной фазы составляет 1190 ± 100, а для неполярной фазы 380 ± 50 за исключением газа-носителя СО2, для которого, после проведения коррекции исходных данных, наблюдалось сильное уменьшение величины фазового отношения β. В то же время отмечено, что хроматографически находимые значения фазового соотношения сильно отличаются от величин, сообщаемых производителями колонок, тогда как мертвое время системы tМ и значение энергии сорбции метиленового звена гомологического ряда $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$ надежно определяются экстраполяционным методом.
Применение газовой хроматографии для определения физико-химических характеристик аналитов неизбежно связано с определением таких характеристик хроматографической системы как мертвое время системы tM и фазовое соотношение β, необходимых для расчета чистого времени удерживания $t_{{\text{R}}}^{{^{ \circ }}}$, исправленного объема удерживания $V_{{\text{R}}}^{{^{ \circ }}}$, фактора удерживания k и т.д. При определении термодинамических параметров сорбции – энтальпии ΔH и энтропии ΔS сорбции, мертвое время системы tM обычно определяют по времени выхода “несорбируемого” соединения, например, метана ($t_{{\text{M}}}^{{{\text{C}}{{{\text{H}}}_{{\text{4}}}}}}$) или легких инертных газов [1, 2]. В то же время, при построении теоретических моделей для предсказания времен удерживания при программировании температуры и/или давления в капиллярной газовой хроматографии широко используется мертвое время $t_{{\text{M}}}^{{{\text{th}}}}$, находимое из уравнения Пуазейля–Дарси, адаптированного для сжимаемого флюида [3, 4]:
(1)
$t_{M}^{{{\text{th}}}} = \frac{4}{3}\frac{{{{L}^{2}}\eta }}{{{{K}_{V}}}}\frac{{({{P}^{3}} - 1)}}{{{{{({{P}^{2}} - 1)}}^{2}}{{p}_{{\text{o}}}}}},$Альтернативный метод нахождения мертвого времени газохроматографической системы заключается в использовании известной полуэмпирической линейной корреляции логарифма чистого времени удерживания гомологов алканов с числом атомов углерода n в их структуре [1, 2, 5]:
C термодинамической точки зрения, более обосновано использовать в корреляции (2) не чистое время удерживания сорбата, а фактор удерживания k = (tR – tM)/tM. В этом случае коэффициенты a и b приобретают смысл энергии сорбции нулевого члена гомологического ряда (а = ΔGo) и энергии сорбции метиленового звена (b = $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{2}}}}}$):(3)
$ - RT\ln k\beta = - RT\ln \frac{{{{t}_{{\text{R}}}} - {{t}_{{\text{M}}}}}}{{{{t}_{{\text{M}}}}}}\beta = \Delta {{G}_{{\text{o}}}} + n * \Delta {{G}_{{{\text{C}}{{{\text{H}}}_{2}}}}}.$(5)
$\begin{gathered} a = \frac{{\Delta {{S}_{{\text{o}}}}}}{R} - \ln \beta \quad b = \frac{{\Delta {{S}_{{{\text{C}}{{{\text{H}}}_{2}}}}}}}{R}, \\ c = - \frac{{\Delta {{H}_{{\text{o}}}}}}{R},\quad d = - \frac{{\Delta {{H}_{{{\text{C}}{{{\text{H}}}_{2}}}}}}}{R}. \\ \end{gathered} $Однако методы современной нелинейной аппроксимации позволяют обходиться без знания первичного мертвого времени и позволяют находить не только мертвое время системы tM, но и фазовое соотношение колонки β, равное отношению объема подвижной фазы в колонке VM к объему стационарной фазы VS [9]. Обычно объем стационарной фазы VS находят делением массы стационарной фазы в колонке на ее плотность [10]. В случае капиллярной колонки масса стационарной фазы составляет всего нескольких миллиграммов, и точность определения фазового соотношения и рассчитываемой из него толщины пленки стационарной фазы df оставляют желать лучшего. Кроме того, колонки в ГХ обычно работают при повышенной температуре, что предполагает знание зависимости плотности стационарной фазы от температуры. Еще менее изучен вопрос о влиянии природы газа-носителя на величину фазового соотношения. Газ-носитель принято считать инертной средой, осуществляющей транспортировку сорбата по колонке и не оказывающей существенного влияния на результаты разделения. Однако в ряде публикаций этот подход был подвергнут критике (см. обзор [11] и ссылки там) и, если точка зрения этих авторов справедлива, то растворение газа-носителя в стационарной фазе может заметно влиять на величину фазового соотношения колонки. Цель данной публикации – проверить возможность определения фазового соотношения хроматографическим методом и проследить влияние природы газа-носителя на величину этого соотношения на примере ряда традиционных для ГХ стационарных фаз и газов-носителей.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Все хроматографические измерения проведены на газовых хроматографах фирмы Shimadzu моделей GC-2010 или GC-17A с газами носителями гелием, азотом, углекислым газом и оксидом азота в изотермическом режиме при 70°С. Свойства капиллярных колонок, использованных в работе, приведены в табл. 1. Температура испарителя 250°С, деление потока 1:50, детектор ПИД при температуре 250°С.
Таблица 1.
Свойства колонок, использованных для экспериментов
| Номер | Производитель | Обозначение | Тип стационарной фазы | L, м | d, мм | l, мкм |
|---|---|---|---|---|---|---|
| 1 | Phenomenex | ZB-1 | 100% ПДМС | 30.0 | 0.25 | 0.25 |
| 2 | J&W Scientific | DB-WAX | 100% ПЭГ | 30.0 | 0.25 | 0.25 |
| 3 | J&W Scientific | DB-WAX | 100% ПЭГ | 30.0 | 0.25 | 0.25 |
| 4 | Chrompack | CP-Sil 8CB | 5% фенил-силоксана в ПДМС | 30.0 | 0.25 | 0.5 |
| 5 | GL Science | TC-1 | 100% ПДМС | 30.0 | 0.25 | 1.0 |
| 6 | Chrompack | CP-Sil 8CB | 5% фенил-силоксана в ПДМС | 25.0 | 0.15 | 2.0 |
Стандартная смесь нормальных углеводородов С5–С10 была приготовлена растворением индивидуальны компонентов в хлористом метилене в концентрации от 0.2 до 1.5%.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Аппроксимация экспериментально измеренных зависимостей времени удерживания сорбатов С1 и С6-С10 от числа атомов угдерода проводилась уравнением (3), в форме, предложенной в работе [9]:
(8)
${{t}_{{\text{R}}}} = {{t}_{{\text{M}}}}\left( {1 + \frac{1}{\beta }\exp \left( { - \frac{{\Delta {{G}_{{\text{o}}}}}}{{RT}} - \frac{{n*\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}}}{{RT}}} \right)} \right).$Рис. 1.
Аппроксимация уравнением (7) экспериментальной зависимости времени удерживания углеводородов С1, С6–С10 от числа атомов углерода n. Полярная колонка с ПЭГ фазой (номер 2, табл. 1), газ-носитель азот, температура колонки 70°С, давление на колонке 30 кПа (Р = 1.3).

Рис. 2.
Зависимость мертвого времени tM (1), фазового отношения β (2) и энергии сорбции метиленового звена $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$ (3) от величины фактора Халаша. Колонка и условия разделения те же, что на рис. 1.
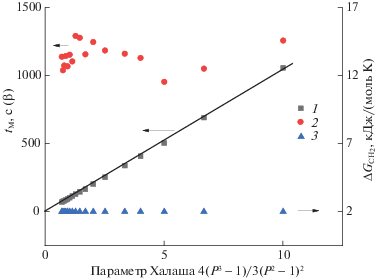
Рис. 3.
Коррекция экспериментальных данных линейной аппроксимацией для колонок приведенных в табл. 1.

Таблица 2.
Параметры линейной аппроксимации a + b*x (коррекция 1) экспериментальной зависимости времени удерживания сорбатов tR от относительного давления газа-носителя Р (R2 > 0.999)
| Стационарная фаза | Сорбат | Газ-носитель | |||||||
|---|---|---|---|---|---|---|---|---|---|
| гелий | азот | углекислый газ | закись азота | ||||||
| a | b | a | b | a | b | a | b | ||
| SE-30 (полидиметил-силоксан) | метан | 0 | 106.0 | –4.5 | 132.9 | –12.3 | 91.2 | –13.5 | 91.5 |
| н-гексан | 0 | 130.2 | –5.1 | 163.7 | –16.2 | 113.2 | –16.6 | 112.2 | |
| н-гептан | 0 | 159.9 | –6.9 | 200.1 | –20.1 | 138.6 | –20.6 | 137.3 | |
| н-октан | 0 | 223.6 | –10.3 | 279.2 | –29.0 | 193.3 | –24.1 | 191.0 | |
| н-нонан | 0 | 359.8 | –14.7 | 443.7 | –48.3 | 310.2 | –48.3 | 306.0 | |
| н-декан | 0 | 650.4 | –48.6 | 815.1 | –89.1 | 535.8 | –88.9 | 550.4 | |
| DB-WAX (полиэтилен-гликоль) | метан | –3.1 | 112.4 | –7.9 | 105.5 | –8.2 | 92.7 | –5.4 | 89.6 |
| н-гексан | –3.5 | 117.9 | –5.0 | 109.7 | –7.5 | 96.3 | –5.7 | 93.7 | |
| н-гептан | –3.5 | 123.3 | –8.3 | 115.7 | –8.0 | 100.7 | –6.0 | 97.9 | |
| н-октан | –4.0 | 134.2 | –7.7 | 124.3 | –8.7 | 109.4 | –4.0 | 105.1 | |
| н-нонан | –4.7 | 155.5 | –10.8 | 144.6 | –10.6 | 126.5 | –8.1 | 123.0 | |
| н-декан | –5.6 | 197.7 | –18.9 | 182.6 | –14.1 | 159.9 | –11.2 | 155.6 | |
Рис. 4.
Зависимость мертвого времени tM, фазового отношения β и энергии сорбции метиленового звена $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$ от величины фактора Халаша для той же колонки 2 (рис. 2), после коррекции экспериментальных данных.

Интересно отметить, что для системы полидиметилсилоксан/гелий, когда свободный параметр линейной функции равен 0 (табл. 2), фазовое отношение β от давления не зависит (рис. 5). Равным образом, если коррекцию экспериментальных данных проводить линейной функцией из табл. 1, положив свободный параметр а равным 0 (коррекция 2), то находимая величина фазового соотношения β также оказывается независимой от давления газа-носителя, как это показано на рис. 5 в качестве примера. Взаимосвязь этих параметров позволяет предположить, что появление отрицательного свободного параметра a в линейной аппроксимации и зависимость фазового отношения от давления вызваны неидеальностью газа-носителя. Коррекция экспериментальных данных линейной функцией без свободного параметра (коррекция 2) позволяет устранить это влияние, но мы не уверены, что подобная коррекция допустима, и поэтому величины фазового отношения β были найдены для двух серий данных (табл. 3), “корректированных” как это описано выше. Как видно из табл. 3, выполненные “коррекции” мало сказываются на величине энтальпии сорбции метиленового звена $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$, которая сохраняется на уровне 1.9 ± 0.1 кДж/(моль К) для полярной ПЭГ фазы и на уровне 2.1 ± 0.1 кДж/(моль К) для неполярной ПДМС фазы, независимо от природы газа-носителя (за исключением углекислого газа, который после коррекции показывает уменьшение $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$/(RT)). Величины фазового отношения β оказываются более чувствительными к проводимой коррекции, так что среднее значение для полярной фазы составляет 1190 ± 100, а для неполярной фазы 380 ± 50, независимо от природы газа-носителя. Исключение опять представляет углекислый газ, для которого проведение коррекции на полярной фазе вызывает особенно сильное уменьшение находимого значения фазового отношения β (табл. 3).
Рис. 5.
Зависимость мертвого времени tM, фазового отношения β и энергии сорбции метиленового звена $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$ от величины фактора Халаша для колонки с неполярной стационарной фазой (номер 1 в табл. 1), после коррекции данных линейной аппроксимацией.

Таблица 3.
Влияние коррекции экспериментальных данных на величины фазового соотношения β и энергии сорбции метиленового звена $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$ (rsd ~7%)
| Стационарная фаза | Коррекция данных | Гелий | Азот | Закись азота | Углекислый газ | ||||
|---|---|---|---|---|---|---|---|---|---|
| β | $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$ | β | $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$ | β | $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$ | β | $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$ | ||
| – | кДж/(моль К) | кДж/(моль К) | кДж/(моль К) | кДж/(моль К) | |||||
| DB-WAX (полиэтилен-гликоль) | б/корр. | 1236 | –1.95 | 1143 | –1.91 | 1165 | –1.85 | 1153 | –1.92 |
| корр. 1 (линейная аппроксимация) | 1165 | –1.97 | 1141 | –1.92 | 1190 | –1.91 | 662 | –1.74 | |
| корр. 2 (линейная аппроксимация без свободного члена) | 1138 | –1.94 | 1247 | –1.95 | 1447 | –1.99 | 816 | –1.80 | |
| SE-30 (полидиметил-силоксан) | б/корр. | 390 | –2.17 | 384 | –2.16 | 390 | –2.16 | 376 | –2.16 |
| корр. 1 (линейная аппроксимация) | – | – | 334 | –2.12 | 342 | –2.16 | 420 | –2.17 | |
| корр. 2 (линейная аппроксимация без свободного члена) | 393 | 2.17 | 420 | –2.16 | 389 | –2.16 | 261 | –2.15 | |
Однако наиболее существенным является то обстоятельство, что две колонки одинакового внутреннего диаметра dc = 0.25 мм и одинаковой толщины пленки df = 0.25 мкм (согласно данным производителей, см. табл. 1) показали различающиеся более чем в 3 раза значения фазового отношения и, тем не менее, ни одно из этих значений не совпало со значением фазового соотношения β = 250, рассчитанного на основании данных о параметрах колонок, сообщаемых производителями (β = dc/(4df)). Различие между найденными и рассчитанными значениями фазового соотношения β, особенно сильное в случае полярной стационарной фазы, может быть вызвано неправильной оценкой энергии сорбции нулевого члена гомологического ряда ΔGo, которая была фиксирована на значении 0, как это отмечено в предыдущем разделе. Чтобы оценить возможную величину этой энергии, мы провели аппроксимацию экспериментальных данных уравнением 8, фиксировав теперь величину фазового отношения β, равным 250. Оказалось, что подобная замена не оказывает влияния на величину мертвого времени tM и величину энтальпии сорбции метиленового звена $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$, но приводит к положительным значениям ΔGo, что не имеет физического смысла.
Чтобы проверить корреляцию величин фазового отношения β, находимых экстраполяцией, и величин, рассчитываемых из толщины пленки стационарной фазы, сообщаемой производителем, измерения были выполнены для неполярных колонок с толщиной пленки варьировавшейся от 0.25 до 2.0 мкм. Данные были скорректированы линейной экстраполяцией, как это описано выше (коррекция 1), и экспериментальные зависимости времени удерживания гомологов tR от числа атомов углерода n, в предположении ΔGo = = 0, были аппроксимированы уравнением (8). Найденные величины фазового соотношения β и величины свободной энергии сорбции метиленового звена $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$ приведены в табл. 4. Свободная энергия сорбции метиленового звена $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$ практически индифферентна к толщине пленки стационарной фазы, тогда как величина фазового отношения β уменьшается с ростом толщины пленки df, причем экспериментальная величина превосходит величину фазового отношения, рассчитываемую из толщины пленки стационарной фазы (табл. 4). Соотношение между экспериментально находимой и рассчитываемой величинами β линейно (рис. 6), но наклон линейной зависимости равен 1.6, что указывает на 60% превышение экспериментальных величин над рассчитанными. К сожалению, в нашем распоряжении не было колонок с разной толщиной пленки полярной стационарной фазы, и мы не могли проверить сохраняется ли такая же линейная корреляция и для полярных стационарных фаз.
Таблица 4.
Сравнение рассчитанных (β1) и экспериментально найденных (β2) величин фазового соотношения β и энергии сорбции метиленового звена $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$ для колонок с различной толщиной пленки стационарной фазы
| Kолонка | l, мкм | β1 | β2 | –$\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$, кДж/(мольК) |
|---|---|---|---|---|
| 1 | 0.25 | 250 | 390 ± 45 | 2.17 ± 0.05 |
| 3 | 0.5 | 125 | 205 ± 23 | 2.16 ± 0.05 |
| 5 | 1.0 | 62.5 | 102 ± 12 | 2.19 ± 0.05 |
| 6 | 2.0 | 31.25 | 36 ± 6 | 2.23 ± 0.05 |
Рис. 6.
Корреляция найденных и рассчитанных из толщины пленки стационарной фазы величин фазового отношения β для неполярных колонок (номера 1, 4–6 табл. 1).

В любом случае, проведенные эксперименты показали, что хроматографическое определение фазового отношения β колонки требует знания энергии сорбции нулевого члена гомологического ряда ΔGo, поскольку эти две величины взаимозависимы и не могут быть разделены аппроксимацией экспериментальных данных уравнением (8). Априорная фиксация ΔGo =0, хотя и кажется логичной, приводит к значениям β превышающим величины, находимые по толщине пленки стационарной фазы. Выяснение причин такого несоответствия будет продолжено в дальнейших исследованиях. В то же время мертвое время системы tМ и значение энергии сорбции метиленового звена гомологического ряда $\Delta {{G}_{{{\text{C}}{{{\text{H}}}_{{\text{2}}}}}}}$ надежно определяются экстраполяционным методом даже без знания “первичного” мертвого времени.
Работа выполнена в рамках Государственного задания ИНХС РАН
Список литературы
Wainwright M.S., Haken J.K. // J. Chromatogr. 1985. V. 334. P. 95.
Smith R.J., Haken J.K., Wainwright M.S. // Ibid. 1980. V. 184. P. 1.
Nahir T.M., Morales K.M. // Anal. Chem. 2000. V. 72. P. 4667.
Castello G., Moretti P., Vezzani S. // J. Chromatogr. A. 2009. V. 1216. P. 1607.
Набивач В.М., Дмитриков В.П. // Успехи химии. 1993. Т. 62. С. 7–38.
Vigh Gy., Varga-Puchony Z. // J. Chromatogr. 1980. V. 196. P. 1.
Krisnangkura K., Tancharoon A., Konkao C., Jeyashoke N. // J. Chromatogr. Sci. 1997. V. 35. P. 329.
Watanachaiyong T., Jeyashoke N., Krisnangkura K. // Ibid. 2000. V. 38. P. 67.
Ширяева В.Е., Попова Т.П., Канатьева А.Ю. и др. // Журн. физ. химии. 2019. Т. 93. № 11. С. 1731.
González F.R. // J. Chromatogr. A. 2004. V. 1037. P. 233.
Березкин В.Г. // Рос. хим. журн. 2003. Т. 47. С. 35.
Tremblay P., Savard M.M., Vermette J., Paquin R. // J. Membrane Sci. 2006. V. 282. P. 245.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии


