Журнал физической химии, 2020, T. 94, № 4, стр. 590-594
Гидратация и состояние кислородо-водородных групп в сложном оксиде BaLaIn0.9Nb0.1O4.1 со структурой раддлесдена–поппера
Н. А. Тарасова a, *, А. О. Галишева a, И. Е. Анимица a, Д. В. Корона a
a ьский федеральный университет им. Первого Президента России Б.Н. Ельцина
620002 Екатеринбург, Россия
* E-mail: Natalia.Tarasova@urfu.ru
Поступила в редакцию 06.05.2019
После доработки 03.06.2019
Принята к публикации 18.06.2019
Аннотация
Синтезированы соединения BaLaInO4 и BaLaIn0.9Nb0.1O4.1, характеризующиеся структурой Раддлесдена–Поппера. Доказана способность исследуемых фаз к гидратации. Показано, что допирование не приводит к изменению типа протонсодержащих частиц, единственная форма кислородно-водородных групп – три типа энергетически неэквивалентных гидроксогрупп. Установлено, что введение ниобия приводит к увеличению степени гидратации относительно недопированного состава за счет увеличения доли изолированных ОН–-групп, размещающихся в солевом блоке.
На сегодняшний день исследование и разработка новых керамических материалов с протонной проводимостью является актуальной задачей вследствие их возможного применения в качестве электролита протон-проводящих твердооксидных топливных элементов [1–5]. Наиболее известные протонные проводники – сложные оксиды со структурой перовскита или производной от нее [6]. Однако дальнейшее развитие протон-проводящих материалов предполагает исследование соединений с иным типом структуры.
Недавно появились сведения о проявлении ионного транспорта в соединениях со структурой Раддлесдена–Поппера [7–9]. Соединение BaNdInO4 было описано как смешанный кислородно-ионный проводник [7–9], допирование Nd- и In-подрешеток которого приводило к росту ионной проводимости [10, 11]. Было показано, что рост кислородно-ионной проводимости в случаях акцепторного допирования подрешетки Nd был обусловлен появлением в структуре вакансий кислорода:
(1)
${\text{2MO}}\;\xrightarrow{{{{{\text{B}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}}}}\;{\text{2M}}_{{\text{B}}}^{'} + 2{\text{O}}_{{\text{O}}}^{ \times } + V_{{\text{O}}}^{{ \bullet \bullet }}.$(2)
${\text{2M}}{{{\text{O}}}_{{\text{2}}}}\;\xrightarrow{{{{{\text{B}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}}}}\;{\text{2M}}_{{\text{B}}}^{ \bullet } + {\text{O}}_{i}^{{''}} + 3{\text{O}}_{{\text{O}}}^{ \times }{\text{.}}$Несмотря на то, что процессы транспорта ионов кислорода в системах на основе BaNdInO4 широко обсуждаются, возможность гидратации и соответственно протонный транспорт в данных фазах не исследован. Тем не менее, о наличии протонного переноса для фаз со структурой Раддлсдена–Поппера ранее сообщалось для оксифторидов Ba2InO3F и Ba3In2O5F2 [12], составов Pr1 – xM1 + xInO4 (M = Ba2+, Sr2+; x = 0, 0.1), характеризующихся структурой K2NiF4 [13], а также слоистых перовскитов Sr1 + xSm1 – xAlO4 – δ и Sr1 + xPr1 – xAlO4 – δ [14]. Ранее нами была показана принципиальная возможность протонного переноса в составах на основе BaLaInO4, в которых часть позиций La была замещена атомами Ca [15].
В настоящей работе изучена возможность проведения донорного допирования фазы BaLaInO4 в подрешетке In на атомы Nb, а также влияние допанта на процессы гидратации и состояние кислородно-водородных групп.
ЭКСПЕРИМЕНТАЛЬНЫАЯ ЧАСТЬ
Образцы BaLaInO4 и BaLaIn0.9Nb0.1O4.1 получали методом твердофазного синтеза из предварительно осушенных BaCO3, La2O3, In2O3, Nb2O5. Синтез проводили на воздухе при ступенчатом повышении температуры (800–1350°С) и многократных перетираниях в агатовой ступке в среде этилового спирта. Время отжига на каждой стадии составляло 24 ч.
Рентгенографический анализ выполняли на дифрактометре Bruker Advance D8 в СuKα-излучении при напряжении на трубке 40 кВ и токе 40 мА. Съемку производили в интервале 2θ = = 20°–80° с шагом 0.05° и экспозицией 1 с на точку. Расчеты параметров решетки проводили методом полнопрофильного анализа Ритвельда с помощью программы FullProf Suite.
Безводные образцы получали путем выдержки вещества при высоких температурах (1300°С) с последующим постепенным охлаждением в атмосфере сухого воздуха (${{р}_{{{{{\text{Н}}}_{{\text{2}}}}{\text{О}}}}}$ = 3.5 × 10–5 атм) и закалкой при 100–150°С. Гидратированные образцы получали путем медленного охлаждения от 1000 до 200°C со скоростью 1 К/мин в атмосфере влажного воздуха (${{р}_{{{{{\text{Н}}}_{{\text{2}}}}{\text{О}}}}}$ = 2 × 10–2 атм).
Парциальное давление паров воды задавали путем барботирования воздуха при комнатной температуре последовательно через реактив АСКАРИТ, содержащий твердую щелочь (для улавливания CO2), гранулированный хлорид кальция CaCl2 и порошок оксида фосфора P2O5 (${{р}_{{{{{\text{Н}}}_{{\text{2}}}}{\text{О}}}}}$ = 3.5 × × 10–5 атм); а также через 30%-ный раствор NаОН, дистиллированную воду и насыщенный раствор KBr (${{р}_{{{{{\text{Н}}}_{{\text{2}}}}{\text{О}}}}}$ = 2 × 10–2 атм).
Термический анализ предварительно гидратированных образцов проводили на приборе NETZSCH STA 409 PC в комплекте с квадрупольным масс-спектрометром QMS 403C Aëolos (NETZSCH), позволяющим одновременно выполнять термогравиметрические измерения (ТГ) и анализ отходящих газов (масс-спектрометрия МС) в интервале температур 25–1000°С и со скоростью нагрева 10 К/мин.
Для идентификации кислородно-водородных групп использовали метод ИК-спектроскопии. Исследования проводили на ИК-фурье-спектрометре Nicolet 6700 в диапазоне частот от 400 до 4000 см–1 методом диффузного отражения с использованием приставки Smart Diffuse Reflectance.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Методом рентгенофазового анализа было установлено, что образцы BaLaInO4 и BaLaIn0.9Nb0.1O4.1 однофазным и характеризуются орторомбической симметрией (пространственная группа Pbca). Значения параметров решетки, полученные для BaLaInO4, хорошо согласуются с описанными ранее [15]. Введение ниобия в In-подрешетку приводит к изменению объема элементарной ячейки (табл. 1). Объем элементарной ячейки увеличивается, несмотря на уменьшения ионного радиуса металла в катионной подрешетке [16]. Следует отметить, что это увеличение обусловлено увеличением параметров а и b; параметр с уменьшается при введении допанта. Данное увеличение параметров может быть объяснено введением межузельного кислорода в слои La–O, которое сопровождается расширением межслоевого пространства в плоскости (aOb) [17].
Таблица 1.
Параметры элементарных ячеек
| Образец | a, Å | b, Å | c, Å | β, град | Объем, Å3 |
|---|---|---|---|---|---|
| BaLaInO4 | 12.932(3) | 5.906(1) | 5.894(2) | 90 | 450.195(8) |
| BaLaIn0.9Nb0.1O4.1 | 12.961(8) | 5.938(5) | 5.878(5) | 90 | 452.709(5) |
| BaLaInO4 · nH2O | 12.683(6) | 14.708(1) | 7.169(9) | 92.81(9) | 1335(9) |
| BaLaIn0.9Nb0.1O4.1 · nH2O | 12.685(1) | 14.722(3) | 7.181(6) | 92.89(8) | 1339(4) |
Гидратация образцов BaLaInO4 и BaLaIn0.9Nb0.1O4.1 приводила к изменению их симметрии с орторомбической на моноклинную (P2/m). Как для безводных, так и для гидратированных образцов введение допанта приводило к увеличению объема элементарной ячейки. Рентгенограммы для безводного BaLaIn0.9Nb0.1O4.1 и гидратированного BaLaIn0.9Nb0.1O4.1 · nH2O представлены на рис. 1.
Рис. 1.
Рентгенограммы безводного BaLaIn0.9Nb0.1O4.1 (а) и гидратированного BaLaIn0.9Nb0.1O4.1 · nH2O (б) образцов. Показаны экспериментальные (точки), расчетные (линия), разностные (внизу) данные и угловые положения рефлексов (штрихи).

Исследование гидратированных форм исследуемых образцов выполняли с помощью спектроскопических и гравиметрических методов. Анализ форм кислородно-водородных групп проводили методом ИК-спектроскопии (рис. 2). В области деформационных колебаний (ниже 2000 см–1) регистрируется сигнал при 1420 см–1, принадлежащий деформационным колебаниям гидроксогрупп, связанных с атомами металла M–OH [18, 19]. Сигналов, относящихся к колебаниям молекулярной воды и катионам гидроксония (~1600 и ~1700 см–1) зарегистрировано не было.
Асимметричный вид широкой полосы в области валентных колебаний 2800–3600 см–1 свидетельствует о наложении нескольких сигналов, т.е. о наличии ОН–-групп с различным кристаллографическим положением и соответственно с различной степенью их участия в водородных связях. Четко прослеживается наличие трех полос. Полосы при 2800, (3200) и 3520 см–1 соответствуют ОН–-группам, вовлеченным в сильные и более слабые водородные связи соответственно. Узкая полоса с большей частотой (~3600 см–1) указывает на наличие изолированных ОН–-групп, т.е. введение ниобия в подрешетку индия приводит к уменьшению доли ОН–-групп, вовлеченных в сильные водородные связи и увеличению доли изолированных групп.
Появление в структуре гидратированных образцов ОН–-групп с различным кристаллографическим положением может быть описано в рамках квазихимического подхода следующим уравнением:
(3)
${\text{O}}_{{\text{o}}}^{{ \times }} + {{{\text{H}}}_{{\text{2}}}}{\text{O}} \Leftrightarrow {\text{(OH)}}_{{\text{o}}}^{ \bullet } + ({\text{OH)}}_{{\text{i}}}^{{\text{'}}}.$(4)
${\text{O}}_{{\text{i}}}^{{{\text{''}}}} + {{{\text{H}}}_{{\text{2}}}}{\text{O}} \Leftrightarrow 2({\text{OH)}}_{{\text{i}}}^{{\text{'}}}.$Таким образом, гидратированный Nb-замещенный образец BaLaIn0.9Nb0.1O4.1 · nH2O, как и недопированный состав BaLaInO4 · nH2O, содержит энергетически неравноценные ОН–-группы, что подтверждается наличием трех сигналов в области валентных колебаний. Введение допанта приводит к перераспределению вкладов от различных ОН–-групп. Новых форм кислородно-водородных групп при допировании не образуется.
Для определения количества поглощаемой воды из газовой фазы для предварительно гидратированных образцов BaLaInO4 · nH2O и BaLaIn0.9Nb0.1O4.1 · nH2O были проведены термические и масс-спектрометрические исследования. По убыли массы гидратированных составов была определена степень гидратации. Для удобства сравнения данные приведены в пересчете на число молей воды на формульную единицу сложного оксида (рис. 3). Совместно с ТГ-кривыми представлены результаты ДСК и масс-спектрометрии для BaLaIn0.9Nb0.1O4.1 · nH2O.
Рис. 3.
Данные термогравиметрии (ТГ) для образцов BaLaInO4 · nH2O (1) и BaLaIn0.9Nb0.1O4.1 · nH2O (2), а также данные и масс-спектрометрии для образца BaLaIn0.9Nb0.1O4.1 · nH2O (3).
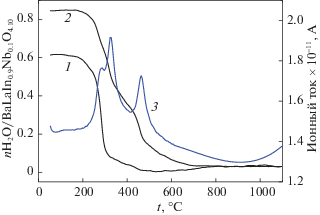
Основная потеря массы наблюдается в температурном интервале 200–700оС, что, согласно результатам масс-спектрометрического анализа, обусловлено выходом H2O. Выделения других возможных летучих веществ (СО2, О2) не было обнаружено, т.е. исследуемый в работе Nb-замещенный образец BaLaIn0.9Nb0.1O4.1, как и недопированный BaLaInO4, способен к поглощению воды из газовой фазы. Очевидно, способность к гидратации данных фаз обусловлена способностью к гидратации блоков La–O. Для блочных структур возможность поглощения паров воды вследствие гидратации солевых блоков, чередующихся с блоками перовскитной матрицы, была описана ранее для состава Ba2ZrO4 [20].
Введение допанта приводит к росту степени гидратации (~0.85 моль для BaLaIn0.9Nb0.1O4.1 и ~0.62 моль для BaLaInO4), что может быть обусловлено увеличением параметров a и b при введении допанта и увеличением межслоевого пространства.
Как для базового, так и для допированного образцов, процесс выделения воды происходит ступенчато, что соответствует трем сигналам на спектрометрической кривой. Основной сигнал на ТГ-кривых лежит в температурном интервале 200–350°C и включает две плохо разрешившиеся ступени. Данный сигнал соответствует наименее термически стойким ОН–-группам, т.е. группам, вовлеченным в сильные и слабые водородные связи. Как видно, основное различие в ТГ-кривых рассматриваемых в работе соединений проявляется в различии вкладов высокотемпературного эффекта (300–600°C), обусловленного наличием в структуре образцов наиболее термически стойких изолированных ОН–-групп. С ростом степени гидратации (т.е. при введении допанта) вклад высокотемпературного эффекта возрастает, в то время как основной эффект потери массы не претерпевает существенных изменений. Данные результаты хорошо коррелируют с результатами спектроскопических исследований, продемонстрировавшими увеличение доли изолированных ОН–-групп при допировании.
Таким образом, в работе осуществлен синтез соединений BaLaInO4 и BaLaIn0.9Nb0.1O4.1, характеризующихся структурой Раддлестена–Поппера, рентгенографически подтверждена их однофазность. Установлено, что введение ниобия приводит к увеличению объема элементарной ячейки. Доказана способность исследуемых фаз к диссоциативному поглощению воды из газовой фазы, сопровождающаяся появлением в структуре энергетически неэквивалентных ОН–-групп. Показано, что допирование In-подрешетки не приводит к изменению формы кислородно-водородных групп и обусловливает увеличение степени гидратации за счет увеличения доли изолированных ОН–-групп. Очевидно, такой тип допирования благоприятнен с точки зрения реализации протонного переноса.
Работа выполнена при финансовой поддержке гранта Президента РФ (проект МК-24.2019.3).
Список литературы
Shim J.H. // Nature Energy. 2018. V. 3. P. 168.
Fabbri E., Bi L., Pergolesi D., Traversa E. // Advanced Materials. 2012. V. 24. P. 195.
Marrony M., Dailly J. // ECS Transactions. 2017. V. 78. P. 3349.
Norby T. // ECS Transactions. 2017. V. 80. P. 23.
Colomban Ph., Zaafrani O., Slodczyk A. // Membranes. 2012. V. 2. P. 493.
Kochetova N., Animitsa I., Medvedev D., Demin A., Tsiakaras P. // RSC Advances. 2016. V. 6. P. 73222.
Fujii K., Shiraiwa M., Esaki Y. // J. Mater. Chem. A. 2015. V. 3. P. 11985.
Yang X., Liu S., Lu F., Xu J., Kuang X. // J. Phys. Chem. C. 2016. V. 120. P. 6416.
Shiraiwa M., Fujii K., Esaki Y., Kim S.J., Lee S., Yashima M. // J. Electrochem. Soc. 2017. V. 164. P. F1392.
Ishihara T., Yan Yu., Sakai T., Ida S. // Solid State Ionics. 2016. V. 288. P. 262.
Yang X., Liu S., Lu F., Xu J., Kuang X. // J. Phys. Chem. C. 2016. V. 120. P. 6416.
Tarasova N., Animitsa I. // Solid State Ionics. 2015. V. 275. P. 53.
Li X., Shimada H., Ihara M. // ECS Transactions. 2013. V. 50. P. 3.
Matsuhira T., Kurahashi Y., Hasegawa K., Ihara M. // Book of Abs. of 232nd ECS Meeting 2017, 1710.
Корона Д.В., Обрубова А.В., Козлюк А.О., Анимица И.Е. // Журн. физ. химии. 2018. Т. 92. С. 1439.
Shannon R.D. //Acta Crystallographica. 1976. V. A32. P. 155.
Aguadero A., Alonso J.A., Martínez-Lope M.J., Fernández-Díaz M.T., Escudero M.J., Daza L. // J. Mater. Chem. 2006. V. 16. P. 3402.
Юхневич Г.В. Инфракрасная спектроскопия воды. М.: Наука, 1973. 205 с.
Карякин А.В., Кривенцова Г.А. Состояние воды в органических и неорганических соединениях. М.: Наука, 1973. 176 с.
Шпанченко Р.В., Антипов Е.В., Ковба Л.М. // Журн. неорган. химии. 1993. Т. 38. С. 599.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии



