Физика металлов и металловедение, 2021, T. 122, № 10, стр. 1075-1082
Особенности микроструктуры и поведение при коррозии высокоэнтропийных сплавов Al0.5FeCrNiTi0.25 – xSix
А. Ибрахим a, М. Али b, *, М. А. Сиддики b, c, М. Шакеель d, В. Ахмад d, С. Джамеель d, С. Хайат d, М. Дж. Афзал d, А. С. Шейх d, М. А. Имам d, М. А. Аршад d
a Кафедра металлургии и материаловедения, Факультет химической,
металлургической и полимерной инженерии, Иженерно-технологический университет,
Grand Trunk Road (“Великий Колесный Путь”)
54890 пров. Пенджаб, Лахор, Пакистан
b Институт материаловедения, Научно-технический университет Китая
230026 пров. Аньхой, Хэфэй,
ул. Цзиньчжай, 96, Китайская Народная Республика
c Кафедра металлургии, Химико-технологический факультет, Иженерно-технологический
университет им. Н.Э. Диншоу, Университетская Road
75270 пров. Синд, Карачи, Пакистан
d Институт перспективных материалов, Университет Бахауддина Закарии
60800 пров. Пенджаб, Мултан, Пакистан
* E-mail: ali1@mail.ustc.edu.cn
Поступила в редакцию 31.12.2020
После доработки 23.03.2021
Принята к публикации 17.06.2021
Аннотация
Разработаны новые высокоэнтропийные композиции сплавов с одинаковой концентрацией валентных электронов (Al0.5FeCrNiTi0.25 –xSix), и с молярным отношением x = 0.09, 0.125 и 0.25. Микроструктуру и коррозионное поведение исследовали с помощью рентгеновской дифракции, сканирующей электронной микроскопии и электрохимических исследований в 3.5 вес. %-ном растворе NaCl при комнатной температуре. Увеличение молярного отношения x в сплавах Al0.5FeCrNiTi0.25 – xSix стабилизировало гранецентрированную кубическую фазу. Среди изученных композиций, сплав Al0.5FeCrNiTi0.12Si0.12 обладал хорошей коррозионной стойкостью, проявляя наименьшую плотность коррозионного тока Icorr, самое высокое сопротивление переносу заряда Rct (RПЗ) с емкостным значением Cdl (CДС) двойного слоя и самым низким коэффициентом Варбурга (σ).
ВВЕДЕНИЕ
После публикации пионерских работ [1, 2] были изучены сотни высокоэнтропийных сплавов (ВЭС), обнаружены перспективные для применения механические и коррозионные характеристики [3], а также необъяснимые свойства, поставившие перед исследователями ряд фундаментальных вопросов [4–9]. Ключевая концепция, лежавшая в основе целесообразности создания ВЭС, состояла в том, чтобы способствовать образованию в них неупорядоченного твердого раствора благодаря максимальному значению конфигурационной энтропии системы. Вместе с тем конфигурационная энтропия не всегда является единственным фактором, определяющим выделение равновесных фаз. Равновесие между твердыми растворами и упорядоченными интерметаллидами определяется энтропией и энтальпией смешения как твердых растворов, так и интерметаллидов, как обсуждалось Рогачевым [4]. В более чем четырехстах ВЭС были идентифицированы двадцать три кристаллические фазы, принадлежащие к кристаллографическим ОЦК-, ГЦК и ГПУ-классам симметрии, как отмечено Miracle и Сенковым в [10]. Среди них наиболее распространенными фазами (в порядке убывания) являются: неупорядоченная ГЦК-фаза, ОЦК фаза, упорядоченная интерметаллическая фаза B2, σ‑фаза и гексагональная фаза Лавеса C14. В предыдущем исследовании сплав AlCoCrFeNiTix был модифицирован путем удаления Co и снижения содержания Ti (т.е. AlxCrFeNiTi0.25, где индексы показывают молярное соотношение) с целью снижения себестоимости ВЭС и предотвращения образования в нем фаз Лавеса соответственно [11, 12]. Эта работа была направлена на замену Ti на Si в сплаве AlxCrFeNiTi0.25, без изменения концентрации валентных электронов (КВЭ) сплава. Затем было исследовано влияние комбинаций Ti0.25 –xSix на микроструктуру и коррозионную стойкость сплавов Al0.5FeCrNiTi0.25 – xSix. КВЭ была рассчитана как средневзвешенное значение компонентов сплава, т. е., КВЭ = $\sum\nolimits_{i = 1}^n {{{c}_{i}}} $ × (КВЭ)i; где ci и (КВЭ)i представляют концентрацию и КВЭ отдельных элементов соответственно.
МЕТОДИКА ЭКСПЕРИМЕНТА
Разработка сплавов и микроструктурные исследования
Три слитка ВЭС с номинальным составом Al0.5FeCrNiTi0.25 –xSix (где молярное соотношение x принимало значения x = 0.09, 0.125 и 0.25, причем, полученные образцы были обозначены как Сплавы Si0.09, Si0.125 и Si0.25 соответственно) были получены электродуговой плавкой составляющих химических элементов чистотой 99.99 вес. % или выше в атмосфере аргона (Ar). Свежелитые слитки гомогенизировали при температуре 1150°C в течение 70 ч в трехзонной вакуумной муфельной печи марки Nabertherm-RS-50/500/A3 в атмосфере Ar (при скорости потока ${{v}_{{{\text{Ar}}}}}$ = 1.6 л/ч). Кристаллическую структуру полученных образцов определяли методом рентгеноструктурного анализа с использованием дифрактометра марки Bruker D-8 Advance с излучением Cu-Kα в диапазоне 2θ = 20°–100°. Микроструктурные наблюдения проводили на растровом электронном микроскопе (РЭМ) MIRA3 TESCAN после стандартной металлографической подготовки и травления образцов в растворе HNO3 : HCl : H2O (в объемном соотношении 3 : 2 : 1).
Электрохимические исследования
Электрохимическое коррозионное поведение образцов ВЭС исследовали с помощью потенциостата марки Gamry Reference 3000TM в 3.5 вес. % растворе NaCl (при доступе воздуха). Электрохимические анализы проводили с использованием стандартной трехэлектродной ячейки с графитовым стержнем в качестве вспомогательного электрода и Ag/AgCl электродом сравнения. Каждый образец диаметром 10 мм и толщиной 10 мм с припаянной к его задней стенке медной проволокой был смонтирован с фиксацией эпоксидной смолой и использовался в качестве рабочего электрода. Значения всех потенциалов устанавливались с “привязкой” к Ag/AgCl электроду. Перед испытаниями применяли стандартный метод подготовки поверхности. Электрический потенциал на “питающей” клемме при разомкнутой цепи VПРЦ контролировали в течение 1800 с, чтобы обеспечить относительно стабильное состояние системы. Потенциодинамические тесты проводили от значений –1 VПРЦ до +1 VПРЦ со скоростью сканирования 1 мВ/с. Спектроскопию электрохимического импеданса (СЭИ) проводили в диапазоне частот от 100 кГц до 1 Гц, с шагом по частоте, равным 10 значениям на единицу значения десятичного логарифма частоты в Гц.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Микроструктура
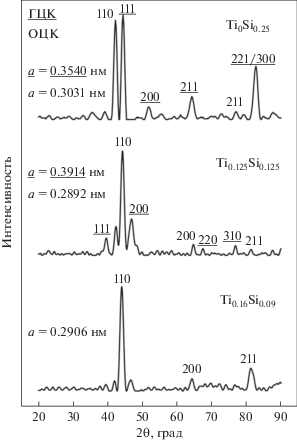
На рис. 1 показаны рентгенограммы для трех сплавов, а также оцененный параметр решетки каждой фазы. Незначительные по величине неидентифицированные пики естественно не индексировали. Сплав Si0.09 в основном состоял из неупорядоченной ОЦК-фазы, обычно называемой фазой со структурой А2 [11]. Образцы с более высоким содержанием Si (Si0.125 и Si0.25) представляли собой двухфазные сплавы, содержащие неупорядоченную ОЦК-фазу (присутствовали только фундаментальные отражения) и упорядоченную ГЦК-фазу (присутствовали как фундаментальные, так и сверхструктурные отражения). Параметр решетки ОЦК-фазы в сплавах Si0.09 и Si0.125 был примерно одинаковым, однако в сплаве Si0.25 его значение было больше. В случае ГЦК-фазы параметр решетки значительно отличается в сплавах Si0.125 и Si0.25. Используя концепцию, лежащую в основе метода отношения эталонной интенсивности, увеличение доли ГЦК-фазы с очевидностью наблюдается при росте содержания Si. Этот эффект далее иллюстрируется наряду с описанием РЭМ-изображений структуры сплавов.
Рис. 1.
Рентгенограммы сплавов Si0.09, Si0.125 и Si0.25 с данными по параметрам решетки (ГЦК фазу можно рассматривать как примитивную кубическую из-за наличия так называемых сверхструктурных отражений). Подчеркнутые значения параметров решетки и индексов Миллера дифракционных линий относятся к ГЦК фазе.
Из рис. 2 ясно, что в микроструктуре каждого сплава присутствует две фазы: непрерывная (яркая область на РЭМ-изображении) и прерывистая (темная область на РЭМ-изображении). Элементный состав, отвечающий темным и светлым областям, оцененный с помощью РЭМ-ЭДС метода (энерго-дисперсионной спектроскопии), приведен в табл. 1. В сплаве с наименьшим содержанием Si (Si0.09) сегрегация Ti в матрице привела к образованию богатой Ti вторичной фазы, с очень малой объемной долей (темная область). Объемная доля этой фазы была слишком мала, чтобы привести к появлению пиков заметной интенсивности на рентгеновских дифрактограммах. Это означало, что ОЦК-фаза, идентифицированная на соответствующих рентгенограммах, принадлежала основной фазе (рис. 2а). Уменьшение содержания Ti (и увеличение содержания Si) повлияло на относительную растворимость химических компонентов сплава, и микроструктуры содержали две составляющие фазы, что также видно из соответствующих рентгенограмм. Рентгенограмма образца Si0.125 (рис. 1) показывает, что объемная доля ГЦК фазы была меньше, чем доля ОЦК-фазы. Следовательно, о фазе малой объемной доли (темная область) на рис. 2б можно говорить, как о ГЦК-структуре, исключительно богатой Fe и Cr. Дальнейшее увеличение содержания Si с 0.125 до 0.25 увеличило объемную долю ГЦК-фазы с 38 до 50%. Это означало, что прерывистая фаза (темная область) на рис. 2в была ГЦК-фазой, и она также была богата Fe и Cr.
Рис. 2.
РЭМ-изображения микроструктуры сплавов (а) Al0.5FeCrNiTi0.16Si0.09, (б) Al0.5FeCrNiTi0.125Si0.125 и (в) Al0.5FeCrNiSi0.25.

Таблица 1.
Оценка величины объемной доли и элементный состав двух фаз в сплавах Al0.5FeCrNiTi0.25 –xSix, по данным РЭМ-ЭДС анализа
| Сплав | Область | Объемная доля | Al | Fe | Cr | Ni | Ti | Si |
|---|---|---|---|---|---|---|---|---|
| Al0.5FeCrNiTi0.16Si0.09 | Номинально | 13.3 | 26.6 | 26.6 | 26.6 | 4.2 | 2.4 | |
| светлая | 12.0 | 25.4 | 27.9 | 28.6 | 3.3 | 2.5 | ||
| темная | 1.9 | 18.5 | 24.7 | 5.8 | 46.9 | 1.9 | ||
| Al0.5FeCrNiTi0.125Si0.125 | Номинально | 13.3 | 26.6 | 26.6 | 26.6 | 3.3 | 3.3 | |
| светлая | 62% | 24.1 | 13.3 | 6.8 | 46.2 | 7.8 | 1.6 | |
| темная | 38% | 11.2 | 26.5 | 28.0 | 26.7 | 4.1 | 3.2 | |
| Al0.5FeCrNiSi0.25 | Номинально | 13.3 | 26.6 | 26.6 | 26.6 | 0 | 6.6 | |
| светлая | 49% | 24.3 | 17.5 | 12.6 | 42.4 | 0 | 3.0 | |
| темная | 51% | 5.0 | 33.3 | 36.3 | 18.9 | 0 | 6.2 |
Стабильность фазы обычно обсуждается на основе соображений о концентрации валентных электронов. Ожидается [9], что при КВЭ ≥ 8 должна наблюдаться одиночная ГЦК фаза, при КВЭ ≤ 6.87 – одиночная ОЦК фаза, а в промежуточной области должна быть стабильна двухфазная (ГЦК + ОЦК) микроструктура. Поскольку в настоящей работе КВЭ в изучаемых ВЭС была зафиксирована на уровне 7.0, можно сделать вывод, что только КВЭ не может означать стабильность ГЦК или ОЦК фаз.
Электрохимические исследования
Коррозионные свойства с точки зрения плотности коррозионного тока (Iкор) и коррозионного потенциала (Eкор) изучали с помощью потенциодинамического (ПД) анализа, в то время как сопротивление переносу заряда (RПЗ) и емкость двойного слоя (CДС) изучали с помощью электрохимического анализа импеданса. На рис.3а показаны ПД кривые, полученные по результатам электрохимических исследований поведения трех образцов в 3.5-вес. % растворе NaCl. Из-за электрохимических реакций (в полу-ячейке), соответствующая катодная ветвь для каждого сплава двигалась в сторону большей отрицательной плотности тока, что соответственно влияло на его анодную ветвь. Увеличение содержания Si (и уменьшение содержания Ti) первоначально привело к увеличению отрицательных значений Eкор: со значения –562 мВ для сплава Si0.09 до значения –786 мВ для сплава Si0.125 (см. табл. 2). Для тех же сплавов значение Iкор увеличилось с 1.5 × 10–6 до 2.1 × 10–6 А/см2 (см. табл. 2). Дальнейшее увеличение числа атомов Si и удаление Ti (сплав Si0.25) уменьшило значения Eкор до ‒595 мВ и Iкор до 1.3 × 10–6 А/см2. Эти значения Iкор показали ту же величину плотности электрического тока (в мкА/см2), которая наблюдалась в других исследованиях по ВЭС сплавам [7, 8].
Таблица 2.
Значения плотности электрического тока коррозии (Iкор) и потенциала коррозии (Eкор) ВЭС в 3.5-вес. % растворе NaCl, полученные при обработке данных по ПД поляризации
| Сплав | Iкор, A/cм2 | Eкор, мВ |
|---|---|---|
| Al0.5CrFeNiTi0.16Si0.09 | 1.5 × 10–6 | –562 |
| Al0.5CrFeNiTi0.125Si0.125 | 2.1 × 10–6 | –786 |
| 0.72 × 10–6 | –597 | |
| Al0.5CrFeNiSi0.25 | 1.3 × 10–6 | –595 |
Рис. 3.
(а) Кривые потенциодинамической (ПД) поляризации сплавов Al0.5FeCrNiTi0.16Si0.09, Al0.5FeCrNiTi0.125Si0.125 и Al0.5FeCrNiSi0.25 и (б) та же ПД кривая сплава Al0.5FeCrNiTi0.125Si0.125, показывающая “вторые” значения Eкор и Iкор.
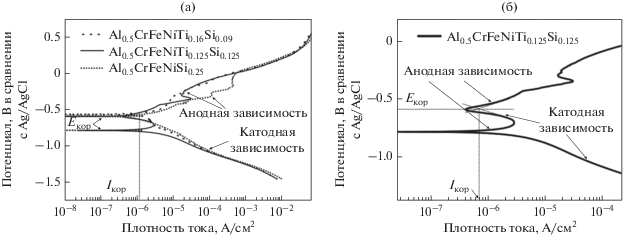
Кроме того, в сплаве Si0.125 дальнейшее увеличение потенциала коррозии уменьшало ток, и, следовательно, наблюдались также вторые значения Iкор и Eкор, как показано на рис. 3б. Значения Eкор сплава Si0.125 и сплава Si0.25 стали одинаковыми (т.е., ~–595 мВ). Однако самое низкое значение Iкор (т.е., 0.72 × 10–6 А/см2) показывает высокую коррозионную стойкость сплава Si0.125 в исследуемом водном растворе (3.5 вес. % NaCl). Подобная тенденция коррозионной стойкости также может быть объяснена с точки зрения высокого сопротивления переносу заряда (RПЗ) и емкости двойного слоя (CДС), как это наблюдается в СЭИ анализе и обсуждается ниже.
На рис. 4а показаны кривые Найквиста для трех образцов, полученные по результатам испытания этих образцов в 3.5 вес. % растворе NaCl. Каждый график Найквиста имеет вид полуокружностей с центром, лежащим ниже оси x, во всем диапазоне частот. Такая конфигурация кривых описывает типичную особенность, характерную для пассивирующих пленок, разработанных для металлических материалов, таких как сплавы на основе Fe [13], и сплавы на основе Ti [14]. Описанная особенность – протяженная по масштабу немонотонность на годографе Найквиста (большая полуокружность) – наблюдалась для сплава Si0.125, что свидетельствовало о высоком межфазном сопротивлении переносу заряда (RПЗ). С другой стороны, меньшие полуокружности для других образцов отвечали более низкому межфазному RПЗ, что свидетельствовало о более высокой электропроводности образцов этих композиций. Высокая электропроводность поддерживает свободный поток электронов на границе раздела электрод–электролит [15], что указывает на более низкую стойкость к электрохимической коррозии.
Диаграммы Боде представлены на рис. 4б. В диапазоне низких и средних частот график величины Боде каждого сплава демонстрировал линейную зависимость с наклоном –0.46, –0.42 и –0.45 для сплавов Si0.09, Si0.125 и Si0.25, соответственно (а не знакомый наклон “минус один” связан с простой RC-электрической схемой), в то время как значения фазового угла приближались к значениям от 15° до 20°. В высокочастотной области линии стали (как минимум) горизонтальными, а фазовый угол приблизился к 0°. Это характерный отклик емкостного поведения при высокой частоте с импедансом Варбурга (Zw) при переходе на более низкую частоту. Для интерпретации электрохимического отклика соответствующие данные были смоделированы с помощью электрической эквивалентной схемы, показанной на рис.4в. Эта модель-схема состоит, с одной стороны, из емкости ZCPE(o) и сопротивления Ro внешней оксидной пленки, а также емкости ZCPE(i) и сопротивления Ri внутренней (барьерной) оксидной пленки и, с другой стороны, из диффузионных процессов, представленных импедансом Варбурга (Zw), и “включенного последовательно” сопротивления (Rs) 3.5-вес. % раствора NaCl, что было хорошо согласуется с экспериментальными данными. Величина сопротивлений Ro и Ri складывалась из значений сопротивления переносу заряда (RПЗ) через пассивирующий слой. В свою очередь, ZCPE(o) и ZCPE(i) связаны с величинами емкостного сопротивления двухслойной пассивирующей пленки CДС [16, 17]. Вместо емкостного сопротивления использовался элемент с постоянным сдвигом по фазе (CPE) в степени n для учета неидеального поведения емкостных элементов, из-за различных неоднородностей поверхности, таких как локальные неоднородности заряда, многофазные области, дислокации, границы зерен, шероховатость поверхности, примеси, адсорбированные частицы, изменения состава и стехиометрии и т.д. [10, 18]. Импеданс CPE был представлен ZCPE = (1/Y(o)) (i ω)–n [13]; здесь ZCPE – импеданс CPE, Y(o) – постоянный параметр CPE (Ом–1 см2 с–n), i – мнимая единица (i 2 = –1), угловая частота ω (рад с–1), и, обычно, 0 < n < 1 (n = 1 означает, что CPE эквивалентен емкости “чистого” конденсатора). Импеданс Варбурга был рассчитан в терминах коэффициента Варбурга (σ), который рассчитывается по формуле $\sigma = 1{\text{/}}\sqrt {2({\text{Y}}^\circ )} ;$ где Y(o) – постоянный параметр Варбурга, рассчитанный на основе подгонки экспериментальных данных. В табл. 3 приведены параметры эквивалентной электрической схемы для трех сплавов, полученные путем подгонки экспериментальных данных по импедансу. Сопротивление внутреннего барьерного слоя во всех сплавах выше, чем сопротивление внешнего слоя пассивирующей оксидной пленки. Это указывает на то, что коррозионная стойкость сплавов была обеспечена “дуплексной” пассивирующей пленкой, которая связана с внутренним барьерным слоем. Аналогично, во всех исследованных сплавах значения емкости внутреннего слоя выше, чем внешнего слоя. Надо отметить, что оба слоя во всех образцах демонстрировали менее выраженное (чем у простого конденсатора) емкостное поведение (0.75 < n < 0.80) [19]. В целом, подобранная электрическая “эквивалентная” схема подразумевала, что величины сопротивления переносу заряда (связанные с Ro и Ri) и емкости ZCPE(o) и ZCPE(i) сплава Si0.125 показали самые высокие значения, указывающие на хорошую коррозионную стойкость. Было получено хорошее согласие между экспериментом и подгонкой для всех условий с приемлемой добротностью подгонки, о чем свидетельствуют низкие значения χ-квадрата (10–3).
Рис. 4.
Спектры импеданса для сплавов Al0.5FeCrNiTi0.16Si0.09, Al0.5FeCrNiTi0.125Si0.125 и Al0.5FeCrNiSi0.25. (а) График Найквиста, (б) диаграмма Боде, (в) эквивалентная электрическая схема.
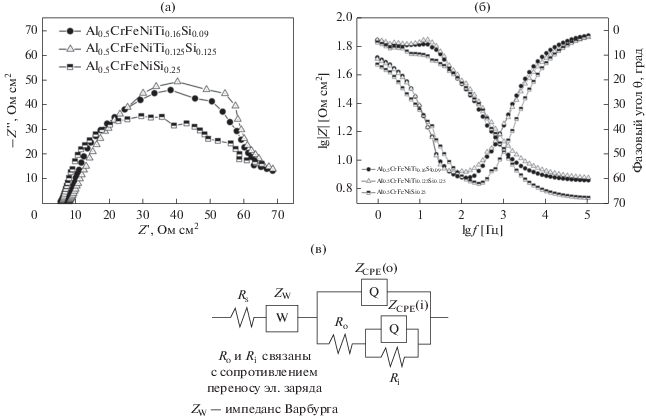
Таблица 3.
Параметры эквивалентной электрической схемы исследуемых высокоэнтропийных сплавов (в 3.5 вес. % растворе NaCl)
| Параметры | Al0.5FeCrNiTi0.16Si0.09 | Al0.5FeCrNiTi0.125Si0.125 | Al0.5FeCrNiSi0.25 |
|---|---|---|---|
| Rs, Ом см2 | 0.02 (±xy) | 0.05 (±xy) | 1.86 (±xy) |
| σ, коэффициент Варбурга | 216.47 (±xy) | 192.08 (±xy) | 223.04 (±xy) |
| Ro, внешний слой, Ом см2 | 7.28 (±xy) | 7.79 (±xy) | 3.40 (±xy) |
| Ri, внутренний слой, Ом см2 | 78.42 (±xy) | 83.72 (±xy) | 69.18 (±xy) |
| ZCPE(o), внешний слой, мФ см–2 | 4.39 (±xy) | 4.67 (±xy) | 3.72 (±xy) |
| ZCPE(i), внутренний слой, мкФ см–2 | 44.37 (±xy) | 44.79 (±xy) | 35.88 (±xy) |
| n1, внешний слой | 0.76 | 0.77 | 0.75 |
| n2, внутренний слой | 0.77 | 0.80 | 0.78 |
| χ2 | 5.1 × 10–3 | 6.1 × 10–3 | 7.5 × 10–3 |
Как видно из рис. 3а и 4в, формирование пассивирующей пленки (ее внутреннего и внешнего слоев) определяется влиянием химических элементов, входящих в состав сплавов, на электрохимические реакции. На основе теории пассивации можно выдвинуть гипотезу о том, что наиболее электрохимически активный элемент в сплаве образует внутренний (барьерный) слой и обычно, но не всегда, предпочтительно окисляется на границе раздела металл/барьерный слой по сравнению с менее активным элементом. Согласно стандартным значениям электродного потенциала, сплавы, изученные в этой работе, могли подвергнуться серии электрохимических окислительно-восстановительных “цепных” реакций с образованием оксидов Ti, Al, Cr, Fe, Ni и Si в 3.5-вес. % водном растворе NaCl. Аналогичное исследование сплава AlCoCrFeNiTix показало сложную природу пассивирующей пленки, в которой внешний слой содержал только TiO2, Ti2O3, Al2O3 Cr2O3 и Cr(OH)3, как было установлено по результатам анализа данных рентгеновской фотоэмиссионной спектроскопии (РФС) [12]. Ni в указанном сплаве образовывал интерметаллидные соединения Ni2Ti и NiTi, что препятствовало образованию на поверхности сплава слоя TiO2, тем самым снижая коррозионную стойкость сплава [20]. При подобных электрохимических условиях исключено, что Si (в отличии от Ti) способен образовывать SiO2; поэтому Si может присутствовать в междоузлиях тех участков материала, где локализованы интерметаллидные или оксидные фазы [7, 14].
ЗАКЛЮЧЕНИЕ
В работе установлено влияние относительной доли Ti и Si на микроструктуру и коррозионные свойства сплавов Al0.5FeCrNiTi0.25 –xSix. Увеличение молярного отношения Si с 0.09 до 0.25 способствовало формированию ГЦК-фазы. Потенциодинамические тесты и электрохимическая спектроскопия импеданса показали, что сплав Al0.5FeCrNiTi0.125Si0.125 в 3.5-вес. % растворе NaCl продемонстрировал наименьшую плотность тока коррозии (Iкор), наибольшие значения сопротивления переносу заряда (RПЗ) и емкости CДС дуплексной оксидной пленки и наименьшее значение постоянной Варбурга (σ).
Список литературы
Cantor B., Chang I.T.H., Knight P., Vincent A.J.B. Microstructural development in equiatomic multicomponent alloys // Mater. Sci. Eng. A. 2004. V. 375–377. P. 213–218.
Yeh J.-W., Chen S.-K., Lin S.-J., Gan J.-Y., Chin T.-S., Shun T.-T., Tsau C.-H., Chang S.-Y. Nanostructured High-Entropy Alloys with Multiple Principal Elements: Novel Alloy Design Concepts and Outcomes // Adv. Eng. Mater. 2004. V. 6. P. 299–303.
Senkov O.N., Woodward C., Miracle D.B. Microstructure and Properties of Aluminum-Containing Refractory High-Entropy Alloys // JOM 2014. V. 66. P. 2030–2042.
Rogachev A.S. Structure, Stability, and Properties of High-Entropy Alloys // Phys. Met. Metall. 2020. V. 121. P. 733–764.
Gorban V.F., Krapivka N.A., Firstov S.A., Kurilenko D.V. Role of Various Parameters in the Formation of the Physicomechanical Properties of High-Entropy Alloys with BCC Lattices // Phys. Met. Metall. 2018. V. 119. P. 477–481.
Ivchenko M.V., Pushin V.G., Uksusnikov A.N., Wanderka N. Microstructure features of high-entropy equiatomic cast AlCrFeCoNiCu alloys // Phys. Met. Metall. 2013. V. 114. P. 514–520.
Gorban’ V.F., Krapivka N.A., Firstov S.A. High-entropy alloys: Interrelations between electron concentration, phase composition, lattice parameter, and properties // Phys. Met. Metall. 2017. V. 118. P. 970–981.
Gorbachev I.I., Popov V.V, Katz-Demyanetz A., Popov V., Eshed E. Prediction of the Phase Composition of High-Entropy Alloys Based on Cr–Nb–Ti–V–Zr Using the Calphad Method // Phys. Met. Metall. 2019. V. 120. P. 378–386.
Guo S., Ng C., Lu J., Liu C.T. Effect of valence electron concentration on stability of fcc or bcc phase in high entropy alloys // J. Appl. Phys. 2011. V. 109. P. 103505
Miracle D.B., Senkov O.N. A critical review of high entropy alloys and related concepts // Acta Mater. 2017. V. 122. P. 448–511.
Liu S., Gao M.C., Liaw P.K., Zhang Y. Microstructures and mechanical properties of AlxCrFeNiTi0.25 alloys // J. Alloys Compd. 2015. V. 619. P. 610–615.
Liu J., Liu H., Chen P., Hao J. Microstructural characterization and corrosion behaviour of AlCoCrFeNiTix high-entropy alloy coatings fabricated by laser cladding // Surf. Coatings Technol. 2019. V. 361. P. 63–74.
Jiang R., Wang Y., Wen X., Chen C., Zhao J. Effect of time on the characteristics of passive film formed on stainless steel // Appl. Surf. Sci. 2017. V. 412. P. 214–222.
Munirathinam B., Narayanan R., Neelakantan L. Electrochemical and semiconducting properties of thin passive film formed on titanium in chloride medium at various pH conditions // Thin Solid Films. 2016. V. 598. P. 260–270.
Martha S., Mansingh S., Parida K.M., Thirumurugan A. Exfoliated metal free homojunction photocatalyst prepared by a biomediated route for enhanced hydrogen evolution and Rhodamine B degradation // Mater. Chem. Front. 2017. V. 1. P. 1641–1653.
Souza M.E.P., Lima L., Lima C.R.P., Zavaglia C.A.C., Freire C.M.A. Effects of pH on the electrochemical behaviour of titanium alloys for implant applications // J. Mater. Sci. Mater. Med. 2009. V. 20. P. 549–552.
Navarro Laboulais J., Amigó Mata A., Amigó Borrás V., Igual Muñoz A. Electrochemical characterization and passivation behaviour of new beta-titanium alloys (Ti35Nb10Ta–xFe) // Electrochim. Acta. 2017. V. 227. P. 410–418.
Shi Y., Yang B., Xie X., Brechtl J., Dahmen K.A., Liaw P.K. Corrosion of Al xCoCrFeNi high-entropy alloys: Al-content and potential scan-rate dependent pitting behavior // Corros. Sci. 2017. V. 119. P. 33–45.
Robin A., Carvalho O.A.S., Schneider S.G., Schneider S. Corrosion behavior of Ti–xNb–13Zr alloys in Ringer’s solution // Mater. Corros. 2008. V. 59. P. 929–933.
Ohtsu N., Masahashi N., Mizukoshi Y. Angle resolved XPS studies on an anodic oxide formed on Ti–Nb–Sn alloy and the photo-induced change in carbon contaminants adsorbed on its surface // Appl. Surf. Sci. 2012. V. 258. P. 6052–6055.
Дополнительные материалы отсутствуют.
Инструменты
Физика металлов и металловедение


