Химическая физика, 2020, T. 39, № 12, стр. 74-80
Новый подход к анализу инициированной термодеструкции поликарбоната
А. В. Куценова 1, *, В. Б. Иванов 1, О. Е. Родионова 1, А. Л. Померанцев 1
1 Федеральный исследовательский центр химической физики им. Н.Н. Семёнова
Российской академии наук
Москва, Россия
* E-mail: ivb@chph.ras.ru
Поступила в редакцию 22.11.2019
После доработки 25.03.2020
Принята к публикации 20.04.2020
Аннотация
Методом динамического термогравиметрического анализа установлено, что диметилдитиокарбамат висмута, защищающий ряд полимеров от действия тепла и света, ускоряет термодеструкцию поликарбоната на основе бисфенола А и является в данном случае инициатором. Методом нелинейного регрессионного анализа проведено моделирование кинетики многостадийного процесса инициированной термодеструкции поликарбоната. Особенность предложенного подхода заключается в оценке параметров уравнения Аррениуса для каждой из стадий совместно при всех температурных программах. Показано, что такой анализ позволяет избежать ограничений, характерных для методов Kissinger и Kissinger–Akahira–Sunose, традиционно используемых для определения энергий активации термодеструкции полимеров.
ВВЕДЕНИЕ
Поликарбонат (ПК) на основе бисфенола А, благодаря хорошим термическим и механическим свойствам, является одним из широко используемых в технике конструкционных полимеров. Поликарбонат и пленки из него используют также и как замедлители горения (антипирены).
Механизм термодеструкции ПК на воздухе и в атмосфере азота рассмотрен в работах [1, 2] и цитируемых в них публикациях. В основном, авторы изучали образование продуктов как функцию потери массы. На начальной стадии при температурах ниже 310 °С основную роль играет процесс окисления, который сопровождается отщеплением водорода от изопропилиденовой связи и дальнейшим разрывом углерод–углеродной связи. Окисление является прелюдией к более поздней стадии термической деструкции. Однако чисто термическая деструкция может иметь место при повышенных температурах и независимо от окисления. В области более высоких температур (450–560 °С) деструкция протекает по закону случая. Основной реакцией является разрыв сложноэфирных связей с выделением диоксида углерода. Однако изучению кинетики процесса термодеструкции не уделено достаточного внимания.
Простым и надежным методом, позволяющим оценить термостойкость различных полимеров и полимерных композиций, а также получить информацию о кинетике и механизме процессов термодеструкции и, в частности, определить энергию активации процесса, является термогравиметрический анализ (ТГА) [3–10]. Самое общее описание одностадийного процесса термодеструкции в динамическом режиме ТГА имеет вид
где α – конверсия, определяемая выражением
(2)
$\alpha = {{({{m}_{{\text{0}}}}--m)} \mathord{\left/ {\vphantom {{({{m}_{{\text{0}}}}--m)} {({{m}_{{\text{0}}}}--{{m}_{\infty }})}}} \right. \kern-0em} {({{m}_{{\text{0}}}}--{{m}_{\infty }})}},$где m0, m, m∞ – начальная, текущая и конечная масса образца соответственно, k(T) – константа скорости процесса, f(α) – кинетическая функция, зависящая от конкретного механизма деградации. В литературе [11, 12] приведена классификация основных функций, используемых для описания термических процессов в твердой фазе, так называемых идеальные реакционные модели. Зависимость константы скорости от температуры обычно описывается уравнением Аррениуса:
где А – предэкспоненциальный фактор, Е – энергия активации, R – газовая постоянная, Т – абсолютная температура. Наиболее распространенной неизотермической программой изменения температуры со временем является линейное изменение Т, так что скорость нагрева β = dT/dt = const. В случае, когда процесс термодеструкции включает в себя несколько параллельных стадий, выражение для скорости изменения конверсии имеет вид
(4)
${{d\alpha } \mathord{\left/ {\vphantom {{d\alpha } {dt}}} \right. \kern-0em} {dt}} = \sum\limits_{i = 1}^j {{{b}_{i}}_{~}{{A}_{i}}{\text{exp}}({{ - {{E}_{i}}} \mathord{\left/ {\vphantom {{ - {{E}_{i}}} {RT}}} \right. \kern-0em} {RT}})f({{\alpha }_{i}})} ,~$где индекс i относится к i-той стадии, j – число стадий, bi – весовой коэффициент, представляющий долю стадии в общем процессе деструкции, при этом bi ≥ 0 и bi + … +bj = 1, а общая конверсия α = bi αi +… +bjαj.
Для кинетического анализа термограмм ТГА используют те или иные приближенные решения уравнения (1) в виде линейных аппроксимаций, в частности, интегральный изоконверсионный метод КАS (Kissinger–Akahira–Sunose) [13] и метод Kiss (Kissinger) [14]. Можно также обрабатывать данные ТГА методом нелинейной регрессии [15], при этом уравнение (1) решается численно. Ранее на примере деструкции ПК без добавок было показано, что модернизированный метод нелинейной регрессии, предложенный в работе [16], позволяет достаточно точно описать кинетику этого процесса и выявить ряд его особенностей, не доступных при изучении стандартными методами. Основные цели нашей работы – исследование возможности применения разработанного подхода [16] для анализа и моделирования кинетики термодеструкции ПК в присутствии диметилдитиокарбамата (ДМДТК) висмута и определение кинетических параметров (Ai, Ei и bi) отдельных стадий этого сложного многостадийного процесса.
МЕТОДИКА ЭКСПЕРИМЕНТА
В работе использовали нестабилизированный коммерческий ПК на основе бисфенола А (Оргсинтез, Казань, Россия) без дополнительной очистки со средневязкостной молекулярной массой Мn = = 30 000. Диметилдитиокарбамат висмута дважды перекристализировали из хлороформа. Добавку вводили в раствор полимера. Пленки толщиной 10–20 мкм формировали медленным испарением растворителя из 5%-ного раствора полимера в хлороформе, нанесенного на полированную стеклянную поверхность, а затем отслаивали дистиллированной водой. Следы растворителя удаляли хранением пленки в вакуумной камере при комнатной температуре в течении суток. Измерения предварительно измельченных образцов проводили на воздухе с использованием дериватографа Q-15000D (МОМ, Будапешт, Венгрия). Регистрацию осуществляли с помощью аналого-цифрового блока фирмы “Экохром” (Россия), связанного с персональным компьютером. Потерю массы регистрировали как функцию температуры и времени при трех скоростях нагрева (5, 10 или 20 °С/мин) в температурной области 130–900 °С. Первичные экспериментальные данные по потере массы экспоненциально сглажены и при необходимости трансформированы в конверсию согласно выражению (2).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Как показано на рис. 1, термостойкость ПК в присутствии ДМДТК висмута существенно уменьшается. Так, например, 3%-ные потери массы достигаются уже при температуре 262 °С, в то время как для чистого ПК – лишь при 357 °С (при β = = 5 °С/мин).
Рис. 1.
Термограммы потери массы ПК в отсутствии (1) и в присутствии ДМДТК висмута (2) при скорости нагрева 5 °С/мин.
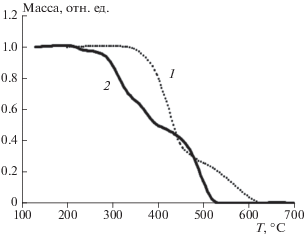
Анализ методом ТГА термодеструкции на воздухе вплоть до существенного изменения массы образцов (~80%) свидетельствует о сложном механизме процесса (рис. 1). Особенно четко это проявляется при небольшой скорости нагрева.
Для обработки термограмм ТГА в динамическом режиме использовали два широко применяемых метода, основанных на линейных аппроксимациях: метод Kiss [13] и метод KAS [14]. Первый из ниx основан на зависимости температуры Тmax, соответствующей точке перегиба на кривой потери массы, или максимуму на кривой ДТГА от скорости нагрева (β):
(5)
$\ln ({\beta \mathord{\left/ {\vphantom {\beta {T_{{max}}^{2}}}} \right. \kern-0em} {T_{{max}}^{2}}}) = \ln \left( {{{AR} \mathord{\left/ {\vphantom {{AR} {{{E}_{a}}}}} \right. \kern-0em} {{{E}_{a}}}}} \right)--{{{{E}_{a}}} \mathord{\left/ {\vphantom {{{{E}_{a}}} {(R{{T}_{{max}}})}}} \right. \kern-0em} {(R{{T}_{{max}}})}},$где Еа – энергия активации процесса, Тmax – температура максимальной скорости потери массы, R – газовая постоянная, А = const. Наклон прямой в координатах уравнения (5), дает величину энергии активации. Однако даже при относительно небольших значениях β точки перегиба могут смещаться в область более высоких температур из-за наложения отдельных стадий. В общем случае, для выделения этих стадий необходимо дополнительное моделирование. На рис. 2 в качестве примера представлена экспериментальная кривая потери массы при скорости нагрева 5°С/мин и ее первая производная (верхний рисунок), а также моделирование дифференциальной кривой с помощью набора гауссовых пиков (нижний рисунок). Поиск параметров гауссовых пиков проводили, минимизируя среднеквадратичную ошибку между теоретическими и экспериментальными кривыми. Экспериментальные и моделированные данные были обработаны в соответствии с методом Kiss. Как следует из данных табл. 1, уравнение (5) достаточно хорошо выполняется, однако между экспериментальными и полученными в результате моделирования величинами энергий активации наблюдаются заметные отличия, особенно для третьей и четвертой стадий.
Рис. 2.
Кривая потери массы ПК в присутствии ДМДТК висмута при скорости нагрева 5°С/мин на воздухе и ее первая производная (вверху); моделирование дифференциальной кривой с помощью набора гауссовых пиков (внизу).
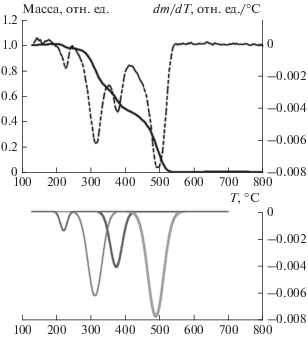
Таблица 1.
Оценка параметров для четырех пиков при трех скоростях нагрева методом Kiss (R2 – коэффициент детерминации для линейной линии тренда)
| β, °C/мин | Тmax, °С (эксперимент) |
Еа, кДж/моль |
R2 | Тmax, °С (моделирование по Гауссу) |
Еа, кДж/моль | R2 |
|---|---|---|---|---|---|---|
| 5 10 20 |
222.2 240.6 250.9 |
94.1 | 0.964 | 222.2 239.0 249.3 |
101.0 | 0.973 |
| 5 10 20 |
313.6 331.4 360.6 |
87.4 | 0.985 | 313.6 328.4 355.3 |
91.3 | 0.972 |
| 5 10 20 |
373.9 390.7 401.6 |
170.0 | 0.980 | 375.1 391.5 414.9 |
119.2 | 0.991 |
| 5 10 20 |
488.7 511.2 545.7 |
113.8 | 0.986 | 490.7 516.1 558.931 |
94.2 | 0.979 |
Интегральный изоконверсионный метод KAS основан на связи между температурой, при которой достигается заданная конверсия, и скоростью нагрева:
(6)
${\text{ln}}({{{{\beta }_{i}}} \mathord{\left/ {\vphantom {{{{\beta }_{i}}} {T_{{a,\,\,i}}^{2}}}} \right. \kern-0em} {T_{{a,\,\,i}}^{2}}}) = {\text{const}}--{{{{E}_{a}}} \mathord{\left/ {\vphantom {{{{E}_{a}}} {(R{{T}_{a}}_{{,\,\,i}})}}} \right. \kern-0em} {(R{{T}_{a}}_{{,\,\,i}})}},$где βi – скорость нагрева при i-той температурной программе; Тa, i – температура, при которой достигается степень конверсии a при заданном значении βi; Ea – энергия активации процесса при степени конверсии a; R – универсальная газовая постоянная. Как видно из рис. 3, зависимость Еа от степени конверсии имеет сложный характер, поэтому энергию активации можно оценить лишь в области температур 300–400 °С, что соответствует значениям конверсии 0.2–0.4. Найденное значение Еа составляет порядка 100 кДж/моль. Таким образом, методами линейной аппроксимации, даже с привлечением дополнительного моделирования, не удается адекватно описать кинетику термодеструкции ПК в присутствии ДМДТК висмута и корректно определить значения энергий активации отдельных стадий, важных для понимания механизма деструкции и прогнозирования этого процесса.
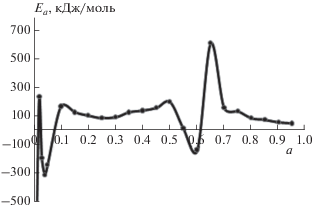
Рис. 3.
Зависимость энергии активации термодеструкции в присутствии ДМДТК висмута, рассчитанные по экспериментальным данным методом KAS.
Для определения кинетических параметров (A, E, b) было проведено моделирование термодеструкции с помощью модернизированного метода нелинейной регрессии, так называемого “серое моделирование”, применимого к S-образным термогравиметрическим кривым [16]. Основная идея состоит в последовательном оценивании параметров, когда общая модель закономерно изменяется от одного уровня моделирования к другому. На первом этапе используется функция Аврами–Eрофеева (АЕ) [17, 18]:
далее – функция Sestak–Berggren (SB) [19]:
которая при введении соответствующей константы C в правую часть уравнения охватывает как бы “зонтиком” различные кинетические функции [20].
Для подгонки модели и оценивания неизвестных параметров применяли программное обеспечение FITTER [15]. Эта программа использует модифицированный метод градиентного поиска, а ее отличительной чертой является аналитическое вычисление производных, которое обеспечивает высокую точность счета модели и установления неизвестных параметров. В случае, если f(a) определяется уравнением (7) дифференциальное уравнение (1) имеет точное решение [16]:
Интегрируя уравнение (9), получаем выражение
(10)
$p(t) = A\int\limits_0^t {\exp \left( {\frac{{{E \mathord{\left/ {\vphantom {E R}} \right. \kern-0em} R}}}{{{{T}_{0}} + \beta \tau }}} \right)} d\tau ,$где τ – переменная интегрирования, а $p(t)$ – так называемый температурный интеграл. В работе [16] предложена аппроксимация выражения (10)
где
(12)
$x = \frac{{{E \mathord{\left/ {\vphantom {E R}} \right. \kern-0em} R}}}{{{{T}_{0}} + \beta t}};\,\,\,\,G(x) = \frac{{{\text{0}}{\text{.7284}}x + {\text{0}}{\text{.2387}}{{x}^{2}}}}{{1 + {\text{1}}{\text{.2056}}x + {\text{0}}{\text{.2387}}{{x}^{2}}}}.$При расчетах использовали масштабирование переменных с целью уменьшения разброса между ними. Например, время t (мин), делилось на 60, температура T (К), делилась на 1000. Таким образом, получены следующие области изменения масштабированных переменных: 0 < t < 1, 0.4 < T < 1.2, 0.3 < β < 1.2.
На первом этапе моделирования проводили одновременную подгонку данных ТГА при всех температурных программах для I-cтадий с использованием модели Аврами–Ерофеева (далее АЕ-модель), уравнение (7). Результатом этого этапа является установление числа стадий. Для каждой стадии i = 1…I оценены параметры Арениуса, Ai и Ei, а также весовой коэффициент bi и параметр Aврами–Eрофеева qi.
На втором этапе для каждой стадии проводили аппроксимацию индивидуальной АЕ-модели (с учетом значений qi) функцией Sestak–Berggren, далее SB-модель (уравнение 8). Поиск параметров проводили путем минимизации среднеквадратичной ошибки между функциями АЕ и SB. Для каждой отдельной стадии i = 1…I получены параметры функции SB mi и ni, а также масштабирующие факторы Ci. Эти факторы использованы для корректировки значений Аi, найденных на первом этапе. Результаты аппроксимации представлены на рис 4. Параметры, полученные на этом этапе, использованы в качестве начальных значений для финальной оптимизационной процедуры (этап 3).
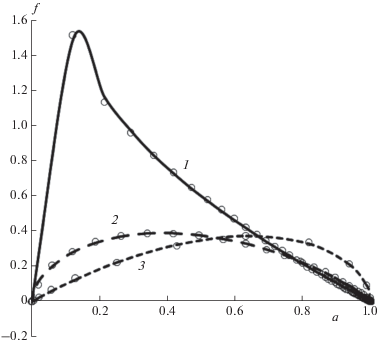
Рис. 4.
Данные моделированния. Подгонка AЕ-модели (маркеры) SB-моделью (сплошные кривые) для стадий 1, 2, 3.
На этом, последнем этапе проводили одновременную подгонку данных ТГА при всех температурных программах для I-стадий моделью в форме системы дифференциальных уравнений с SB-функцией. В результате для каждой стадии i = 1…I находили параметры Аррениуса Ai и Ei, а также весовой коэффициент bi и параметры функции Sestak–Berggren mi и ni.
Результаты моделирования представлены на рис. 5 и в табл. 2. Видно, что экспериментальные данные (открытые маркеры) удовлетворительно описываются кинетической моделью, учитывающей три основные стадии деструкции (сплошные кривые). На первой стадии термодеструкции поликарбоната, в соответствии с имеющимися представлениями [1, 2], происходит преимущественно окисление изопропилиденовых групп. Реакции с промежуточным участием пероксидных и алкоксильных радикалов приводят к образованию CO, CO2, ацетальдегида, формальдегида и воды [1]. Значение энергии активации первой стадии, полученное в работе (табл. 2), находится в том же ряду, что и энергии активации термоокисления большинства полимеров (70–120 кДж/моль). Вторую стадию можно отнести к процессу деполимеризации с образованием бисфенола А. Механизм третьей стадии остается дискуссионным из-за трудностей анализа остатков веществ, участвующих в данном процессе. Можно предположить, что на этой стадии происходит окисление и деструкция полисопряженных структур. Оценки энергии активации для каждой стадии, полученные при обработке моделированных кривых методом линейной аппроксимации (KAS, рис. 6, 79.0, 76.8 и 37.2 кДж/моль) согласуются со значениями, приведенными в табл. 2.
Рис. 5.
Экспериментальные данные (маркеры) и результаты моделирования (сплошные кривые) инициированной деструкции ПК при трех скоростях нагрева: 5, 10, 20 °С/мин; вклад каждой из стадий (вторые цифры) показан точечными кривыми.
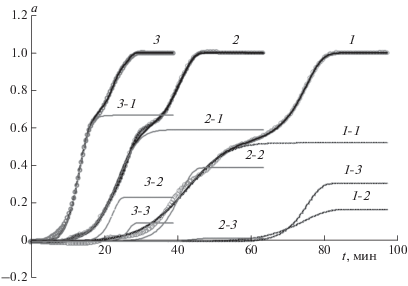
Таблица 2.
Оценка параметров при “сером моделировании”
| Параметр | Этап 1 АЕ-модель |
Этап 2 SB-модель |
Этап 3 SB-модель |
|---|---|---|---|
| RSS | 0.051 | (2.4) · 10–6 – (7.4) · 10–6 | 0.049 |
| A1 (мин–1 ) | (5.3 ± 0.12) · 105 | (4.6 ± 0.0005) · 105 | (6.3 ± 0.18) · 105 |
| Е1 (кДж/моль ) | 78.3 ± 2.0 | 78.26 ± 0.01 | 79 ± 2.7 |
| q1 | 0.885 ± 0.024 | – | – |
| m1 | – | 1.048 ± 0.0002 | 1.269 ± 0.118 |
| n1 | – | –0.134 ± 0.0002 | –0.071 ± 0.0.037 |
| A2 (мин–1 ) | (1.4 ± 0.1) · 104 | (2.6 ± 0.0005) · 104 | (3.03 ± 0.32) · 104 |
| Е2 (кДж/моль ) | 75.95 ± 5.9 | 75.87 ± 0.01 | 78.2 ± 10.5 |
| q2 | 1.716 ± 0.131 | – | – |
| m2 | – | 0.837 ± 0.0006 | 0.711 ± 0.134 |
| n2 | – | 0.424 ± 0.0002 | 0.361 ± 0.125 |
| А3 (мин–1 ) | (0.22 ± 0.009) · 102 | (1.3 ± 0.00026) · 102 | (1.04 ± 0.05) · 102 |
| Е3 (кДж/моль) | 39.2 ± 1.7 | 39.2 ± 0.01 | 38.4 ± 1.8 |
| q3 | 5.543 ± 0.847 | – | – |
| m3 | – | 0.675 ± 0.001 | 0.641 ± 0.157 |
| n3 | – | 0.828 ± 0.0002 | 0.812 ± 0.063 |
| Nl | 6 | 4 | 7 |
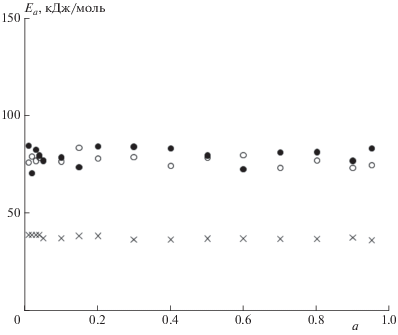
Рис. 6.
Зависимость энергии активации от степени конверсии для трех основных стадий инициированной деструкции ПК, рассчитанных для моделированных данных (рис. 5) методом KAS (закрытые маркеры – первая стадия, открытые – вторая, крестики – третья ).
ЗАКЛЮЧЕНИЕ
Для анализа термодеструкции поликарбоната на основе бисфенола А в присутствии ДМДТК висмута использован метод, отличительной особенностью которого является одновременный нелинейный регрессионный анализ всех кривых ТГА с использованием общей кинетической модели, включающей несколько стадий. Параметры Аррениуса для каждой стадии, число стадий, также как и доля каждой индивидуальной стадии оценены одновременно для всех температурных программ. Вычислительные трудности, связанные с нелинейной подгонкой многостадийных данных, преодолены последовательной оценкой неизвестных параметров, когда общая модель изменяется при переходе от одного этапа моделирования к другому. Полученные параметры использованы в качестве начальных значений для согласования данных ТГА моделью в форме системы дифференциальных уравнений. Данный подход свободен от ограничений и недостатков, свойственных широко используемым методам линейной аппроксимации (Kiss и KAS), что позволяет адекватно и точно описать форму кинетических кривых ТГА, а также определить кинетические параметры отдельных стадий многостадийной инициированной деструкции полимера.
Работа выполнена в соответствии с госзаданием № 0082-18-006, номер государственной регистрации AAAA-A18-118020890097-1.
Список литературы
Lee L.H. // J. Polym. Sci. 1964. V. 2. P. 2859.
Jang B.N., Wilkie C.A. // Thermochim. Acta. 2005. V. 426. P. 73.
Иванов В.Б., Солина Е.В., Староверова О.В. и др. // Хим. физика. 2017. Т. 36. № 11. С. 1.
Ivanov V.B., Zavodchikova A.A., Popova T.I. et al. // Thermochim. Acta. 2014. V. 589. P. 70.
Ломакин С.М., Шаулов А.Ю., Коверзанова Е.В. и др. // Хим. физика. 2019. Т. 38. № 4. С. 74.
Хватов А.В., Бревнов Н.Н., Шилкина Н.Г. и др. // Xим. физика. 2019. Т. 38. № 6. С. 71.
Захаров В.В., Чуканов Н.В., Зюзин И.Н. и др. // Хим. физика. 2019. Т. 38. № 2. С. 3–8.
Захаров В.В., Чуканов Н.В., Шилов Г.В. и др. // Хим. физика. 2019. Т. 38. № 4. С. 45.
Стовбун С.В., Ломакин С.М., Щеголихин А.И. и др. // Хим.физика. 2018. Т. 37. № 1. С. 21.
Быстрицкая Е.В., Карпухин О.Н., Куценова А.В. // Хим. физика. 2013. Т. 32. № 8. С. 65.
Vyazovkin S., Burnham A.R., Criado J.M. et al. // Thermochim. Acta. 2011. V. 520. P. 1.
Opfermann J.J. // J. Therm. Anal. Calorim. 2000. V. 60. P. 641.
Kissinger H. // Anal. Chem. 1957. V. 29. № 11. P. 1072.
Akahira T., Sunose T. // Res. Report. Chiba Inst. Technol. (Japan) 1971. V. 16. P. 22.
Bystritskaya E.V., Pomerantsev A.L., Rodionova O.Y. // J. Chemom. 2000. V. 14. P. 667.
Pomerantsev A.L., Kutsenova A.V., Rodionova O.Y. // Phys. Chem. Chem. Phys. 2017. V. 19 (5). P. 3606.
Avrami M. // J. Chem. Phys. 1939. V. 7. P. 1103.
Ерофеев Б.В. // Докл. АН СССР. 1946. Т. 52. № 6. С. 515.
Sestak J., Berggren G. // Thermochim. Acta. 1971. V. 3. P. 1.
Perez-Maqueda L.A., Criado J.M., Sanchez-Jimenez P.E. // J. Phys. Chem. A. 2006. V. 110. P. 12456.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика


