Координационная химия, 2019, T. 45, № 2, стр. 99-105
Молекулярная и кристаллическая структура 1-(2-метоксифенил)-1,4-дегидро-5H-тетразол-5-тиона и его комплекса с Cd(II)
Р. К. Аскеров 1, *, А. М. Магеррамов 1, В. К. Османов 2, Е. В. Баранов 3, 4, Г. Н. Борисова 2, А. Д. Самсонова 2, А. В. Борисов 2
1 Бакинский государственный университет
, Азербайджанская Республика
2 Нижегородский государственный технический университет им. Р.Е. Алексеева
, Россия
3 Институт металлоорганической химии им. Г.А. Разуваева РАН
Нижний, Новгород, Россия
4 Нижегородский государственный университет им. Н.И. Лобачевского
, Россия
* E-mail: rizvankam@bk.ru
Поступила в редакцию 29.05.2018
После доработки 24.08.2018
Принята к публикации 21.08.2018
Аннотация
Методом РСА изучена молекулярная и кристаллическая структура 1-(2-метоксифенил)-1,4-дегидро-5H-тетразол-5-тион (L) и его комплекса с кадмием(II) (II), CIF files CCDC № 1567109 (L), 1547252 (II). Свободный лиганд L, являющийся тионом, неплоский. Двугранный угол между тетразольным и бензольным циклами равен 85.21(7)°. Эти циклы образуют в кристалле центросимметричные димеры посредством двух водородных связей N–H···S. Димеры включают центральный плоский восьмичленный цикл {S=C–N–H···S=C–N–H···}. Комплекс II имеет цепочечное строение состава [(C8H7N4OS)2Cd]n. Координация атома Сd(II) искаженная тетраэдрическая из двух атомов азота и двух атомов серы четырех лигандов L. Одномерные цепочки содержат восьмичленные циклы {←S=C–N–Cd ← S=C–N–Cd} в конформации ванны. В кристалле между соседними одномерными цепочками вдоль оси с существуют слабые межмолекулярные водородные связи C–H···N.
В данной статье изучено строение 1-(2-метоксифенил)-1,4-дегидро-5H-тетразол-5-тиона (L) и его комплекса с кадмием(II) (II).
N-замещенные меркаптотетразолы с несколькими электронодонорными центрами можно использовать как лиганды для получения различных координационных соединений [1–6].
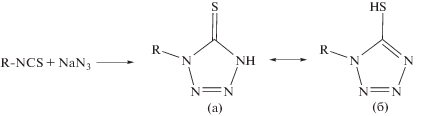
Из литературных данных известно, что подобные гетероциклические соединения могут существовать как в тионной (a), так и в тиольной форме (б) (схема 1).
Схема 1.
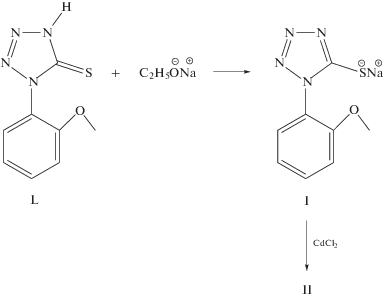
Считается, что более устойчива для меркаптотетразолов тионая форма [7]. Для замещения таких соединений по атому серы их необходимо переводить в тиоляты щелочных металлов. Мы синтезировали лиганд L. Действием этилата натрия L переводили в соответствующий тиолят (I), который без выделения использовали в реакции с хлоридом кадмия с образованием комплекса II (схема 2).
Схема 2.
Строение полученных соединений L и II установлено методом РСА.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Исходные реагенты NaN3, CdCl2 (квалификации не ниже “х. ч.”) и o-метоксифенилизотиоцианат (Acros Organics, Бельгия) использовали без дополнительной очистки.
Синтез тиона L. К раствору 2.53 г (39 ммоль) NaN3 в 50 мл Н2О при 20°С прибавляли 6.431г (39 ммоль) o-метоксифенилизотиоцианата. Реакционную смесь кипятили 2 ч, охлаждали до 20°С и отфильтровывали от нерастворившихся примесей. Далее при перемешивании к раствору добавляли 10%-ный водный раствор HCl до рН 2. Выпавший осадок отфильтровывали, промывали 200 мл воды и сушили при 353 К. Продукт для РСА перекристаллизовывали из этанола. Выход НL 7.036 г (33.82%). Белые кристаллы. Тпл = 162–164°С (с разл.).
Синтез II. К раствору 0.416 г (2 ммоль) тиона L в 25 мл абсолютного C2H5OH прибавляли раствор 0.136 г (2 ммоль) этилата натрия в 15 мл абсолютного C2H5OH. Затем добавляли раствор 0.184 г (1 ммоль) CdCl2 в 15 мл абсолютного C2H5OH. Реакционную смесь кипятили 5 ч и охлаждали до 20°С. Выпавший осадок отфильтровывали, промывали 50 мл C2H5OH и сушили при 353 К. Продукт для РСА перекристаллизовывали из этанола. Выход II 0.093 г (18.06%). Белые кристаллы. Тпл = = 202–204°С (с разл.).
РСА соединений L и II проведен на дифрактометре Bruker Smart Apex (ω-сканирование, МоКα-излучение, λ = 0.71073 Å, T = 296 K). Экспериментальные наборы интенсивностей отражений собраны и интегрированы по программе SMART [8] и SAINT [9] соответственно. Структуры решены прямым методом и уточнены полноматричным МНК по $F_{{hkl}}^{{\text{2}}}$ в анизотропном приближении для неводородных атомов. Атом водорода, участвующий в межмолекулярной водородной связи (ВС) N–H···S в L, локализован из разностного синтеза электронной плотности и уточнен в изотропном приближении. Остальные водородные атомы в L и II помещены в геометрически рассчитанные положения и уточнены изотропно с фиксированными тепловыми параметрами Uiso(H) = 1.2Uiso(C). Уточнение структуры и учeт поглощения проведены с использованием программных пакетов SHELXTL [10] и SADABS [11]. Кристаллографические данные и параметры рентгеноструктурных экспериментов приведены в табл. 1.
Таблица 1.
Основные кристаллографические данные и параметры уточнения для соединений L и II
| Параметр | Значение | |
|---|---|---|
| L | II | |
| Эмпирическая формула | C8H8N4OS | C16H14N8 O2S2Cd |
| М | 208.24 | 526.87 |
| Размеры кристалла, мм | 0.21 × 0.17 × 0.10 | 0.65 × 0.074 × 0.06 |
| Сингония | Моноклинная | Орторомбическая |
| Пр. гр. | P21 /c | Pccn |
| a, Å | 5.0808(7) | 12.8945(8) |
| b, Å | 19.402(3) | 18.9350(12) |
| c, Å | 9.9024(14) | 8.5599(6) |
| β, град | 90.967(3) | 90 |
| V, Å3 | 976.0(2) | 2090(6) |
| Z | 4 | 4 |
| ρ(выч.), г/см3 | 1.417 | 1.674 |
| µ, мм–1 | 0.303 | 1.274 |
| F(000) | 432 | 1048 |
| Область сбора данных по θ, град | 25 | 25 |
| Измерено отражений | 10 754 | 19 754 |
| Независимых отражений | 2793 | 2517 |
| Число уточняемых параметров | 131 | 133 |
| R1 (I > 2σ(I)) | 0.0471 | 0.0216 |
| wR2(все данные) | 0.0943 | 0.0565 |
| GOОF | 1.007 | 1.007 |
| Tmin; Tmax | 0.6474; 0.7461 | 0.384; 0.746 |
| Остаточная электронная плотность (ρmin/ρmax), e Å–3 | –0.318/0.378 | –0.156/0.781 |
Структуры зарегистрированы в Кембриджском банке структурных данных (№ 1567109 (L), 1547252 (II); ccdc.cam.ac.uk/getstructures).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
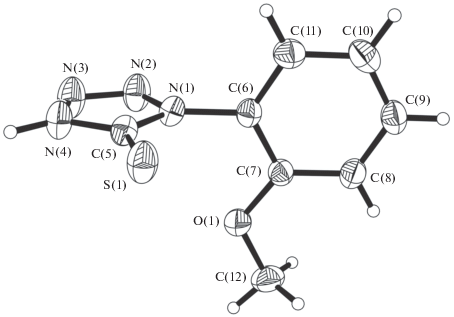
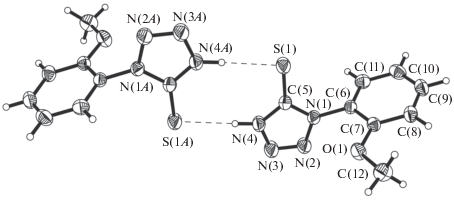
Молекулярная структура L показана на рис. 1. Избранные длины связей, значения валентных и торсионных углов в L представлены в табл. 2.
Таблица 2.
Избранные длины связей (d), валентные (ω) и торсионные (γ) углы в соединениях L и II
| L | |||||
|---|---|---|---|---|---|
| Связь | d, Å | Связь | d, Å | Связь | d, Å |
| S(1)–C(5) | 1.6680(18) | N(3)–N(4) | 1.354(2) | O(1)–C(12) | 1.427(2) |
| N(1)–C(5) | 1.351(2) | N(4)–C(5) | 1.346(2) | C(6)–C(11) | 1.374(2) |
| N(1)–N(2) | 1.3675(19) | N(1)–C(6) | 1.437(2) | ||
| N(2)–N(3) | 1.2773(19) | O(1)–C(7) | 1.356(2) | ||
| Угол | ω, град | Угол | ω, град | Угол | γ, град |
| N(1)C(5)N(4) | 102.11(15) | N(4)C(5)S(1) | 129.35(14) | C(5)N(1)C(6)C(11) | 87.3(2) |
| C(5)N(1)N(2) | 111.00(14) | N(1)C(5)S(1) | 128.53(13) | C(5)N(1)C(6)C(7) | 93.3(2) |
| C(5)N(4)N(3) | 111.79(16) | C(11)C(6)N(1) | 118.52(15) | C(12)O(1)C(7)C(8) | 0.4(3) |
| N(3)N(2)N(1) | 107.48(15) | C(7)C(6)N(1) | 117.65(14) | C(6)N(1)C(5)S(1) | 3.0(3) |
| N(2)N(3)N(4) | 107.62(15) | C(7)O(1)C(12) | |||
| II | |||||
| Связь | d, Å | Связь | d, Å | Связь | d,Å |
| Cd(1)–N(4) | 2.228(4) | N(2)–N(3) | 1.280(2) | C(6)–C(7) | 1.392(3) |
| Cd(1)–S(1) | 2.4972(11) | N(3)–N(4) | 1.357(2) | C(6)–C(11) | 1.374(2) |
| S(1)–C(5) | 1.7155(16) | N(4)–C(5) | 1.326(2) | O(1)–C(7) | 1.354(2) |
| N(1)–C(5) | 1.349(2) | N(1)–C(6) | 1.434(2) | O(1)–C(12) | 1.427(3) |
| N(1)–N(2) | 1.3616(19) | ||||
| Угол | ω, град | Угол | ω, град | Угол | γ, град |
| N(4)Cd(1)N(4A) | 119.80(7) | C(11)C(6)N(1) | 119.17(16) | C(7)C(6)N(1)C(5) | 69.6(2) |
| S(1)Cd(1)S(1E) | 129.12(2) | N(1)C(5)S(1) | 127.52(12) | C(8)C(7)O(1)C(12) | 4.5(3) |
| C(5)N(1)C(6) | 131.99(14) | C(7)C(6)N(1) | 119.16(15) | ||
| N(2)N(1)C(6) | 118.97(14) | N(4)C(5)S(1) | 126.35(12) | ||
Соединение L состоит из двух плоских фрагментов – o-метоксифенильного и меркаптотетразольного циклов. Двугранный угол между их плоскостями равен 85.21(7)°, торсионный угол C(7)–C(6)–N(1)–C(5) 93.3(2)°. Метильная группа в метоксифенильном фрагменте находится в плоскости цикла. Торсионный угол C(8)–C(7)–O(1)–C(12) составляет 0.4(2)°. Расстояния N(1)–N(2) 1.3675(19), N(1)–C(5) 1.351(2), N(3)–N(4) 1.354(2) и N(4)–C(5) (1.346(2) Ǻ в меркаптотетразольном фрагменте соответствуют одинарным связям, в то время как N(2)=N(3) 1.2773(19) и С(5)=S(1) 1.6680(18) – двойным, что подтверждает существование соединения L в тионной форме в свободном состоянии. Все связи в структуре L соответствуют среднестатистическим значениям [12].
Молекулы L в кристалле образуют центросимметричные димеры посредством двух ВС N(4)–H(4)···S(1) (1 – x, 1 – y, 1 – z) (N–H 0.93(2), H···S 2.30(2) Å, угол N–H–S 178(3)°) (рис. 2). Димеры включают центральный плоский (+0.0169 Å) восьмичленный цикл {S=C–N–H···S=C–N–H}.
Рис. 2.
Строение H-связанных димеров в кристалле соединения L. Тепловые эллипсоиды приведены с 30%-ной вероятностью.
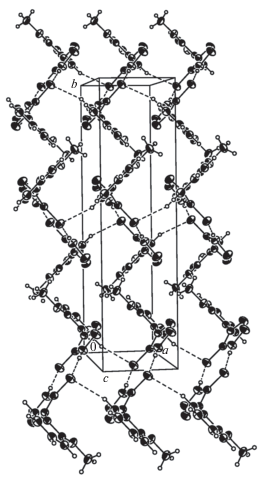
Димеры соединения L соединяются в зигзагообразные слои вдоль оси b. Слои соединены слабыми межмолекулярными ВС C(11)–H(11A)···S(1) (x – 1, y, z) (C–H 0.930(2), H···S 2.915(2) Å, угол C–H···S 156(2)°) [13] вдоль оси а (рис. 3)
Рис. 3.
Фрагмент кристаллической упаковки зигзагообразных слоев соединения L вдоль оси b. Пунктирными линиями указаны слабые водородные связи C–H…S.
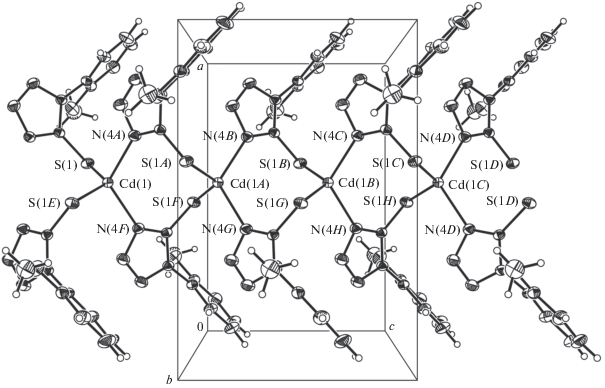
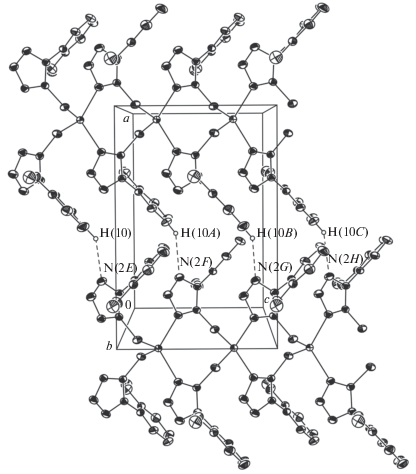
Комплекс II имеет 1D-цепочечное строение состава [(C8H7N4OS)2Cd]n. Координационный полиэдр катиона кадмия(II) – искаженный тетраэдр, включающий два атома азота и два атома серы четырех лигандов L [6]. Расстояния Cd–S и Cd–N 2.5035(4) и 2.2300(14) Å, а также углы NCdN и SCdS 119.80(7)° и 129.12(2)° равны соответственно. Следует заметить, что характер связей в тетразольном фрагменте лиганда L меняется при образовании комплекса II. Так, связь C(5)–S(1) (1.716(2) Å) становится одинарной, а N(4)=C(5) (1.326(2) Å) – двойной (табл. 2), что определяется большим химическим сродством катиона кадмия к атому серы, чем к атому азота. Следовательно, в отличие от свободного состояния, в комплексе II тетразольный лиганд L принимает тиольную форму. Двугранный угол между плоскостями фенильного и меркаптотетразольного фрагментов составляет 66.34(7)°, торсионные углы C(7)–C(6)–N(1)–C(5) и C(8)–C(7)–O(1)–C(12) равны 69.6(2)° и 4.5(3)° соответственно. Одномерные цепочки кристала II содержат восьмичленные циклы {←N=C–S–Cd–S–C=N → Cd} в конформации ванны. Расстояние Cd···Cd равно 4.280 Ǻ. Цепочки комплекса II в кристалле расположены вдоль оси с (рис. 4).
В кристаллической упаковке комплекса II между соседними одномерными цепочками вдоль оси с существуют слабые межмолекулярные ВС C(10)–H(10A)···N(2) (–x + 3/2, y, –1/2 + z) (C–H 0.930(2), H···S 2.706(2) Å, угол C–H···N 148(2)° [13] (рис. 5))
Список литературы
Ma C.L., Zhang Q., Sun J.F., Zhang R.F. // J. Organomet. Chem. 2006. V. 691. P. 2567.
Ilie A., Rat C.I., Scheutzow S., Kiske C. et al. // Inorg. Chem. 2011. V. 50. P. 2675.
Li Y., Wang C.Q., Bian H.D. et al. // J. Coord. Chem. 2012. V. 65. № 20. P. 3665.
Sanina N.A., Kozub G.I., Kondrat T.A. // J. Mol. Struc. 2013. V. 1041. P. 183.
Bharty M.K., Dani R.K., Kushawaha S.K. // Polyhedron. 2015. V. 88. P. 208.
Song J.F., Wang J., Li S.Z. // J. Mol. Struc. 2017. V. 1129. P. 1.
Штефан Е.Д., Введенский В.Ю. // Успехи химии. 1995. Т. 65. № 4. С. 326–333.
SMART. Bruker Molecular Analysis Research Tool. Version 5.632. Madison (WI, USA): Bruker AXS, 2005.
SAINT. Data Reduction and Correction Program. Version 8.34A. Madison (WI, USA): Bruker AXS, 2014.
Sheldrick G.M. SADABS. Program for Absorption Correction. Göttingen (Germany): Univ. of Göttingen, 1996.
Sheldrick G.M. Acta Crystallogr. C. 2015. V. 71. P. 3.
Allen F.H., Watson D.G., Brammer L. et al. International Tables for Crystallography. 2006. Ch. 9.5. P. 790.
Зефиров Ю.В., Зоркий П.М. // Успехи химии. 1995. Т. 64. № 4. С. 446.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия