Координационная химия, 2022, T. 48, № 5, стр. 269-276
Слоистые транс-1,4-циклогександикарбоксилаты двухвалентных металлов: синтез, кристаллическая структура и термические свойства
П. А. Демаков 1, В. П. Федин 1, *
1 Институт неорганической химии им. А.В. Николаева СО РАН
Новосибирск, Россия
* E-mail: cluster@niic.nsc.ru
Поступила в редакцию 12.11.2021
После доработки 29.11.2021
Принята к публикации 30.11.2021
- EDN: LRQPDT
- DOI: 10.31857/S0132344X22050048
Аннотация
Реакцией нитрата магния с транс-1,4-циклогександикарбоновой кислотой (H2Сhdc) в растворителях N,N-диметилформамиде (DMF) и N-метилпирролидоне (NMP) получены новые координационные полимеры [Mg3(DMF)4(Chdc)3] (I), [Mg3(DMF)2(NMP)2(Сhdc)3] (II) и [Mg3(NMP)4(Сhdc)3] (III). Из ацетата кальция и H2Chdc в NMP получен координационный полимер [Ca3(NMP)4(Chdc)3] (IV). Реакцией нитрата кадмия с H2Сhdc и уротропином (Ur) в DMF получен координационный полимер [Cd(Ur)(DMF)(Chdc)] (V). Строение полученных соединений установлено методом рентгеноструктурного анализа монокристаллов (CIF files CCDC № 2120662 (I), 2120666 (II), 2120664 (III), 2120663 (IV), 2120665 (V)). Координационные полимеры щелочноземельных металлов I–IV построены на основе трехъядерных карбоксилатных блоков {M3(OOC)6}, связанных мостиковыми дикарбоксилатными линкерами в слои тригональной геометрии. Соединение кадмия V построено на основе одноядерных фрагментов {Cd(NUr)2(DMF)(OOC)2}, связанных мостиковыми транс-1,4-циклогександикарбоксилатами и молекулами уротропина также в полимерные слои. Соединения I–III охарактеризованы методами ИК-спектроскопии, элементного и термогравиметрического анализов.
Металл-органические координационные полимеры (МОКП) активно исследуются в последние два десятилетия как перспективные сорбенты, катализаторы, люминофоры, сенсоры. Значительная часть МОКП построена на основе полиядерных фрагментов или кластеров, использование которых позволяет задавать топологию, связность и необходимые физико-химические свойства координационной решетки [1–7], в то время как варьирование длины и природы мостикового лиганда открывает возможность управления пористостью и сорбционными свойствами полимера [8–13].
Синтез и исследование низкоразмерных координационных полимеров представляют большой интерес для получения функциональных пленок, мембран и каталитически активных материалов [14–18]. Использование топологически “плоских” металлоцентров, в том числе и полиядерных, является методом направленной генерации двумерных структур.
Большой интерес для синтеза МОКП представляют катионы легких металлов (Li+, Mg2+, Al3+, Ca2+, Sc3+). Низкая атомная масса металлоцентра позволяет максимизировать удельные физико-химические характеристики [19–26]. Соли легких щелочноземельных металлов легкодоступны и дешевы, а МОКП на их основе получено сравнительно немного. С другой стороны, Cd2+, несмотря на свою высокую токсичность, широко используется в химии МОКП благодаря интересным оптическим и люминесцентным свойствам его координационных соединений [27–32].
В настоящей работе проведены синтез, установление кристаллической структуры и физико-химическая характеризация пяти новых слоистых транс-1,4-циклогександикарбосилатов двухвалентных щелочноземельных металлов и кадмия – [Mg3(DMF)4(Сhdc)3] (I), [Mg3(DMF)2(NMP)2(Chdc)3] (II), [Mg3(NMP)4(Chdc)3] (III), [Ca3(NMP)4(Chdc)3] (IV) и [Cd(Ur)(DMF)(Chdc)] (V).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Все исходные вещества использовали в виде коммерчески доступных реактивов без дополнительной очистки. В качестве растворителя использовали N,N-диметилформамид (DMF) квалификации “х. ч.”, N-метилпирролидон (NMP) квалификации “ч. д. а.” и смесь DMF c NMP соответственно.
ИК-спектры в диапазоне 4000–400 см−1 регистрировали в таблетках с KBr на Фурье-спектрометре Scimitar FTS 2000. Термогравиметрический анализ (ТГА) проводили на термоанализаторе NETZSCH TG 209 F1 при линейном нагревании образцов в атмосфере He со скоростью 10 град мин−1. Элементный анализ выполнен на CHNS-анализаторе varioMICROcube.
Синтез [Mg3(DMF)4(Chdc)3] (I). В стеклянной банке с завинчивающейся крышкой смешивали 375 мг (1.45 ммоль) гексагидрата нитрата магния, 250 мг (1.45 ммоль) транс-1,4-циклогександикарбоновой кислоты и 12.5 мл N,N-диметилформамида. Смесь обрабатывали в ультразвуковой бане в течение 5 мин и нагревали при 120°С в течение 24 ч. Полученный бесцветный крупнокристаллический осадок отфильтровывали на бумажном пористом фильтре, промывали DMF (2 × 10 мл), затем ацетоном (5 мл) и сушили на воздухе. Строение продукта установлено методом РСА. Выход 147 мг (35%). ИК-спектр (KBr; ν, см–1): 3440 ш.cл ν(O–H), 2916 ср ν(Csp3–H), 2854 ср ν(Csp3–H), 1660 с ν(C=O), 1616 с ν(C=O), 1570 ср νas(COO), 1417 с νs(COO). ТGА: потеря массы в интервале ~240–280°C Δm = 33% (расчет на 4DMF).
Синтез [Mg3(DMF)2(NMP)2(Chdc)3] (II). В стеклянной банке с завинчивающейся крышкой смешивали 375 мг (1.45 ммоль) гексагидрата нитрата магния, 250 мг (1.45 ммоль) транс-1,4-циклогександикарбоновой кислоты, 6.25 мл N-метилпирролидона (NMP) и 6.25 мл N,N-диметилформамида. Смесь обрабатывали в ультразвуковой бане в течение 5 мин и нагревали при 120°С в течение 24 ч. Полученный бесцветный крупнокристаллический осадок отфильтровывали на бумажном пористом фильтре, промывали DMF (2 × 10 мл), затем ацетоном (5 мл) и сушили на воздухе. Строение продукта установлено методом РСА. Выход 148 мг (33%).
ИК-спектр (KBr; ν, см–1): 3430 ш.о.cл ν(O–H), 2940, 2913 ср ν(Csp3–H), 2853 ср ν(Csp3–H), 1661 с ν(C=O), 1614 с ν(C=O), 1563 ср νas(COO), 1416 с νs(COO). ТGА: потеря массы при ~220°C Δm = 16% (расчет на 2DMF); в интервале 280–380°C Δm = = 21% (расчет на 2NMP).
Синтез [Mg3(NMP)4(Chdc)3] (III). В стеклянной банке с завинчивающейся крышкой смешивали 100 мг (0.39 ммоль) гексагидрата нитрата магния, 67 мг (0.39 ммоль) транс-1,4-циклогександикарбоновой кислоты и 5.00 мл NMP. Смесь обрабатывали в ультразвуковой бане в течение 10 мин и нагревали при 120°С в течение 48 ч. Полученный бесцветный крупнокристаллический осадок отфильтровывали на бумажном пористом фильтре, промывали NMP (2 × 10 мл), затем ацетоном (5 мл) и сушили на воздухе. Строение продукта установлено методом РСА. Выход 102 мг (27%). ИК-спектр (KBr; ν, см–1): 3420 ш.cл ν(O–H), 2941, 2910 с ν(Csp3–H), 2853 ср ν(Csp3–H), 1665 ср ν(C=O), 1562 ср νas(COO), 1412 с νs(COO). ТGА: потеря массы при ~190°C Δm = 21% (расчет на 2NMP); в интервале 200–350°C Δm = 20% (расчет на 2NMP).
Синтез [Ca3(NMP)4(Chdc)3] (IV). В стеклянной ампуле смешивали 16.0 мг (0.101 ммоль) ацетата кальция, 17.0 мг (0.099 ммоль) транс-1,4-циклогександикарбоновой кислоты и 1.00 мл N-метилпирролидона. Смесь обрабатывали в ультразвуковой бане в течение 10 мин, ампулу запаивали и нагревали при 130°С в течение 24 ч. Полученные крупные кристаллы отбирали для РСА. Строение и состав продукта установили методом РСА.
Синтез [Cd(Ur)(DMF)(Chdc)] (V). В стеклянной банке с завинчивающейся крышкой смешивали 30.0 мг (0.097 ммоль) тетрагидрата нитрата кадмия, 17.0 мг (0.099 ммоль) транс-1,4-циклогександикарбоновой кислоты, 30.0 мг (0.214 ммоль) уротропина, 1.00 мл N,N-диметилформамида и 20.0 мкл (0.216 ммоль) 65%-ного водного раствора HClO4. Смесь обрабатывали в ультразвуковой бане в течение 5 мин и нагревали при 90°С в течение 48 ч. Полученный бесцветный крупнокристаллический осадок отфильтровывали на бумажном пористом фильтре, промывали DMF (3 × 2 мл) и сушили на воздухе. Строение и состава продукта установили методом РСА. Выход 6.7 мг (14%).
ИК-спектр (KBr; ν, см–1): 3394 ш.c ν(O–H), 2990 сл ν(Csp2–H), 2934, 2917 с ν(Csp3–H), 2853 ср ν(Csp3–H), 1650 с ν(C=O), 1556 с νas(COO), 1412 с νs(COO).
РСА. Дифракционные данные для монокристаллов соединений I–IV получены при 130 K на автоматическом дифрактометре Agilent Xcalibur, оснащенном двухкоординатным детектором AtlasS2 (графитовый монохроматор, λ(MoKα) = = 0.71073 Å, ω-сканирование). Интегрирование, учет поглощения, определение параметров элементарной ячейки проводили с использованием пакета программ CrysAlisPro [33]. Дифракционные данные для монокристаллов соединения V накоплены на станции “Белок” Курчатовского источника синхротронного излучения (детектор Rayonix SX165; λ = 0.79272 Å). Интегрирование, учет поглощения, определение параметров элементарной ячейки проводили с использованием программного пакета XDS [34]. Кристаллические структуры расшифрованы с использованием программы SHELXT [35] и уточнены полноматричным МНК в анизотропном (за исключением атомов водорода) приближении с использованием программы SHELXL [36]. Позиции атомов водорода органических лигандов рассчитаны геометрически и уточнены по модели “наездника”. Кристаллографические данные и детали дифракционных экспериментов приведены в табл. 1.
Таблица 1.
Кристаллографические параметры и детали рентгеноструктурного эксперимента структур I–V
| Параметр | Значение | ||||
|---|---|---|---|---|---|
| I | II | III | IV | V | |
| Брутто-формула | C36H58N4O16Mg3 | C40H62N4O16Mg3 | C44H66N4O16Mg3 | C44H66N4O16Ca3 | C17H29N5O5Cd |
| M | 875.79 | 927.86 | 979.93 | 1027.24 | 495.85 |
| Сингония | Моноклинная | Моноклинная | Ромбическая | Моноклинная | Моноклинная |
| Пр. группа | P21/n | P21/n | Pbca | P21/c | P21/n |
| a, Å | 14.1965(12) | 14.3851(12) | 9.7689(4) | 27.4596(10) | 11.464(2) |
| b, Å | 9.8578(8) | 9.7670(6) | 17.7212(7) | 10.4047(3) | 9.728(2) |
| c, Å | 16.8763(14) | 17.1475(13) | 27.0559(13) | 17.7601(6) | 17.056(3) |
| α, град | 90 | 90 | 90 | 90 | 90 |
| β, град | 111.143(10) | 112.257(9) | 90 | 104.697(4) | 92.82(3) |
| γ, град | 90 | 90 | 90 | 90 | 90 |
| V, Å3 | 2202.8(3) | 2229.7(3) | 4683.8(3) | 4908.2(3) | 1899.8 (6) |
| Z | 2 | 2 | 4 | 4 | 4 |
| ρ(выч.), гсм–3 | 1.320 | 1.382 | 1.390 | 1.390 | 1.734 |
| μ, мм–1 | 0.14 | 0.14 | 0.14 | 0.41 | 1.57 |
| F(000) | 932 | 988 | 2088 | 2184 | 1016 |
| Размер кристалла, мм | 0.30 × 0.07 × 0.07 | 0.30 × 0.13 × 0.04 | 0.52 × 0.49 × 0.05 | 0.26 × 0.25 × 0.08 | 0.24 × 0.24 × 0.04 |
| Область сканирования по θ, град | 3.31–25.35 | 3.31–25.35 | 3.45–29.46 | 3.45–25.35 | 2.3–28.5 |
| Диапазон индексов hkl |
–17 ≤ h ≤ 17, –8 ≤ k ≤ 11, –20 ≤ l ≤ 16 |
–14 ≤ h ≤ 17, –11 ≤ k ≤ 11, –20 ≤ l ≤ 17 |
–13 ≤ h ≤ 8, –24 ≤ k ≤ 15, –21 ≤ l ≤ 33 |
–32 ≤ h ≤ 33, –10 ≤ k ≤ 12, –21 ≤ l ≤ 21 |
–13 ≤ h ≤ 3, –11 ≤ k ≤ 11, –20 ≤ l ≤ 20 |
| Измерено отражений/ независимых (Rint) |
10 118/4000 (0.0366) |
10 238/4058 (0.0291) |
16 873/5627 (0.0230) |
24 119/8956 (0.0327) |
12 057/3459 (0.0621) |
| Отражений с I > 2σ(I) | 3177 | 3283 | 4618 | 7932 | 3023 |
| GOOF | 1.122 | 1.019 | 1.031 | 1.230 | 1.038 |
| R-факторы (I > 2σ(I)) |
R1 = 0.0700 , wR1 = 0.154 |
R1 = 0.0595, wR1 = 0.1428 |
R1 = 0.0414, wR1 = 0.0934 |
R1 = 0.0600, wR1 = 0.1195 |
R1 = 0.0321, wR1 = 0.0725 |
| R-факторы (по всем отражениям) | R2 = 0.0883 , wR2 = 0.1610 |
R2 = 0.0786 , wR2 = 0.1560 |
R2 = 0.0556 , wR2 = 0.0986 |
R2 = 0.0694 , wR2 = 0.1223 |
R2 = 0.0382 , wR2 = 0.0750 |
| Δρmax/Δρmin, е Å–3 | 0.69/–0.52 | 0.86/–0.88 | 0.43/–0.39 | 0.61/–0.56 | 0.57/–0.68 |
Полные таблицы межатомных расстояний и валентных углов, координаты атомов и параметры атомных смещений депонированы в Кембриджский банк структурных данных (CIF files CCDC № 2120662 (I), 2120666 (II), 2120664 (III), 2120663 (IV), 2120665 (V); deposit@ccdc.cam.ac.uk или http://www.ccdc.cam.ac.uk), а также могут быть получены у авторов.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Соединения магния I–III получены в сходных сольвотермальных условиях реакцией между гексагидратом нитрата магния и транс-1,4-циклогександикарбоновой кислотой (H2Chdc) при 120°С. Соединения I и II изоструктурны друг другу и кристаллизуются в моноклинной сингонии с пространственной группой P21/n и Z = 2. Неожиданно полученное в NMP соединение III не является изоструктурным его аналогам I и II, полученным в присутствии DMF, и кристаллизуется в ромбической сингонии с пространственной группой Pbca и Z = 4.
Независимая часть структур I–III включает по два атома магния. Ион Mg(1) занимает частное положение и находится в близком к правильному октаэдрическом окружении, состоящем из двух атомов О координированных молекул амидных растворителей, двух атомов О от двух мостиковых карбоксильных групп и двух атомов О хелатирующей карбоксильной группы. Длины связей Mg(1)–Oамид лежат в интервале 2.0344(12)…2.1332(11) Å. Длины связей Mg(1)–OCOO cоставляют от 2.0141(11) до 2.182(3) Å. Ион Mg(2) находится в общем положении и принимает правильное октаэдрическое окружение шестью атомами О от шести карбоксильных групп с длинами связей Mg(2)–OCOO, лежащими в интервале 2.0256(19)–2.1272(10) Å. Два иона Mg(1) и один ион Mg(2) объединены в трехъядерные карбоксилатные блоки {Mg3(O)4-(κ1,κ1-OOCR)4(κ1,κ2-OOCR)2} (рис. 1a–1в), весьма распространенные для Mg2+ и ряда двухвалентных катионов переходных металлов, таких как Zn2+, Co2+ и Mn2+ [37–42]. Блоки соединены мостиковыми транс-1,4-циклогександикарбоксилатами в тригональные слои (рис. 2a, 2б) с однослойной (АА) упаковкой в случаях I, II и двухслойной (ABAB) упаковкой в случае III. Кристаллическая структура соединений I–III является плотноупакованной и не содержит пустот.
Рис. 1.
Трехъядерные карбоксилатные блоки {M3(амид)4(OOCR)6} в структурах I (а), II (б), III (в) и IV (г). Вторые позиции разупорядоченных молекул DMF и NMP изображены полупрозрачными. (На рис. 1–3 атомы M – зеленый, N – синий, О – красный; атомы водорода не показаны.)
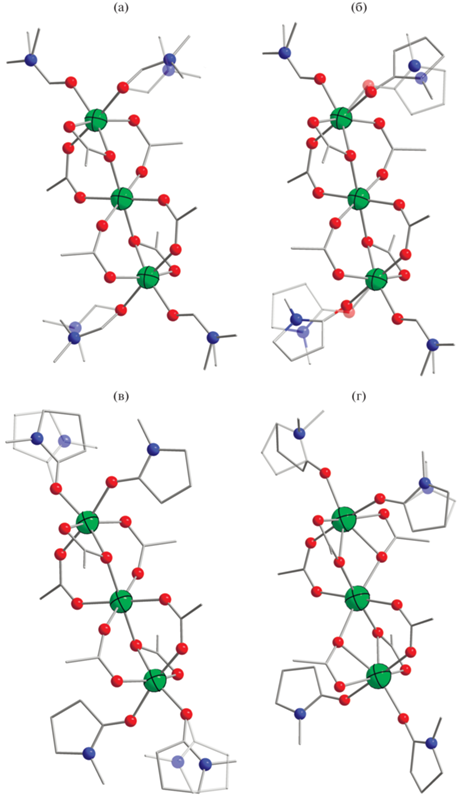
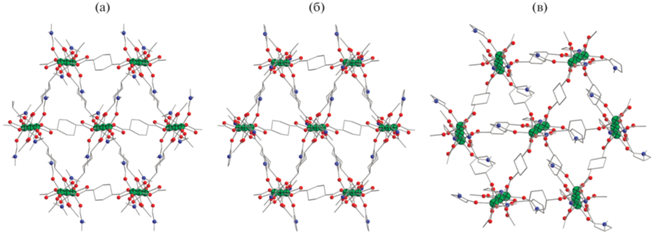
Рис. 2.
Координационные слои {M3(амид)4(Chdc)3} в структурах I (а), III (б) и IV (в). Показана только одна из возможных позиций DMF и NMP.
Соединение IV получено реакцией между ацетатом кальция и H2Chdc в NMP при 130°С. Оно не изоструктурно магниевым I–III и кристаллизуется в моноклинной сингонии с пространственной группой P21/c и Z = 4. Независимая часть включает три атома кальция. Координационная геометрия Ca(1) и Сa(3) принимает вид одношапочного октаэдра с КЧ 7 за счет смены типа координации еще одной карбоксильной группы с κ1,κ1 на κ1,κ2. Длины связей Сa(1/3)–Oамид лежат в интервале 2.287(2)–2.363(3) Å. Длины связей Ca(1/3)–OCOO cоставляют от 2.308(2) до 2.509(2) Å. Ион Ca(2) принимает октаэдрическое окружение с длинами связей Ca(2)–OCOO, лежащими в интервале 2.284(2)–2.348(2) Å. Увеличение КЧ терминальных Ca2+ с 6 до 7 приводит, таким образом, к трехъядерным блокам {Ca3(O)4(κ1,κ1-OOCR)2(κ1,κ2-OOCR)4} (рис. 1г). Несмотря на различие в типе координации, блоки сохраняют связность 6 и формируют аналогичные тригональные слои, включающие мостиковые транс-1,4-циклогександикарбоксилатами (рис. 2в). Слои имеют упаковку АВАВ. Кристаллическая структура IV также является плотной и не содержит пустот.
Соединения I–III являются первыми известными примерами транс-1,4-циклогександикарбоксилатов магния. В литературе ранее был описан один транс-1,4-циклогександикарбоксилат кальция [Ca(H2O)2(Сhdc)] · H2O [43], имеющий трехмерную структуру, построенную на основе полимерных металл-карбоксилатных цепочек, и полученный в водной среде. По всей видимости, химическая природа амидного растворителя (DMF или NMP) является определяющим фактором в образовании новых координационных полимеров щелочноземельных металлов I–IV.
Соединение V получено реакцией между тетрагидратом нитрата кадмия, H2Chdc и уротропином Ur в среде DMF при 90°С. Для полного растворения реагентов производили добавление сильной хлорной кислоты HClO4 в эквимолярном отношении к основанию Ur. Соединение V кристаллизуется в моноклинной сингонии с пространственной группой P21/n и Z = 4. Независимая часть включает один атом кадмия. Его координационное окружение состоит из двух атомов азота от двух бидентатно-мостиковых молекул уротропина, одного атома кислорода координированного растворителя DMF и четырех атомов О от двух бидентатно-хелатирующих карбоксильных групп. Длины связей Сd–N составляют 2.342(2) и 2.487(2) Å. Длина связи Сd–ODMF равна 2.406(2) Å. Длины связей Cd–OCOO лежат в интервале 2.3190(18)–2.4857(19) Å. Координационное число Cd(II), таким образом, равно 7. Металлоцентры (узлы), показанные на рис. 3a, являются четырехсвязными и соединены транс-1,4-циклогександикарбоксилатами вдоль кристаллографической оси c в зигзагообразные цепочки. Цепочки соединены мостиковыми лигандами Ur вдоль оси b с образованием двумерных координационных слоев (рис. 3б). Двуслойная (АВАВ) упаковка слоев в трехмерной кристаллической структуре V также является плотной и не содержит пустот.
Рис. 3.
Фрагмент {Cd(DMF)(Ur)2(OOCR)2} в V и его связывание с соседними атомами Cd(II) (a). Координационный слой в V, вид вдоль оси a (б).

Три транс-1,4-циклогександикарбоксилата кадмия, полученные без использования дополнительных N-донорных лигандов, были известны ранее. Цепочечное соединение [Cd(H2O)2(C8H10O4)], построенное на основе одноядерных фрагментов, было получено в водной среде [38] с использованием пиперидина как модулятора основности среды. Трехмерный МОКП [Cd(H2O)(Сhdc)] ⋅ 0.5CH3CN, построенный на основе полимерных металл-карбоксилатных цепочек, был получен нами ранее в смеси воды и ацетонитрила с использованием 1,4-диазабицикло[2.2.2]октана (Dabco) как модулятора основности [44]. В DMF без использования модуляторов был получен трехмерный каркас [Cd2(DMF)(Chdc)2], также построенный на основе полимерных карбоксилатных цепочек [45]. По всей видимости, уротропин в среде DMF является достаточно сильным лигандом для образования координационных решеток c его участием, в отличие от рассмотренных выше случаев пиперидина в воде и Dabco в водно-ацетонитрильных смесях. Подобные примеры проявления двойственной природы уротропина (основание–лиганд) в синтезе МОКП были опубликованы ранее [40, 44, 46–48].
Термическая стабильность соединений магния I–III охарактеризована методом ТГА (рис. 4). Соединение [Mg3(DMF)4(Chdc)3] (I) теряет координированный растворитель при 240–280°С. Масса твердого остатка при 600°С составляет 21% и соответствует оксиду магния (теор. 17%) с примесью углерода, возникающей, по всей видимости, из-за неполного улетучивания органических линкеров. Соединение [Mg3(DMF)2(NMP)2(Chdc)3] (II) ступенчато теряет координированный растворитель при 220°С (DMF) и в интервале 280–380°C (NMP). Масса твердого остатка при 600°С составляет 20% и соответствует оксиду магния (теор. 13%) с продуктами термического разложения органических лигандов. Соединение [Mg3(NMP)4-(Chdc)3] (III) ступенчато теряет координированный растворитель при 190°С (2NMP) и в интервале 200–350°C (2NMP). Масса твердого остатка при 600°С составляет 17% и также соответствует оксиду магния (теор. 12%) с продуктами термического разложения органических лигандов. Снижение термической стабильности в ряду I > II > III, находящееся в необычной обратной зависимости от температуры кипения растворителя (Ткип(DMF) = 153°C < Ткип(NMP) = 202 °C), вероятно, связано с увеличением молекулярного размера растворителя, приводящим к “разрыхлению” кристаллической структуры координационных полимеров, выражаемому рядом V/Z: 1101.4 Å3 (I) < 1114.9 Å3 (II) < 1171.0 Å3 (III).
Таким образом, в работе получены и структурно охарактеризованы пять новых слоистых м-еталл-органических координационных полимеров – транс-1,4-циклогександикарбоксилатов двухвалентных металлов. Соединения магния I–III и кальция IV построены на основе трехъядерных карбоксилатных блоков {M3(OOCR)6}, которые формируют шестисвязанные координационные слои тригональной геометрии. Соединение кадмия V построено на основе одноядерных фрагментов {Cd(NUr)2-(DMF)(OOCR)2}, однако также является слоистым за счет мостиковой координации дитопных уротропина и Chdc2–. Соединения I–III охарактеризованы методами ИК-спектроскопии, элементного и термогравиметрического анализов. По данным ТГА получен необычный ряд термической стабильности структурно близких МОКП магния [Mg3(DMF)4(Сhdc)3] > > [Mg3-(DMF)2(NMP)2(Сhdc)3] > [Mg3(NMP)4-(Сhdc)3], находящейся в обратной зависимости от температуры кипения координированного растворителя. Подобный эффект отнесен к увеличению молекулярного размера растворителя, приводящему к “разрыхлению” упаковки координационных решеток в кристалле.
Авторы заявляют, что у них нет конфликта интересов.
Список литературы
Ha J., Lee J.H., Moon H.R. // Inorg. Chem. Front. 2020. V. 7. P. 12.
Sapianik A.A., Fedin V.P. // Russ. J. Coord. Chem. 2020. V. 46. P. 443. https://doi.org/10.1134/S1070328420060093
Litvinova Y.M., Gayfulin Y.M., Samsonenko D.G. et al. // Russ. Chem. Bull. 2020. V. 69. P. 1264.
Ji Q.-S., Wen W.-F., Liu S.Z. et al. // Inorg. Chim. Acta. 2021. V. 519. P. 120278.
Łyszczek R., Rusinek I., Ostasz A. et al. // Materials. 2021. V. 14. 4871.
Grebenyuk D., Zobel M., Polentarutti M. et al. // Inorg. Chem. 2021. V. 60. P. 8049.
Kalmutzki M.J., Hanikel N., Yaghi O.M. // Sci. Adv. 2018. V. 4. 9180.
Bolotov V.A., Kovalenko K.A., Samsonenko D.G. et al. // Inorg. Chem. 2018. V. 57. P. 5074.
Demakov P.A., Volynkin S.S., Samsonenko D.G. et al. // Molecules. 2020. V. 25. 4396.
Lysova A.A., Samsonenko D.G., Kovalenko K.A. et al. // Angew. Chem. Int. Ed. 2020. V. 59. P. 20561.
Yuan R., Chen H., Zhu Q.-Q. et al. // J. Solid. State Chem. 2021. V. 297. 122036.
Jiang H., Alezi D., Eddaoudi M. // Nat. Rev. Mater. 2021. V. 6. P. 466.
He T., Kong X.-J., Li J.-R. // Acc. Chem. Res. 2021. V. 54. P. 3083.
Tan Y.C., Zeng H.C. // ChemCatChem. 2019. V. 11. P. 3138.
Koshevoi E.I., Samsonenko D.G., Dorovatovskii P.V. et al. // J. Struct. Chem. 2020. V. 61. P. 431.
Warfsmann J., Tokay B., Champness N.R. // CrystEngComm. 2020. V. 22. P. 1009.
Demakov P.A., Yudina Y.A., Samsonenko D.G. et al. // J. Struct. Chem. 2021. V. 62. P. 403.
Zorina-Tikhonova E.N., Chistyakov A.S., Matyukhina A.K. et al. // J. Struct. Chem. 2021. V. 62. P. 1209.
Marakulin A.V., Lysova A.A., Samsonenko D.G. et al. // Russ. Chem. Bull. 2020. V. 69. P. 360.
Dubskikh V.A., Lysova A.A., Samsonenko D.G. et al. // CrystEngComm. 2020. V. 22. P. 6295.
Xian S., Lin Y., Wang H. et al. // Small. 2021. V. 17. P. 2005165.
Rambabu D., Lakraychi A.E., Wang J. et al. // J. Am. Chem. Soc. 2021. V. 143. P. 11641.
Zorina-Tikhonova E.N., Chistyakov A.S., Kiskin M.A. et al. // Russ. J. Coord. Chem. 2021. V. 47. P. 409. https://doi.org/10.1134/S1070328421060099
Steinke F., Javed A., Wöhlbrandt S. et al. // Dalton Trans. 2021. V. 50. P. 13572.
Barsukova M.O., Kovalenko K.A., Nizovtsev A.S. et al. // Inorg. Chem. 2021. V. 60. P. 2996.
Wang T., Chang M., Yan T. et al. // Ind. Eng. Chem. Res. 2021. V. 60. P. 5976.
Guo X.-Z., Chen S.-S., Li W.-D. et al. // ACS Omega. 2019. V. 4. P. 11540.
Marchenko R.D., Lysova A.A., Samsonenko D.G. et al. // Polyhedron. 2020. V. 177. 114330.
Zhang L.-Y., Lu L.-P., Zhu M.-L. // J. Chem. Cryst. 2020. V. 50. P. 122.
Pavlov D.I., Ryadun A.A., Samsonenko D.G. et al. // Russ. Chem. Bull. 2021. V. 70. P. 857.
Zhang Y.-N., Chen J.-L., Su C.-Y. et al. // J. Solid State Chem. 2021. V. 302. P. 122407.
Smirnova K.S., Sukhikh T.S., Adonin S.A. et al. // J. Struct. Chem. 2021. V. 62. P. 718.
CrysAlisPro Software system. Version 1.171.40.84a. 2020.
Kabsch W. // Acta Crystallogr. D. 2010. V. 66. P. 125.
Sheldrick G.M. // Acta Crystallogr. A. 2015. V. 71. P. 3.
Sheldrick G.M. // Acta Crystallogr. C. 2015. V. 71. P. 3.
Williams C.A., Blake A.J., Hubberstey P. et al. // Chem. Commun. 2005. V. 43. P. 5435.
Thirumurugan A., Avinash M.B., Rao C.N.R. // Dalton Trans. 2006. V. 1. P. 221.
Wang L., Wang L., Song T. et al. // J. Solid State Chem. 2012. V. 190. P. 208.
Demakov P.A., Sapchenko S.A., Samsonenko D.G. et al. // Russ. Chem. Bull. 2018. V. 67. P. 490. https://doi.org/10.1007/s11172-018-2098-3
Lysova A.A., Samsonenko D.G., Kovalenko K.A. et al. // Russ. Chem. Bull. 2019. V. 68. P. 793.
Dubskikh V.A., Lysova A.A., Samsonenko D.G. et al. // Molecules. 2021. V. 26. 1269.
Wang X., San L.K., Nguyen H. et al. // J. Coord. Chem. 2013. V. 66. P. 826.
Demakov P.A., Bogomyakov A.S., Urlukov A.S. et al. // Materials. 2020. V. 13. 486.
Yoon M., Sun H.J., Lee D.H. et al. // Bull. Korean Chem. Soc. 2012. V. 33. P. 3111.
Sapchenko S.A., Saparbaev E.S., Samsonenko D.G. et al. // Russ. J. Coord. Chem. 2013. V. 39. P. 549. https://doi.org/10.1134/S1070328413080071
Sapchenko S.A., Samsonenko D.G., Fedin V.P. // Polyhedron. 2013. V. 55. P. 179.
Sapchenko S.A., Barsukova M.O., Nokhrina T.V. et al. // Russ. Chem. Bull. 2020. V. 69. P. 461.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия



