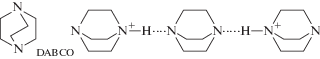Кристаллография, 2022, T. 67, № 2, стр. 249-253
Кристаллическая и молекулярная структура анион-радикальной соли (N-Me-DABCO)(TCNQ)2
Т. Н. Стародуб 1, *, М. А. Колосов 2, Д. Фенске 3, 4, 5, О. Фур 4, 5, С. В. Шишкина 6, В. Пиотровска 1
1 Институт химии Университета им. Яна Кохановского
Кельце, Польша
2 Харьковский национальный университет им. В.Н. Каразина
Харьков, Украина
3 Институт неорганической химии Технологического института
Карлсруэ, Германия
4 Институт нанотехнологии и Карлсруэ наномикроотделение Технологического института Карлсруэ
Еггеншттайн-Деопольдсгафен, Германия
5 Лен-институт функциональных материалов Института химии и химической инженерии
Университета Сень-Ят-Сена
Гуанчжоу, Китай
6 НПО “Институт монокристаллов”, НАНУ
Харьков, Украина
* E-mail: tstarodub@ujk.edu.pl
Поступила в редакцию 21.01.2021
После доработки 04.03.2021
Принята к публикации 15.03.2021
- EDN: LYEZZO
- DOI: 10.31857/S0023476122020217
Аннотация
Синтезирована анион-радикальная соль 7,7,8,8-тетрацианохинодиметана (TCNQ) сложного состава: (N–Me–DABCO)(TCNQ)2 (1). Кристаллическая структура 1 определена методом рентгеновской дифракции. Структура соли представляет собой практически гомогенные стопки частиц TCNQ, разделенные слоями катионов. В стопках наблюдается чередование межплоскостных расстояний: 3.25 и 3.29 Å соответственно. Вследствие чередования расстояний и гомогенного распределения заряда в стопках в структуре формируются проводящие каналы, обусловливающие проявление свойств органического металла или узкозонного полупроводника, что подтверждается ИК-спектрами: в них наблюдаются особенности, связанные с электрон-фононным взаимодействием. В частности, колебательные линии наблюдаются на фоне непрерывного поглощения – ширина запрещенной зоны не превышает 0.06 эВ. В результате проявляются линии полносимметричных колебаний (эти линии в отсутствие электрон-фононного взаимодействия в ИК-спектрах запрещены).
ВВЕДЕНИЕ
Анион-радикальные соли (АРС) на основе 7,7,8,8-тетрацианохинодиметана (TCNQ) привелекают интерес с 60-х годов прошлого столетия [1, 2]. Такое внимание обусловлено тем, что АРС TCNQ обладают рядом необычных свойств: среди них обнаружены первые органические металлы; АРС TCNQ могут плавиться без разложения, что открывает широкие возможности использования органических проводников, например, при производстве батарей с твердым электролитом [3, 4]; на основе АРС TCNQ можно создавать ультратонкие пленки. Эти АРС могут быть использованы для производства электронных устройств, размеры которых сравнимы с молекулярными размерами [5]; проводящие АРС TCNQ можно применять для получения эффективных переходов в кремниевых полупроводниках или в полупроводниковых устройствах на основе сульфида кадмия [6]. Использование в синтезе АРС катионов TCNQ, содержащих донорные атомы, способных к образованию межмолекулярных связей, открывает возможность синтеза проводящих АРС TCNQ и спиновых лестниц [7, 8].
В [9] описаны использование одного из таких катионов, а именно, 1,4-диазабицикло[2.2.2]октана (DABCO), и его реакция с пара-бис (дицианометил)-бензолом (H2TCNQ). В результате этой реакции образуются бесцветные кристаллы соли, содержащей дианион TCNQ2– и супрамолекулярный катион [(DABCO–H)2DABCO]2+ (рис. 1). Заметим, что в этом случае TCNQH2 ведет себя как кислота C–H, а DABCO – как акцептор протонов (основание).
С целью расширения данных проведено исследование новой АРС TCNQ с катионом на основе DABCO: представлены результаты структурных и оптических измерений. Использование данного катиона интересно и с той точки зрения, что DABCO образует кристаллические аддукты состава 2 : 1 с пероксидом водорода и диоксидом серы, является тушителем синглетного кислорода и эффективным антиоксидантом, может быть применен для повышения качества красителей. DABCO используют в лазерах, а также для фиксации образцов во флуоресцентной микроскопии (в комбинации с глицерином) [10].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе TCNQ фирмы Aldrich был дополнительно очищен перекристаллизацией. Соль (N–Me–DABCO)+I– синтезировали по реакции
Для синтеза АРС использовали реакцию
Горячие растворы {N(C2H4)3N+–CH3}I– и TCNQ в ацетонитриле смешивали и помещали в сосуд Дьюара для медленного охлаждения. В течение недели образовывались темно-зеленые кристаллы, которые отделяли, промывали холодным ацетонитрилом и диэтиловым эфиром и сушили на воздухе.
Состав АРС был определен спектрофотометрически, как описано в [7]. Он соответствует формуле {N (C2H4)3N+–CH3} (TCNQ)–2 (1). Элементный анализ синтезированной АРС выполнен с помощью анализатора VarioMICRO Superuser. Найдено: C 69.43, N 26.30, H 4.42 мас. %. Для C31H23N10 вычислено: C 69.52, N 26.15, H 4.33 мас. %. Температура плавления 217°C.
Рентгенографическое исследование 1 проведено на монокристальном дифрактометре Stoe StadiVari при 180 К (мультислойная оптика, метод вращений). Коррекция сферического поглощения проведена с помощью STOE LANA. Структура расшифрована прямыми методами с последующим построением разностного синтеза Фурье с использованием программного обеспечения SHELXS [12] и уточнена полноматричным методом наименьших квадратов в анизотропном приближении смещений всех атомов аниона TCNQ, кроме водорода, с помощью программного обеспечения SHELXTL [13].
Катион разупорядочен по двум одинаково заселенным позициям. Разупорядоченные части симметричны относительно центра инверсии. Поэтому все атомы, из которых состоит катион, кроме атомов водорода, уточнены в изотропном приближении смещений, также были наложены ограничения на длины связей N–Csp3 (1.47 Å) и Csp3–Csp3 (1.54 Å). Позиции атомов водорода определены из разностных карт электронной плотности и уточнены в изотропном приближении для аниона TCNQ. Атомы водорода в катионе были помещены в идеализированные положения и уточнены по модели “наездника” с Uiso = = nUeq (n = 1.5 для метильной группы и n = 1.2 для других атомов водорода) атома-носителя.
Основные кристаллографические и экспериментальные данные представлены в табл. 1. Длины связей и углы указаны в табл. 2, 3.
Таблица 1.
Кристаллографические характеристики, данные эксперимента и результаты уточнения структуры 1
| Брутто-формула | C31H23N10 |
|---|---|
| Система, пр. гр., Z | Триклинная, P, 1 |
| Т, К | 180 |
| а, b, c, Å | 7.36 (1), 7.55 (1), 13.765 (2) |
| α, β, γ, град | 92.3 (1), 92.60 (14), 117.46 (14) |
| V, Å3 | 677.49 (2) |
| Dвыч, г/см3 | 1.313 |
| μ, мм–1 | 0.084 |
| Размеры образца, мм | 0.18 × 0.04 × 0.03 |
| Излучение; λ, Å | MoKα; 0.71073 |
| Дифрактометр | Stoe StadiVari |
| Тип сканирования | ω |
| 2θmax, град | 56 |
| Число отражений: измеренных, Rint/независимых с I > 2σ (I) | 5621, 0.026/3155 |
| Rsigma | 0.060 |
| R1/wR2 | 0.095/0.314 |
| Δρmin/Δρmax, э/Å3 | –0.61/1.62 |
| Программы | SHELXS [12], SHELXTL [13] |
Таблица 2.
Длины связей в структуре 1
| Связь | Длина, Å | Связь | Длина, Å |
|---|---|---|---|
| N1–C8 | 1.141(4) | C7–С9 | 1.438(4) |
| N2–C9 | 1.142(4) | C10–C11 | 1.429(5) |
| N3–C11 | 1.139(4) | C10–C12 | 1.419(5) |
| N4–C12 | 1.150(5) | N5–C13 | 1.337(9) |
| C1–C2 | 1.432(4) | N5–C14 | 1.531(9) |
| C1–C6 | 1.435(4) | N5–C16 | 1.512(9) |
| C1–C7 | 1.388(4) | N5–C18 | 1.468(10) |
| C2–C3 | 1.354(5) | N6–C15 | 1.541(9) |
| C3–C4 | 1.440(4) | N6–C17 | 1.476(9) |
| C4–C5 | 1.425(4) | N6–C19 | 1.492(9) |
| C4–C10 | 1.403(4) | C14–C15 | 1.436(10) |
| C5–C6 | 1.353(4) | C16–C17 | 1.507(11) |
| C7–C8 | 1.423(5) | C18–C19 | 1.533(10) |
Таблица 3.
Валентные углы в структуре 1
| Связь | Угол, град | Связь | Угол, град |
|---|---|---|---|
| C2–C1–С6 | 117.6(3) | N3–С11–С10 | 178.8(4) |
| C7–С1–С2 | 121.3(3) | N4–С12–С10 | 178.7(4) |
| C7–С1–С6 | 121.1(3) | C13–N5–C14 | 116.4(11) |
| C3–С2–С1 | 121.1(3) | C13–N5–C16 | 103.3(10) |
| C2–С3–С4 | 121.0(3) | C13–N5–C18 | 121.7(11) |
| C5–С4–С3 | 117.9(3) | C16–N5–C14 | 102.8(6) |
| C10–С4–С3 | 121.2(3) | C18–N5–C14 | 103.5(6) |
| C10–С4–С5 | 120.9(3) | C18–N5–C16 | 107.2(7) |
| C6–С5–С4 | 121.0(3) | C17–N6–C15 | 106.6(6) |
| C5–С6–С1 | 121.4(3) | C17–N6–C19 | 107.6(6) |
| C1–С7–С8 | 122.0(3) | C19–N6–C15 | 105.4(6) |
| C1–С7–С9 | 122.6(3) | C15–C14–N5 | 117.0(7) |
| C8–С7–С9 | 115.4(3) | C14–C15–N6 | 110.5(6) |
| N1–С8–С7 | 178.8(4) | C17–C16–N5 | 113.3(7) |
| N2–С9–С7 | 178.8(4) | N6–C17–C16 | 112.7(7) |
| C4–С10–С11 | 121.7(3) | N5–C18–C19 | 114.0(7) |
| C4–С10–С12 | 122.3(3) | N6–C19–C18 | 111.3(7) |
| C12–С10–С11 | 116.0(3) |
Спектры ИК-поглощения порошкообразных образцов 1 регистрировали в диапазоне частот от 500 до 4000 см–1 при комнатной температуре на спектрометре Nicolet 380, диск KBr.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Исследуемая соль образована двумя анион-радикалами TCNQ и катионом N–Me–DABCO (рис. 2). Анион-радикал практически плоский, все его атомы лежат внутри плоскости с точностью до 0.05 Å. Катион находится в особом положении по отношению к центру симметрии и разупорядочен по двум одинаково заселенным позициям.
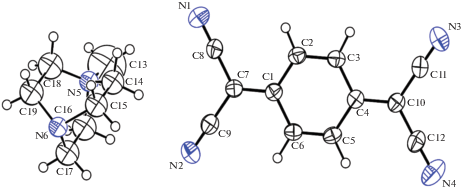
Рис. 2.
Структуры молекул анион-радикала ${\text{TCN}}{{{\text{Q}}}^{{ \bullet --}}}$ и катиона N–Me–DABCO согласно данным рентгеноструктурного анализа. Тепловые эллипсоиды для TCNQ даны для уровня вероятности 50%.
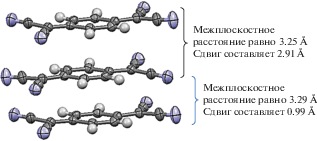
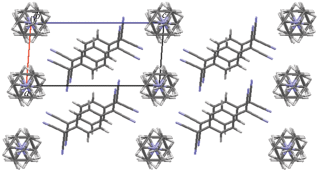
В кристаллах АРС 1 можно выделить слои катионов и анионов (рис. 3). Слои анионов образованы стопками, в которых молекулы TCNQ связаны стэкинг-взаимодействиями. Стэкинг-взаимодействия молекулы TCNQ с двумя соседними молекулами внутри стопки разные (рис. 4). Катионы и анионы соединены очень слабыми водородными связями: C(18)–H(18b)⋅⋅⋅N(4) (x, y, 1 + z; H⋅⋅⋅N 2.62 Å, C–H⋅⋅⋅N 151°); C(17)–H(17a)⋅⋅⋅N(1) (x – 1, y – 1, z; H⋅⋅⋅N 2.60 Å, C–H⋅⋅⋅N 99°); C(13)–H(13c)⋅⋅⋅N(4) (–x, 1 – y, 1 – z; H⋅⋅⋅N 2.39 Å, C–H⋅⋅⋅N 117°).
Рис. 3.
Упаковка катионов и анионов в кристаллах 1. Проекция вдоль кристаллографического направления [010].
Как следует из формулы АРС 1, средний заряд на частице TCNQ равен –1/2e. Заряд можно оценить на основе структурных данных: если заряд на частице TCNQ–q уменьшается, это сопровождается изменением структуры от хиноидной до ароматической. При этом происходит закономерное изменение длин связей C–C.
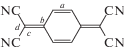
Кистенмахером [14, 15] предложена формула, позволяющая рассчитать заряд молекулы TCNQ на основе длин связей (табл. 2) b, c и d в частице TCNQ:
Используя длины связей в АРС 1 (табл. 2), получили заряд частицы TCNQ в АРС 1: q = –0.43e.Обычно в АРС состава Kt+ (${\text{TCN}}{{{\text{Q}}}^{{ \bullet --}}}$)2 стопки TCNQ тетрамеризованы из-за неустойчивости Пайерлса [1]. Если учесть, что в АРС 1 стопки однородны, то она должна обладать свойствами органического металла. Переход Пайерлса должен реализовываться при низких температурах. Как видно из рис. 2, АРС 1 должна быть сильно анизотропной, поскольку стопки TCNQ разделены слоями катионов, которые не образуют коротких контактов с анион-радикалами.
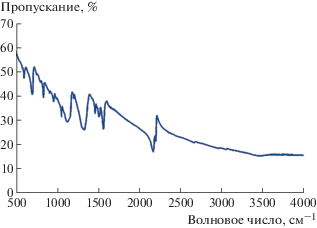
Вывод о высокой электропроводности АРС 1 подтверждают данные ИК-спектроскопии (рис. 5). Как известно [16, 17], в АРС TCNQ имеет место сильное взаимодействие электронов проводимости с внутримолекулярными фононами. Это взаимодействие определяет ряд особенностей ИК-спектров солей TCNQ, в частности наличие очень интенсивных и аномально широких линий поглощения в области 500, 1100–1300 и 2100–2200 см–1 в ИК-спектре соли 1 (рис. 5). В спектре АРС 1 наблюдается непрерывное поглощение излучения во всем исследуемом диапазоне на фоне электрон-фононного взаимодействия, в результате которого становятся активными полносимметричные колебания (тип Ag), разрешенные только в спектрах комбинационного рассеяния света. Начало непрерывного поглощения в ИК-спектре соли 1 – 500 см–1 – позволяет оценить ширину запрещенной зоны (hν0= Δ, где ν0 – начало непрерывного поглощения, Δ – ширина запрещенной зоны) в 0.06 эВ. Таким образом, АРС 1 представляет собой либо органический металл, либо узкозонный полупроводник.
ЗАКЛЮЧЕНИЕ
Синтезирована новая анион-радикальная соль TCNQ с алициклическим диамином, которая содержит почти однородные стопки молекул TCNQ. Эти стопки практически изолированы. Согласно теории одномерных систем в стопках должна происходить тетрамеризация. Однако данные рентгеноструктурного анализа показывают, что тетрамеризация стопок очень слабая. Строение кристаллов 1 благоприятствует образованию проводящего состояния соли, что подтверждается данными ИК-спектроскопии. Использование в качестве противоиона органического катиона N–Me–DABCO либо других катионов на основе DABCO может привести к появлению новых органических проводников на основе АРС TCNQ.
Окончательные координаты атомов и кристаллографические данные АРС 1 депонированы в Кембриджский кристаллографический центр, 12 Union Road, CB2 1EZ, UK (факс +44 1223 336 033; электронная почта: deposit@ccdc.cam.ac.uk) и доступны по запросу с указанием CCDC 2007582.
Список литературы
Melby L.R., Harder R.J., Hertler W.R. et al. // J. Am. Chem. Soc. 1962. V. 84. P. 3374. https://doi.org/10.1021/ja00876a029
Starodub V.A., Starodub T.N. // Russ. Chem. Rev. 2014. V. 83. № 5. P. 391. https://doi.org/10.1070/RC2014v083n05ABEH004299
Starodub V.A., Gluzman E.M., Krikunov K.V. et al. // SSSR Byull. Izobret. 1991. V. 45. P. 92.
Starodub V.A., Gluzman E.M., Pokhodnya K.I., Va-lakh M.Ya. // Theor. Exper. Chem. 1993. V. 29. P. 240. https://doi.org/10.1007/BF00530303
Murata T., Enomoto Y., Saito G. // Solid State Sci. 2008. V.10. P. 1364. https://doi.org/10.1016/j.solidstatesciences.2008.01.007
Jeszka J.K., Tracz A., Boiteux G. et al. // Synth. Met. 1995. V. 71. P. 2205. https://doi.org/10.1016/0379-6779(94)03223-S
Ziolkovsky D.V., Kravchenko A.V., Starodub V.A. et al. // Functional Mater. 2005. V. 12. P. 577. http://dspace.nbuv.gov.ua/handle/123456789/138860
Lapinski A., Golub M., Starodub V.A. Proceed. 10th Int. Conf. ERPOS (Electrical and Related Properties of ORGANIC Solids and Polymers). Cargese, 2005. P. A094.
Hudson T.A., Robson R. // Cryst. Growth Des. 2009. V. 9. P. 1658. https://doi.org/10.1021/cg801400j
Bugaenko D.I., Karchava A.V., Yurovskaya M.A. // Chem. Heterocyclic Comp. 2020. V. 56. № 2. P. 128. https://doi.org/10.1007/s10593-020-02636-1
Samulak B.M., Niu Sh., Andrews Ph.C., Ruotolo B.T. // Anal. Chem. 2016. V. 88. № 10. P. 5290. https://doi.org/10.1021/acs.analchem.6b00518
Sheldrick G.M. // Acta Cryst. A. 2008. V. 64. P. 112. https://doi.org/10.1107/S0108767307043930
Sheldrick G.M. // Acta Cryst. C. 2015. V. 71. P. 3. https://doi.org/10.1107/S2053229614024218
Kistenmacher Th.J., Emge Th.J., Bloch A.N., Cowan D.O. // Acta Cryst. B. 1982. V. 38. P. 1193. https://doi.org/10.1107/S0567740882005275
Üngör Ö., Phan H., Choi E.S. et al. // J. Magn. Magn. Mater. 2020. V. 497. P. 165984. https://doi.org/10.1016/j.jmmm.2019.165984
Starodub V.A., Starodub T.N., Kazheva O.N., Bregadze V.I. Materials of Modern Electronics and Spintronics. M.: Fizmatlit, 2018. 424 p.
Lipari N.O., Duke C.B., Pietronero L. // J. Chem. Phys. 1976. V. 65. P. 1165. https://doi.org/10.1063/1.433192
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография