Кристаллография, 2022, T. 67, № 4, стр. 617-622
Структурные особенности комплекса Cu(II) с 5-фенилтетразолат анионом и 4,4'-диметил-2,2'-бипиридином
К. С. Смирнова 1, Ю. А. Голубева 1, Е. В. Лидер 1, *
1 Институт неорганической химии им. А.В. Николаева СО РАН
Новосибирск, Россия
* E-mail: lisalider@ngs.ru
Поступила в редакцию 23.12.2021
После доработки 23.12.2021
Принята к публикации 09.02.2022
- EDN: UXXAIO
- DOI: 10.31857/S0023476122040154
Аннотация
Определена кристаллическая структура биядерного комплекса Cu(II) с 5-фенилтетразолом и 4,4'-диметил-2,2'-бипиридином (dmbipy) – [Cu2(dmbipy)2L4]. Комплекс кристаллизуется в моноклинной пр. гр. P21/c. Искаженное квадратно-пирамидальное окружение атомов Cu(II) образовано пятью атомами азота, принадлежащих трем 5-фенилтетразолат анионам и одной молекуле dmbipy. Благодаря наличию межмолекулярных взаимодействий π⋅⋅⋅π и C–H⋅⋅⋅π биядерные фрагменты соединяются в супрамолекулярную слоистую структуру. Энергия связи рассчитана в рамках теории функционала плотности для двух моделей комплекса [Cu2(dmbipy)2L4] с различными способами координации мостикового 5-фенилтетразола.
ВВЕДЕНИЕ
Азотсодержащие гетероциклы широко используются в качестве строительных блоков при синтезе потенциальных лекарственных средств, поскольку атомы азота способны легко образовывать водородные связи с различными биологическими мишенями [1, 2]. В частности, большой интерес вызывает возможное использование тетразолов и их комплексов в медицине [3, 4]. Известно более 20 различных видов биологической активности соединений, в состав которых входит тетразольный цикл [5]. Однако до недавнего времени тетразол и комплексы на его основе редко изучали в качестве противоопухолевых агентов. Одной из возможных причин является склонность тетразолов к образованию практически нерастворимых координационных полимеров, что ограничивает их использование в медицине.
Удалось частично решить проблему растворимости координационных соединений на основе тетразола за счет синтеза разнолигандных комплексов с производными тетразола и пиридина. В частности, получена серия цитотоксичных комплексов Cu(II) на основе тетразола, 5-фенилтетразола, 5-метилтетразола, 5-бензилтетразола и 2,2'-бипиридина/1,10-фенантролина [6–9]. Синтез комплекса Cu(II) с 5-фенилтетразолом и 4,4'-диметил-2,2'-бипиридином описан в [9], однако комплекс не был структурно охарактеризован. Чтобы прогнозировать количественные характеристики биологической активности, необходимо знать структурные особенности соединений. В связи с этим в настоящей работе определена кристаллическая структура биядерного комплекса Cu(II) с 5-фенилтетразолом и 4,4'-диметил-2,2'-бипиридином (dmbipy) – координационного соединения [Cu2(dmbipy)2L4] – и проведен анализ его структурных особенностей.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Комплекс [Cu2(dmbipy)2L4] синтезирован по методике, описанной в [9]. После отделения осадка комплекса через неделю из водно-этанольного маточного раствора удалось получить монокристаллы [Cu2(dmbipy)2L4], пригодные для рентгеноструктурного анализа (РСА).
Рентгенофазовый анализ (РФА) проводили на дифрактометре Shimadzu XRD-7000 (CuKα-излучение, Ni-фильтр, диапазон 2θ 5°–50°, шаг 0.03°, накопление 1 с). Поликристаллы для РФА истирали в агатовой ступке в присутствии гептана. Полученную суспензию наносили на полированную сторону стандартной кварцевой кюветы. После высыхания гептана образец представлял собой тонкий ровный слой (толщина ~100 мкм).
Дифрактометр Bruker D8 Venture (излучение MoKα, λ = 0.71073 Å, графитовый монохроматор) применяли для сбора данных РСА. Поправки на поглощение вводили с использованием программы SADABS [10]. Кристаллическая структура комплекса Cu(II) была расшифрована и уточнена с помощью программного обеспечения OLEX2 [11], SHELXT [12] и SHELXL [13]. Параметры смещений всех атомов, кроме водорода, уточнены в анизотропном приближении. Положения атомов водорода были рассчитаны в соответствии с их геометрическими позициями и уточнены с использованием модели “наездника”. Кристаллографические данные и информация об уточненной структуре приведены в табл. 1. Они депонированы в Кембриджскую базу структурных данных (CCDC № 2110408) и могут быть получены у авторов или по адресу: https://www.ccdc.cam. ac.uk/structures/.
Таблица 1.
Кристаллографические характеристики, данные эксперимента и результаты уточнения структуры [Cu2(dmbipy)2L4]
| Брутто-формула | C52H44Cu2N20 |
|---|---|
| Молярная масса | 1076.15 |
| Т, К | 100.0 |
| Сингония, пр. гр., Z | Моноклинная, P21/c, 2 |
| a, b, c, Å | 13.8324(6), 10.2228(4), 16.9577(8) |
| β, град | 95.503(2) |
| V, Å3 | 2386.87(18) |
| ρвыч, г/см3 | 1.497 |
| μ, мм–1 | 0.953 |
| Размер кристалла, мм | 0.162 × 0.04 × 0.018 |
| 2θ, град | 4.66–61.11 |
| Пределы h, k, l | –19 ≤ h ≤ 19, –14 ≤ k ≤ 14, –24 ≤ l ≤ 24 |
| Общее число отражений | 95250 |
| Число независимых отражений | 7297 [Rint = 0.0526, Rσ = 0.0232] |
| Число уточняемых параметров/ограничений | 336/0 |
| GooF по F 2 | 1.042 |
| R1/wR2 [I > = 2σ (I)] | 0.0309/0.0749 |
| R1/wR2 [все данные] | 0.0397/0.0794 |
| Δρmin/Δρmax, э/Å3 | –0.45/0.42 |
Квантово-химические расчеты проведены на вычислительном кластере ИНХ СО РАН с помощью программы Amsterdam Density Functional (ADF) в рамках теории функционала плотности (Density Functional Theory – DFT) [14]. В расчетах использовали обобщенно-градиентное приближение (Generalized Gradient Approximation – GGA), функционал плотности Perdew–Burke–Ernzerhof (PBE) [15] в комбинации с полноэлектронным базисным набором TZ2P [16]. Анализ поверхности Хиршфельда для комплекса Cu(II) был проведен с помощью программы CrystalExplorer17 [17], и получена 2D-развертка этой поверхности.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
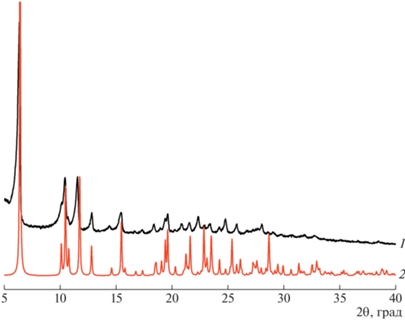
Комплекс Cu(II) с 5-фенилтетразолом и 4,4'-диметил-2,2'-бипиридином [Cu(dmbipy)L2] был получен ранее в результате взаимодействия водного раствора ацетата Cu(II) c dmbipy, растворенным в этаноле, и последующим добавлением этанольного раствора фенилтетразола [9]. Комплекс не был структурно охарактеризован, однако на основании данных электронного парамагнитного резонанса (ЭПР) было сделано предположение, что он является моноядерным ввиду отсутствия расщепления в нулевом поле и разрешенного по g-тензору ЭПР-спектра, что характерно для моноядерных комплексов Cu(II). В настоящей работе для получения комплекса использована методика [9], в результате чего после отделения основного осадка комплекса спустя неделю из водно-этанольного маточного раствора удалось выделить монокристаллы [Cu2(dmbipy)2L4], пригодные для РСА. Сравнение дифрактограммы комплекса, полученного по приведенной выше методике, и теоретической дифрактограммы, построенной на основе данных РСА (рис. 1), доказывает, что поликристаллическая фаза соответствует биядерному комплексу [Cu2(dmbipy)2L4], а не моноядерному, как предполагалось ранее.
Соединение [Cu2(dmbipy)2L4] кристаллизуется в моноклинной пр. гр. P21/c. Катионы меди окружены пятью атомами азота, которые образуют вокруг центрального атома немного искаженную квадратную пирамиду. 5-Фенилтетразолат анион проявляет два способа координации: монодентатный (атомом азота N2 тетразольного цикла) и бидентатно-мостиковый (атомами N1 и N2 тетразольного цикла). Молекула 4,4'-диметил-2,2'-бипиридина хелатирует центральный атом двумя атомами азота (рис. 2а). Таким образом, наличие мостиковой координации у 5-фенилтетразолата приводит к образованию биядерного соединения. Благодаря наличию межмолекулярных взаимодействий π⋅⋅⋅π и C–H⋅⋅⋅π биядерные фрагменты соединяются в супрамолекулярную слоистую структуру. Похожие биядерные соединения Cu(II) с различной координацией мостикового тетразолат аниона уже установлены и описаны для [Cu2(phen)2(тетразолат)4] [8], [Cu2(bipy/phen)2(5-(4-хлорфенил)тетразолат)4] [18], [Cu2(phen)2L4] [19], [Cu2(bipy)2L4] [20], [Cu2(bipy)2(5-бензилтетразолат)4] и [Cu2(dmbipy)2(5-бензилтетразолат)4] [6].
Рис. 2.
Структура комплекса [Cu2(dmbipy)2L4] (а) и межмолекулярный π⋅⋅⋅π-стэкинг (б). Атомы водорода не показаны.
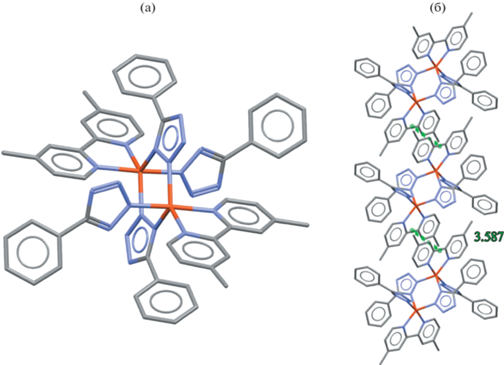
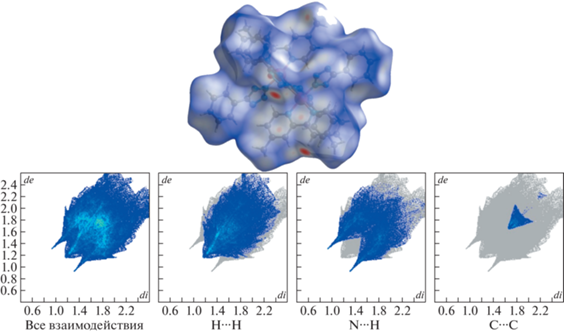
Анализ поверхности Хиршфельда для кристаллической структуры комплекса Cu(II) был проведен с целью исследовать межатомные контакты и их вклад в кристаллическую упаковку. На поверхности нормированных контактов dnorm (рис. 3) имеются несколько областей, которые показывают наличие донора и акцептора (атомы азота и водорода), образующих межмолекулярные взаимодействия [21]. По данным 2D-развертки поверхности Хиршфельда вклад межмолекулярных контактов N⋅⋅⋅H составляет 27.1%, H⋅⋅⋅H – 45%, C⋅⋅⋅H – 22.2%, C⋅⋅⋅C – 3.6%, N⋅⋅⋅C – 1.8% и Cu⋅⋅⋅H – 0.3% (рис. 3). Область при de = di ≈ 1.8 Å на 2D-развертке контактов C⋅⋅⋅C демонстрирует наличие π⋅⋅⋅π-стэкинга (~3.6 Å) между соседними молекулами 4,4'-диметил-2,2'-бипиридина, что также продемонстрировано на рис. 2б [22].
Рис. 3.
Поверхность Хиршфельда, отображенная в виде dnorm (сверху) и 2D-развертка поверхности, показывающая все межмолекулярные взаимодействия, контакты H⋅⋅⋅H, N⋅⋅⋅H и C⋅⋅⋅C (снизу).
Помимо межмолекулярного π–π-взаимодействия в комплексе наблюдается внутримолекулярное взаимодействие между 4,4'-диметил-2,2'-бипиридином и бензольным циклом 5-фенилтетразолат аниона (рис. 4а). Этот π-стэкинг (3.691 Å) возникает при повороте бензольного цикла вокруг оси, проходящей вдоль 5-фенилтетразола. В результате двугранный угол между плоскостями, проходящими через фрагменты мостикового лиганда (тетразольный и бензольный циклы), равен 60.21°. В Кембриджской базе структурных данных имеется структура похожего соединения [Cu2(bipy)2L4], содержащего вместо 4,4'-диметил-2,2'-бипиридина молекулу 2,2'-бипиридина [20]. В отличие от комплекса [Cu2(dmbipy)2L4] лиганд L в соединении [Cu2(bipy)2L4] координируется атомами N2 и N3 (рис. 4б). Таким образом, бензольный цикл находится достаточно далеко для образования π–π-взаимодействия с 2,2'-бипиридином, а двугранный угол равен 15.57°, что намного меньше, чем в случае комплекса [Cu2(dmbipy)2L4]. Для монодентатно координированного 5-фенилтетразолата также наблюдается поворот бензольного цикла: двугранный угол равен 33.13° для комплекса [Cu2(dmbipy)2L4] и 4.17° для [Cu2(bipy)2L4]. Таким образом, наблюдаются заметные различия в строении похожих систем (табл. 2).
Рис. 4.
Внутримолекулярный π-стэкинг в комплексе [Cu2(dmbipy)2L4] (а) и строение [Cu2(bipy)2L4] (б). Атомы водорода не показаны.
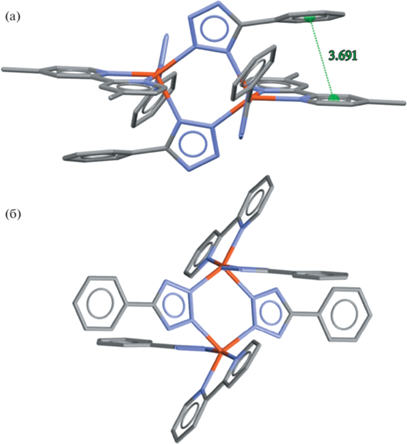
Таблица 2.
Различия в строении комплексов [Cu2(dmbipy)2L4] и [Cu2(bipy)2L4]
| Параметр | [Cu2(dmbipy)2L4] | [Cu2(bipy)2L4] |
|---|---|---|
| Тип мостиковой координации L– | Атомы N1 и N2 | Атомы N2 и N3 |
| Двугранный угол (монодентатный лиганд), град | 33.13 | 4.17 |
| Двугранный угол (мостиковый лиганд), град | 60.21 | 15.57 |
| Энергия связи при координации N1 и N2, эВ | –793.51 | –726.70 |
| Энергия связи при координации N2 и N3, эВ | –793.87 | –727.13 |
Расчеты методом DFT проводили для оценки относительной устойчивости комплексов [Cu2(dmbipy)2L4] и [Cu2(bipy)2L4], в частности получены значения энергии связи. Энергию связи рассчитывают как разность между энергией молекулы и суммой значений энергии атомов [23, 24]. Были спроектированы две модели для каждого соединения: экспериментально полученная по результатам РСА и модель с другой координацией мостикового лиганда (табл. 2). Таким образом, для [Cu2(dmbipy)2L4] и [Cu2(bipy)2L4] рассмотрены четыре системы с различной координацией ионов меди – атомами N1 и N2 или N2 и N3. Из данных табл. 2 видно, что соединение [Cu2(bipy)2L4] с координацией N1 и N2 примерно на 0.43 эВ (41.5 кДж/моль) менее стабильно по сравнению с соединением с координацией лигандов по N2- и N3-положениям. Из-за разницы в энергии образование комплекса [Cu2(bipy)2L4] с координацией лиганда по N1 и N2 менее выгодно и маловероятно. В случае комплекса [Cu2(dmbipy)2L4] наблюдается аналогичный результат: энергетически более выгодно образование соединений с мостиковой координацией лигандов атомами N2 и N3, разница в энергии связи при разных типах координации составляет 0.36 эВ (34.7 кДж/моль). Следовательно, образование изомера с координацией лигандов атомами N1 и N2, по-видимому, обусловлено стерическими факторами, возникающими при упаковке молекул в кристаллах.
ЗАКЛЮЧЕНИЕ
Получены монокристаллы биядерного комплекса меди [Cu2(dmbipy)2L4]. Согласно рентгеноструктурному анализу 5-фенилтетразолат анион проявляет как бидентатно-мостиковую, так и монодентатную координацию. Анализ поверхности Хиршфельда показал наличие донорно-акцепторных межмолекулярных взаимодействий N⋅⋅⋅H, а также π–π-стэкинга между соседними молекулами 4,4'-диметил-2,2'-бипиридина. В результате мостиковой координации L– атомами N1 и N2 наблюдается поворот бензольного цикла вокруг оси, проходящей вдоль 5-фенилтетразолата. С помощью квантово-химических расчетов показано, что в биядерных комплексах меди на основе бипиридина и L– энергетически более предпочтительна координация мостикового лиганда L– атомами N2 и N3. Однако при упаковке молекул в кристаллах могут возникать стерические затруднения, приводящие к образованию изомеров с другим типом координации мостикового лиганда.
Авторы выражают благодарность Т. Сухих за предоставление рентгенодифракционных данных, полученных в ЦКП ИНХ СО РАН, и А. Матвеевой за выполнение рентгенофазового анализа.
Работа выполнена при поддержке Российского научного фонда (проект № 20-73-10207) и Министерства науки и высшего образования Российской Федерации (проект № 121031700321-3).
Список литературы
Kerru N., Gummidi L., Maddila S. et al. // Molecules. 2020. V. 25. № 8. https://doi.org/10.3390/molecules25081909
Heravi M.M., Zadsirjan V. // RSC Adv. 2020. V. 10. № 72. P. 44247. https://doi.org/10.1039/D0RA09198G
Popova E.A., Trifonov R.E., Ostrovskii V.A. // Russ. Chem. Rev. 2019. V. 88. № 6. P. 644. https://doi.org/10.1070/RCR4864
Popova E.A., Protas A.V., Trifonov R.E. // Anti-Cancer Agents Med. Chem. 2017. V. 17. № 14. P. 1856. https://doi.org/10.2174/1871520617666170327143148
Kaushik N., Kumar N., Kumar A., Singh U.K. // Immunol., Endocr. Metab. Agents Med. Chem. 2018. V. 18. № 1. P. 3. https://doi.org/10.2174/1871522218666180525100850
Eremina J.A., Smirnova K.S., Klyushova L.S. et al. // J. Mol. Struct. 2021. V. 1245. P. 131024. https://doi.org/10.1016/j.molstruc.2021.131024
Eremina J.A., Lider E.V., Kuratieva N.V. et al. // Inorg. Chim. Acta. 2021. V. 516. P. 120169. https://doi.org/10.1016/j.ica.2020.120169
Eremina J.A., Lider E.V., Samsonenko D.G. et al. // Inorg. Chim. Acta. 2019. V. 487. P. 138. https://doi.org/10.1016/j.ica.2018.12.011
Eremina J.A., Ermakova E.A., Smirnova K.S. et al. // Polyhedron. 2021. V. 206. P. 115352. https://doi.org/10.1016/j.poly.2021.115352
Bruker Apex3 Software Suite: Apex3, SADABS-2016/2 and SAINT, version 2018.7-2; Bruker AXS Inc.: Madison, WI, 2017.
Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. V. 42. № 2. P. 339. https://doi.org/10.1107/S0021889808042726
Sheldrick G.M. // Acta Cryst. A. 2015. V. 71. № 1. P. 3. https://doi.org/10.1107/S2053273314026370
Sheldrick G.M. // Acta Cryst. C. 2015. V. 71. P. 3. https://doi.org/10.1107/S2053229614024218
ADF2013, Software for Chemistry and Materials, Theoretical Chemistry, Vrije Universiteit, Amsterdam (The Netherlands), 2013.
Perdew J.P., Burke K., Ernzerhof M. // Phys. Rev. Lett. 1996. V. 77. № 18. P. 3865. https://doi.org/10.1103/PhysRevLett.77.3865
Van Lenthe E., Baerends E.J. // J. Comput. Chem. 2003. V. 24. № 9. P. 1142. https://doi.org/10.1002/jcc.10255
Turner M.J., McKinnon J.J., Wolff S.K. et al. CrystalExplorer17. University of Western Australia, 2017. http://hirshfeldsurface.net
Kumari J., Mobin S.M., Mukhopadhyay S. et al. // Inorg. Chem. Commun. 2019. V. 105. P. 217. https://doi.org/10.1016/j.inoche.2019.05.006
Saha M., Vyas K.M., Martins L.M.D.R.S. et al. // Polyhedron. 2017. V. 132. P. 53. https://doi.org/10.1016/j.poly.2017.04.016
Shao Z.-H., Luo J., Cai R.-F. et al. // Acta Cryst. E. 2004. V. 60. № 2. P. m225. https://doi.org/10.1107/S1600536804001345
McKinnon J.J., Jayatilaka D., Spackman M.A. // Chem. Commun. 2007. № 37. P. 3814. https://doi.org/10.1039/B704980C
Spackman M.A., McKinnon J.J. // CrystEngCommun. 2002. V. 4. № 66. P. 378. https://doi.org/10.1039/b203191b
Te Velde G., Bickelhaupt F.M., Baerends E.J. et al. // J. Comput. Chem. 2001. V. 22. № 9. P. 931. https://doi.org/10.1002/jcc.1056
Bickelhaupt F.M., Baerends E.J. // Rev. Comput. Chem. 2000. V. 15. P. 1. https://doi.org/10.1002/9780470125922.ch1
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография