Микроэлектроника, 2021, T. 50, № 1, стр. 43-48
Влияние состава смеси на электрофизические параметры и спектры излучения плазмы хлороводорода с хлором и гелием
С. А. Пивоваренок a, *, Д. Б. Мурин a, **, Д. В. Ситанов a
a Ивановский государственный химико-технологический университет
153000 г. Иваново, пр. Шереметевский, 7, Россия
* E-mail: sap@isuct.ru
** E-mail: dim86@mail.ru
Поступила в редакцию 24.03.2020
После доработки 24.03.2020
Принята к публикации 24.03.2020
Аннотация
Проведен анализ влияния состава смеси на электрофизические параметры и спектры излучения плазмы HCl/Cl2 и HCl/He в условиях тлеющего разряда постоянного тока. Получены данные по температуре газа и приведенной напряженности электрического поля. Установлено, что приведенная напряженность электрического поля в плазме HCl/Cl2 линейно возрастает с увеличением доли второго газа в смеси, а в плазме HCl/He – уменьшается. Показано, что в плазме переменного состава HCl/Cl2 концентрация атомарного хлора остается практически неизменной, тогда как в плазме HCl/He монотонно уменьшается.
ВВЕДЕНИЕ
Методы жидкостного травления в электронной промышленности вытесняются процессами “сухой” обработки металлических и полупроводниковых слоев посредством неравновесной низкотемпературной газоразрядной плазмы вследствие того, что происходит снижение физических размеров элементов (увеличивается плотность упаковки, степень интеграции элементов интегральных микросхем).
В технологии интегральной электроники изначально использовались фторсодержащие газы (CxHyFz) в качестве плазмообразующих сред. Однако это ограничивало применение в технологии большинство полупроводниковых материалов (GaAs, InP и др.) и металлов (Cu, Al, Cr и др.), так как во фторуглеродной плазме образуются труднолетучие продукты реакции, а также происходит высаживание полимерной пленки на поверхностях, контактирующих с плазмой.
Альтернативой может служить низкотемпературная плазма галогеноводородов. В частности, используя хлористый водород (HCl) в качестве плазмообразующего газа, за счет химических реакций с участием атомов водорода можно добиться лучшей равномерности и чистоты процесса травления. Также, вследствие низких степеней диссоциации молекул хлороводорода можно достигнуть более высокой степени анизотропии и селективности процесса.
Однако в технологии наибольшее распространение получили бинарные газовые смеси. Суть в том, что присутствие газа-добавки может повлиять на электрофизические параметры плазмы и, как следствие, на поведение скоростей травления материала. Тем самым, варьируя начальный состав смеси, имеется возможность управлять конечным результатом обработки. Например, в работе [1] было показано, что при увеличении доли водорода в смеси HCl/H2 происходит медленное снижение относительной концентрации атомов и молекул хлора (основных химически активных частиц), причем это снижение не согласуется с эффектом концентрационного разбавления.
Цель данной работы – исследование влияния добавки хлора и гелия на электрофизические параметры разряда (приведенную напряженность электрического поля E/N и температуру газа T) и спектры излучения в хлороводороде.
МЕТОДИЧЕСКАЯ ЧАСТЬ
Эксперименты проводились в плазмохимической установке с цилиндрическим (радиус r = 1.4 см, длина зоны разряда l = 36 см) реактором проточного типа, изготовленного из молибденового стекла С-49. Электроды располагались в боковых отростках и имели вид полых цилиндров из анодированного алюминия. Тлеющий разряд постоянного тока возбуждался от высоковольтного трансформатора НОМ 6000/100, первичная обмотка которого питалась от ЛАТРа, что позволяло плавно изменять выходное напряжение. Выход высоковольтного трансформатора соединен с выпрямительным устройством (диодным мостом) и конденсатором (10 мкФ) для сглаживания пульсации напряжения, питающего разряд. Сила тока в цепи разряда измерялась миллиамперметром М340 электромагнитной системы. Откачка системы осуществлялась вращательно-масляным форвакуумным насосом ВН-461 (предельное остаточное давление ~2 × 10–2 Па). Контроль давления остаточных газов осуществлялся с помощью манометрического термопарного датчика ПМТ-2, соединенного с вакуумметром ВТ-2. Измерение давления и расхода газа проводили U-образным масляным манометром и капиллярным реометром, соответственно.
Хлористый водород был получен химическим методом, основанным на реакции между хлористым натрием и концентрированной серной кислотой [2]. Для получения хлора был использован метод термического разложения хлорной меди (CuCl2 ⋅ 2H2O) в вакууме. Хлорная медь марки “ч. д. а.” содержала не менее 99.9% основного вещества и не более 0.01% нерастворимых веществ, 0.05% щелочных и щелочноземельных металлов, 0.03% Fe, 0.002% As и 0.005% SO4. Первоначально производили процесс обезвоживания CuCl2 ⋅ 2H2O в сушильном шкафу при атмосферном давлении и температуре порядка 100–120°С в течение 6–8 ч. Далее обезвоженную соль насыпали в сухую стеклянную ампулу, которую присоединяли к вакуумной системе экспериментальной установки и подвергали процедуре финального обезгаживания. На этом этапе соль выдерживали при температуре 200–250°С и непрерывной откачке до тех пор, пока давление в системе не достигало предельного минимума (обычно для этого требовалось порядка 3 ч). Для получения хлора ампулу с обезгаженной солью нагревали до температуры порядка 300–350°С, инициируя тем самым реакцию 2CuCl2 ↔ Cl2↑ + 2CuCl. Первые порции газа откачивали, а последующие использовались для проведения экспериментов. Гелий набирался в предварительно откачанную хлорвиниловую емкость из баллона с маркой “чистый” (МРТУ 51-77-66) с содержанием основного газа не менее 99.985%. Газовые смеси готовились непосредственно в самой вакуумной системе методом объемного смешения компонентов. Начальный состав плазмообразующей смеси задавался изменением парциальных давлений компонентов в рамках постоянного общего давления.
Контроль примесей компонентов атмосферного воздуха в основном газе осуществлялся качественно, по наличию или отсутствию полос излучения N2, OH и CO в спектрах излучения. Во всех случаях, режимы набора газов и конструкции соответствующих установок оптимизировались таким образом, чтобы интенсивности излучения полос указанных примесей были минимальными.
В качестве внешних (задаваемых) параметров разряда выступали ток разряда (i = 10–35 мА), давление газа (p = 40–200 Па) и расход газа (q = 2 см3/с при нормальных условиях).
Для определения температуры нейтральных частиц (T) был использован расчетный метод, основанный на решении уравнения теплового баланса разрядной трубки в условиях естественного охлаждения [3]. Расчеты основывались на двух основных предпосылках: 1) основным механизмом передачи тепла из объема газа к стенкам реактора является конвекционный теплообмен (теплопроводность) и 2) потери вкладываемой мощности за счет теплопроводности WT значительно выше потерь мощности с излучением разряда We. С учетом вышесказанного, уравнение теплового баланса разрядной трубки может быть представлено в виде W = iE ≈ WT, при этом для определения температуры газа достаточно провести измерение температуры наружной стенки реактора (Tout).
Предполагая, что профили распределения температуры в стенке реактора и в газе вблизи стенки близки к линейным, расчет температуры газа может быть произведен по следующим соотношениям:
Измерения осевой напряженности электрического поля (E, с погрешностью 10%) в плазме осуществлялось двухзондовым методом с использованием компенсационной методики. Разность потенциалов между двумя остеклованными зондами (вольфрам, ∅ 0.05 мм), которые вводились в зону разряда на оси разрядной трубки, компенсировалась с помощью универсального источника питания УИП-1. При помощи нуль-индикатора (миллиамперметр М906) регистрировалось отсутствие тока в цепи зондов, а напряжение компенсации определялось с помощью цифрового мультиметра True RMS Fluke 289. Величина напряженности электрического поля на оси разряда E определялась по соотношению: E = U/l (где U – напряжение компенсации зондового тока, а l = = 7.7 см – расстояние между зондами).
При определении приведенной напряженности электрического поля E/N, (где N = p/kBT – общая концентрация частиц в реакторе) использовалась величина T0.5r. Допустимость такого подхода была показана в работе [4], а в его основе лежит компенсация радиального падения температуры, констант скоростей пороговых процессов и концентрации электронов и роста концентраций нейтральных частиц. Это позволяет определять не максимальные (осевые), а средние по объему плазмы скорости процессов и концентрации частиц.
Запись спектров излучения плазмы HCl/Cl2 и HCl/He осуществлялась с помощью оптоволоконных спектрометров AvaSpec-2048-2 и AvaSpec-3648 с фотоэлектрической системой регистрации сигнала и накоплением данных на ЭВМ. Рабочий диапазон длин волн составлял 200–1000 нм. Отбор излучения для анализа проводился через кварцевое окно в торцевой части реактора. При расшифровке спектров излучения использовались справочники [5, 6].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Интерес к варьированию параметрами плазмохимических процессов связан в первую очередь с необходимостью прецизионной обработки материалов в газовом разряде. Несмотря на общую тенденцию преимущественного использования разрядов атмосферного давления, плазма пониженного давления остается востребованной в ряде практических применений. В первую очередь, когда необходимо использовать в качестве плазмообразующих сред токсичные и высоко реакционно-способные газы, такие как бром, хлор, хлороводород и т.д. Востребованность последних оказывается достаточно высокой ввиду того, что они хорошо взаимодействуют с медью, которая по своим электрофизическим свойствам, а также технологической совместимости является более предпочтительным материалом (по сравнению с такими материалами как Al, Au, Ag) для создания межэлементных соединений в ИМС на основе кремния. Также, в этих газах отсутствуют такие эффекты как полимеризация и/или высаживание на внутренней поверхности реактора и обрабатываемого материала ненасыщенных продуктов реакций, которые свойственны углеродсодержащим плазмообразующим газам. С другой стороны, для лучшего контроля процесса травления малых структур (на уровне десятков или сотен нанометров) необходимо иметь возможность влиять на скорость целевого процесса не только за счет концентрационного параметра (уменьшения или увеличения концентрации травителя), но и за счет изменения электрофизических параметров плазмы.
Хлороводород сам по себе достаточно широко используемый в технологии плазмообразующий газ [7–9]. Наличие в нем двух диаметрально противоположных составляющих – хлора и водорода, роднит этот газ с часто используемой плазмообразующей смесью Cl2/H2. В обоих случаях в газовом разряде образуются как атомы хлора, так и водорода, следовательно, в этой плазме могут не только травиться материалы, но и может наблюдаться очистка поверхности от возможных окислов, за счет их взаимодействия с водородом [10].
Если к хлороводороду дополнительно добавлять другие газы, подобрав их по свойствам диаметрально противоположными, то в результате можно ожидать изменение свойств плазмы на основе такой плазмообразующей смеси и соответственно изменение ее электрофизических параметров. На рис. 1 показано изменение приведенной напряженности электрического поля в плазме смеси хлороводорода с хлором и гелием переменного состава. Результат оказался предсказуемым.
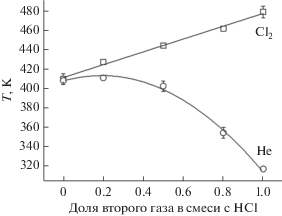
Рис. 1.
Зависимость приведенной напряженности электрического поля от доли второго газа в исходной смеси (p = 100 Па, i = 15 мА).
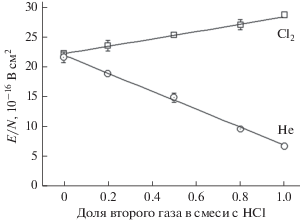
Приведенное поле в смеси HCl/Cl2 растет с увеличением доли хлора в смеси. Ток разряда в этом случае поддерживался на постоянном уровне и составлял 15 мА. Такой результат объясняется относительно высокими полями в чистом хлоре, при этом степень диссоциации Cl2 не превышала 30% в исследованном диапазоне условий возбуждения разряда [11].
Гелий достаточно легкий газ, хорошо ионизируется в плазме, ионы которого обладают высокими подвижностями, не создавая при этом изменение импеданса разрядного промежутка. Поэтому поля в плазме смеси HCl/Не падают по мере увеличения доли гелия в смеси. Сказанное подтверждается данными рис. 2.
Ход температурных зависимостей практически совпадает с ходом приведенной напряженности электрического поля для разрядов в смесях рассматриваемых газов. Тепловыделения растут (409–479 К) при увеличении концентрации хлора в смеси HCl/Cl2 и уменьшаются (408–317 К) при увеличении концентрации гелия в смеси HCl/He (рис. 2). Аналогичным образом выглядят и зависимости удельной мощности, вкладываемой в разряд, для поддержания заявленных в работе токов (рис. 3).
Рис. 3.
Зависимость удельной мощности, вкладываемой в разряд, от доли второго газа в исходной смеси (p = 100 Па, i = 15 мА).

Для практического использования плазмы смесей HCl с молекулярным хлором и гелием важно знать концентрации частиц в плазме, а для целей математического моделирования ее электрофизические характеристики. Интересно также сравнить электрофизические параметры плазмы с ходом концентраций основных частиц в плазме. В плазме смеси HCl/Cl2 молекулярный хлор выступает в качестве второго (добавляемого) газа к плазмообразующей смеси. Относительную концентрацию частиц в плазме можно определить спектрально, отслеживая интенсивности излучения их возбужденных состояний: Cl 725.7 нм (4p4S0 → 4s4P, εth = 10.6 эВ), Cl2 256.4 нм (23Πg → → 13Πu, εth = 8.2 эВ), Hα 656.4 нм (3d2D → 2p2P0, εth = 12.09 эВ), H2 602.3 нм (a3∑g → ${{a}^{{\text{3}}}}\Pi _{{\text{u}}}^{--},$ εth = = 13.9 эВ), He 587.7 нм (3d3D → 2p3P0, εth = 23.07 эВ). Правомочность такого подхода была показана в ряде работ [9, 10, 12]. Таким образом, в дальнейшем мы будем ассоциировать спектральные данные с ходом концентраций соответствующих частиц. Основные каналы образования частиц в плазме чистого HCl (εth – пороговая энергия процесса, k – константа скорости процесса, γ – вероятность рекомбинации на стенке):
(1)
${\text{HCl}} + {\text{e}} \to {\text{H}} + {\text{Cl}} + {\text{e}};{\text{ }}\left( {{{\varepsilon }_{{{\text{th}}}}} = 5.0{\text{ эВ}}} \right),$(2)
$\begin{gathered} {\text{HC}}{{{\text{l}}}_{{V{\text{ }} = {\text{ }}0,{\text{ }}1,{\text{ }}2,{\text{ }}3}}} + {\text{e}} \to {\text{C}}{{{\text{l}}}^{--}} + {\text{H }}\,\,{\text{и}}\,\,{\text{ Cl}} + {{{\text{H}}}^{--}}; \\ \left( {{{\varepsilon }_{{{\text{th}}}}} = 5.0{\text{ эВ}}} \right), \\ \end{gathered} $(3)
${\text{C}}{{{\text{l}}}_{2}} + {\text{e}} \to {\text{Cl}} + {\text{Cl}} + {\text{e}};{\text{ }}\left( {{{\varepsilon }_{{{\text{th}}}}} = 3.0{\text{ эВ}}} \right),$(4)
${\text{C}}{{{\text{l}}}_{2}} + {\text{e}} \to {\text{Cl}} + {\text{C}}{{{\text{l}}}^{--}};{\text{ }}\left( {{{\varepsilon }_{{{\text{th}}}}} = 0{\text{ эВ}}} \right),$(5)
${{{\text{H}}}_{2}} + {\text{e}} \to {\text{H}} + {\text{H}} + {\text{e}};{\text{ }}\left( {{{\varepsilon }_{{{\text{th}}}}} = 11.2{\text{ эВ}}} \right),$(6)
${\text{HCl}} + {\text{Cl}} \to {\text{C}}{{{\text{l}}}_{2}} + {\text{H}};{\text{ }}\left( {k = 3.2 \times {{{10}}^{{--20}}}\,{\text{с}}{{{\text{м}}}^{3}}{\text{/с}}} \right),$(7)
${\text{HCl}} + {\text{H}} \to {{{\text{H}}}_{2}} + {\text{Cl}};{\text{ }}\left( {k = 5.0 \times {{{10}}^{{--14}}}\,{\text{с}}{{{\text{м}}}^{3}}{\text{/с}}} \right),$(8)
${\text{C}}{{{\text{l}}}_{2}} + {\text{H}} \to {\text{HCl}} + {\text{Cl}};{\text{ }}\left( {k = 2.0 \times {{{10}}^{{--11}}}\,{\text{с}}{{{\text{м}}}^{3}}{\text{/с}}} \right),$(9)
${\text{Cl}} + {{{\text{H}}}_{2}} \to {\text{HCl}} + {\text{H}};{\text{ }}\left( {k = 8.0 \times {{{10}}^{{--14}}}\,{\text{с}}{{{\text{м}}}^{{\text{3}}}}{\text{/с}}} \right),$(10)
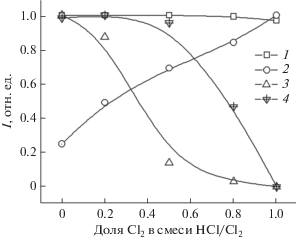
${\text{Cl}} + {\text{Cl}}\left( {\text{s}} \right) \to {\text{C}}{{{\text{l}}}_{2}}\left( {\text{s}} \right) \to {\text{C}}{{{\text{l}}}_{2}};\,{\text{ }}{{\gamma }_{{{\text{Cl}}}}}\sim 5 \times {{10}^{{--4}}}.$Данные рис. 4 показывают, что наблюдается увеличение концентрации Cl2 в плазме смеси хлороводорода с хлором по мере увеличения доли молекулярного хлора в составе плазмообразующего газа. Однако при высокой доле молекулярного хлора происходит небольшой спад концентрации Cl2, что говорит о различных каналах образования и гибели Cl2 в плазме переменного состава (процессы 3, 4, 6, 8 и 10), а не только за счет рекомбинации продуктов диссоциации HCl электронным ударом (процесс 10). Некоторое уменьшение темпов роста Cl2 при высоких процентных содержаниях молекулярного хлора в составе плазмообразующего газа объясняется более эффективной диссоциацией Cl2 (процессы 3 и 4), а также эффективной гибелью данных частиц в процессе (8) в условиях возрастания мощности, вкладываемой в разряд (рис. 3), и увеличения приведенной напряженности электрического поля (рис. 1). Вклад процесса (7) в общий баланс процессов образования и гибели частиц в плазме объясняет нелинейный спад концентрации молекулярного водорода, образующегося как результат нескольких плазмохимический процессов (1, 2, 5, 6, 7 и 9). Однако, каналы образования атомов водорода в процессах (5) и (6) менее эффективны по сравнению с процессами (1) и (2). На протекание процессов (7) и (8) также указывает быстрое уменьшение концентрации атомарного водорода. При преимущественном вкладе диссоциации HCl при электронном ударе (процессы 1 и 2) спад концентрации молекулярного водорода должен бы быть более равномерным. При доле молекулярного хлора в смеси более 0.5 наблюдается резкий спад концентрации молекулярного водорода, что объясняется эффективной гибелью как атомов водорода в процессе (8), так и молекулярного водорода в процессе (9) с учетом неизменной концентрации атомарного хлора. В результате протекания процессов (7) и (8) и форсированной диссоциации Cl2 (процессы 3 и 4) в плазме переменного состава при высокой концентрации последних в составе плазмообразующего газа концентрация атомарного хлора остается практически неизменной для всех составов газовых смесей. Основным объяснением данного факта может служить увеличение степени диссоциации хлороводорода в плазме смеси HCl/Cl2 за счет изменения электрофизических параметров плазмы (увеличения приведенной напряженности электрического поля) при высоких концентрациях молекулярного хлора в составе плазмообразующего газа. Данный факт может быть полезным для интенсификации процесса плазмохимического травления полупроводников, где в качестве основного плазмообразующего газа используется хлороводород.
Рис. 4.
Зависимость интенсивностей излучения плазмы смеси HCl/Cl2 от доли хлора в исходной смеси (p = 100 Па, i = 15 мА): 1 – Cl (725.7 нм), 2 – Cl2 (256.4 нм), 3 – Hα (656.4 нм), 4 – H2 (602.3 нм).
Напротив, плазма смеси хлороводорода с гелием может быть предложена для снижения деструктивного действия разряда на обрабатываемые образцы. Основные процессы генерации активных частиц в этом разряде аналогичны ранее рассмотренным, однако в условиях снижения приведенной напряженности электрического поля при увеличении концентрации гелия в составе плазмообразующей смеси основной вклад в схему формирования активных частиц вносят процессы диссоциации HCl электронным ударом (процессы 1 и 2). Так из рис. 5 видно, что концентрации всех активных частиц плазмы уменьшаются при увеличении доли гелия в составе плазмообразующего газа. Одновременно с уменьшением мощности, вкладываемой в разряд (рис. 3), и уменьшением приведенной напряженности электрического поля (рис. 1) этот факт можно рекомендовать в технологических целях для подбора относительно мягких режимов плазмохимического травления сверхмалых структур, где высокие скорости процессов обработки не всегда технологически оправданы.
ЗАКЛЮЧЕНИЕ
В условиях тлеющего разряда постоянного тока проведены измерения электрофизических параметров плазмы переменного состава смесей HCl/Cl2 и HCl/He. В системе HCl/Cl2 при увеличении доли второго газа в смеси происходит увеличение приведенной напряженности электрического поля в плазме, температуры газа и удельной мощности, вкладываемой в разряд, при этом в системе HCl/He данные параметры уменьшаются.
В плазме смеси HCl/Cl2 при высоких концентрациях второго компонента (Cl2) в составе плазмообразующего газа наблюдается постоянство концентрации атомарного хлора за счет того, что происходит изменение электрофизических параметров плазмы. В плазме смеси хлороводорода с гелием концентрации атомарного хлора монотонно уменьшаются.
Работа выполнена в рамках государственного задания на выполнение НИР. Тема № FZZW-2020-0007.
Список литературы
Мурин Д.Б., Ефремов А.М., Светцов В.И., Пивоваренок С.А., Годнев Е.М. Интенсивности излучения и концентрации нейтральных частиц в плазме тлеющего разряда постоянного тока в смесях HCl–H2 и HCl–O2 // Изв. вузов. Химия и хим. технология. 2013. Т. 56. № 8. С. 41–44.
Карякин Ю.В., Ангелов И.И. Чистые химические вещества. М.: Химия, 1974. 408 с.
Рохлин Г.Н. Разрядные источники света. 2-е изд.; перераб. и доп. М.: Энергоатомиздат, 1991. 720 с.
Лебедев Ю.А., Иванов Ю.А., Полак Л.С. Методы контактной диагностики в неравновесной плазмохимии. М.: Наука, 1981. 142 с.
Pearse R.W.B., Gaydon A.G. The identification of molecular spectra. Ed. 4th. N.Y.: John Wiley & Sons, Inc. 1976. 407 p.
Стриганов А.Р., Свентицкий Н.С. Таблицы спектральных линий нейтральных и ионизированных атомов. М.: Атомиздат., 1966. 899 с.
Ефремов А.М., Пивоваренок С.А., Светцов В.И. Параметры плазмы и механизмы травления металлов и полупроводников в хлороводороде // Микроэлектроника. 2009. Т. 38. № 3. С. 163–175.
Пивоваренок С.А., Дунаев А.В., Ефремов А.М., Светцов В.И. Плазменное наноразмерное травление GaAs в хлоре и хлороводороде // Нанотехника. 2011. № 1. Вып. 25. С. 69–71.
Пивоваренок С.А., Дунаев А.В., Мурин Д.Б., Ефремов А.М., Светцов В.И. Электрофизические параметры и эмиссионные спектры плазмы тлеющего разряда в хлористом водороде // Изв. вузов. Химия и хим. технология. 2011. Т. 54. № 9. С. 48–52.
Дунаев А.В., Пивоваренок С.А., Капинос С.П., Ефремов А.М., Светцов В.И. Спектральное исследование травления арсенида галлия в плазме HCl // Микроэлектроника. 2011. Т. 40. № 6. С. 413–417.
Ситанов Д.В., Светцов В.И., Ефремов А.М. Диссоциация молекул хлора в плазме тлеющего разряда в смесях с аргоном, кислородом, азотом // ХВЭ. 1999. Т. 32. № 2. С. 148–151.
Пивоваренок С.А. Влияние состава смеси на электрофизические параметры и спектры излучения плазмы CF2Cl2/Ar и CF2Cl2/He // Микроэлектроника. 2017. Т. 46. № 4. С. 290–294.
Дополнительные материалы отсутствуют.
Инструменты
Микроэлектроника