Нефтехимия, 2019, T. 59, № 3, стр. 304-314
Катализаторы конверсии диметилового эфира в низшие олефины: влияние кислотности, постсинтетической обработки и содержания водяного пара и метанола в сырье
С. Н. Хаджиев 1, Н. В. Колесниченко 1, *, Е. Н. Хиврич 1, Т. И. Батова 1
1 Институт нефтехимического синтеза им. А.В. Топчиева РАН
Москва, Россия
* E-mail: nvk@ips.ac.ru
Поступила в редакцию 05.11.2018
После доработки 28.11.2018
Принята к публикации 10.12.2018
Аннотация
Систематизированы и обобщены наиболее важные и интересные результаты, полученные в ИНХС РАН, за период 2008–2015 гг., по конверсии диметилового эфира в низшие олефины на цеолитных катализаторах на основе HZSM-5. Рассмотрено влияние природы модифицирующего элемента, а также высокотемпературной обработки катализатора водяным паром на структурные, кислотные характеристики и каталитические свойства цеолитного катализатора. Освещены некоторые особенности влияния водяного пара в исходной газовой смеси в зависимости от природы модифицирующего элемента. Приведены данные по влиянию примесей в исходной смеси (метанола и водяного пара).
Производство низших олефинов является многотоннажным и постоянно растущим [1]. Процессы термического пиролиза и каталитического крекинга углеводородного сырья остаются основным способом получения этилена и пропилена. Темпы роста потребления этих ценных химических продуктов значительно опережают масштабы их производства, что заставляет искать другое, более дешевое и доступное, углеводородное сырье. Таким сырьем является природный газ, добыча и крупномасштабное использование которого прогнозируется на длительный период. Наиболее известным и изученным способом получения химических продуктов из природного газа является их получение через предварительную конверсию природного газа в синтез-газ (СО/Н2).
В настоящее время большой интерес вызывает вариант получения олефинов С2–С3 из синтез-газа через диметиловый эфир (ДМЭ), позволяющий производить низшие олефины с высоким выходом и c более высокой селективностью [2, 3]. ДМЭ можно рассматривать как один из возможных ключевых агентов в превращении ненефтяного сырья в ценные химические продукты, такие как олефины [4]. Наиболее распространенной основой катализаторов синтеза низших олефинов из ДМЭ является высококремнеземный цеолит типа ZSM-5. Направленное воздействие на свойства цеолитных катализаторов заключается в модифицировании соединениями металлов [5–9], что может приводить к изменению их текстурных и кислотных характеристик [10–12]. В литературе появилось множество работ, в которых широко исследуется влияние природы модифицирующего элемента на свойства цеолитных катализаторов [13–17], однако, до сих пор не выработана концепция в понимании роли природы модифицирующего элемента в изменении их каталитических свойств. Вследствие этого, важное значение имеет выработка общего подхода к подбору катализаторов превращения углеводородов (УВ), которая позволила бы дифференцировать влияние модифицирования цеолитов на изменение их кислотных, молекулярно-ситовых и каталитических свойств в зависимости от природы модифицирующего элемента. Изменения кислотных свойств можно также добиться предварительной высокотемпературной обработкой катализаторов или изменением содержания воды в исходном сырье. В связи с этим, получение данных по влиянию кислотных свойств на каталитические свойства цеолитных катализаторов конверсии ДМЭ в олефины является весьма актуальным. При этом важны исследования, позволяющие оценить влияние природы модифицирующего элемента не только на активность, но и стабильность каталитических свойств. Особенно это ценно при осуществлении реакции в среде водяного пара, используемого в технологии ряда промышленных процессов [18–21], так как водяной пар может оказывать существенное влияние не только на распределение продуктов превращения ДМЭ, но и изменять структурные характеристики цеолитного катализатора.
В данной работе обобщены результаты по разработке принципиально новых высокоэффективных каталитических систем на основе цеолита ZSM-5, модифицированного различными элементами, и рассмотрено влияние природы модифицирующего элемента, а также высокотемпературной обработки водяным паром на структурные, кислотные характеристики и каталитические свойства цеолитного катализатора в конверсии ДМЭ в низшие олефины.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе рассмотрены каталитически активные системы синтеза низших олефинов из ДМЭ на основе цеолита ZSM-5 в аммонийной форме (${\text{NH}}_{4}^{ + }$) с мольным отношением SiO2/Al2O3 = 37 (производство ОАО “Ангарский завод КиОС”, содержит не более 0.04 мас. % оксида натрия). Водородную форму цеолита (H+) получали при прокаливании в течение 4 ч при 500°С. Катализаторы получали путем смешения цеолита НZSM-5 со связующим – суспензией оксида алюминия (содержит 23 мас. % сухого Al2O3 производства ЗАО “Промышленные катализаторы”, Рязань) и последующего формования экструдатов (содержание Al2O3 в готовом катализаторе 33–34 мас. %). Модифицирование осуществляли соединениями магния, лантана и циркония. Эти активные элементы были определены как наиболее перспективные для создания промышленных катализаторов [22–29]. Для каждого элемента был выявлен наиболее оптимальный способ его введения в катализатор. Так, лантан вводился непосредственно в цеолит методом ионного обмена его водородной формы с водным раствором соли металла, цирконий – методом безостаточной пропитки цеолита до смешения со связующим. Введение магния осуществляли методом пропитки готовых экструдатов цеолита со связующим водным раствором соли металла. Характеристики исходного цеолита и модифицированных катализаторов на его основе приведены в табл. 1.
Таблица 1.
Характеристики цеолитных катализаторов
| Образец | Степень кристал-личности**,% | SВЕТ, м2/г | Vпор, см3/г | Vмикропор, см3/г | VмезопорBJH, см3/г | Ссылка |
|---|---|---|---|---|---|---|
| NH4ZSM-5* | 100 | 314 | 0.201 | 0.154 | 0.047 | – |
| HZSM-5/Al2O3 | 91 | 311 | 0.200 | 0.152 | 0.048 | [30] |
| La-HZSM-5/Al2O3 | 93 | 313 | 0.214 | 0.145 | 0.069 | [30] |
| Zr-HZSM-5/Al2O3 | 90 | 324 | 0.222 | 0.146 | 0.076 | [30] |
| La-Zr-HZSM-5/Al2O3 | 90 | 305 | 0.224 | 0.138 | 0.086 | [30] |
| Mg-HZSM-5/Al2O3 | 92 | 286 | 0.214 | 0.133 | 0.081 | [31] |
** Степень кристалличности рассчитывали согласно [32].
Испытания катализаторов проводили на установке с реактором проточного типа при температуре 320–380°С и атмосферном давлении. Загрузка катализатора в реактор составляла 3–10 см3.
В качестве исходного сырья использовали ДМЭ (мас. доля ДМЭ 99.99%); разбавитель ДМЭ – азот и/или водяной пар и метанол. Концентрация ДМЭ в исходной газовой смеси составляла от 10 до 75 об. %, метанола от 10 до 30 об. %. Объемную скорость подачи исходной газовой смеси варьировали в пределах 2000–15 000 ч–1. Методика проведения эксперимента и анализа продуктов реакции приведены в [33].
Предварительную высокотемпературную обработку цеолита осуществляли согласно [34, 35] при температуре 750°С в атмосфере воздуха в течение 4 ч. Обработку катализаторов водяным паром при 500 и 750°С проводили на установке проточного типа по методике, описанной в [32].
Методами ИК-спектроскопии, рентгенофазового анализа, адсорбции бензола, ЯМР твердого тела были изучены структурные характеристики исходного цеолита и модифицированных образцов до и после их обработки, кислотные свойства катализаторов – методом температурно-программированной десорбции аммиака (ТПД NH3).
Инфракрасная спектроскопия диффузного отражения (ИКСДО). Регистрацию спектров при повышенных температурах в инертной атмосфере (Ar) и при пропускании смеси ДМЭ с азотом или водяным паром осуществляли методом ИКСДО в режиме in situ. Спектры регистрировали в интервале температур 25–450°C в высокотемпературной ячейке PIKE Diffus IR, сопряженной ИК Фурье-спектрометром VERTEX-70 “Bruker”. Спектр записывали в непрерывном режиме в течение 5 мин (200 сканирований/спектр) с разрешением 2 см–1 в диапазоне 600–4000 см–1. Математическую обработку ИК-спектров проводили в программном пакете OPUS-7.
Рентгенофазовый анализ (РФА). Данные рентгенофазового анализа были получены на порошковом дифрактометре Stoe STADT P, CuKα излучение с длиной волны λ = 1.5418 Å, напряжение 40 кВ, ток 30 мA.
ЯМР твердого тела. Спектры ЯМР твердого тела были получены на приборе 11.7 Т Varian Unity Inova 500. Ларморовы частоты составляли 130 и 99 МГц для 27Al и 29Si соответственно. Для получения спектров на ядрах 27Al использовался 3.2-датчик; скорость вращения составляла 15 кГц, длина π/2 импульса – 1 мкс, время накопления – 0.015 с, промежуток между сканами составлял 0.5 с. Спектры 29Si ЯМР ВМУ получены на 7.5-датчике при скорости вращения 4.5 кГц. При снятии спектров 29Si применялся π/6 импульс длиной 2 мкс, время накопления составляло 0.01 с, промежуток между сканами – 30 с. В качестве стандартов для определения положений линий спектров 29Si и 27Al использовали тетраметилсилан и хлорид алюминия соответственно.
Адсорбцию бензола проводили в динамическом режиме при 200°С методом газо-адсорбционной хроматографии согласно [36]. Расчет изотерм осуществляли по методу Глюкауфа [37].
Температурно-программированная десорбция NH3. Данные ТПД аммиака для приготовленных образцов были получены по методике, описанной в [32] и обработаны методом согласования экспериментальной и расчетной форм кривых согласно [38].
Текстурные характеристики образцов (удельной площади поверхности, суммарного объема пор и распределения пор по размерам) исследовали методом низкотемпературной адсорбции-десорбции молекулярного азота на установке ASAP-2010 фирмы Micromeritics. Предварительно все образцы были вакуумированы при температуре 350°С до 4 × 10–1 Па. Адсорбцию N2 проводили при температуре 77 K.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Определяющим фактором эффективности цеолитных катализаторов в различных превращениях оксигенатов в УВ являются их кислотные свойства, которые можно изменять модифицированием цеолитов, постсинтетической высокотемпературной обработкой исходного цеолита HZSM-5, либо высокотемпературной обработкой цеолитного катализатора водяным паром. Последняя приводит не только к изменению их кислотных свойств, но и генерации дополнительных кислотных центров, что оказывает влияние на каталитические и физико-химические свойства цеолитсодержащего катализатора. Распределение кислотных центров по силе в зависимости от природы вводимого элемента и способа постсинтетической обработки цеолитных катализаторов представлены в табл. 2.
Таблица 2.
Кислотные свойства изученных цеолитных катализаторов
| Образец | Суммарная кислотность, мкмоль/г | Число центров с Еd < 130 кДж/моль (I) | Число центров с Еd > 130 кДж/моль (II) | I/II* |
|---|---|---|---|---|
| HZSM-5 | 778 | 227 (30%) | 551 (70%) | 0.4 |
| HZSM-5/Al2O3* | 757 | 275 (36%) | 482 (64%) | 0.6 |
| La-НЦВМ/Al2O3 | 634 | 258 (41%) | 376 (59%) | 0.7 |
| Zr-НЦВМ/Al2O3 | 880 | 383 (44%) | 497 (56%) | 0.8 |
| Mg-HZSM-5/Al2O3 | 534 | 256 (48%) | 278 (52%) | 0.9 |
| La-Zr-НZSM-5/Al2O3 | 586 | 261 (45%) | 325 (55%) | 0.8 |
| Высокотемпературная обработка цеолита (Т) | ||||
| La-Zr-НZSM-5(Т)/Al2O3 | 461 | 265 (58%) | 196 (42%) | 1.4 |
| Mg-HZSM-5(Т)/Al2O3 | 367 | 242 (66%) | 125 (34%) | 1.9 |
| Высокотемпературная обработка катализатора водяным паром | ||||
| Mg-HZSM-5/Al2O3 (500°С) | 491 | 191 (39%) | 300 (61%) | 0.6 |
| Mg-HZSM-5/Al2O3 (750°С) | 197 | 156 (79%) | 41 (21%) | 3.8 |
| La-Zr-HZSM-5/Al2O3 (500°С) | 319 | 172 (54%) | 147 (46%) | 1.2 |
| La-Zr-HZSM-5/Al2O3 (750°С) | 170 | 137 (81%) | 33 (19%) | 4.2 |
В результате модифицирования образцов соединением магния, а также двойного модифицирования лантаном и цирконием наблюдается существенное снижение общей кислотности; при этом доля кислотных центров средней силы (I/II) несколько повышается.
Высокотемпературная обработка исходного цеолита приводит к значительному снижению общей кислотности и повышению доли средних кислотных центров. Высокотемпературная обработка водяным паром при 500°С также приводит к снижению общей кислотности, однако, если в случае Mg-HZSM-5/Al2O3 доля сильных кислотных центров повышается, то в случае La-Zr-HZSM-5/Al2O3 наблюдается обратная картина. Высокотемпературная обработка водяным паром при 750°С приводит к резкому снижению общей кислотности и доли сильных кислотных центров.
При высокотемпературной обработке водяным паром цеолитных катализаторов может происходить частичное разрушение их структуры. С целью проверки воздействия высокотемпературной обработки водяным паром на структурные свойства цеолитов был проведен рентгенофазовый анализ образцов катализаторов La-Zr-HZSM-5/Al2O3 и Mg-HZSM-5/Al2O3 до и после обработки по сравнению с исходным HZSM-5/Al2O3.
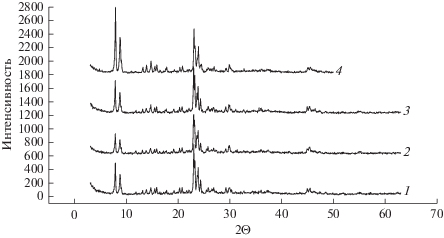
По данным РФА, приведенным на рис. 1 для ряда модифицированных цеолитов, все изученные образцы, независимо от природы модифицирующего агента, способа модифицирования и температуры обработки, отвечают кристаллографическому типу цеолита ZSM-5. Рассчитанные параметры элементарной ячейки составляют: a = = 20.09, b = 19.96, c = 13.40 Å (по литературным данным a = 20.02, b = 19.89, c = 13.38 Å [39]). Таким образом, обработка паром не привела к полному разрушению кристаллической решетки цеолита. Параметры элементарной ячейки цеолита также практически не изменились.
Рис. 1.
Рентгенограммы цеолитных катализаторов: 1 – HZSM-5/Al2O3, 2 – Mg-HZSM-5/Al2O3, 3 – La-Zr-HZSM-5/Al2O3, 4 – La-Zr-HZSM-5/Al2O3, обработанный водяным паром при 500°С.
На рис. 2 показаны спектры 29Si ЯМР образцов La-Zr-HZSM-5 и Mg-HZSM-5 до и после обработки водяным паром. Сопоставление положения сигналов с литературными данными [40] для немодифицированного цеолита позволяет отнести рефлекс при –108.5 м.д. в спектре 29Si ЯМР к структуре Si(OSi)4, а сигнал вблизи –104.2 м.д. отвечает гидратированным группам Si(OH)(OSi)3. В результате обработки водяным паром при 500°С La-Zr-HZSM-5 плечо при –104.5 м.д. исчезает, а у Mg-HZSM-5 снижается.
Рис. 2.
Спектры 29Si ЯМР ВМУ твердого тела для катализаторов La-Zr-HZSM-5 (а) и Mg-HZSM-5 (б): 1 – HZSM-5, 2 – La-Zr-HZSM-5, 3 – La-Zr-HZSM-5, обработанный водяным паром при 500°С, 4 – La-Zr-HZSM-5, обработанный водяным паром при 750°С, 5 – Mg-HZSM-5, 6 – Mg-HZSM-5, обработанный водяным паром при 500°С, 7 – Mg-HZSM-5, обработанный водяным паром при 750°С.
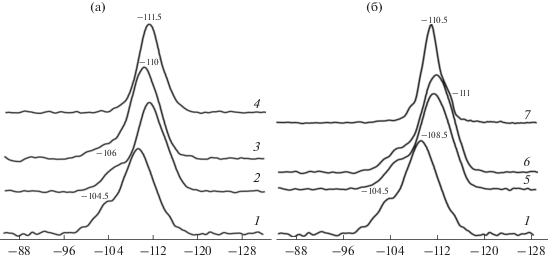
Подобный эффект может быть обусловлен деалюминированием цеолита при высокой температурной обработке катализаторов водяным паром. Для образцов, модифицированных соединениями лантана и циркония, а также магния происходило смещение рефлекса 29Si от –108.5 к –110 м.д., что свидетельствует об изменении локального окружения атомов кремния в кристаллической структуре цеолита.
Более существенные изменения наблюдались в спектре 27Al ЯМР (рис. 3). Рефлекс 27Al при 58.5 м.д., соответствующий тетрагонально-координированным атомам алюминия в структуре цеолита, при обработке соединениями модификаторов смещался к 56 м.д., а при высокотемпературной обработке катализатора Mg-HZSM-5 водяным паром – к 53.6 м.д. Кроме того, в спектре появился широкий сигнал, совпавший с резонансом стандарта вблизи 0 м.д. Таким образом, можно заключить, что часть атомов алюминия в ходе модифицирования и обработки водяным паром извлекалась из структуры цеолита и переходила в ионы Al3+.
Рис. 3.
Спектры 27Al ЯМР ВМУ твердого тела для катализаторов La-Zr-HZSM-5 (а) и Mg-HZSM-5 (б): 1 – HZSM-5, 2 – La-Zr-HZSM-5, 3 – La-Zr-HZSM-5, обработанный водяным паром при 500°С, 4 – La-Zr-HZSM-5, обработанный водяным паром при 750°С, 5 – Mg-HZSM-5, 6 – Mg-HZSM-5, обработанный водяным паром при 500°С, 7 – Mg-HZSM-5, обработанный водяным паром при 750°С.
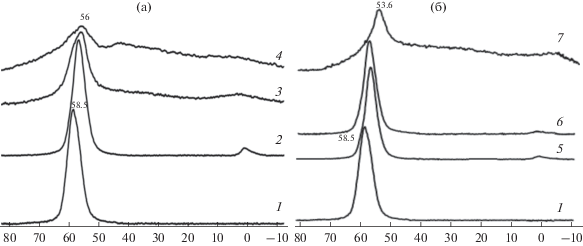
В спектрах 27Al ЯМР обращает на себя факт заметного уменьшения интенсивности сигнала в районе 56 м.д., наблюдаемого для катализатора La-Zr-HZSM-5, обработанного водяным паром, особенно при 750°С. Учитывая, что накопление сигналов во всех случаях одинаково, возможно данное явление обусловлено понижением степени кристалличности цеолита, в том числе в результате деалюминирования. Сопоставление интенсивности сигналов 27Al ЯМР для этих катализаторов позволяет предположить, что наличие оксида магния в образце способствует некоторой стабилизации структуры при высокотемпературной обработке водяным паром.
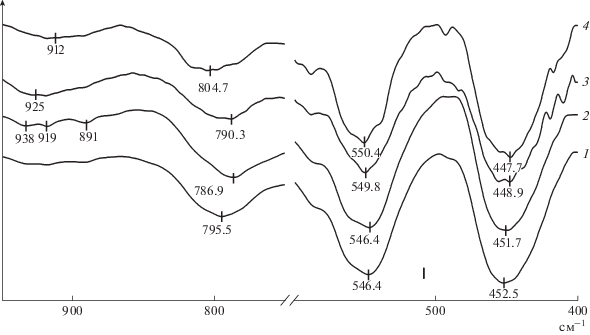
На рис. 4 приведены данные по исследованию кристаллической структуры La-Zr-HZSM-5/Al2O3 до и после высокотемпературной обработки водяным паром, полученные методом ИК-спектроскопии. В спектре исходного HZSM-5/Al2O3 обнаружены полосы поглощения (п.п.) в области 720–780 см–1, которые характеризуют связь Al–O с тетраэдрическим окружением вокруг алюминия. В случае цеолитного катализатора HZSM-5/Al2O3, модифицированного La и Zr (спектр 2), происходит смещение полосы от 795.5 до 786.9 см–1, что указывает на появление гетероатомов в составе цеолита. Обработка катализатора La-Zr-HZSM-5/Al2O3 водяным паром при 500°С приводит к смещению этой полосы поглощения в сторону коротких волн до 790.3 см–1 (спектр 3), а обработка катализатора водяным паром при 750°С к еще большему смещению этой полосы до 804.7 см–1 (спектр 4). Такое смещение полосы поглощения указывает на уменьшение числа атомов алюминия в тетраэдрической конфигурации и увеличение координационного числа оставшегося алюминия. При этом не обнаружено заметных изменений интенсивности и положения п.п. деформационных колебаний в области структурных колебаний каркаса цеолита при 450 и 550 см–1. Таким образом, обработка катализаторов водяным паром приводит к деалюминированию, при этом оставшийся алюминий частично теряет тетраэдрическое окружение [32].
Рис. 4.
ИК-спектры образцов катализаторов: HZSM-5/Al2O3 (1), La-Zr-HZSM-5/Al2O3 (2) и La-Zr-HZSM-5/Al2O3, обработанные водяным паром при 500 (3) и 750°С (4).
Были изучены адсорбционные свойства катализаторов La-Zr-HZSM-5/Al2O3 и Mg-HZSM-5/Al2O3 до и после обработки водяным паром. Для катализатора La-Zr-HZSM-5/Al2O3 объем адсорбированного бензола с ростом температуры обработки паром снижается, а для образца Mg-HZSM-5/Al2O3 возрастает (табл. 3). Маловероятно, чтобы это было связано с разным ходом разрушения кристаллической решетки цеолита, так как лантансодержащие формы более стабильны. По-видимому, здесь решающую роль играет миграция катионов, интенсивно протекающая при высокотемпературной обработке катализаторов водяным паром. При этом лантан и цирконий, вероятно, преимущественно концентрируются в цеолите, уменьшая тем самым объем пор, а магний в связующем веществе – оксиде алюминия, освобождая поры цеолита. Вместе с тем, следует учитывать разный характер адсорбции бензола на данных образцах катализаторов, приводящий к возможно завышенному значению предельной адсорбции для Mg-HZSM-5/Al2O3. Высокотемпературная обработка водяным паром при 750°С приводит к частичному разрушению кристаллической структуры цеолита, что подтверждается существенным уменьшением величины адсорбции аммиака по данным ТПД аммиака (табл. 2).
Таблица 3.
Рассчитанные значения предельной адсорбции, характеристических энергий и дифференциальных мольных теплот адсорбции
| Образец | а0, мкмоль/г |
Е, кДж/моль ±0.5 | Q, кДж/моль ± 1.0 | ||
|---|---|---|---|---|---|
| а = 10 мкмоль/г |
а = 100 мкмоль/г |
а = 200 мкмоль/г |
|||
| HZSM-5/Al2O3 | 1219 | 19.6 | 112 | 67 | 52 |
| La-Zr-HZSM-5/Al2O3 | 1121 | 16.9 | 94 | 56 | 43 |
| La-Zr-HZSM-5/Al2O3, обработанный водяным паром при 500°С | 987 | 16.1 | 87 | 51 | 39 |
| La-Zr-HZSM-5/Al2O3, обработанный водяным паром при 750°С | 590 | 20.6 | 103 | 54 | 38 |
| Mg-HZSM-5/Al2O3 | 813 | 19.9 | 104 | 59 | 44 |
| Mg-HZSM-5/Al2O3, обработанный водяным паром при 500°С | 997 | 17.3 | 94 | 55 | 48 |
| Mg-HZSM-5/Al2O3, обработанный водяным паром при 750°С* | 1050 | 16.0 | 88 | 51 | 39 |
Из экспериментальных данных по уравнению Дубинина были рассчитаны характеристические энергии адсорбции Е для бензола [41]. Как видно из табл. 3, характеристические энергии адсорбции для бензола различаются в зависимости от природы модификатора и температуры прокаливания. Наблюдается почти антибатное изменение характеристической энергии адсорбции и предельной адсорбции бензола. Для образцов катализатора La-Zr-HZSM-5/Al2O3 при снижении предельной адсорбции бензола наблюдается рост характеристической энергии адсорбции, что может указывать на роль катионов лантана и циркония, сконцентрировавшихся в цеолите. В противоположность этому для образца катализатора Mg-HZSM-5/Al2O3 при высокотемпературной обработке водяным паром с ростом предельной адсорбции снижается характеристическая энергия адсорбции бензола, что соответствует концентрированию магния в связующем.
Максимальная теплота адсорбции при всех приведенных значениях а получена для исходного цеолита HZSM-5/Al2O3. С увеличением величины а значения Q адсорбированного бензола для всех образцов закономерно падают.
В работе [42] было отмечено, что при неспецифической адсорбции н-парафинов в каналах пентасилов характеристическая энергия адсорбции не превышает ~22 кДж/моль. В настоящем случае для бензола установлена Е от 16 до 21 кДж/моль. Таким образом, характер адсорбции молекул бензола носит, вероятнее всего, неспецифический характер и наблюдаемые изменения в значениях характеристической энергии адсорбции, по-видимому, связаны с диффузионными факторами.
Полученные катализаторы с различными модификаторами и различной постсинтетической обработкой были исследованы в конверсии ДМЭ в низшие олефины при двух температурах реакции (320 и 380°С), которые соответствуют температурам входа и выхода из реакционной зоны промышленного адиабатического реактора (табл. 4).
Введение активного элемента в цеолитный катализатор изменяет не только кислотные, но и каталитические свойства. Во всех случаях при Т = 320°С модифицирование приводит к снижению каталитической активности, кроме магния. Селективность образования этилена и пропилена изменяется симбатно изменению доли кислотных центров средней силы (I) по отношению к сильным кислотным центрам (II). Именно кислотные центры средней силы участвуют в каталитических актах образования этилена и пропилена, а конверсия ДМЭ протекает на всех кислотных центрах [32].
Таблица 4.
Конверсия диметилового эфира в низшие олефины на цеолитных катализаторах (Р = 0.1 МПа, сырье: 10 об. % ДМЭ + 90 об. % N2, WДМЭ = 0.9 ч–1, Т = 320°С, WДМЭ = 3.7 ч–1, Т = 380°С, данные приведены за 4 ч работы)
| Катализатор | Т, °С | Конверсия ДМЭ, % | Селективность по УВ, мас. % | Σ
олефинов С2–С5 |
|||
|---|---|---|---|---|---|---|---|
| ${\text{C}}_{2}^{ = }$ | ${\text{C}}_{3}^{ = }$ | Σ${\text{C}}_{4}^{ = }$ | парафины ${\text{C}}_{1}^{ + }$ | ||||
| HZSM-5/Al2O3 | 320 | 67.4 | 9.2 | 14.9 | 19.5 | 55.3 | 44.7 |
| 380 | 94.3 | 21.6 | 23.3 | 11.5 | 36.9 | 63.2 | |
| Mg-HZSM-5/Al2O3 | 320 | 72.6 | 30.2 | 31.5 | 12.8 | 22.2 | 77.8 |
| 380 | 97.3 | 13.7 | 31.6 | 17.4 | 31.6 | 68.4 | |
| La-HZSM-5/Al2O3 | 320 | 46.9 | 18.6 | 38.0 | 14.1 | 25.5 | 74.5 |
| 380 | 96.6 | 13.0 | 25.9 | 13.9 | 43.0 | 57.0 | |
| Zr-HZSM-5/Al2O3 | 320 | 47.3 | 22.3 | 36.0 | 13.1 | 25.4 | 74.6 |
| 380 | 87.2 | 14.3 | 25.8 | 11.5 | 44.6 | 55.4 | |
| La-Zr-HZSM-5/Al2O3 | 320 | 50.1 | 21.9 | 36.1 | 13.0 | 25.2 | 74.8 |
| 380 | 91.5 | 13.0 | 27.1 | 13.0 | 42.6 | 57.4 | |
| Высокотемпературная обработка цеолита (Т) | |||||||
| La-Zr-HZSM-5(T)/Al2O3 | 320 | 65.0 | 25.1 | 30.0 | 8.4 | 26.7 | 73.3 |
| 380 | 95.4 | 20.9 | 29.2 | 8.9 | 34.4 | 65.6 | |
| Высокотемпературная обработка водяным паром при 500°С | |||||||
| Mg-HZSM-5/Al2O3 | 320 | 93.4 | 26.8 | 24.1 | 14.6 | 30.1 | 69.9 |
| 380 | 93.2 | 10.4 | 36.0 | 17.2 | 30.5 | 69.5 | |
| La-HZSM-5/Al2O3 | 320 | 99.7 | 20.0 | 16.0 | 14.8 | 44.5 | 55.5 |
| 380 | 98.4 | 11.9 | 29.2 | 15.7 | 38.0 | 62.0 | |
| Zr-HZSM-5/Al2O3 | 320 | 99.2 | 19.0 | 16.1 | 13.5 | 47.0 | 53.0 |
| 380 | 95.0 | 13.1 | 29.8 | 14.3 | 38.5 | 61.5 | |
| La-Zr-HZSM-5/Al2O3 | 320 | 95.9 | 24.8 | 20.9 | 14.7 | 35.0 | 65.0 |
| 380 | 90.8 | 12.1 | 33.6 | 14.8 | 34.3 | 65.7 | |
| Высокотемпературная обработка водяным паром при 750°С | |||||||
| La-Zr-HZSM-5/Al2O3 | 380 | 2.9 | 8.7 | 36.1 | 13.4 | 19.6 | 80.4 |
Повышение температуры реакции с 320 до 380°С приводит к возрастанию активности при снижении выхода олефинов, что связано с возрастанием скорости вторичных реакций.
Высокотемпературная обработка исходного цеолита приводит к повышению селективности по олефинам и демонстрирует высокую и стабильную во времени конверсию ДМЭ, существенно превосходящую наблюдаемую для исходного катализатора [32].
Высокотемпературная обработка катализаторов водяным паром при 500°С приводит к значительному повешению активности как при 320°С, так и при 380°С, при этом наблюдается незначительное снижение селективности, что в основном связано с изменением кислотности (табл. 4). Обработка катализатора водяным паром при 750°С приводит к резкому снижению конверсии ДМЭ (с 99.8 до 2.9 мас. %) при росте селективности образования олефинов и снижении селективности образования алканов, что вероятнее всего связано с частичным разрушением кристаллической структуры цеолита [32].
Процесс синтеза низших олефинов обычно проводят в среде инертного газа при концентрации ДМЭ не более 30 об. % Если процесс ведут в среде водяного пара, что используется в технологии ряда промышленных процессов [18–21], соотношение водяной пар/сырье может оказывать существенное влияние на распределение продуктов превращения ДМЭ [43]. Изменение этого соотношения может приводить как к повышению, так и к снижению содержания низкомолекулярных олефинов С2–С4. Кроме того, при проведении процесса синтеза низших олефинов из СО и Н2 через ДМЭ на стадии получения ДМЭ из СО и Н2 также образуется вода, которая может переходить на стадию синтеза низших олефинов.
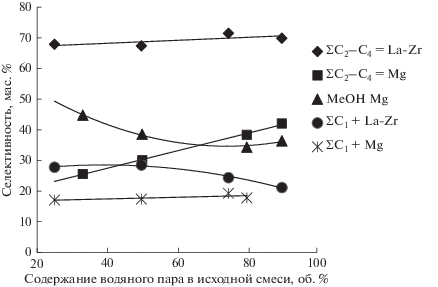
Исследование влияния соотношения ДМЭ/водяной пар на распределение продуктов реакции в отсутствии азота проводили при постоянной нагрузке по ДМЭ. Замена азота на водяной пар оказывает значительное влияние на каталитические свойства цеолитных катализаторов, и это влияние также сильно зависит от природы модифицирующих элементов (рис. 5). Так, при добавлении водяного пара в сырье, когда концентрация ДМЭ составляет 20 об. %, на катализаторе La-Zr-HZSM-5/Al2O3 суммарная селективность по олефинам С2–С4 практически не меняется, и слабо зависит от содержания водяного пара в сырье (от 25 до 90 об. %). Метанола в продуктах реакции обнаружено не было, а содержание алканов уменьшилось с увеличением концентрации водяного пара в сырье. На цеолитном катализаторе, модифицированном магнием, в присутствии водяного пара селективность по низшим олефинам резко снижается. Однако с ростом содержания водяного пара селективность по олефинам повышается, селективность по алканам практически не изменяется, при этом в продуктах реакции наблюдается высокое содержание метанола. Содержание метанола, хотя и падает с увеличением содержания водяного пара, количество его остается превалирующим.
Рис. 5.
Влияние разбавления сырья водяным паром на каталитические свойства La-Zr-HZSM-5/Al2O3 и Mg-HZSM-5/Al2O3.
Методом ИКСДО in situ было показано, что при пропускании ДМЭ через Mg-HZSM-5/Al2O3 появляются полосы от связей С–О в метокси-группах в области 1084 см–1 [44], однако при пропускании ДМЭ с Н2О в спектре Mg-HZSM-5/Al2O3, зарегистрированного в тех же условиях, она уже отсутствует, но резко увеличивается интенсивность полосы 1047 см–1, которая является самой сильной полосой в спектре метанола. Образование метокси-групп на поверхности цеолита может происходить при взаимодействии ДМЭ с основными центрами на поверхности цеолита (п.п. 3720 см–1) с выделением метанола, как показано в [45].
При синтезе низших олефинов из ДМЭ во многих случаях наблюдается образование метанола, который в свою очередь может оказывать влияние на состав продуктов конверсии ДМЭ.
Данные по влиянию метанола на каталитические свойства La-Zr-HZSM-5/Al2O3 приведены в табл. 5. Как видно из таблицы, добавление метанола к ДМЭ практически не влияет на суммарную селективность по олефинам, при этом с повышением концентрации метанола с 10 до 30 об. % повышается содержание этилена с 25.8 до 30.9 мас. %, а количество пропилена несколько снижается и в продуктах реакции содержится много алканов, состоящих примерно на 15 мас. % из метана. При увеличении концентрации ДМЭ в сырье до 30 об. % в присутствии метанола снижается селективность по олефинам, в частности, по этилену, и повышается содержание алканов. Снижение объемной скорости исходной смеси до 4000 ч–1 приводит к снижению содержания алканов и к повышению селективности по олефинам.
Таблица 5.
Влияние добавления метанола в исходную смесь на каталитические свойства La-Zr-HZSM-5/Al2O3 (Р = 0.1 МПа, Т = 340°С, данные приведены за 4 ч работы)
| Исходная смесь, об. % | Параметры | Селективность по УВ, мас. % | Σ олефинов С2–С5 | |||
|---|---|---|---|---|---|---|
| ${\text{C}}_{2}^{ = }$ | ${\text{C}}_{3}^{ = }$ | Σ${\text{C}}_{4}^{ = }$ | парафины ${\text{C}}_{1}^{ + }$ | |||
| ДМЭ(20) + N2(80) | Vсмеси = 6000 ч–1 Wдмэ = 4.1 ч–1 |
26.4 | 34.8 | 9.4 | 21.6 | 78.4 |
| ДМЭ(20) + МеOH(10) + N2(70) | Vсмеси = 6000 ч–1 Wдмэ = 4.1 ч–1 WМеOH = 1.6 ч–1 |
25.8 | 33.8 | 8.2 | 25.1 | 74.9 |
| ДМЭ(20) + МеOH(20) + N2(60) | Vсмеси = 6000 ч–1 Wдмэ = 4.1 ч–1 WМеOH = 3.2 ч–1 |
28.1 | 33.2 | 7.9 | 23.8 | 76.2 |
| ДМЭ(20) + МеOH(30) + N2(50) | Vсмеси = 6000 ч–1 Wдмэ = 4.1 ч–1 WМеOH = 4.8 ч–1 |
30.9 | 32.5 | 7.1 | 24.2 | 75.8 |
| ДМЭ(30) + МеOH(30) + N2(40) | Vсмеси = 6000 ч–1 Wдмэ = 6.8 ч–1 WМеOH = 4.8 ч–1 |
25.4 | 31.1 | 7.2 | 30.5 | 69.5 |
| ДМЭ(30) + МеOH(30) + N2(40) | Vсмеси = 4000 ч–1 Wдмэ = 4.6 ч–1 WМеOH = 3.2 ч–1 |
27.5 | 33.3 | 7.6 | 25.7 | 74.3 |
| МеOH(20) + N2(80) | Vсмеси = 6000 ч–1 WМеOH = 3.2 ч–1 |
25.8 | 23.1 | 7.5 | 38.7 | 71.8 |
Таким образом, при проведении реакции в среде азота, присутствие метанола в зоне реакции при концентрации ДМЭ 20 об. % не оказывает существенного влияния на каталитические свойства La-Zr-HZSM-5/Al2O3; однако, при концентрации ДМЭ до 30 об. % присутствие метанола приводит к снижению селективности по этилену и пропилену.
При замене азота на водяной пар (табл. 6) в присутствии метанола суммарная селективность по олефинам практически не изменилась, при использовании в качестве сырья равновесной смеси оксигенатов с водяным паром возрастает доля этилена в продуктах реакции.
Таблица 6.
Конверсия оксигенатов в низшие олефины на катализаторе La-Zr-HZSM-5/Al2O3 (Р = 0.1МПа, Т = 340°С; Vсмеси= 4000 ч–1, данные приведены за 4 ч работы)
| Исходная смесь | Параметры | Селективность по УВ, мас. % | Σ олефинов С2–С5 | |||
|---|---|---|---|---|---|---|
| С2= | С3= | ΣС4= | Парафины С1+ | |||
| ДМЭ(30) + МеOH(30) + N2(40) | Wдмэ = 4.6 ч–1 WМеOH = 3.2 ч–1 |
27.5 | 33.3 | 7.6 | 25.7 | 74.3 |
| ДМЭ(30) + МеOH(30) + H2O(40) | Wдмэ = 4.0 ч–1 WМеOH = 3.2 ч–1 ${{W}_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}$ = 2.0 ч–1 |
31.9 | 33.4 | 6.1 | 25.3 | 74.7 |
ЗАКЛЮЧЕНИЕ
Природа активного элемента оказывает существенное влияние на каталитические и кислотные свойства модифицированного цеолитного катализатора превращения диметилового эфира в низшие олефины. Селективность образования низших олефинов изменяется симбатно повышению доли кислотных центров средней силы по отношению к сильным кислотным центрам при снижении суммарной кислотности. Таким образом, кислотные центры средней силы участвуют в каталитических актах образования этилена и пропилена, а конверсия ДМЭ протекает на всех кислотных центрах.
Постсинтетическая высокотемпературная обработка цеолита НZSM-5, а также высокотемпературная обработка катализатора водяным паром при 500°С приводит к существенному повышению его стабильности.
Присутствие водяного пара в сырье по-разному влияет на каталитические свойства цеолитного катализатора. Так, для La-Zr-НZSM-5/Al2O3 водяной пар повышает его стабильность и селективность, а для Mg-HZSM-5/Al2O3 селективность по низшим олефинам резко падает и в продуктах реакции обнаруживается большое количество метанола.
При использовании в качестве сырья равновесной смеси оксигенатов с водяным паром (ДМЭ + МеOH + H2O) возрастает доля этилена в продуктах реакции.
Исследование выполнено на базе ИНХС РАН за счет гранта Российского научного фонда (проект № 17-73-30046).
Список литературы
Брагинский О.Б. Нефтехимический комплекс мира. М.: Academia, 2009. 800 с.
Hajjar Z., Khodadadi A., Mortazavi Y., Tayyebi S., Soltanali S. // Fuel. 2016. V. 179. P.79.
Kolesnichenko N.V., Kolesnikova E.E., Kitaev L.E., Biryukova E.N., Trukhmanova N.I., Khadzhiev S.N. // Petrol. Chemistry. 2012. V. 52. № 3. P. 155.
Khadzhiev S.N., Kolesnichenko N.V., Ezhova N.N. // Petrol. Chemistry. V. 48. № 5. P. 325.
Tamm S., Ingelsten H.H., Skoglundh M., Palmqvist A.E.C. // J. of Catalysis. 2010. V. 276. P. 402.
Миначев Х.М., Дергачев А.А. //Изв. АН СССР. Сер. Хим. 1993. № 6. С. 1018.
Seddon D. // Catal. Today. 1998. № 6. P. 351.
Choudhary V.R., Banerjee S., Devadas P. // J. Catal. 2002. № 2. V. 205. P. 398.
Dmitriev R.V., Shevchenko D.P., Shpiro E.S, Dergachev A.A., Tkachenko O.P., Minachev Kh.M. // Stud. Surf. Sci. Catal. 1991. V. 69. P. 381.
Freeman D., Wells R.P.K., Hutschings G.J. // J. Catal. 2002. V. 205. № 2. P. 358.
Kolesnichenko N.V., Goryainova T.I., Biryukova E.N., Yashina O.V., Khadzhiev S.N. // Petrol. Chemistry. 2011. V. 51. № 1. P. 55.
Mikhailov M.N., Kazansky V.B., Kustov L.M. // Catal. Lett. 2007. V. 116. P. 81.
Zhidomirov G.M., Shubin A.A., Kazansky V.B., Van Santen R.A. // Theoret. Chem. Account. 2005. V. 114. P. 90.
Borman S. // Chem. and Eng. News. 2005. V. 83. P. 15.
Stewart E. A., Johnson D.W., Shannon M.D. // Innovation in Zeolite Materials Science. 1988. V. 37. P. 57.
Vosmerikova L.N., Vagin A.I., Vosmerikov A.V. // Nefteper. i Neftehim. 2002. V. 2. P. 27.
Kubasov A.A., Kitaev L.E., Malyshev S.V., Novakovskaya Yu.V. // Vest. Mosk. Univer. Khim. 2010. V. 51. P. 339.
Birke G., Koempel H., Liebner W., Bach H. / Pat. USA № 7923591. 2011.
McGlamery Jr. G.G., Beech Jr. Jam. H., Nicoletti M.P., Van Egmond C.F. / Pat. USA 7989669. 2011.
Bozzano A.G., Bradley S.A., Castillo R. L., Chen John Q. / Pat. USA № 7763766. 2010.
Vermeiren W., Nesterenko N. / Pat. 8362183 USA. 2013.
Хаджиев С.Н. Крекинг нефтяных фракций на цеолитсодержащих катализаторах. М.: “Химия”, 1982. 280 с.
Шеманаева М.Н., Мельник Л.В., Крюков С.И., Москвичев Ю.А., Среднев С.С., Суровцев А.А., Карпов О.П. / Пат. РФ № 2174113. 2001.
Al- Jarallah A.M., El- Natafy U.A., Abdillahi M.M. // Appl. Catal. A: General. 1997. V. 154. P. 117.
Baltes H., Litterer H., Leupold E.I., Wunder F. Deutsche Offenlegungsschrift DE 3141 283 A1. 1983.
Dettmeier U., Baltes H., Litterer H., Leupold E.I., Herzog W., Wunder F. // Chem. Ing. Technol. 1982. V. 54. P. 593.
Dehertog W.J.H., Froment G.F. // Appl. Catal. 1991. V. 71. P. 193.
Cai G., Chen G., Wang Q., Xin Q., Wang X., Li X., Liang J., in: Drzaj B., Hocevar S., Pejovnik S. (Eds.). Zeolites. Amsterdam: Elsevier, 1985. P. 319.
Balkrishnan I., Rao B.S., Hegde S.G., Kotasthane A.N., Kulharni S.B., Ratnaswamy P. // J. Mol. Catal. 1982. V. 17. P. 261.
Kolesnichenko N.V., Yashina O.V., Markova N.A., Biryukova E.N., Goryainova T.I., Kulumbegov R.V., Khadzhiev S.N., Kitaev L.E., Yushchenko V.V. // Petrol. Chemistry. 2009. V. 49. № 1. P. 42.
Goryainova T.I., Biryukova E.N., Kolesnichenko N.V., Khadzhiev S.N. // Petrol. Chemistry. 2011. V. 51. № 3. P. 169.
Khadzhiev S.N., Kolesnichenko N.V., Khivrich E.N., Kolesnikova E.E., Batova T.I. // Petrol. Chemistry. 2013. V. 53. № 4. P. 225.
Хиврич Е.Н., Батова Т.И., Колесникова Е.Е., Колесниченко Н.В., Туркова Т.В. // Химическая промышленность сегодня. 2014. № 6. С. 9.
Хаджиев С.Н., Гайрбекова С.М., Дорогочинский А.З. Лабораторные методы оценки активности и селективности алюмосиликатных катализаторов крекинга. Аналитический и сопоставительный обзор. М.: ЦНИИТЭНефтехим, 1972. 67 с.
Barger P.T., Heights A. // Pat. USA № 5095163. 1992.
Kolesnikova E.E., Kitaev L.E., Biryukova E.N., Kolesnichenko N.V., Khadzhiev S.N. // Petrol. Chemistry. 2013. V. 53. № 1. P. 33.
Древинг В.П., Муттик Г.Г, Безус А.Г. Под ред. Никитина Ю.С., Петровой Р.С. Экспериментальные методы в адсорбции и молекулярной хроматографии. М.: Изд-во МГУ, 1990. 315 с.
Ющенко В.В. // Журн. физ. химии. 1997. Т. 71. № 4. С. 6.
Treacy M.M.J., Higgins J.B. Collection of Simulated XRD Powder Patterns for Zeolites. Elsevier. 2001. P. 493.
Zhang F.Z., Guo X.W., Wang X.S.,Li G.Y., Zhao Q., Bao X.H., Xan X.W., Lin L.W. // Materials Chemistry and Physics. 1999. V. 60. P. 215.
Китаев Л.Е., Кубасов А.А., Шахновская О.Л., Дорожко С.П., Нефедов Б.К., Абрамова А.В., Алексеенко Л.Н., Фрейман Л.Л. // Вестн. Моск. Ун-та. Сер. 2. Химия. 1995. Т. 36. № 6. С. 530.
Китаев Л.Е., Колдашева Е.М., Кубасов А.А., Кострико Е.Э. // Вестн. Моск. Ун-та. Сер. 2. Химия. 1997. Т. 38. № 1. С. 26.
Лаврентьева Т.А., Каратун О.Н. // Вестник АГТУ. 2009. Т. 48. № 1. С. 42.
Давыдов А.А. ИК-спектроскопия в химии поверхности окислов. Новосибирск: Наука, 1984. С. 222.
Batova T.I., Khivrich E.N., Shirobokova G.N., Kolesnichenko N.V., Pavlyuk Yu.V., Bondarenko G.N. // Petr-ol. Chemistry. 2013. V. 53. № 6. P. 383.
Дополнительные материалы отсутствуют.


