Нефтехимия, 2019, T. 59, № 6-1, стр. 674-683
Исследование Pt-содержащих катализаторов на основе упорядоченного алюмосиликата типа Al-МСМ-41 и природных нанотрубок галлуазита в изомеризации ксилолов
А. П. Глотов 1, *, М. И. Артемова 1, Н. Р. Демихова 1, Е. М. Смирнова 1, Е. В. Иванов 1, П. А. Гущин 1, С. В. Егазарьянц 2, В. А. Винокуров 1
1 РГУ нефти и газа (НИУ) имени И.М. Губкина
119991 Москва, Россия
2 Московский государственный университет имени М.В. Ломоносова
119991 Москва, Россия
* E-mail: glotov.a@gubkin.ru
Поступила в редакцию 13.06.2019
После доработки 01.07.2019
Принята к публикации 02.07.2019
Аннотация
Синтезированы и исследованы иерархические композитные материалы на основе упорядоченных алюмосиликатов типа Al-MCM-41 и галлуазитных нанотрубок (ГНТ) с различным массовым соотношением Al-MCM-41/галлуазит в качестве компонентов носителей Pt-содержащих катализаторов изомеризации ароматической фракции С-8 риформинга. На каждом этапе синтеза материалы были охарактеризованы методами просвечивающей электронной микроскопии (ПЭМ), низкотемпературной адсорбции азота, рентгенофлуоресцентного анализа, рентгенофазового анализа (РФА) и термопрограммируемой десорбцией аммиака (ТПД NH3). В изомеризации ксилолов наиболее эффективно проявили себя каталитические системы с массовым соотношением Al-MCM-41/ГНТ = 90 : 10 мас. %, обеспечив бóльшую конверсию этилбензола и м-ксилола, чем катализатор на основе ГНТ. Установлено, что синтезированные катализаторы обладают большей селективностью по целевому продукту процесса, n-ксилолу, чем промышленный аналог в диапазоне температур 360–440°C. Максимальное значение селективности по n-ксилолу достигнуто в присутствии катализатора Pt/Al-MCM-41/ГНТ(90 : 10)/Al2O3 при 360°C (70%).
Фракция, поступающая с установок риформинга, богата ароматическими соединениями состава С8H10 (пара-, орто-, мета-ксилолы и этилбензол). Основная часть ксилолов идет на дальнейшую переработку с целью извлечения изомеров, в первую очередь n- и о-ксилолов. Так фталевый ангидрид, получаемый из о-ксилола, является сырьем для производства пластификаторов и алкидных смол, а переработка n-ксилола в терефталевую кислоту и диметилтерефталат создает сырьевую базу для производства синтетических (полиэфирных) волокон и пластмасс, в частности, полиэтилентерефталата (ПЭТ) [1].
На сегодняшний день катализаторы и процессы изомеризации нефтехимического ароматического сырья достаточно хорошо изучены [2–4]. Несмотря на это, по-прежнему актуальна задача разработки и модификации катализаторов процесса изомеризации С-8 фракции с целью достижения высокого выхода n-ксилола при одновременном снижении общих потерь ксилолов, а также возможностью переработки сырья с высоким содержанием этилбензола.
Ключевую роль в активности катализатора играют природа и свойства используемого носителя, важными характеристиками которого являются удельная площадь поверхности, кислотность, объем пор, термостабильность и др. [5–8]. В качестве активной фазы носителя, как правило, используют цеолиты. В литературе чаще всего упоминаются цеолиты типа ZSM-5 и MOR [9]. Однако их микропористая структура затрудняет диффузию углеводородного сырья к активным центрам катализатора, что снижает конверсию и увеличивает коксообразование с последующей дезактивацией катализатора [10]. Потенциальным решением данной проблемы является применение в качестве компонента носителя мезопористых аналогов цеолитов [11]. Наиболее известным и хорошо изученным представителем семейства структурированных мезопористых материалов на основе оксида кремния является материал типа MCM-41, обладающий регулярной гексагональной упаковкой с диаметром пор в диапазоне 2–4 нм и высокой удельной площадью поверхности (1000–1200 м2 г–1). [12]. Для получения такой структуры используют метод темплатного синтеза, подробно описанный в [13]. Однако сам по себе оксид кремния обладает низкой кислотностью. В тоже время наличие в катализаторах изомеризации сильных кислотных центров во многом определяет их активность. Дополнительно увеличить кислотность MCM-41 можно за счет внедрения в его структуру атомов алюминия на этапе синтеза. Получаемые в ходе такой процедуры мезопористые алюмосиликаты типа Al-МСМ-41 содержат большое количество сильных кислотных центров и представляют интерес в качестве компонентов носителей катализаторов [14].
Тем не менее, алюмосиликаты Al-MCM-41 обладают существенным недостатком: стенки их пор на молекулярном уровне аморфны и имеют малую толщину (порядка 0.8 нм), что обусловливает их плохую термическую стабильность по сравнению с кристаллическими алюмосиликатами. Стабильность таких материалов можно улучшить путем их армирования на стадии синтеза более прочными материалами, например галлуазитом.
Галлуазит способен выдерживать воздействие высоких температур, его кристаллическая структура сохраняется до 400°С, а трубчатая морфология – до 1100°С [15, 16]. Помимо термической устойчивости, галлуазит обладает уникальными химическими свойствами. При сворачивании алюмосиликата в трубки слой положительно заряженного оксида алюминия находится внутри, а отрицательно заряженного оксида кремния – снаружи. Это позволяет проводить селективную модификацию внутренней/внешней поверхностей нанотрубок, что делает галлуазит перспективной основой для синтеза иерархической структуры алюмосиликатов [17–19].
Ранее нами было показано, что введение галлуазитных нанотрубок в структуру MCM-41 позволяет значительно улучшить термомеханические характеристики материала [20]. В этой же работе было предположено, что полученные нанокомпозиты могут быть эффективно использованы в качестве катализаторов или сорбентов.
Таким образом, представляло интерес исследование возможности использования композитных материалов на основе алюмосиликатов типа Al-MCM-41 и нанотрубок галлуазита в качестве компонентов катализаторов изомеризации фракции С-8 риформинга.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез упорядоченных мезопористых алюмосиликатов Al-MCM-41-ГНТ. Упорядоченный мезопористый композит типа Al-MCM-41/ГНТ был синтезирован методом темплатного синтеза по модифицированной методике [21]. Для определения допустимого содержания галлуазита в функциональном материале были изготовлены два образца с различным массовым соотношением Al-MCM-41 : ГНТ – 90 : 10 и 60 : 40 мас. %
Галлуазит (фирмы Aldrich) диспергировали в смесь цетилтриметиламмоний бромида (C-TMABr, A-ldrich) и изопропилового спирта (ИПС, ЭКОС-1) непосредственно перед стадией добавления тетраэтоксисилана (Aldrich). В качестве источника алюминия использовали изопропоксид алюминия (Aldrich).
Полученный гель состава Al2O3/40 SiO2/ 2 CTMABr/1555 H2O/150 ИПС/3.76 ГНТ термостатировали при 90°Св течение 48 ч, фильтровали и промывали дистиллированной водой до отсутствия бромид-ионов в маточном растворе, сушили при 80, 90, 100 и 110°С по 4 ч, а затем прокаливали в токе воздуха при 550°С в течение 4 ч.
Формовка носителя Al-MCM-41-Галлуазит/Al2O3. В качестве связующего вещества для приготовления носителя катализаторов в виде экструдатов использовали бемит фирмы Sasol марки Pural SB в соотношении алюмосиликат : бемит = 60 : 40 мас. %; пептизирующий раствор состоял из 94 мас. % дистиллированной воды, 1 мас. % азотной кислоты и 5 мас. % полиэтиленгликоля. После сушки и прокаливания были получены носители состава Al-MCM-41-ГНТ(60 : 40)/Al2O3 и Al-MCM-41-ГНТ(90 : 10)/Al2O3 в виде экструдатов диаметром около 1 мм и длиной 1.5–2 мм.
Синтез катализаторов Pt/Al-MCM-41-ГНТ(60 : 40)/ Al2O3 и Pt/Al-MCM-41-ГНТ(90 : 10)/Al2O3. В качестве активного металла использовали платину, способность которой эффективно переносить водород позволяет значительно снизить дезактивацию катализатора, обусловленную коксообразованием, а также повысить эффективность изомеризации этилбензола, протекающую через стадию образования продуктов гидрирования — нафтеновых интермедиатов [22]. Нанесение платины на сформованные в виде экструдатов носители осуществляли в одну стадию методом пропитки по влагоемкости. В качестве источника платины использовали хлорид тетрааминплатины(II) (Аурат). Количество соли рассчитывали исходя из того, чтобы содержание платины в катализаторе составило 0.5 мас. % Полученные образцы катализаторов поэтапно сушили при комнатной температуре, а затем при 60, 65, 85, 120 и 160°С. Катализаторы подвергали восстановлению в токе водорода (10 мл мин–1) при ступенчатом повышении температуры от комнатной до 250°С (со скоростью 2°С мин–1), выдерживали в течение 1 ч, а затем температуру поднимали до 450°С (скорость нагрева 10°С мин–1) и восстанавливали в течение 3 ч.
Физико-химические методы исследования материалов и катализаторов на их основе. Удельную площадь поверхности образцов определяли на приборе Micromeritics Gemini VII 2390t с использованием модели полимолекулярной адсорбции Брунауэра–Эммета–Теллера на основании адсорбционных данных в диапазоне относительных давлений (Р/Р0) = 0.04–0.25. Объем и распределение пор по размерам определяли с использованием модели Баррета–Джойнера–Халенда.
Кислотность образцов определяли на приборе Micromeritics AutoChem HP2950 в кварцевом реакторе. Насыщение проводили в токе аммиака, разбавленного азотом при температуре 100°С в течение 30 мин. Удаление физически адсорбированного аммиака проводили при 100°С в токе азота в течение 30 мин со скоростью продувки азотом 50 мл мин–1. Для получения кривой ТПД-NH3 постепенно повышали температуру до 700°С со скоростью 10 град мин–1.
Структуру и морфологию поверхности полученных образцов исследовали методом просвечивающей электронной микроскопии на проборе Jeol JEM-2100 с кратностью увеличения 50–1 500 000 раз и разрешением изображения 0.19 нм при 200 кВ.
Атомное соотношение Si/Al в образцах определяли на энергодисперсионном рентгенофлуоресцентном анализаторе Thermo Fisher Scientific-ARLQuant’X в вакууме. Обработку результатов производили с помощью бесстандартного метода UniQuant.
РФА-анализ образцов проводили на приборе Rigaku SmartLab в диапазоне углов 1.5-8°2θ с шагом 0.05°2θ и временем накопления сигнала не менее 0.3 с/точка.
Каталитические эксперименты. Активность каталитических систем Pt/Al-MCM-41-ГНТ/Al2O3 на основе полученных материалов была изучена в реакции изомеризации ксилольной фракции С-8, полученной с промышленной установки риформинга, состав которой представлен в табл. 1.
Активность полученных образцов исследовали на установке проточного типа с закрепленным слоем катализатора. Загрузка катализатора составляла 5 мл. Каталитические испытания проводили в следующих условиях: давление водорода 1 МПа, объемная скорость подачи сырья 1 ч–1, мольное соотношение водород/сырье = 0.5 в диапазоне температур 360–440°С с шагом 20°С. В качестве образца сравнения использовали промышленный цеолитсодержащий катализатор изомеризации, испытанный в тех же условиях.
Анализ состава продуктов изомеризации. Анализ газообразных продуктов изомеризации проводили на газовом хроматографе “Хромос ГХ-1000”, снабженном четырьмя детекторами (3 ДТП, 1 ПИД), тремя набивными насадочными и одной капиллярной колонкой ValcoPiotVP-AluminaNa2SO4 50 м × 0.53 мм × 10.0 мкм, газы-носители – аргон и гелий. Количественный анализ жидких продуктов изомеризации проводили на газожидкостном хроматографе “Хромос ГХ-1000” с детектором ПИД и капиллярной колонкой MEGA-WAXSpirit (0.32 мм × 60 м × 0.25 мкм), газ-носитель – гелий. Обсчет хроматограмм производили при помощи программного обеспечения “Хромос”. Концентрацию компонентов в жидких продуктах изомеризации рассчитывали методами простой нормализации.
Отбор проб газообразных и жидких продуктов реакции осуществляли раз в час. Для расчета количественных показателей процесса выбирали результаты трех экспериментов, погрешность которых не превышала 1%.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Физико-химические характеристики
Результаты исследования физико-химических свойств синтезированных функциональных материалов Al-MCM-41/ГНТ(60 : 40), Al-MCM-41/ГНТ(90 : 10) и ГНТ, а также носителей и катализаторов на их основе представлены в табл. 2.
Таблица 2.
Текстурные характеристики и показатели кислотности материалов, носителей и катализаторов на их основе
| Этап синтеза | Образец | Текстурные характеристики | Показатели кислотности | ||||
|---|---|---|---|---|---|---|---|
| Sуд, м2 г–1 | Dпор, Å | Vпор, см3 г–1 | кислотные центры слабой и средней силы* | сильные кислотные центры** | общее количество аммиака, мкмоль/г | ||
| Функциональный материал | ГНТ | 49 | 157 | 0.22 | 22 | 122 | 144 |
| Al-MCM-41/ГНТ(60 : 40) | 286 | 62 | 0.43 | 35 | 495 | 530 | |
| Al-MCM-41/ГНТ(90 : 10) | 597 | 36 | 0.82 | 91 | 592 | 683 | |
| Al-MCM-41 | 635 | 35 | 0.41 | 150 | 613 | 763 | |
| Носитель | ГНТ/Al2O3 | 118 | 91 | 0.35 | 137 | 56 | 193 |
| Al-MCM-41/ГНТ(60 : 40)/Al2O3 | 246 | 40 | 0.50 | 278 | 192 | 470 | |
| Al-MCM-41/ГНТ(90 : 10)/Al2O3 | 416 | 39 | 0.56 | 342 | 211 | 553 | |
| Катализатор | Pt/ ГНТ/Al2O3 | 114 | 88 | 0.34 | 140 | 126 | 266 |
| Pt/Al-MCM-41/ГНТ(60 : 40) /Al2O3 | 239 | 41 | 0.49 | 250 | 189 | 439 | |
| Pt/Al-MCM-41/ГНТ(90 : 10) /Al2O3 | 397 | 36 | 0.41 | 403 | 127 | 530 | |
| Промышленный катализатор | 313 | 72 | 0.61 | 259 | 1318 | 1577 | |
Исходный галлуазит обладает весьма малой удельной площадью поверхности (49 м2 г−1), добавление фазы Al-MCM-41 значительно увеличивает данный показатель. Для материалов Al-MCM-41/ГНТ(60 : 40) и Al-MCM-41/ГНТ(90 : 10) характерна изотерма низкотемпературной адсорбции/десорбции азота IV типа с петлей гистерезиса, что свидетельствует о наличии в образцах мезопористой структуры (рис. 1). Изотерма адсорбции азота природного галлуазита относится ко второму типу, такая изотерма присуща непористым или макропористым адсорбентам.
Рис. 1.
Изотермы низкотемпературной адсорбции азота образцов Al-MCM-41/ГНТ(90 : 10)/ Al2O3, Al-MCM-41/ГНТ(60 : : 40)/Al2O3 и ГНТ/Al2O3.

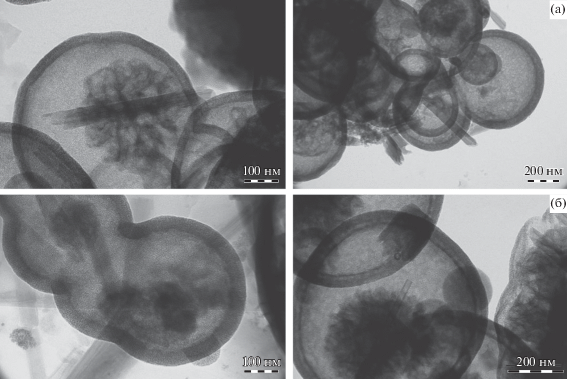
Для доказательства наличия мезопористой структуры функциональные материалы были исследованы методом ПЭМ. На микрофотографиях ПЭМ образцов Al-MCM-41/ГНТ (рис. 2) отчетливо видно наличие фазы Al-MCM-41, закристаллизованной внутри и на поверхности нанотрубок галлуазита в виде глобул, обладающих упорядоченной гексагональной упаковкой.
Рис. 2.
Микрофотографии ПЭМ образцов материалов Al-MCM-41/ГНТ(60 : 40) (а) и Al-MCM-41/ГНТ(90 : 10) (б). *Микрофотографии для каждого образца с разрешением 100 и 200 нм.
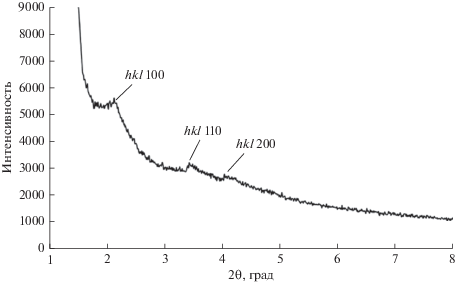
Формирование мезопористой фазы Al-MCM-41 также подтверждено результатами РФА (рис. 3) в области малых углов (2θ = 1.5°–8°). На рентгенограмме образца присутствуют рефлексы с индексами hkl 100, 110, 200, характерные для упорядоченных молекулярных сит с гексагональной симметрией и полностью согласующиеся с литературными данными для Al-MCM-41 [23].
При добавлении к галлуазиту бемита удельная площадь поверхности и объем пор материала существенно возрастают (118 м2 г–1 и 0.35 см3 г–1 соответственно). После формовки носителей в виде экструдатов у образцов Al-MCM-41/ГНТ(60 : 40)/Al2O3 и Al-MCM-41/ГНТ(90 : 10)/Al2O3, напротив, наблюдается снижение удельной площади поверхности, а также незначительные изменения диаметра и объема пор.
После нанесения платины текстурные характеристики образцов практически не изменяются, однако наблюдается незначительное снижение удельной площади поверхности, а также диаметра и объема пор, что может быть связано с блокировкой пор частицами металла. Для всех образцов характерно наличие петли гистерезиса IV типа, что свидетельствует о сохранении мезопористой структуры на всех стадиях синтеза катализатора (рис. 4).
Рис. 4.
Изотермы низкотемпературной адсорбции азота для катализаторов Pt/Al-MCM-41/ГНТ(60 : 40)/Al2O3, Pt/Al-MCM-41/ГНТ(90 : 10) /Al2O3 и Pt/ГНТ/Al2O3.

Кривые, полученные в результате анализа спектров термопрограммируемой десорбции аммиака для материалов на основе ГНТ имеют максимумы десорбции при температурах до 300°С, соответствующие кислотным центрам слабой и средней силы, и после 300°С, что соответствует сильным кислотным центрам (табл. 1). Следует отметить, что общее число кислотных центров в образцах Al-MCM-41/ГНТ(90 : 10) и Al-MCM-41/ГНТ(60 : 40) (683 и 530 мкмоль г–1 соответственно) в несколько раз превышает их количество в немодифицированном галлуазите (144 мкмоль г–1). Наибольшей кислотностью обладает материал Al-MCM-41/ГНТ(90 : 10), что объясняется наличием на поверхности Al-MCM-41 сильных бренстедовских кислотных центров [22].
После формовки экструдатов общее число кислотных центров у всех образцов практически не меняется. Однако значительно возрастает количество средних и слабых центров, в то время как число центров сильной кислотности уменьшается. При нанесении активного металла кислотность несколько снижается, что может быть обусловлено как частичной блокировкой пор частицами металла, так и их взаимодействием с кислотными центрами композита.
Также необходимо отметить тот факт, что результаты элементного анализа состава полученных катализаторов адекватно согласуются с расчетным содержанием платины, введенной на стадии синтеза.
По текстурным характеристикам катализаторы на основе Al-MCM-41 и галлуазита превосходят катализатор, используемый в промышленности. Однако кислотные характеристики полученных образцов значительно уступают характеристикам промышленного экземпляра.
Катализ
Изомеризация ксилолов может протекать по двум механизмам: мономолекулярному − прямая изомеризация м-ксилола [3] − и бимолекулярному, в котором м-ксилол подвергается диспропорционированию с последующим трансалкилированием и образованием n-ксилола [24]. Бимолекулярный механизм практически не реализуется при использовании цеолитсодержащих катализаторов вследствие стерических затруднений, возникающих при диффузии молекул субстрата в порах носителя [25].
С ростом температуры конверсии м-ксилола и этилбензола плавно возрастают, причем конверсия м-ксилола для всех образцов катализаторов всегда выше. Конверсии м-ксилола и этилбензола на катализаторе Pt/ГНТ/Al2O3 не превышают 5% (рис. 5). Для катализатора Pt/Al-MCM-41/ГНТ(60 : 40)/Al2O3 максимальная конверсия м-ксилола достигается при 440°С и составляет 30%, а конверсия этилбензола - уже при 420°С (41%). В присутствии катализатора Pt/Al-MCM-41/ГНТ(90 : 10)/Al2O3 с ростом температуры конверсии м-ксилола и этилбензола постепенно возрастают в диапазоне от 20 до 45%.
Максимальная селективность по целевому n-ксилолу достигается на катализаторах состава Pt/Al-MCM-41/ГНТ(60 : 40)/Al2O3 и Pt/Al-MCM-41/ГНТ(90 : 10)/Al2O3 при 360°С (69 и 68% соответственно), при дальнейшем увеличении температуры процесса наблюдается снижение выхода n-ксилола (рис. 6). Селективность по целевому продукту на катализаторе Pt/ГНТ/Al2O3 с повышением температуры изменяется в диапазоне от 47 до 28%. Повышенная селективность по n-ксилолу катализаторов на основе Al-MCM-41/ГНТ может быть связана с их мезопористой структурой [26] и бо'льшим числом кислотных центров по сравнению с катализатором Pt/ГНТ/Al2O3. Это свидетельствует о невысокой изомеризующей способности катализатора на основе немодифицированного ГНТ, которая, вероятно, связана с низкой кислотностью образца, а также бо'льшим объемом пор носителя, который, в отличие от катализаторов на основе Al-MCM-41/ГНТ, не обладает высокой субстратной селективностью [27].
Стоит также отметить, что селективность по n‑ксилолу на промышленном катализаторе заметно ниже, чем значения, полученные на катализаторах состава Pt/Al-MCM-41/ГНТ(60 : 40)/Al2O3 и Pt/Al-MCM-41/ГНТ(90 : 10)/Al2O3.
Селективность по о-ксилолу с ростом температуры возрастает на обоих катализаторах на основе Al-MCM-41/ГНТ вследствие меньшего числа кислотных центров по сравнению с промышленным образцом [3]. Однако выше 400°С ее значение постепенно снижается вследствие преобладания реакций деалкилирования.
При изомеризации ксилолов протекают побочные реакции, в частности, деалкилирование и диспропорционирование этилбензола и ксилолов. Об этом свидетельствует наличие в продуктах реакции существенного количества бензола и толуола (рис. 7). Повышение температуры способствует протеканию реакций деалкилирования, что также подтверждается увеличением выхода газообразных продуктов — метана, этана и пропана (табл. 3). С ростом температуры суммарная концентрация бензола и толуола в жидких продуктах реакции возрастает на всех катализаторах. Суммарная концентрация бензола и толуола на промышленном катализаторе достигает 72% при 440°С, что значительно выше, чем на катализаторе на основе ГНТ.
Таблица 3.
Концентрации компонентов в газообразных продуктах реакции изомеризации на исследуемых катализаторах (мол. %)
| Температура, °С | Pt/Al-MCM-41/ГНТ(60 : 40)/Al2O3 | Pt/Al-MCM-41/ГНТ(90 : 10)/Al2O3 | ||||
|---|---|---|---|---|---|---|
| СH4 | C2H6 | C3H8 | СH4 | C2H6 | C3H8 | |
| 360 | 18.5 | 4.4 | 18.7 | 29.5 | 9.7 | 27.3 |
| 380 | 27.9 | 6.2 | 18.6 | 30.9 | 7.2 | 19.5 |
| 400 | 31.8 | 7.1 | 15.1 | 32.0 | 8.4 | 18.9 |
| 420 | 36.7 | 10.4 | 18.7 | 42.1 | 11.4 | 12.4 |
| 440 | 43.7 | 12.0 | 16.7 | 58.0 | 15.7 | 12.2 |
| Температура, °С | Pt/ГНТ/Al2O3 | Промышленный катализатор | ||||
| СH4 | C2H6 | C3H8 | СH4 | C2H6 | C3H8 | |
| 360 | 26.5 | 28.9 | 17.5 | 7.4 | 61.8 | 22.5 |
| 380 | 24.4 | 39.0 | 21.0 | 7.1 | 61.1 | 25.8 |
| 400 | 21.4 | 38.6 | 25.2 | 7.3 | 58.0 | 28.7 |
| 420 | 26.9 | 43.0 | 19.6 | 8.0 | 55.7 | 31.6 |
| 440 | 26.0 | 46.2 | 17.7 | 9.4 | 54.8 | 31.4 |
ВЫВОДЫ
Синтезированы и исследованы иерархические композитные материалы на основе упорядоченных алюмосиликатов типа Al-MCM-41 и галлуазитных нанотрубок. Показана активность катализаторов изомеризации на базе иерархических материалов. Полученные материалы испытаны в качестве носителей катализаторов изомеризации ароматической фракции С-8 риформинга.
В изомеризации ксилолов наиболее эффективно проявляют себя каталитические системы на основе Al-MCM-41/ГНТ, обеспечивая большую конверсию этилбензола и м-ксилола, чем катализатор на основе ГНТ.
Установлено, что синтезированные катализаторы обладают большей селективностью по отношению к целевому продукту процесса, n-ксилолу, чем промышленный аналог в диапазоне температур 360–440°C. Максимальное значение селективности по n-ксилолу достигнуто в присутствии катализатора Pt/Al-MCM-41/ГНТ(90 : 10)/Al2O3 при 360°C (70%). Суммарное содержание продуктов деалкилирования (бензола и толуола) для исследуемых катализаторов увеличивалось по мере возрастания температуры.
Список литературы
Караханов Э.А., Максимов А.Л., Золотухина А.В., Винокуров В.А. // ЖПХ. 2018. Т. 91. № 5. С. 609.
Corma A., Llopis F., Monton J. B. // Stud. Surf. Sci. Catal. 1993. 75. P. 1145.
Guisnet M., Gnep N.S., Morin S. // Microporous Mesoporous Materials. 2000. V. 35–36. P. 47.
Глотов А.П., Ролдугина Е.А., Артемова М.И., Смирнова Е.М., Демихова Н.Р., Стыценко В.Д., Егазарьянц С.В., Максимов А.Л., Винокуров В.А. // ЖПХ. 2018. № 91. С. 1173.
Chirico R.D., Knipmeyer S.E., Nguyen A., Steele W.V. // J. Chem. Eng. Data. 1997. V. 42. № 4. P. 784.
Toch K., Thybaut J.W., Vandegehuchte B.D., Narasimhan C.S.L., Domokos L., Marin G.B. // Appl. Catal. A: General. 2012. V. 425–426. P. 130.
Young L.B., Butter S.A., Kaeding W.W. // J. Catal. 1982. V. 76. № 2. P. 418.
Marcilly C.R. // Top. Catal. 2000. V. 13. № 4. P. 357.
Guillon E., Lacombe S., Sozinho T., Magnoux P., Gnep S., Moreau P., Guisnet M. // Oil Gas Sci. Technol. 2009. V. 64. № 6. P. 731.
Baerlocher C., McCusker L.B. Atlas of Zeolite Framework Types. Elsevier. 2007. P. 398.
Morin S., Ayrault P., El Mouahid S., Gnep N.S., Guisnet M. // Appl. Catal. A-Gen. 1997. V. 159. P. 317.
Kresge C., Vartuli J., Roth W., Leonowicz M. // Stud. Surf. Sci. Catal. 2004. V. 148. P. 53.
Bernal Y.P., Alvarado J., Juarez R.L., Mendez Rojas M., de Vasconcelos E.A., de Azevedo W.M., Iniesta S.A., Cab J.V. // Optik. 2019. V. 185. P. 429.
Čejka J., Krejčí A., Žilková N., Dědeček J., Hanika J.// Microporous Mesoporous Mater. 2001. № 44. P. 499.
Vinokurov V.A., Stavitskaya A.V., ChudakovYa.A., Glotov A.P., Ivanov E.V., Gushchin P.A., Lvov Yu.M., Maximov A.L., Muradov A.V., Karakhanov E.A. // Pure Appl. Chem. 2018. V. 90. № 5. P. 825.
Kadi S., Lellou S., Marouf-Khelifa K., Schott J., Gener-Batonneau I., Khelifa A. // Microp. Mesopor. Mat. 2012. № 158. P. 47.
Lvov Y., Wang W., Zhang L., Fakhrullin R. // Adv. Mater. 2016. V. 28. № 6. P. 1227.
Vinokurov V.A., Glotov A.P., Chudakov Ya.A., Stavitskaya A.V., Ivanov E.V., Gushchin P.A., Zolotukhina A.V., Maximov A.L., Karakhanov E.A. // Ind. Eng. Chem. Res. 2017. V. 56. № 47. P. 14043.
Vinokurov V.A., Stavitskaya A.V., Chudakov Ya.A., Ivanov E.V., Shrestha L.K., Ariga K., Darrat Y.A., Lvov Yu.M. // Sci. Technol. Adv. Mater. 2017. V. 18. № 1. P. 147.
Glotov A., Levshakov N., Stavitskaya A., Artemova M., Gushchin P., Ivanov E., Vinokurov V. Lvov Y. // Chem. Commun. 2019. № 55. P. 5507.
Kwak K.-Y., Kim M.-S., Lee D.-W., Cho Y.-H., Han J., Kwon T.S., LeeK.-Y. // Fuel. 2014. V. 137. P. 230.
Farshadi M., Falamaki C. // Chin. J. Chem. Eng. 2018. V. 26. № 1. P. 116.
Glotov A., Levshakov N., Vutolkina A., Lysenko S., Karakhanov E., Vinokurov V. // Catal. Today. 2019. V. 329. P. 156.
Corma A., Sastre E. // J. Catal. 1991. V. 129. P. 177.
Morin S., Ayrault P., El Mouahid S., Gnep N.S., Guisnet M. // Appl. Catal. A: General. 1997. V. 159. P. 317.
Zhou Y., Liu H., Li Y., Zhou B., Jiang W., Han W., Lan G. // Chin. J. Catal. 2013. V. 34. № 7. P. 1429.
Fernandez C., Stan I., Gilson J. P., Thomas K., Vicente A., Bonilla A., Perez-Ramirez J. // Chem. Eur. J. 2010. V. 16. № 21. P. 6224.
Дополнительные материалы отсутствуют.