Нефтехимия, 2020, T. 60, № 4, стр. 548-555
Новые эффективные каталитические системы на основе алкоксидных комплексов титана(IV) для сополимеризации этилена и гексена-1
В. А. Тускаев 1, 2, *, С. Ч. Гагиева 1, А. С. Лядов 3, Д. А. Курмаев 1, Г. Г. Никифорова 2, В. Г. Васильев 2, С. В. Зубкевич 1, Д. Сарачено 5, А. И. Сизов 1, В. И. Привалов 4, Б. М. Булычев 1
1 Московский государственный университет имени М.В. Ломоносова, Химический факультет
119992 Москва, Россия
2 Институт элементоорганических соединений им. А.Н. Несмеянова РАН
119991 Москва, Россия
3 Институт нефтехимического синтеза им. А.В. Топчиева РАН
119991 Москва, Россия
4 Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Россия
5 Высший химический колледж РАН
119991 Москва, Россия
* E-mail: tuskaev@yandex.ru
Поступила в редакцию 25.11.2019
После доработки 01.03.2020
Принята к публикации 11.03.2020
Аннотация
Исследована каталитическая активность бис-(изопропоксо)титановых(4+) комплексов с 1,2-диолатными лигандами, активированных хлоридами алкилалюминия и дибутилмагнием, в сополимеризации этилена и гексена-1. Изучено влияние структуры прекатализатора и состава алюминийорганического активатора на каталитическую активность, включение гексена-1 и микроструктуру сополимеров. Полученные сополимеры охарактеризованы с помощью дифференциальной сканирующей калориметрии (ДСК), гель-проникающей хроматографии и 13С ЯМР. Комплексы с перфторфенильными заместителями были наиболее активными в данной серии и обеспечивали наибольшую степень включения сомономера. Замена Et2AlCl на Et3Al2Cl2 приводит к значительному снижению как производительности, так и включения гексена-1 в сополимер. Исследованы механические свойства полученных сополимеров.
Сополимеры этилена с высшими олефинами, в особенности, линейный полиэтилен низкой плотности (LLDPE, ПЭНП) и термопластичные эластомеры, играют важную роль в промышленности в силу высокой прочности и низкой плотности получаемых из них материалов, а также экономической эффективности производства [1]. Несмотря на успешное использование в промышленном производстве полимерных материалов классических катализаторов Циглера–Натты, все большее применение стали находить металлоценовые и постметаллоценовые катализаторы [2]. При этом значительные усилия были направлены на поиск новых, более эффективных постметаллоценовых катализаторов для синтеза сополимеров с требуемыми свойствами. Применение комплексов переходных металлов с феноксииминными (FI) [3], тиобис(фенолятными) [4], дитиобис(фенолятными) [5], иминопиррольными [6], 2-имино- и 2,6-бис-(имино)-пиридильными лигандами [7] в качестве катализаторов сополимеризации всесторонне освещено в цитированных обзорах.
В большой группе постметаллоценовых катализаторов, комплексы переходных металлов, стабилизированные алкоксидными лигандами, являются, вероятно, наименее изученными. На рис. 1 приведены структуры этих комплексов, способных катализировать сополимеризацию этилена с олефинами. Так, диастереомеры циркониевых комплексов с аминотриолатными лигандами (соединения A, рис. 1) в присутствии активатора – метилалюмоксана (МАО) катализируют сополимеризацию этилена и циклических олефинов. Активность каталитических систем не превышала 309 кг полимера/моль катализатора ч.; процент включения норборнена зависел от типа симметрии комплекса – до 40% для комплекса с C3-симметрией и до 25% для прекатализатора с псевдо-Cs-симметрией [8]. Фениламино-алкоксититановые комплексы (соединения В, рис. 1) в присутствии МАО также катализируют сополимеризацию этилена и норборнена; стерически менее нагруженный комплекс (R = Me) обеспечивает большее включение норборнена (до 43 мол. %), в сравнении с изопропильным аналогом [9]. Ряд комплексов ванадия(5+) (соединения C и D, рис. 1), с тетрадентатыми бис-феноламиноспиртовыми или фениламинодиольными лигандами в присутствии Et2AlCl катализируют полимеризацию этилена и его сополимеризацию с норборненом [10]. Комплекс дихлорида титана с 2-(α,α-дифенилгидроксиметил)-8-гидроксихинолином (соединение E, рис. 1), активированный смесью {3AlEt2Cl/MgBu2}, катализирует сополимеризацию этилена и 1-октена с активностью до 2040 кг/мольTi ч; степень включения сомономера достигает 10.4% [11].
Рис. 1.
Структуры комплексов переходных металлов с алкоксидными или феноксид-алкоксидными лигандами, способных катализировать сополимеризацию этилена с различными олефинами.
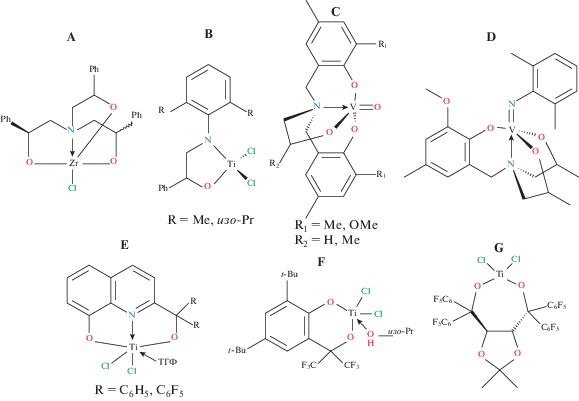
Прекатализаторы с лигандным окружением, содержащим только донорные кислородные атомы, известны в меньшей степени. Комплекс дихлорида титана с феноксид-алкоксидным лигандом (соединение F, рис. 1) в присутствии МАО или бинарного сокатализатора {3AlEt2Cl + Bu2Mg} катализирует сополимеризацию этилена с гексеном-1, октеном-1 и деценом-1 [12]. Титановые комплексы G с фторированным ТАДДОЛьнымлигандом в присутствии МАО катализируют получение стереоблочного высокомолекулярного этилен-пропиленового каучука с включением пропиленовых звеньев до 25 мол. % [13].
Ранее использовали титан-дихлоридные и титан-диалкоксидные комплексы с 1,4- и 1,2-диолатными лигандами для получения сверхвысокомолекулярного полиэтилена (СВМПЭ) с низкой степенью переплетения макромолекул [14, 15]. В ряде случав ди-(изопропоксо)-комплексы превосходили по активности дихлоридные аналоги, что, по-видимому, объясняется спецификой их активации смесями алкилалюминийхлоридов и дибутилмагния. В отсутствие магнийорганики, алкоксиды титана с алюминийорганическими соединениями являются катализаторами димеризации или олигомеризации олефинов [16–18]. В работе Л.А. Ришиной с соавт. показано, что добавление Bu2Mg к смеси Ti(OизоPr)4 + Et2AlCl формирует каталитическую систему, способную сополимеризовать этилен и гексен-1 [19].
Основная цель настоящей работы – изучение каталитической активности серии 1,2-диолатных алкоксотитановых комплексов в сополимеризации этилена и гексена-1, а также поиск закономерностей, связывающих структуру прекатализатора и состав активатора с продуктивностью каталитической системы и свойствами получаемого полимера.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез и кристаллические структуры алкоксо-комплексов Ti(4+) 1–6 (рис. 2) приведены в работе [15]. Аргон (“ос. ч.”) и этилен (Lindegas) подвергали финишной очистке пропусканием через колонки SuperClean™ GasFilters. Толуол (“х. ч.”) дополнительно очищали согласно известной методике [14]. Содержание воды в растворителях периодически проверяли кулонометрическим титрованием по Карлу–Фишеру при помощи аппарата Methrom 756 KF. Растворы диэтилалюминийхлорида, этилалюминийсесквихлорида и дибутилмагния в гептане использовали без дополнительной очистки. Спектры ЯМР 1Н, 13C регистрировали на приборе “Bruker Avance-400”.
Сополимеризация этилена и гексена-1
Сополимеризацию осуществляли в стальном реакторе (Parr Instrument Co.) объемом 450 см3. Предварительно реактор вакуумировали в течение 1 ч при 90°С, охлаждали до 30°С, добавляли при перемешивании 100 мл толуола и 10 мл гексена-1, насыщали этиленом, вводили необходимое количество сокатализатора – {3Et2AlCl + Bu2Mg} или {1.5Et3Al2Cl3 + Bu2Mg} и перемешивали 5 мин. Полимеризацию начинали добавлением к реакционной смеси раствора прекатализатора в 1 мл толуола. Давление этилена – 0.17 МПа поддерживали постоянным на протяжении всего процесса. Полимеризацию прекращали стравливанием избыточного давления и добавлением в реактор 10%-ного раствора HСl в этиловом спирте. Полимерный продукт отфильтровывали, многократно промывали водой и спиртом, сушили в вакууме при 60°C до постоянной массы.
Определение физико-химических свойств полученных полимеров
Калориметрические исследования проводили на калориметре DSC-822e (“Mettler-Toledo”) при скорости нагрева 10°C/мин в атмосфере аргона. Температуру плавления определяли по второму плавлению, так как на первое влияет механическая и термическая “история” образцов.
Молекулярно-массовые характеристики (Mw, Mn, MMP) полимеров изучали для растворов полимеров в 1,2,4-трихлорбензоле при 135°С методом ГПХ на приборе Waters GPCV-2000, снабженном двумя колонками (PLgel, 5μ и Mixed-C, 3007.5 мм) и рефрактометром. Скорость элюирования составляла 1 мл мин–1.
Молекулярные массы полимеров определяли с использованием универсальной калибровочной зависимости относительно полистирольных стандартов: для полистирола К = 2.88 10−4, α = 0.64; для полиэтилена К = 6.14 10−4, α = 0.67.
13C ЯМР-спектры этилен-гексеновых сополимеров (~5 мас. % растворв o-дихлорбензоле) регистрировали при 150°C на спектрометре Bruker Avance-400 при 10.613 MГц. Время релаксации составляло 15 с, количество сканирований варьировалось от 500 до 2000. Константы сополимеризации для этилена и гексена-1 были рассчитаны с использованием модели Маркова первого порядка по расчету экспериментальных определений триад по следующимуравнениям [20]:
Механические характеристики полученных пленок сополимеров измеряли на универсальной испытательной машине LLOYD Instruments LR. Скорость растяжения составляла 50 мм/мин. Образцы готовили методом прессования полимера под давлением 0.55 МПа при температуре выше температуры плавления на 10°C. В результате были получены прозрачные пленки одинаковой толщины
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
По методике работы [15] были синтезированы кристаллические структуры алкоксо-комплексов Ti(4+) 1–6 (рис. 2):
В табл. 1 представлены наиболее значимые результаты изучения сополимеризации этилена и гексена-1. Все условия процесса сополимеризации – время, температура, давление этилена и молярные отношения Ti/Al/Mg были идентичны использованным для гомополимеризации этилена [15], что позволяет сравнивать особенности этих двух процессов. Для достижения более высокого уровня включения сомономера была использована достаточно высокая концентрация гексена-1 – 0.799 моль/л. Увеличение концентрации сомономера обычно сопровождается уменьшением концентрации этилена вблизи активного центра, что, в итоге, приводит к росту степени включения сомономера.
Таблица 1.
Сополимеризация этилена и гексена-1 на комплексах 1–6a
| Опыт | Комплекс | Сокатализаторb | Ac | Содержание гексена-1, моль %d | Tme, °С | χf, % | Mw, Mng | Mw/Mn |
|---|---|---|---|---|---|---|---|---|
| 1 | 1 | Et2AlCl/Bu2Mg | 2571 | 7.18 | 127.03 | 12.52 | 1.02 × 105 | 4.34 |
| 2.34 × 104 | ||||||||
| 2 | 1 | Et3Al2Cl3/Bu2Mg | 1086 | 1.17 | 129.67 | 38.43 | 4.8 × 105 | 13.56 |
| 4.27 × 104 | ||||||||
| 3 | 2 | Et2AlCl/Bu2Mg | 4914 | 20.12 | 127.70 | 3.43 | – | – |
| 4 | 2 | Et3Al2Cl3/Bu2Mg | 2714 | 13.29 | 127.74 | 5.96 | – | – |
| 5 | 3 | Et2AlCl/Bu2Mg | 4857 | 18.10 | 127.53 | 3.62 | – | – |
| 6 | 3 | Et3Al2Cl3/Bu2Mg | 2143 | 8.42 | 125.53 | 10.26 | – | – |
| 7 | 4 | Et2AlCl/Bu2Mg | 3314 | 16.02 | 127.70 | 2.69 | 0.9 × 105 | 5.59 |
| 0.2 × 104 | ||||||||
| 8 | 4 | Et3Al2Cl3/Bu2Mg | 1829 | 3.34 | 126.33 | 31.17 | 4.1 × 105 | 15.75 |
| 2.6 × 104 | ||||||||
| 9 | 5 | Et2AlCl/Bu2Mg | 2171 | 7.71 | 121.11 | 9.02 | 2.5 × 105 | 15.63 |
| 1.6 × 104 | ||||||||
| 10 | 5 | Et3Al2Cl3/Bu2Mg | 1429 | 5.45 | 123.70 | 19.18 | 3.8 × 105 | 20.0 |
| 1.9 × 104 | ||||||||
| 11 | 6 | Et2AlCl/Bu2Mg | 1429 | 2.83 | 126.40 | 31.17 | – | – |
| 12 | 6 | Et3Al2Cl3/Bu2Mg | 1829 | 2.57 | 124.41 | 24.30 | – | – |
a Сополимеризацию проводили в100 мл толуола; количество катализатора 5 × 10–6 моль, давление этилена – 0.17 МПа, время – 30 мин, температура –30°C. b Молярное отношение [Al]/[Mg]/[Ti] = 300 : 100 : 1. c Активность, кг сополим./моль Ti ч атм. d Определено по данным 13C ЯМР. e Определено по данным ДСК; второе плавление. f Степень кристалличности определяли по данным ДСК, χ = $\left( {{{\Delta {{H}_{m}}} \mathord{\left/ {\vphantom {{\Delta {{H}_{m}}} {\Delta H_{m}^{0}}}} \right. \kern-0em} {\Delta H_{m}^{0}}}} \right)$ × 100%, где $\Delta H_{m}^{0}$ = 293.0 Дж/г [12]. g Определено по данным ГПХ.
Все комплексы в присутствии бинарных сокатализаторов {3Et2AlCl + Bu2Mg} или {1.5Et3Al2Cl3 + + Bu2Mg} проявляли умеренную или высокую активность в сополимеризации этилена с гексеном-1 (1086–4914 кг сополим./моль Ti ч атм). Как видно из результатов, представленных в табл. 1, лигандное окружение оказывает существенное влияние на каталитическую активность комплексов, которая уменьшается в следующем порядке:
2 (R = Ph, R1= C6F5) > 3 (R = R1 = C6F5) > 4 (R = = R1= CH3) > 1 (R = R1 = Ph) > 5 (R = R1= CF3) > 6 (R = R1 = CF3, спирокомплекс) при использовании активатора {3Et2AlCl + Bu2Mg}. Замена диэтилалюминийхлорида в составе бинарного активатора на этилалюминийсесквихлорид, обладающий большей льюисовой кислотностью, меняет эту последовательность: 2 > 3 > 4 = 6 > 5 > 1. Однако, в обоих случаях, комплексы 2 и 3 с перфторфенильными фрагментами проявили как максимальную активность – 4914 и 4857 кг сополим./ моль Ti ч, так и наибольшую степень включения сомономера – гексена-1 (20.1 и 18.1%, соответственно). Для прекатализаторов 2 и 3 отчетливо проявился положительный эффект сомономера (продуктивность этих систем примерно в два раза превосходит показатели, зафиксированные в процессе гомополимеризации этилена [15]).
Комплексы 4–5 с алифатическими диольными лигандами показали заметно более низкую каталитическую активность по сравнению с комплексами 2–3, содержащими перфторфенильные фрагменты. Интересно, чтокомплекс 4 с нефторированным лигандом, активированным Et2AlCl, превзошел фторированный аналог 5 как по производительности, так и по включению гексена-1.
Замена Et2AlCl на Et3Al2Cl2 при прочих равных условиях полимеризации во всех случаях (кроме комплекса 6) приводит к значительному снижению как производительности, так и включения гексена-1 (рис. 3, табл. 1). Тенденция Et3Al2Cl3-содержащего активатора увеличивать молекулярную массу полимера, наблюдаемая ранее при полимеризации этилена [14, 15], также проявляется для этилен-гексеновых сополимеров (табл. 1, сравни опыты 1 и 2; 9 и 10).
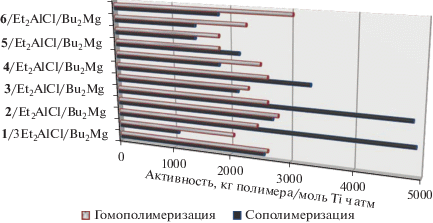
Рис. 3.
Зависимость активности каталитических систем в гомополимеризации этилена (по данным работы [15]) и в сополимеризации этилена с гексеном-1 от состава каталитических систем.
Полученные сополимеры, которые варьируются от полукристаллических до аморфных, характеризуются относительно высокими значениями молекулярных масс (0.9–4.8 × 105 Да) и широкими молекулярно-массовыми распределениями (Mw/Mn = 4.3–20.0). Для сравнения, молекулярная масса полиэтилена, полученного на этих катализаторах в одинаковых условиях, варьировалась в диапазоне 1.08–7.73 × 106 [15]. На кривых ДСК сополимеров проявляется единственный пик в диапазоне 121.1–129.7°С, что значительно ниже температуры плавления гомополимеров (135–142°С [15]).
Заметной зависимости между степенью включения сомономера и температурой плавления не обнаружено. С ростом включения сомономера степень кристалличности уменьшается (рис. 4); такая зависимость типична [20].
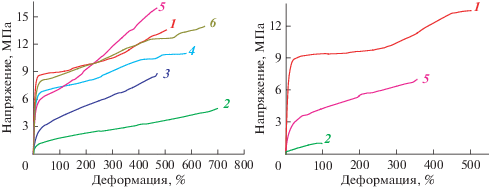
Рис. 4.
Кривые напряжение–деформация для пленок из этилен-гексеновых сополимеров, полученных с использованием комплексов 1–6, активированных {3Et2AlCl + Bu2Mg} (слева) и {1.5Et3Al2Cl3 + Bu2Mg} (справа).
Микроструктура этилен-гексеновых сополимеров оценивалась по распределению триад в 13C ЯМР-спектрах по методу, предложенному J.C. Randall с соавт. [21, 22], результаты приведены в табл. 2.
Таблица 2.
Распределение триад в 13C ЯМР-спектрах этилен-гексеновых сополимеровa
| Опыт | E, % | H, % | Распределение триад, % | rE | rH | rErH | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| EEE | EEH | HEH | EHE | HHE | HHH | ||||||
| 1 | 0.928 | 0.072 | 0.752 | 0.147 | 0.029 | 0.062 | 0.001 | 0.015 | 24.34 | 0.06 | 1.51 |
| 2 | 0.988 | 0.012 | 0.939 | 0.042 | 0.007 | 0.023 | 0.001 | 0.001 | 87.16 | 0.02 | 1.39 |
| 3 | 0.799 | 0.201 | 0.412 | 0.296 | 0.092 | 0.126 | 0.063 | 0.012 | 8.16 | 0.07 | 0.56 |
| 4 | 0.867 | 0.133 | 0.597 | 0.212 | 0.058 | 0.088 | 0.008 | 0.037 | 14.48 | 0.11 | 1.62 |
| 5 | 0.819 | 0.181 | 0.448 | 0.285 | 0.087 | 0.119 | 0.041 | 0.021 | 9.02 | 0.07 | 0.67 |
| 6 | 0.915 | 0.085 | 0.709 | 0.172 | 0.035 | 0.073 | 0.006 | 0.006 | 19.97 | 0.03 | 0.59 |
| 7 | 0.839 | 0.160 | 0.365 | 0.388 | 0.086 | 0.155 | 0.001 | 0.105 | 6.39 | 0.17 | 1.09 |
| 8 | 0.967 | 0.033 | 0.872 | 0.080 | 0.015 | 0.029 | 0.009 | 0.001 | 46.22 | 0.04 | 1.89 |
| 9 | 0.923 | 0.077 | 0.713 | 0.173 | 0.037 | 0.077 | 0.001 | 0.011 | 19.54 | 0.04 | 0.73 |
| 10 | 0.946 | 0.055 | 0.803 | 0.121 | 0.022 | 0.049 | 0.001- | 0.019 | 31.50 | 0.09 | 3.11 |
| 11 | 0.972 | 0.028 | 0.890 | 0.067 | 0.015 | 0.023 | 0.001 | 0.011 | 44.18 | 0.12 | 5.41 |
| 12 | 0.974 | 0.026 | 0.872 | 0.087 | 0.015 | 0.026 | 0.001 | 0.023 | 52.62 | 0.22 | 11.68 |
a Нумерация соответствует табл. 1.
Поскольку свойства и технологические характеристики (например, пластическое и эластомерное поведение) олефиновых сополимеров сильно зависят не только от количества включенного сомономера, но и от распределения сомономерных звеньев вдоль главной цепи [23], были оценены константы сополимеризации для этилена и гексена-1 (табл. 2). Распределения сомономеров для сополимеров, полученных с использованиемпредкатализаторов 2–3 с перфторированными фрагментами и активированных Et2AlCl, являются статистическими, так как произведение констант сополимеризации rErH меньше 1 [24]. Напротив, для полимеров, полученных с комплексами 1, 4 и особенно со спиро-комплексом 6, эти значения превышают единицу, что указывает на наличие длинных последовательностей звеньев этилена. Действительно, эти полимеры характеризуются высокими значениями кристалличности и температур плавления. В целом, для всех полимеров, полученных с использованием Et2AlCl, значение rE значительно ниже, чем при использовании Et3Al2Cl2. По-видимому, это может объяснить более высокое включение сомономера прииспользовании активатора состава {3Et2AlCl + Bu2Mg}.
Для исследования механических характеристик синтезированных этилен-гексеновых сополимеров, были изготовлены прозрачные, однородные по толщине пленки, результаты исследования механических характеристик которых приведеныв табл. 3 и на рис. 4.
Таблица 3.
Механические характеристики пленок из этилен-гексеновых сополимеров
| Опыт | Каталитическая система | ε, % | σ, MПa | Опыт | Каталитическая система | ε, % | σ, MПa |
|---|---|---|---|---|---|---|---|
| 1 | 1/Et2AlCl/Bu2Mg | 500 | 11 | 8 | 4/Et3Al2Cl3/Bu2Mg | 580 | 11 |
| 2 | 1/Et3Al2Cl3/Bu2Mg | 500 | 13 | 9 | 5/Et2AlCl/Bu2Mg | 340 | 7 |
| 3 | 2/Et2AlCl/Bu2Mg | 100 | 1 | 10 | 5/Et3Al2Cl3/Bu2Mg | 470 | 16 |
| 4 | 2/Et3Al2Cl3/Bu2Mg | 700 | 5 | 12 | 6/Et3Al2Cl3/Bu2Mg | 650 | 14 |
| 6 | 3/Et3Al2Cl3/Bu2Mg | 470 | 9 |
a Нумерация опытов соответствует табл. 1.
Деформация сополимеров с низким содержанием гексена типична для полукристаллических термопластов. С увеличением содержания сомономера (и уменьшением кристалличности) сополимеры проявляют меньшую устойчивость к деформации. Кривые напряжения–деформации для этих экспериментов показаны на рис. 4.
ЗАКЛЮЧЕНИЕ
Алкоксо-титановые(4+) комплексы 1–6 с 1,2-диолатными лигандами при активации {3Et2AlCl + + Bu2Mg} или {1.5Et3Al2Cl3 + Bu2Mg} проявляют умеренную или высокую активность в сополимеризации этилена и гексена-1, образуя достаточно высокомолекулярные сополимеры со степенью включения гексена в пределах 1.17–20.12%. В отличие от высокоактивных бис-феноксииминных титановых комплексов (катализаторы FI), которые требуют больших количеств дорогого активатора метилалюмоксана, комплексы 1–6 “работают” в присутствии обычных алюминийорганических и магнийорганических соединений.
Использование смеси {3Et2AlCl + Bu2Mg} в качестве сокатализатора позволяет достичь более высоких значений активности и более высоких степеней включения сомономера посравнению со смесью {1.5Et3Al2Cl3 + Bu2Mg}.
Комплексы с перфторфенильными заместителями 2–3 проявляют более высокую активность и позволяют достичь более высоких степеней включения сомономера. Распределения сомономеров для сополимеров, полученных с этими комплексами, являются статистическими.
Список литературы
Galli P., Vecelli, G. // J. Polym. Sci. Part A. Polym. Chem. 2004. V. 42. P. 396.
Baier M.C., Zuideveld M.A., Mecking S. // Angew. Chem. Int. Ed. 2014. V. 53. P. 9722. https://doi.org/10.1002/anie.201400799
Makio H., Terao H., Iwashita A., Fujita T. // Chem. Rev. 2011. V. 111. P. 2363. Janas Z. // Coord. Chem. Rev. 2010. V. 254. P. 2227.
Nakata N., Toda T., Ishii A. // Polym. Chem. 2011. V. 2. P. 1597.
Mashima K., Tsurugi H. //J. Organomet. Chem. 2005. V. 690. P. 4414.
Budagumpi S., Kim K.-H., Kim I. // Coord. Chem. Rev. 2011. V. 255. P. 2785.
Padmanabhan S., Vijayakrishna K., Mani R. // Polym. Bull. 2010. V. 65. P. 13.
Vijayakrishna K., Sundararajan G. // Polymer. 2006. V. 47. P. 8289.
Wu J.-Q., Mu J.S., Zhang S.-W., Li Y.-S. // J. Polym. Sci. Part A. Polym. Chem. 2010. V. 48. P. 1122.
Kolosov N.A., Tuskaev V.A., Gagieva S.C., Fedyanin I.V., Khrustalev V.N., Polyakova O.V., Bulychev B.M. // Eur. Polym. J. 2017. V. 87. P. 266.
Rishina L.A., Lalayan S.S., Gagieva S.Ch., Tuskaev V.A., Shchegolikhin A.N., Shashkin D.P., Kissin Y.V. // J. Res. Updates in Polym. Sci. 2014. V. 3. P. 216.
Rishina L.A., Galashina N.M., Gagieva S.Ch., Tuskaev V.A., Bulychev B.M., Belokon’ Yu.N. // Polym. Sci. Ser. A. 2008. V. 50. P. 110.
Gagieva S.Ch., Tuskaev V.A., Fedyanin I.V., Buzin M.I., Vasil’ev V.G., Nikiforova G.G., Afanas’ev E.S., Zubkevich S.V., Kurmaev D.A., Kolosov N.A., Mikhaylik E.S., Golubev E.K., Sizov A.I., Bulychev B.M. // J. Organomet. Chem. 2017. V. 828. P. 89.
Tuskaev V.A., Gagieva S.Ch., Kurmaev D.A., Khrustalev V.N., Dorovatovskii P.V., Mikhaylik E.S., Golubev E.K., Buzin M.I., Zubkevich S.V., Nikiforova G.G., Vasil’ev V.G., Bulychev B.M., Magomedov K.F. // J. Organomet. Chem. 2018. V. 877. P. 85.
Skupiñska J. // Chem. Rev. 1991. V. 91. P. 613.
Illai S.M., Ravindranathan M., Sivaram S. // Chem. Rev. 1986. V. 86. P. 353.
Cazaux J.-B., Braunstein P., Magna L., Saussine L., Olivier-Bourbigou H. // Eur. J. Inorg. Chem. 2009. P. 2942.
Rishina L.A., Kissin Y.V., Lalayan S.S., Krasheninnikov V.G., Perepelitsina E.O., Medintseva T.I. // Polym. Sci. Ser. B. 2016. V. 58. P. 152.
Kiesewetter E.T., Waymouth R.M. // Macromolecules 2013. V. 46. P. 2569.
Quijada R., Scipioni R.B., Mauler R.S., Galland G.B., Miranda M.S.L. // Polym. Bull. 1995. V. 35. P. 299.
Hsieh E.T., Randall J.C. // Macromolecules. 1982. V. 15. P. 1402.
Randall J.C. // J. Macromol. Sci. Part C. Polym. Rev. 1989. V. 29. P. 201.
Yu T.C. // Polym. Engin. Sci. 2001. V. 41. P. 656–671.
Galimberti M., Piemontesi F., Fusco O., Camurati I., Destro M. // Macromolecules. 1998. V. 31. P. 3409.
Дополнительные материалы отсутствуют.



