Неорганические материалы, 2022, T. 58, № 8, стр. 891-896
Коэффициенты разделения и числа Пекле в испарительных процессах рафинирования веществ с простой основой при температурах вблизи от температур плавления
А. И. Кравченко 1, *, А. И. Жуков 1
1 Национальный научный центр “Харьковский физико-технический институт”
Национальной академии наук Украины
61108 Харьков, ул. Академическая, 1, Украина
* E-mail: krwchnko@gmail.com
Поступила в редакцию 22.02.2022
После доработки 17.03.2022
Принята к публикации 22.03.2022
- EDN: EEUOHK
- DOI: 10.31857/S0002337X22080073
Аннотация
С помощью уравнения Бартона-Прима-Слихтера на примерах веществ с простой основой (Sm, Yb, Mg, Eu, Te, Zn, Cd, Be, Tb) показано, что их дистилляционное или сублимационное рафинирование при T = (0.9–1.2)Tm (где Tm – температура плавления) может ухудшаться с повышением температуры вследствие роста эффективного коэффициента разделения β < 1 и/или роста диффузионного числа Пекле Pe = wX/ρD (где w – скорость испарения вещества с единицы поверхности, D – коэффициент диффузии примеси, ρ – плотность вещества, X – размерный фактор испаряемого материала) – с бóльшим или меньшим влиянием β или Pe в зависимости от природы основы и примесей. Также показано, что в кристаллизационных процессах рафинирования Pe малó и основным параметром является коэффициент разделения.
ВВЕДЕНИЕ
Дистилляция, направленная кристаллизация и сублимация – основные методы получения высокочистых веществ [1–3]. В этих методах многокомпонентное вещество подвергается фазовому превращению при перемещении поверхности раздела фаз со скоростью $v$ с перераспределением примесей между фазами.
В испарительных методах (дистилляция и сублимация) скорость v определяется скоростью испарения w вещества с единицы поверхности. Если жидкость содержится в контейнере простой (например, цилиндрической) формы, то $v$ = w/ρ, где ρ – плотность вещества (та же зависимость имеет место при сублимации материала в виде диска, плотно вложенного в цилиндрический тигель). Разработано математическое описание процесса испарения вещества “основа–примесь” – в виде системы уравнений, связывающих чистоту продукта со степенью перегонки g (т.е. с выходом продукта). Параметрами уравнений являются эффективный коэффициент разделения β (отношение концентрации примеси в паре, покидающем поверхность испарения, к концентрации примеси в жидкости, из которой образуется пар – вблизи поверхности испарения) и число Пекле Pe = $v$X/D, где D – коэффициент диффузии примеси, а X – размерный фактор испаряемого материала (начальная толщина слоя жидкости в тигле при дистилляции; или начальная толщина испаряемой пластины, плотно вложенной в тигель; или начальный радиус шара при сублимации) [4, 5].
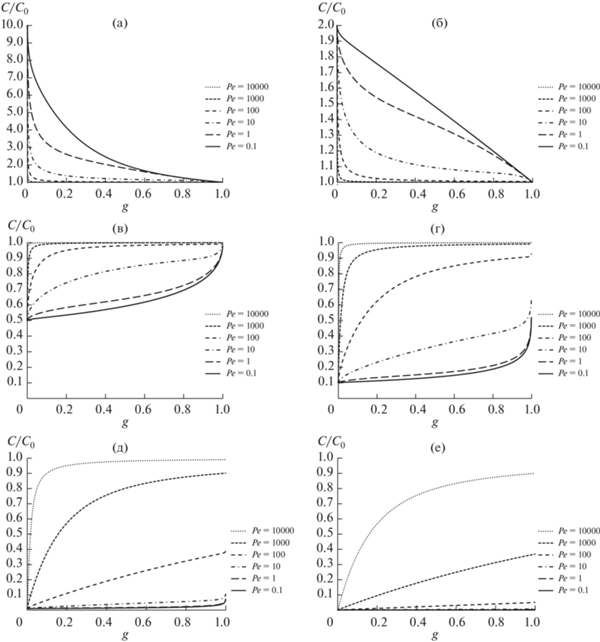
При β < 1 эффективность очистки конденсата повышается с уменьшением числа Pe (рис. 1). Если g = 1, то С/С0 = 1. При заданном β рассматриваемая зависимость при Pe = 0.1 практически совпадает с зависимостью при Pe = 0. Если Pe = 0, то (как это отмечено ранее [5–7]) зависимость С/С0 от g имеет вид известного уравнения дистилляции с идеальным перемешиванием жидкости (которое описывает и нормальную направленную кристаллизацию):
Рис. 1.
Зависимости относительной усредненной концентрации С/С0 примеси в конденсате от степени перегонки g материала в виде плоского слоя при его одностороннем испарении в вакууме при различных значениях числа Пекле Ре и коэффициенте разделения β = 10 (a), 2 (б), 0.5 (в), 0.1 (г), 0.01 (д), 0.001 (е) (С0 – исходная концентрация примеси).
Важно отметить, что описание дистилляции и сублимации с помощью двух параметров (β и Ре) предполагает, что процесс определяется только диффузией примесей. Между тем, факторами реальных процессов могут быть захват примесей паром основного компонента в процессах дистилляции и сублимации, а также конвекция в процессах дистилляции (хотя отмечалось, что конвекция мала при малых X [4]).
Была рассмотрена температурная зависимость числа Пекле как следствия температурных зависимостей $v$(Т) и D(Т): зависимости D(Т) и Pe(Т) для той или иной примеси определяются энергией активации диффузии примеси в системе “основа–примесь” [6, 7].
Напротив, в процессах направленной кристаллизации скорость $v$ задается скоростью изменения тепловых условий процесса – например, скоростью перемещения нагревателя вдоль материала удлиненной формы или скоростью вытягивания кристалла из расплава. Выведены уравнения, связывающие чистоту продукта с долей закристаллизованного материала при заданном эффективном коэффициенте разделения k при кристаллизации [1–3].
Эффективный коэффициент разделения в фазовых превращениях зависит от скорости процесса. Известно уравнение Бартона-Прима-Слихтера, связывающее k с равновесным коэффициентом разделения k0 и линейной скоростью процесса $v$ [1–3, 8, 9]:
(1)
$k = \frac{{{{k}_{0}}}}{{{{k}_{0}} + (1 - {{k}_{0}})\exp \left( { - v\frac{\delta }{D}} \right)}},$Известен порядок значений δ и D в жидкостях при температурах вблизи температуры плавления Tm: в большинстве систем “основа–примесь” δ ~ 10–3–10–2 см, D ~ 10–5 см2/с, т.е. δ/D ~ ~ 102–103 с/см [1–3, 8, 9]. Также известно, что вблизи Tm в твердом теле для большинства систем “основа–примесь” D ~ 10–6 см2/с [11, 12].
Отмечалось подобие уравнений дистилляции и направленной кристаллизации при соответствующей подстановке в них β или k ([2, гл. 15] и [4, 13]). Так, в работе [4] было отмечено, что уравнение (1), изначально выведенное для рассмотрения кристаллизационных процессов, не имеет запретов на применение также для рассмотрения процессов дистилляции или сублимации, если считать, что k – это межфазовый коэффициент разделения в рассматриваемом испарительном процессе. В то же время, применение уравнения (1) для расчета эффективного коэффициента разделения в испарительных процессах при выбранной температуре наталкивается на препятствие, связанное с отсутствием соответствующих данных о значениях δ/D. Между тем, технологические испарительные процессы рафинирования тех или иных веществ с простой основой зачастую проводятся при температурах, не слишком удаленных от Tm, и можно предполагать, что в этих процессах и при кристаллизации значения δ/D близки. Также можно ожидать, что дополнительные (помимо диффузии примесей) факторы этих процессов (конвекция и/или захват примесей паром основного компонента) несильно проявляются при данных температурах.
В то же время, можно отметить, что описание дистилляции и сублимации с помощью двух параметров (β и Ре) [4, 5] не содержит запретов рассматривать подобным образом и кристаллизационные процессы, в связи с чем возникает вопрос о вычислении в них числа Ре.
В настоящем исследовании была поставлена цель, используя уравнение Бартона-Прима-Слихтера, вычислить значения β/β0 в процессах испарения веществ “основа–примесь” (где основа – простое вещество) при температурах вблизи Tm (т.е. в предположении, что δ/D ~ 102–103 с/см, как в процессах кристаллизации), а также вычислить значения диффузионного числа Пекле при этих температурах для выяснения влияния температуры на эффективность рафинирования веществ в испарительных процессах. Также ставилась задача вычислить значения Ре в процессах кристаллизации.
ВЫПОЛНЕНИЕ РАСЧЕТОВ
Вычисление числа Pe в процессах нормальной направленной кристаллизации. В этих процессах Pe = $v$X/D, где $v$ – скорость кристаллизации, D – коэффициент диффузии примеси, X – длина горизонтального контейнера или толщина слоя расплава в тигле.
Коэффициент β и число Pe в процессах дистилляции и сублимации. Рассматривалось испарение веществ с простой основой, для которых дистилляция и сублимация как процессы рафинирования имеют практический смысл [14–16].
Для расчетов β/β0 использовалось уравнение (1) (с заменой k0 и k на β0 и β соответственно) при значениях δ/D = 100 и 1000 с/см (как для процессов кристаллизации [8, 9]). Для простоты расчетов считалось, что материал и контейнер имеют простые формы, при которых $v$ = w/ρ. Скорость w [г/(см2 с)] вычислялась по уравнению Ленгмюра с помощью известной формулы для числовых расчетов [17]
где p – давление пара [мм рт. ст.] при температуре Т [К], М – атомная (или молярная) масса пара вещества [а.е.м. или г/моль].Справочные данные о давлении p почти всех веществ брали из монографии Несмеянова [18] (для Те учитывалась особенность испаряться в виде молекул Те4), а данные о давлении p для Tb – из [16].
Рассматривалось испарение веществ при Tm и T ≠ Tm при не слишком большом отклонении T от Tm. Поскольку повышение (понижение) температуры процесса увеличивает (уменьшает) одновременно как δ, так и D, предполагалось, что отклонение T от Tm не отражается существенно на значении δ/D. Для вычислений числа Пекле использовалась формула [6, 7]
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Число Pe в процессах направленной кристаллизации. При обычных значениях $v$ < 10 см/ч = 3 × × 10–5 м/с, L ~ 0.1 м и D ~ 10–5 м2/с [3, 8, 9] вычисленное значение Pe < 0.1. При этом изменение $v$ в интервале от 0 до 10 см/ч сопровождается изменением k от k = k0 до k = 1. Таким образом, в кристаллизационных процессах рафинирования учет числа Ре не имеет смысла, при этом (как известно [3, 8, 9]) имеет смысл учет зависимости k от скорости кристаллизации.
Коэффициент β и число Pe в процессах дистилляции и сублимации. Результаты вычислений β, отношения β/β0 и числа Пекле при указанных температурах, δ/D и β0 < 1 приведены в табл. 1 и 2. Обращает на себя внимание то, что в отдельных случаях β/β0 сильно зависит от выбора значения δ/D (100 или 1000 с/см). Сопоставление табл. 1 и 2 позволяет оценить влияние температуры на β/β0 и Pe (при заданном значении X) того или иного вещества, т.е. выяснить роль температуры в процессе его очистки.
Таблица 1.
Отношение β/β0 и число Pe = $v$X/D при X = 1 см для веществ при известных Tm и различных значениях β0 и δ/D
| Вещество | Tm, К | рm, мм рт. ст. | M, а. е. м. | ρ, г/см3 | w, г/(см2 с) | $v$, см/с | β/β0 при δ/D = 100 с/см | β/β0 при δ/D = 1000 с/см | $Pe$ при X = = 1 см |
||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| β0 = = 0.1 | β0 = = 0.01 | β0 = = 0.001 | β0 = 0.1 | β0 = = 0.01 | β0 = = 0.001 | ||||||||
| Sm | 1350 | 4.4 | 150 | 7.5 | 0.08 | 0.011 | 3 | 3 | 3 | 10 | 100 | 1000 | ~103 |
| Yb | 1097 | 3.1 | 173 | 7.0 | 0.07 | 0.010 | 2 | 3 | 3 | 10 | 100 | 1000 | ~103 |
| Mg | 923 | 2.8 | 24 | 1.7 | 0.03 | 0.018 | 4 | 6 | 6 | 10 | 100 | 1000 | ~103 |
| Eu | 1099 | 1.1 | 152 | 5.2 | 0.02 | 0.004 | 1.4 | 1.5 | 1.5 | 9 | 36 | 53 | ~102 |
| Te | 723 | 0.18 | 128 × 4 | 6.2 | 0.006 | 0.0009 | 1.1 | 1.1 | 1.1 | 1.1 | 1.1 | 1.1 | ~10 |
| Zn | 693 | 0.15 | 65 | 7.1 | 0.003 | 0.0004 | 1.0 | 1.0 | 1.0 | 1.0 | 1.0 | 1.0 | ~10 |
| Cd | 594 | 0.12 | 112 | 8.7 | 0.003 | 0.0004 | 1.0 | 1.0 | 1.0 | 1.0 | 1.0 | 1.0 | ~10 |
| Be | 1551 | 0.032 | 9 | 1.8 | 0.00014 | 0.00008 | 1.0 | 1.0 | 1.0 | 1.1 | 1.1 | 1.1 | ~1 |
| Tb | 1629 | <0.001 | 159 | 8.2 | <1 × 10–5 | <1 × 10–5 | 1.0 | 1.0 | 1.0 | 1.0 | 1.0 | 1.0 | ≈0 |
Таблица 2.
Отношение β/β0 и число Pe = $v$X/D при X = 1 см для веществ при температуре испарения T ≠ Tm и различных значениях β0 и δ/D (p – давление пара вещества при температуре Т)
| Вещество | Tm, К | T, К | T/Tm | р, мм рт. ст. | w, г/(см2 с) | $v$, см/с | β/β0 при δ/D = 100 с/см |
β/β0 при δ/D = 1000 с/см |
$Pe$ при X = 1 см | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| β0 = = 0.1 | β0 = = 0.01 | β0 = = 0.001 | β0 = 0.1 | β0 = = 0.01 | β0 = = 0.001 | Q/R = 1 × × 104 К | Q/R = 2 × × 104 К | Q/R = 3 × × 104 К | |||||||
| Sm | 1350 | 1200 | 0.9 | 0.63 | 0.013 | 0.0017 | 1.2 | 1.2 | 1.2 | 4 | 5 | 6 | 1 × 103 | 2 × 103 | 5 × 103 |
| Yb | 1097 | 1000 | 0.9 | 0.55 | 0.013 | 0.0019 | 1.2 | 1.2 | 1.2 | 4 | 6 | 7 | 1 × 103 | 2 × 103 | 6 × 103 |
| Mg | 923 | 800 | 0.9 | 0.16 | 0.002 | 0.0009 | 1.1 | 1.1 | 1.1 | 2 | 2 | 2 | 1 × 103 | 6 × 103 | 5 × 105 |
| Eu | 1099 | 1000 | 0.9 | 0.18 | 0.004 | 0.0008 | 1.1 | 1.1 | 1.1 | 2 | 2 | 2 | 4 × 102 | 5 × 102 | 3 × 103 |
| Te | 723 | 800 | 1.1 | 0.18 | 0.008 | 0.0013 | 1.1 | 1.3 | 1.5 | 3 | 12 | 48 | 57 | 14 | 4 |
| Zn | 693 | 800 | 1.2 | 2.40 | 0.040 | 0.0056 | 1.6 | 1.7 | 1.8 | 10 | 73 | 213 | 17 | 2.5 | 0.36 |
| Cd | 594 | 700 | 1.2 | 2.42 | 0.056 | 0.0065 | 1.7 | 1.9 | 1.9 | 10 | 87 | 400 | 11 | 0.9 | 0.07 |
| Be | 1551 | 1700 | 1.1 | 0.24 | 0.001 | 0.0006 | 1.0 | 1.1 | 1.1 | 2 | 2 | 2 | 4.4 | 3.5 | 2.0 |
| Mg | 923 | 1000 | 1.1 | 10.7 | 0.010 | 0.0566 | 9.7 | 74 | 222 | 10 | 100 | 1000 | 510 | 220 | 100 |
| Tb | 1629 | 2100 | 1.2 | 0.9 | 0.004 | 0.0005 | 1.1 | 1.1 | 1.2 | 3 | 4 | 4 | 550 | 150 | 40 |
Снижение Т по отношению к Tm при сублимации Sm, Yb, Mg, Eu заметно понижает β/β0, увеличивая или уменьшая Pe (по сравнению со значениями этих величин при Т = Tm) в зависимости от Q. Повышение Т по отношению к Tm при дистилляции Te, Zn, Cd несколько повышает β/β0, увеличивая или уменьшая Pe в зависимости от Q. Такое же изменение температуры процесса при дистилляции Be и Tb почти не изменяет β/β0, но заметно увеличивает Pe. Влияние коэффициента β и числа Pe на рафинирование того или иного вещества зависит от природы вещества.
Несмотря на отсутствие в литературе надежных данных о Q и Dm для той или иной системы “основа–примесь”, выполненные расчеты дают представление о влиянии температуры на эффективность рафинирования веществ в испарительных процессах.
ЗАКЛЮЧЕНИЕ
Эффективный коэффициент разделения и число Пекле рассматриваются как два параметра процессов рафинирования веществ кристаллизацией, дистилляцией и сублимацией. Показано, что в кристаллизационных процессах рафинирования число Pe малó и основным параметром является коэффициент разделения (для которого известна зависимость от скорости кристаллизации: уравнение Бартона-Прима-Слихтера с известными значениями δ/D). Для дистилляции и сублимации рассматривались коэффициент разделения и число Pe при температурах испарения, не слишком отличающихся от температур плавления вещества (т.е. при тех же значениях δ/D, что и при кристаллизации).
С помощью названного уравнения при δ/D = 100 и 1000 с/см для ряда веществ с простой основой (Sm, Yb, Mg, Eu, Te, Zn, Cd, Be, Tb) сделано сравнение эффективного (β) и равновесного (β0) коэффициентов разделения при температурах испарения T = (0.9–1.2)Tm, а отдельно вычислены значения числа Pe = $v$X/D при X = 1 см и тех же температурах.
Показано, что повышение T может ухудшать дистилляционное и сублимационное рафинирование рассмотренных веществ как вследствие увеличения расхождения между β и β0, так и вследствие увеличения Pe (при заданном X и β < 1), при этом раздельное влияние коэффициента β и числа Pe на процессы рафинирования различных веществ различно.
Выполненные расчеты дают качественное представление о влиянии температуры на эффективность рафинирования веществ в испарительных процессах.
Список литературы
Девятых Г.Г., Еллиев Ю.Е. Глубокая очистки веществ. М.: Высшая школа, 1990. 192 с.
Дытнерский Ю.И. Процессы и аппараты химической технологии. Изд. 2. В 2 кн. Часть 2. Массообменные процессы и аппараты. М.: Химия, 1995. 368 с.
Кристаллизация из расплавов: Справочное изд. Пер. с нем. Бартел И. и др. М.: Металлургия, 1987. 320 с.
Кириллов Ю.П., Кузнецов Л.А., Шапошников В.А., Чурбанов М.Ф. Влияние диффузии на глубину очистки веществ дистилляцией // Неорган. материалы. 2015. Т. 51. № 11. С. 1177–1182. https://doi.org/10.7868/S002337X15100085
Жуков А.И., Кравченко А.И. Расчет сублимации с учетом диффузии примеси // Неорган. материалы. 2017. Т. 53. № 6. С. 662–668. https://doi.org/10.1134/S0020168517060161
Кравченко А.И., Жуков А.И. Температурная зависимость диффузионного числа Пекле в процессах сублимации некоторых простых веществ // Неорган. материалы. 2021. Т. 57. № 7. С. 789–795. https://doi.org/10.1134/S0020168521070101
Kravchenko A.I., Zhukov A.I., Datsenko O.A. Temperature Dependences of the Peclet Number in Sublimation Processes of Simple Substances // Probl. At. Sci. Technol. 2022. № 1. P. 13–16. https://vant.kipt.kharkov.ua/
Burton J.A., Prim R.C., Slichter W.P. The Distribution of Solute in Crystals Growth from the Melt. 1. Theoretical // J. Chem. Phys. 1953. V. 21. № 11. P. 1987–1991.
Бартон Дж.А., Прим Р.К., Слихтер В.Р. Распределение примесей в кристаллах, выращенных из расплава. Ч. 1. Теория // Германий / Под ред. Петрова Д.А. М.: Иностранная литература, 1955. С. 74–81.
Нисельсон Л.А., Ярошевский А.Г. Межфазовые коэффициенты распределения. Равновесия кристалл–жидкость и жидкость–пар. М.: Наука, 1992. 399 с.
Бокштейн Б.С., Ярославцев А.Б. Диффузия атомов и ионов в твердых телах. М.: МИСиС, 2005. 362 с.
Бокштейн Б.С. Атомы блуждают по кристаллу. М.: Наука, 1984. 208 с.
Kravchenko A.I. Simple Substances Refining: Efficiency of Distillation Methods // Funct. Mater. 2000. V. 7. № 2. P. 315–318.
Кравченко А.И. Уравнение распределение примеси в твердом дистилляте // Неорган. материалы. 2007. Т. 43. № 8. С. 1021–1022.
Кравченко А.И. Соотношение между эффективным и идеальным коэффициентами разделения при дистилляции и сублимации // Неорган. материалы. 2016. Т. 52. № 4. С. 423–430. https://doi.org/10.1134/S0020168516040096
Ke L., Zhang L., Zhang X., Li Z., Wang Z., Chen D., Zhou L., Chen S., Zheng L., Zhou X. Medium-Volatile Impurity Distribution in Purification of Terbium Metal by Vacuum Distillation // Sep. and Purif. Technol. 2021. V. 266. https://doi.org/10.1016/j.seppur.2021.118566
Пазухин В.А., Фишер А.Я. Разделение и рафинирование металлов в вакууме. М.: Металлургия, 1969. 204 с.
Несмеянов А.Н. Давление пара химических элементов. М.: Из-во АН СССР, 1961. 396 с.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы


