Неорганические материалы, 2022, T. 58, № 8, стр. 884-890
Получение высокочистого тетрахлорида кремния-28 из тетрафторида кремния-28
О. Ю. Трошин 1, 2, *, А. Д. Буланов 1, 2, Ю. П. Кириллов 1, А. М. Потапов 1, П. А. Отопкова 1, М. Е. Комшина 1, 2, К. Ф. Игнатова 1, А. А. Ермаков 1
1 Институт химии высокочистых веществ им. Г.Г. Девятых Российской
академии наук
603951 Нижний Новгород, ул. Тропинина, 49, БОКС-75, Россия
2 Национальный исследовательский Нижегородский государственный
университет им. Н.И. Лобачевского
603022 Нижний Новгород, пр. Гагарина, 23, Россия
* E-mail: troshin@ihps-nnov.ru
Поступила в редакцию 25.02.2022
После доработки 20.05.2022
Принята к публикации 23.05.2022
- EDN: DHPZLV
- DOI: 10.31857/S0002337X22080127
Аннотация
Изучено взаимодействие тетрафторида кремния с хлоридом алюминия(III) в закрытом реакторе в интервале температур 473–543 К, протекающее в форме последовательных реакций SiF4 → SiClF3 → → SiCl2F2 → SiCl3F → SiCl4. Определены значения эффективных констант скоростей и энергия активации последовательных реакций превращения тетрафторида кремния в тетрахлорид кремния. Разработана методика получения изотопно обогащенного 28SiCl4 из 28SiF4, включающая стадии синтеза и дистилляционной очистки 28SiCl4. Содержание примесей химических элементов в высокочистом 28SiCl4, по данным масс-спектрометрии с индуктивно связанной плазмой, находится на уровне n × 10–1–n × 10–4 мкг/г, содержание изотопа кремния-28 в составе кремния составляет 99.99757 ± 0.00060 ат. %.
ВВЕДЕНИЕ
Одним из активно развивающихся направлений фундаментальных и прикладных исследований является получение, характеризация свойств и практическое применение изотопно модифицированных веществ с высокой степенью химической и изотопной чистоты [1]. Особый интерес вызывает получение и изучение влияния изотопного состава на свойства оптических материалов, таких как кварцевое стекло. В ряде работ [2–5] на основании теоретической оценки отмечается возможность снижения оптических потерь и расширения окна прозрачности оптического волокна за счет светопроводящей сердцевины на основе 30Si18O2 и оболочки на основе 28Si16O2. Также отмечается возможность обеспечения эффекта полного внутреннего отражения в такой кварцевой световодной структуре за счет различия в изотопном составе кремния и кислорода без использования легирующих добавок [6].
Для получения высокочистого кварцевого стекла различными способами (осаждение из паровой фазы, золь–гель-метод) используется тетрахлорид кремния, а в качестве исходного вещества для разделения изотопов кремния методом газового центрифугирования используется его тетрафторид [7]. Поэтому разработка методики получения изотопно обогащенного тетрахлорида кремния из тетрафторида кремния представляется актуальной задачей. Следует отметить, что центробежное разделение изотопов кремния можно проводить с использованием тетрахлорида кремния или трихлорсилана [8], однако недостатком этого способа является низкий выход целевого продукта. В литературе описано получение небольших количеств 28SiCl4 [9] и 29SiCl4 [10] путем хлорирования дефицитных изотопов кремния; сведения о степени изотопной и химической чистоты веществ в этих работах отсутствуют. В патенте [11] разработана методика получения 28SiCl4 со степенью обогащения по 28Si на уровне 99.9% из тетрафторида кремния-28.
В работе [12] изучена конверсия летучих фторидов углерода, кремния, германия в хлориды при помощи хлоридов магния, кальция, железа(III), алюминия(III). Практический выход SiCl4 по SiF4 в статических условиях составил 83% при использовании избытка хлорида алюминия(III), начальном давлении тетрафторида кремния около 9 атм, температуре 195–244°С; кинетические закономерности превращения SiF4 в SiCl4 в работе не рассматривались. Отмечается наличие фторидов-хлоридов кремния SiCl3F, SiCl2F2, SiClF3 в полученном SiCl4 [12]. Эффективным способом очистки SiCl4 от примесей фторидов-хлоридов кремния является дистилляция [13].
Целью данной работы является изучение кинетики взаимодействия тетрафторида кремния с хлоридом алюминия(III) в статических условиях, разработка методики получения 28SiCl4 с высокой химической и изотопной чистотой из 28SiF4, исследование примесного состава 28SiCl4 и изотопного состава кремния в 28SiCl4.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Опыты по изучению кинетики взаимодействия тетрафторида кремния с хлоридом алюминия(III) в статических условиях проводили на установке, которая включает в себя газораспределительную гребенку с вакуумным насосом, горизонтально установленный фланцевый реактор из нержавеющей стали 12Х18Н10Т с резистивным нагревателем и регулятором температуры “Метакон”, баллон с тетрафторидом кремния, приемный баллон для тетрахлорида кремния. Давление в установке контролировали по показаниям образцового вакуумметра ВО и образцового манометра МО 11201. В опытах использовали хлорид алюминия(III) (ультрасухой, 99.99%; ООО “Ланхит”, г. Москва) и тетрафторид кремния, полученный путем термического разложения Na2SiF6 [14].
Методика проведения опытов состояла из следующих этапов. В реактор загружали навеску хлорида алюминия(III), реактор вакуумировали и заполняли тетрафторидом кремния до расчетного давления, обеспечивающего соотношение количеств веществ n(SiF4) : n(AlCl3) = 3 : 8 (двухкратный избыток AlCl3 относительно стехиометрического). Реактор с реагентами нагревали до заданной температуры (скорость нагрева 10 К/мин) и выдерживали до выхода концентрации тетрахлорида кремния в газовой смеси на плато. Опыты проводили при 200, 235, 270°С. Состав газообразных продуктов реакции определяли хроматографическим методом (газовый хроматограф “Цвет 500” с детектором по теплопроводности) по методике, приведенной в работе [15]; газовые пробы отбирали в стеклянные ампулы с фторопластовыми штоками. На основании результатов газохроматографического анализа получали кинетические кривые для веществ-участников последовательной реакции
(1)
$\begin{gathered} {\text{Si}}{{{\text{F}}}_{{\text{4}}}}\xrightarrow{{{{k}_{1}}{\text{\;}}}}{\text{SiCl}}{{{\text{F}}}_{3}}\xrightarrow{{{{k}_{2}}{\text{\;}}}} \\ \to {\text{SiC}}{{{\text{l}}}_{{\text{2}}}}{{{\text{F}}}_{{\text{2}}}}{\text{\;}}\xrightarrow{{{{k}_{3}}{\text{\;}}}}{\text{SiC}}{{{\text{l}}}_{{\text{3}}}}{\text{F}}\xrightarrow{{{{k}_{4}}{\text{\;}}}}{\text{SiC}}{{{\text{l}}}_{{\text{4}}}}. \\ \end{gathered} $Значения эффективных констант скоростей указанных последовательных реакций ki определяли на основании кинетических кривых для галогенидов кремния в газовой смеси (т.н. обратная задача химической кинетики) путем решения системы дифференциальных уравнений для последовательной необратимой четырехстадийной реакции [16] с применением пакета прикладных программ MATLAB 8. На основании температурной зависимости эффективных скоростей последовательных реакций ki рассчитывали значения эффективной энергии активации стадий и общее значение энергии активации последовательной реакции (1).
Изотопно обогащенный тетрахлорид кремния-28 получали по реакции 28SiF4 (обогащение по изотопу 28Si 99.99769 ± 0.00026 ат. %, АО “ПО “Электрохимический завод”, г. Зеленогорск) и хлорида алюминия(III) по описанной выше методике при 270°С. Полученный 28SiCl4 очищали методом изотермической дистилляции в кварцевой аппаратуре [17] со средней скоростью перегонки 1.5 × 10–3 см/мин.
Содержание примесей фторидов-хлоридов кремния и примесей HF, HCl, Si2OF6, Si2OCl6, которые образуются в результате гидролиза галогенидов кремния, в 28SiCl4 определяли методом ИК-спектроскопии на приборе BrukerVertex 80v c детектором DTGS в диапазоне 450–7000 см–1. Разрешение и апертура составляли 1 см–1 и 5 мм соответственно. Пробы отбирали в кювету из нержавеющей стали с окнами из ZnSe (длина оптического пути 10 см), давление пробы 20 мм. рт. ст. Концентрацию примесей фторидов-хлоридов кремния в тетрахлориде кремния рассчитывали по методике, приведенной в работе [18]. Интегральные коэффициенты поглощения для фторидов-хлоридов кремния рассчитывались ab initio неэмпирическим методом SCF с учетом электронной корреляции по теории возмущений Меллера–Плесета (MP2) с использованием базисного набора 6-311G(3df, 3pd) [19].
Содержание примесей химических элементов в 28SiCl4 и изотопный состав кремния в составе 28SiF4, 28SiCl4 определяли методом масс-спектрометрии (масс-спектрометр высокого разрешения с индуктивно связанной плазмой ELEMENT 2 Thermo Scientific) по методике, приведенной в работе [20].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
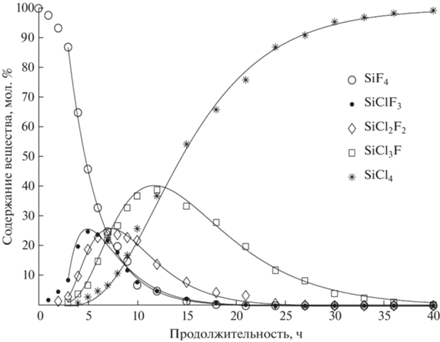
На рис. 1 приведены кинетические кривые для галогенидов кремния SiF4, SiClF3, SiCl2F2, SiCl3F, SiCl4, полученные при температуре 270°С. Значками обозначены экспериментальные данные по содержанию веществ, линиями – расчет содержания веществ по кинетическому уравнению первого порядка. Из рис. 1 видно, что экспериментальные данные удовлетворительно соответствуют расчетным; наблюдаемое различие опытных и расчетных данных по содержанию SiF4, SiClF3 в начале опыта (0–3 ч), по-видимому, обусловлено конечной скоростью процессов нагрева реактора, перехода хлорида алюминия(III) в паровую фазу и взаимодействия его с тетрафторидом кремния. В ходе процесса содержание SiF4 в смеси снижается, образуются промежуточные фториды-хлориды кремния SiClF3, SiCl2F2, SiCl3F и накапливается SiCl4: подобная зависимость характерна для последовательных (консекутивных) реакций, в которых продукт одной стадии является исходным веществом для последующей [21].
Рис. 1.
Кинетические кривые для SiF4, SiClF3, SiCl2F2, SiCl3F, SiCl4 в составе газообразных продуктов реакции 28SiF4 с AlCl3 при температуре 270°С (сплошные линии – расчет по кинетическому уравнению).
Расчетные значения эффективных констант скоростей последовательных реакций (1) при температуре 473 К составляют (ч–1): k1 = 0.11, k2 = 0.30, k3 = 0.19, k4 = 0.04; при 543 К (ч–1): k1 = 0.32, k2 = = 0.57, k3 = 0.42, k4 = 0.16.
При сопоставлении значений эффективных констант скоростей последовательных реакций k1–k4 видно, что лимитирующей стадией процесса синтеза SiCl4 является реакция образования SiCl4 из SiCl3F.
На основании температурной зависимости k определяли значения эффективной энергии активации последовательных реакций (1) (кДж/моль): Еа,1 = 32.6, Еа,2 = 19.6, Еа,3 = 24.2, Еа,4 = 42.3; общая эффективная энергия активации реакции (1) составляет 118.7 кДж/моль.
Отметим, что хлорид алюминия(III) при повышенной температуре обладает заметной летучестью (тройная точка при 192.6°С, 0.228 МПа [22]), что увеличивает скорость реакции тетрафторида кремния с хлоридом алюминия(III). Пары́ непрореагировавшего хлорида алюминия(III) конденсируются на фланце реактора, что позволяет отделять его от нелетучего фторида алюминия. Практический выход 28SiCl4 по 28SiF4 составляет 94 ± 2%.
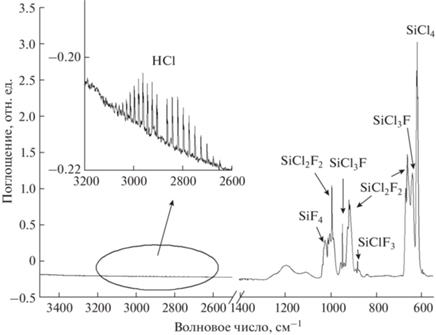
На рис. 2 приведен ИК-спектр 28SiCl4, полученного по реакции 28SiF4 с хлоридом алюминия(III).
В спектре присутствуют полосы поглощения галогенидов кремния SiF4, SiClF3, SiCl2F2, SiCl3F, SiCl4, а также хлороводорода.
В табл. 1 приведены результаты ИК-спектроскопического определения содержания фторидов-хлоридов кремния, HF, HCl, Si2OF6, Si2OCl6 в образцах синтезированного и дистиллированного тетрахлорида кремния-28, а также значения пределов обнаружения указанных веществ. Видно, что в полученном образце тетрахлорида кремния-28 присутствуют примеси SiF4, SiCl3F, SiCl2F2, SiClF3 и HCl на уровне n × 10–3–n × × 10–2 мол. %. В дистиллированном 28SiCl4 содержание примесей SiCl2F2, SiClF3 и HCl находится ниже уровня ПО методики ИК-спектроскопического анализа ((1–3) × 10–3 мол. %), содержание SiCl3F находится на уровне ПО методики. Практический выход очищенного 28SiCl4 составил 90 ± 2%.
Таблица 1.
Значения пределов обнаружения (ПО) и содержание ряда примесей в образцах 28SiCl4 по данным ИК-спектроскопии
| Примесь | ν, см–1 | ПО, мол. % | Содержание примеси, мол. % | |
|---|---|---|---|---|
| 28SiCl4 исходный | 28SiCl4 дистиллят | |||
| SiCl3F | 947 | 3 × 10–3 | (4.7 ± 1.0) × 10–2 | (4.3 ± 1.0) × 10–3 |
| SiCl2F2 | 915 | 1 × 10–3 | (9.0 ± 1.0) × 10–3 | <ПО |
| SiClF3 | 880 | 1 × 10–3 | (1.4 ± 0.2) × 10–3 | <ПО |
| SiF4 | 1031 | 1 × 10–4 | (5.0 ± 1.0) × 10–3 | <ПО |
| HCl | 2887 | 2 × 10–3 | (2.5 ± 0.4) × 10–3 | <ПО |
| HF | 4038 | 1 × 10–2 | <ПО | <ПО |
| Si2OF6 | 838 | 2 × 10–3 | <ПО | <ПО |
| Si2OCl6 | 1115 | 1 × 10–3 | <ПО | <ПО |
В табл. 2 приведены результаты определения содержания примесей химических элементов в 28SiCl4, полученном по реакции 28SiF4 с хлоридом алюминия(III), и в 28SiCl4, очищенном методом изотермической дистилляции, методом масс-спектрометрии с индуктивно связанной плазмой. Из табл. 2 видно, что основной вклад в примесный состав полученного 28SiCl4 вносят примеси алюминия, кальция и железа, содержание которых находится на уровне 1–2 мкг/г 28SiCl4. Дистилляционная очистка позволяет снизить содержание распространенных химических элементов до уровня n × 10–1 мкг/г; содержание примесей металлов (хром, никель, железо, медь, натрий, магний и др.) находится ниже уровня ПО данной методики (n × 10–1–n × 10–3 мкг/г).
Таблица 2.
Содержание примесей химических элементов в образцах 28SiCl4 по данным масс-спектрометрии с индуктивно связанной плазмой
| Примесь | Содержание примеси в образце, мкг/г | |
|---|---|---|
| 28SiCl4 после синтеза | 28SiCl4 дистиллят | |
| Al | 1.4 ± 0.6 | 0.20 ± 0.05 |
| As | <0.1 | <0.1 |
| B | 0.22 ± 0.05 | <0.06 |
| Ba | <0.003 | <0.003 |
| Ca | 1.0 ± 0.4 | 0.24 ± 0.07 |
| Cd | 0.005 ± 0.001 | <0.0002 |
| Co | <0.001 | <0.001 |
| Cr | 0.011 ± 0.004 | <0.001 |
| Cu | 0.03 ± 0.01 | <0.003 |
| Fe | 1.9 ± 0.5 | <0.2 |
| K | 0.08 ± 0.01 | <0.02 |
| Li | <0.002 | <0.002 |
| Mg | 0.052 ± 0.007 | <0.04 |
| Mn | 0.012 ± 0.004 | <0.005 |
| Na | 0.21 ± 0.08 | <0.02 |
| Ni | <0.03 | <0.03 |
| P | <0.05 | <0.05 |
| Pb | 0.0030 ± 0.0005 | 0.0008 ± 0.0001 |
| Sn | 0.5 ± 0.1 | <0.006 |
| Sr | 0.0024 ± 0.0003 | 0.0011 ± 0.0003 |
| Te | <0.004 | <0.004 |
| Ti | 0.011 ± 0.003 | 0.005 ± 0.001 |
| Tl | <0.003 | <0.003 |
| V | <0.002 | <0.002 |
| Zn | 0.08 ± 0.02 | 0.09 ± 0.02 |
В табл. 3 приведены результаты определения изотопного состава кремния в исходном 28SiF4 и дистиллированном 28SiCl4 методом масс-спектрометрии с индуктивно связанной плазмой.
Таблица 3.
Изотопный состав кремния в составе 28SiF4, 28SiCl4 по данным масс-спектрометрии с индуктивно связанной плазмой
| Изотоп кремния | Содержание изотопа кремния в составе Si, ат. % | |
|---|---|---|
| исходный 28SiF4 | 28SiCl4 дистиллят | |
| 28Si | 99.99769 ± 0.00026 | 99.99757 ± 0.00060 |
| 29Si | 0.00226 ± 0.00024 | 0.00223 ± 0.00055 |
| 30Si | 0.00005 ± 0.00003 | 0.00020 ± 0.00006 |
При сопоставлении данных табл. 3 видно, что содержание изотопов 28Si и 29Si в составе исходного 28SiF4 и дистиллированного 28SiCl4 в пределах погрешности определения не изменяется, различие в содержании изотопа 30Si в этих веществах выходит за рамки погрешности определения. Вероятной причиной этого различия является небольшое изотопное разбавление кремния на стадиях синтеза и очистки в кварцевой аппаратуре.
ЗАКЛЮЧЕНИЕ
Изучено взаимодействие тетрафторида кремния с хлоридом алюминия(III) в закрытом реакторе в интервале температур 200–270°С, протекающее в форме последовательных реакций SiF4 → SiClF3 → SiCl2F2 → SiCl3F → SiCl4. Определены значения эффективных констант скоростей этих реакций при 473 и 543 К и энергии активации последовательных реакций превращения тетрафторида кремния в тетрахлорид кремния: Еа,1 = 32.6, Еа,2 = 19.6, Еа,3 = 24.2, Еа,4 = 42.3; общая эффективная энергия активации 118.7 кДж/моль.
Разработана методика получения изотопно обогащенного 28SiCl4 из 28SiF4, включающая стадии синтеза и дистилляционной очистки 28SiCl4. Практический выход 28SiCl4 по 28SiF4 на стадии синтеза составляет 94 ± 2%; практический выход высокочистого 28SiCl4 на стадии очистки – 90 ± 2%. Содержание SiCl3F в 28SiCl4, по данным ИК-спектроскопии составляет (4.3 ± 1.0) × 10–3 мол. %, SiCl2F2 и SiClF3 – менее 1 × 10–3 мол. %. Содержание примесей химических элементов в высокочистом 28SiCl4, по данным масс-спектрометрии с индуктивно связанной плазмой, находится на уровне n × 10–1–n × 10–4 мкг/г, содержание изотопа кремния-28 в составе кремния составляет 99.99757 ± 0.00060 ат. %.
Список литературы
Андреев Б.М., Арефьев Д.Г., Баранов В.Ю. и др. Изотопы: свойства, получение, применение. М.: Физматлит, 2005. Т. 2. 728 с.
Kelsey V., Alexander J.E., Burden S.J. Isotopically Engeneered Optical Materials: Пат. США № 20030039865. Опубл. 27.02.2003.
Allan D.C., Brown J.T., Сhacon L.C. et al. Isotopically Altered Optical Fiber: Пат. США № 6810197. Опубл. 26.10.2004.
Brown T.G., Painter B.A. Low Loss Isotopic Optical Waveguides: Пат. США № 20030002834. Опубл. 02.01.2003.
Heitmann W., Klein K.F. Glass for Optical Waveguides or the like: Пат. США № 6490399. Опубл. 03.12.2002.
Плеханов В.Г. Изотопическая инженерия // Успехи физ. наук. 2003. Т. 173. № 7. С. 711–738. https://doi.org/10.3367/UFNr.0170.200011i.1245
Abrosimov N.V., Aref’ev D.G., Becker P. et al. A New Generation of 99.999% Enriched 28Si Single Crystals for the Determination of Avogadro’s Constant // Metrologia. 2017. № 54. P. 599–609. https://doi.org/10.1088/1681-7575/aa7a62
Тихомиров А.В. Способ разделения изотопов кремния: Пат. РФ № 2172642. Опубл. 27.09.2001.
Bracht H., Staskunaite R., Haller E.E., Fielitz P., Borchardt G., Grambole D. Silicon Diffusion in Sol-Gel Derived Isotopically Enriched Silica Glasses // J. Appl. Phys. 2005. № 97. P. 046107 (1–3). https://doi.org/10.1063/1.1857051
Palmai M., Szalay R., Barczak D., Varga Z., Nagy L.N., Gollwitzer C., Krumrey M. Total Synthesis of Isotopically Enriched Si-29 Silica NPs as Potential Spikes for Isotope Dilution Quantification of Natural Silica NPs // J. Colloid Interface Sci. 2015. № 445. P. 161–165. https://doi.org/10.1016/j.jcis.2014.12.085
Чурбанов М.Ф., Буланов А.Д., Трошин О.Ю., Гребеньков К.С. Способ получения изотопнообогащенного тетрахлорида кремния: Пат. РФ № 2618265. Опубл. 03.05.2017.
Schumb W.C., Breck D.W. Some Metathetical Reactions of the Gaseous Fluorides of Group IV // J. Am. Chem. Soc. 1952. № 74(7). P.1754–1760. https://doi.org/10.1021/JA01127A043
Трошин О.Ю., Буланов А.Д., Чернова О.Ю. Равновесие жидкость–пар в системе SiCl4 – примеси SiCl4 –nFn (n = 1–4) // Неорган. материалы. 2018. Т. 54. № 8. С. 888–891. https://doi.org/10.1134/S0002337X1808016X
Буланов А.Д., Пряхин Д.А., Балабанов В.В. Получение высокочистого тетрафорида кремния термическим разложением Na2SiF6 // Журн. прикл. химии. 2003. Т. 76. № 9. С. 1433–1435.
Сорочкина Т.Г., Чернова О.Ю., Трошин О.Ю., Созин А.Ю., Буланов А.Д., Ермаков А.А. Газохроматографическое определение фторид-хлоридов кремния SiClnF4–n (n = 0–4), полученных по реакции тетр афторида кремния с хлоридом алюминия(III) // Аналитика и контроль. 2019. Т. 23. № 4. С. 525–531. https://doi.org/10.15826/analitika.2019.23.4.011
Родигин Н.М., Родигина Э.Н. Последовательные химические реакции: математический анализ и расчеты. М.: Изд. АН СССР, 1960. 138 с.
Мицуике А. Методы концентрирования микроэлементов в неорганическом анализе: Пер. с англ. М.: Химия, 1986. 152 с.
Чупров Л.А., Сенников П.Г., Тохадзе К.Г., Игнатов С.К., Шремс О. Примеси в тетрафториде кремния и получаемом из него силане по данным ИК-Фурье-спектроскопии высокого разрешения // Неорган. материалы. 2006. Т. 42. № 8. С. 1017–1024.
Burtsev A.P., Bocharov V.N., Ignatov S.K. et al. Integral Intensities of Absorption Bands of Silicon Tetrafluoride in the Gas Phase and Cryogenic Solution: Experiment and Calculation // Opt. Spectrosc. 2005. V. 98. № 2. P. 227–234. https://doi.org/10.1134/1.1870065
Отопкова П.А., Потапов А.М., Сучков А.И., Буланов А.Д., Лашков А.Ю., Курганова А.Е. Изотопный анализ высокообогащенного кристаллического 28Si и исходного 28SiF4 методом масс-спектрометрии высокого разрешения с индуктивно связанной плазмой // Масс-спектрометрия. 2018. Т. 15. № 3. С. 209–215. https://doi.org/10.25703/MS.2018.15.35
Панченков Г.М., Лебедев В.П. Химическая кинетика и катализ // Уч. пособие для вузов. 3-е изд. испр. и доп. М.: Химия, 1985. 592 с.
Фурман А.А. Неорганические хлориды (химия и технология). М.: Химия, 1980. 416 с.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы