Поверхность. Рентгеновские, синхротронные и нейтронные исследования, 2020, № 2, стр. 63-71
Анализ причин неравномерности распределения радионуклида 36Cl в облученном ядерном графите
Е. В. Беспала a, *, А. О. Павлюк b, С. Г. Котляревский b, И. Ю. Новоселов c, **
a ФГУП “Горно-химический комбинат”
636039 Железногорск, Россия
b АО “Опытно-демонстрационный центр вывода
из эксплуатации уран-графитовых ядерных реакторов”
636000 Северск, Россия
c Национальный исследовательский Томский политехнический университет
634050 Томск, Россия
* E-mail: bespala_evgeny@mail.ru
** E-mail: inovoselov@tpu.ru
Поступила в редакцию 26.03.2019
После доработки 18.04.2019
Принята к публикации 22.04.2019
Аннотация
Работа посвящена анализу процессов накопления в облученном графите уран-графитовых ядерных реакторов долгоживущего радионуклида 36Cl, который является одним из наиболее значимых радионуклидов при оценке безопасности захоронения РАО. Проведен анализ так называемого эффекта “самородка” (Nugget effect), обусловленного существенной неравномерностью содержания 36Cl в пробах облученного графита ядерных реакторов. Различия в концентрациях 36Cl в одних и тех же графитовых элементах достигают 100 раз независимо от эксплуатационных факторов (поток нейтронов, температура). Рассмотрены основные процессы, которые могут влиять на формирование загрязнения 36Cl в облученном графите. Особое внимание уделено определению формы нахождения 36Cl в графите с учетом особенностей его изготовления, включая термодинамическое моделирование равновесного состава продуктов реакции при очистке необлученного графита в газовой среде.
ВВЕДЕНИЕ
В процессе эксплуатации уран-графитовых ядерных реакторов и после их окончательной остановки образуются графитовые радиоактивные отходы (РАО), количество которых на сегодняшний день только в Российской Федерации составляет ≈60 000 тонн.
Период потенциальной опасности ≈90% графитовых РАО определяется (главным образом) наличием в составе деталей графитовых кладок долгоживущих радионуклидов 14С, 36Сl и их удельным содержанием. Период полураспада 14С составляет 5370 лет, его удельная активность в графите отечественных уран-графитовых реакторах (УГР) составляет 103–106 Бк/г, для 36Cl – 3.1 × × 105 лет и 101–2 × 103 Бк/г соответственно [1].
Главным условием при обосновании вариантов обращения с графитовыми РАО является обеспечение изоляции содержащихся в них радионуклидов на весь период сохранения ими потенциальной опасности. По оценкам 36Cl по истечении характерного периода ≈104–105 лет будет определять основные параметры потенциального влияния облученного графита на окружающую среду и население при захоронении. Более того данный радионуклид практически не задерживается природными материалами при миграции, в то время как долгоживущие актиниды эффективно сорбируются барьерными материалами и материалами вмещающих пород.
Очевидно, что гарантия изоляции радионуклидов на период потенциальной опасности при захоронении или временнóм хранении графитовых РАО будет определяться не только величиной активности долгоживущих радионуклидов, но и показателями, определяющими прочность фиксации радионуклидов в самом графите. Учитывая тот факт, что графит является практически “неокисляемым” материалом при нормальных температурных условиях, то выход радионуклидов (в том числе 36Cl) из графитовых РАО будет определяться параметрами их селективного выщелачивания, которые, в свою очередь, зависят от формы нахождения и энергии связи долгоживущих радионуклидов со структурой графита. Следовательно, эти данные будут являться определяющими при выполнении прогнозного моделирования миграции радионуклидов, результаты которого являются определяющими при обосновании вариантов захоронения графитовых РАО.
В настоящее время в качестве перспективного подхода к решению проблемы обращения с облученным графитом рассматривается способ приповерхностного захоронения графитовых РАО с предварительной их обработкой. Реализация данного подхода возможна при условии успешного решения задачи селективного удаления доли 14C и 36Cl, характеризуемой более низкой прочностью фиксации в структуре графита. Такой подход может обеспечить снижение потенциальной опасности графита при захоронении и, как следствие, снизить требования к способу и технологии захоронения, что влечет за собой существенное снижение стоимости всего процесса. Эффективность использования данного подхода также определяется формами нахождения и энергией связи долгоживущих радионуклидов со структурой графита.
Таким образом, целью данной работы является оценка возможных соединений, в которых может находиться радионуклид 36Cl, а также анализ причин его образования и накопления в облученном ядерном графите.
АНАЛИЗ НЕРАВНОМЕРНОСТИ СОДЕРЖАНИЯ 36Cl В ГРАФИТЕ УГР
Обобщенная информация об удельной активности радионуклида 36Cl в облученном графите, отобранном из кладок различных УГР, представлена в табл. 1.
Таблица 1.
| Страна | Расположение | Тип реактора | Активность 36Cl, Бк/г |
|---|---|---|---|
| Франция | Маркуль G2 | UNGG | 100–700 |
| Франция | Шинон A3 | UNGG | 7–70 |
| Франция | Сен-Лоран A1 | UNGG | 3–10 |
| Франция | Сен-Лоран A2 | UNGG | 37–100 |
| Франция | Бюже 1 | UNGG | 83–850 |
| Великобритания | Хантерстон А | Magnox | 132–1775 |
| Великобритания | Олдбари | Magnox | ≈425 |
| США | Хэнфорд | Реактор B | ≈2460 |
| США | Хэнфорд | Реактор C | ≈705 |
| США | Хэнфорд | Реактор D | ≈1990 |
| США | Хэнфорд | Реактор DR | ≈1530 |
| США | Хэнфорд | Реактор F | ≈1940 |
| США | Хэнфорд | Реактор KE | ≈1998 |
| США | Хэнфорд | Реактор KW | ≈1920 |
| Россия | ПО Маяк | АВ-1 | <13 500* |
| Россия | ПО Маяк | АВ-2 | <10 800* |
| Россия | ПО Маяк | АВ-3 | <10 800* |
| Россия | ПО Маяк | АИ | <5600 |
| Россия | АО “ОДЦ УГР” | И-1 | 54–110 |
| Испания | Вандельос | UNGG | 14–25 |
| Украина | ЧАЭС (блок № 2) | РБМК-1000 | 700–1500 |
| Литва | ИгАЭС (блок № 1) | РБКМ-1500 | ≈2600 |
| Швейцария | Дайорит (PSI) | PHWR | 22–414 |
| Швейцария | Протеус (PSI) | Исследовательский | 0.003–0.031 |
| Дания | Risoe National Lab. | DR-2 | 0.18–40 |
| Германия | АЭС THTR-300 | THTR-300 | 23–370 |
| Германия | Юлих | AVR | ≈800 |
| Примечание. * – Из результатов расчета. | |||
В настоящей работе проведена оценка содержания 36Cl в графите некоторых промышленных УГР (ПУГР) и реакторов типа РБМК-1000. Результаты сведены в табл. 2.
Таблица 2.
Результаты оценки содержания 36Cl в графите российских УГР [10]
| Расположение | Тип реактора | Тип графитовых деталей | Активность 36Cl, Бк/г |
|---|---|---|---|
| ФГУП ПО “Маяк” | АВ-1 | Блоки | 250–890 |
| ФГУП ПО “Маяк” | АВ-2 | Блоки | 80–400 |
| АО “ОДЦ УГР” | И-1 | Втулки | 90–450 |
| АО “ОДЦ УГР” | АДЭ-3 | Втулки | 240–670 |
| АО “ОДЦ УГР” | АДЭ-4, АДЭ-5 | Блоки | 10–1100 |
| Ленинградская АЭС-2 | РБМК-1000 | Смесь крошки из графитовых блоков | 570 |
| Курская АЭС | РБМК-1000 | Кольца КТК | 260–920 |
Результаты настоящих исследований, а также ряда других свидетельствуют о достаточно широком разбросе значений содержания микропримесей, приводящих к образованию радионуклида 36Cl, а также удельной активности 36Cl в графите УГР (табл. 1, 2), полученных как при расчетных оценках, так и при экспериментальном определении. На рис. 1 представлены полученные в ходе настоящей работы результаты определения удельной активности 36Cl и 14C (для сравнения) блочного графита в трех точках по высоте двух ячеек графитовой кладки ПУГР и по толщине стенок графитовых блоков в точках отбора. Нейтронно-физические и термодинамические параметры эксплуатации графита в обеих ячейках одинаковы.
Рис. 1.
Распределения удельной активности 36Cl и 14C в графитовой кладке ПУГР: а, б – по высоте ячеек; в–з – по толщине стенок графитовых блоков на отметках отбора (наружная поверхность блока, центр стенки блока, внутренняя поверхность отверстия в блоке).
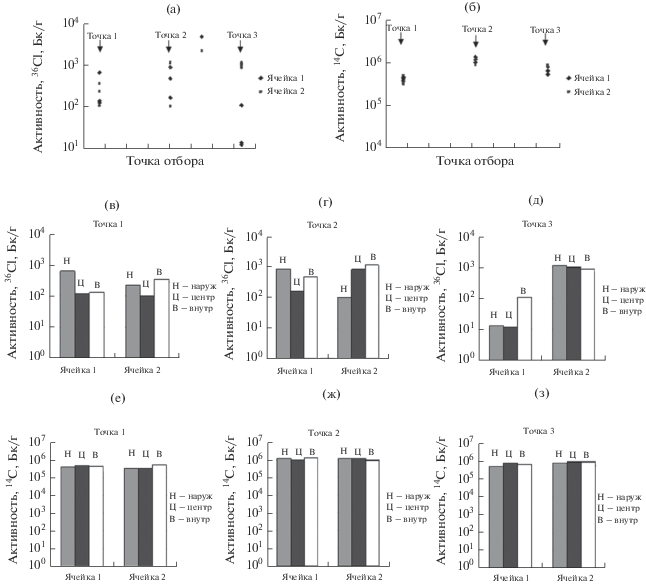
Очевидно, что распределение удельной активности 36Cl варьируется в широких пределах (существенно более широких, чем вариация потока нейтронов, температуры облучения и др., учитывая погрешность измерений ≈10−20%) как по объему кладки в целом (рис. 1а), так и по толщине стенок отдельных графитовых блоков (рис. 1в–1д). Не наблюдается также общих закономерностей по форме кривых высотного распределения и распределения по толщине стенок блоков. Следует отметить, что, несмотря на более сложную (по нескольким независимым каналам) схему образования, активность 14C с учетом погрешности измерений ≈20% практически равномерно распределена (рис. 1е–1з) по сечению графитового блока (существенная неравномерность распределения 14C характерна только для размеров областей графита, сопоставимых с размерами кристаллитов).
Большая вариация величины удельной активности 36Cl, а также отсутствие общих закономерностей распределения 36Cl по объему графитовой кладки и по сечению графитового блока, объясняются, вероятно, тем, что атомы 36Cl содержатся в графите в виде локализованных областей (эффект “самородка”). Распределение данных областей обладает высокой степенью неравномерности, проявляющейся как в объемах графита с характерными размерами не менее ≈1–2 мм (толщина образца), так и в объемах с характерными размерами в десятки сантиметров (размер блоков). Такое распределение можно объяснить (предположительно): 1) исходным распределением примесных материнских атомов в виде локальных образований, сформировавшихся при технологическом процессе производства графитовых блоков; 2) протеканием каких-либо более сложных процессов, способствующих формированию локальных областей скопления атомов 36Cl в процессе эксплуатации.
ОСОБЕННОСТИ ОБРАЗОВАНИЯ 36Cl В ГРАФИТЕ ПРИ ОБЛУЧЕНИИ НЕЙТРОННЫМ ПОТОКОМ
Долгоживущий радионуклид 36Cl образуется в элементах графитовых кладок независимо от особенностей и режимов эксплуатации УГР. Это обусловлено, в первую очередь, активацией примесей, которые не удаляются при изготовлении графита или сорбируются до его загрузки в активную зону реактора. В табл. 3 представлены основные ядерные реакции, по которым образуется радионуклид 36Cl. К основным ядерным реакциям, приводящим к накоплению радиоактивного хлора в графитовых РАО, относятся: 35Cl(n, γ)36Cl (сечение реакции σ = 43 барн); 39K(n, α)36Cl (σ = = 0.004 барн); 34S(n, β–)35Cl(n, γ)36Cl (σ = 0.34 барн). Первые две реакции являются прямыми, последняя – непрямая, период полураспада промежуточного радионуклида 35S равен 87 сут. Стоит заметить, что содержание изотопа 35Cl в естественной смеси составляет 34.97%, 39K – 93.26%, 34S – 4.21% (табл. 3).
ФОРМИРОВАНИЕ ПРИМЕСНОГО СОСТАВА ПРИ ИЗГОТОВЛЕНИИ ГРАФИТА
Рассмотрим процесс производства реакторного графита более подробно с целью определения содержания примесей (хлора, калия, серы) и глубины загрязнения графитовых конструкционных элементов.
Изготовление российского реакторного графита (марки ГР-220, ГР-280, ЭГП-6, ГРП-2, ГР-1 и др.) и европейского/американского (марки TSGBF, TSX, P3AN, PGA, H-327, H-451, IG-11, P3JHA2N и др.) базируется на использовании нефтяных коксов различной микроструктуры, которые являются наполнителем, и каменноугольных пеков, служащими связующим. Вместо каменноугольного пека или вещества для пропитки графитового материала используют также синтетические фурановые смолы, которые получают методом Пааля−Кнорра путем циклизации 1,4-дикарбонильных соединений в присутствии катализаторов P2O5 и ZnCl2. Несмотря на очистку связующего, в нем присутствует до 0.6% серы.
Основными технологическими этапами производства искусственного ядерного графита являются: измельчение и дробление нефтяного кокса; термическое прокаливание кокса; размол и фракционирование; подготовка связующего; дозирование и смешение кокса со связующими веществами; формование необожженных заготовок; высокотемпературный обжиг; графитация; создание конструкционных элементов УГР. Практически на каждом этапе изготовления происходит накопление различных микропримесей, которые активируются при эксплуатации графита в ядерном реакторе.
Формирование структуры и свойств углеграфитовых материалов происходит в процессе термического прокаливания кокса. В Европе и США этот процесс проводят при температуре ≈1300°C [11], в России (ранее в СССР) нефтяной кокс обрабатывают при диапазоне температур 1100–1300°C без доступа воздуха [12, 13]. Повышение температуры прокаливания с одной стороны повышает упорядоченность структуры двухмерных кристаллов, с другой – увеличивает адсорбционную способность коксов. Это приводит к накоплению микропримесей в материале после извлечения из печи, а также в процессе формования необожженных заготовок. Средняя концентрация калия в необожженных заготовках перед процессом высокотемпературной очистки составляет ≈6.08 мкг/г [14].
Наибольшее количество микропримесей в материале накапливается непосредственно при графитации, а также после завершения процесса при извлечении графита из электрических печей сопротивления [15]. Известно, что в печи пространство между заготовками заполняют пересыпкой, которая состоит из литейного кокса, содержащего 0.45–0.50 мас. % серы [16]. В процессе графитации атомы углерода, имеющие на границе обрыва свободные связи, способны присоединять различные элементы (в том числе Cl). Некоторые атомы способны замещать атомы углерода в узлах кристаллической решетки. Отдельные молекулы могут внедряться между слоями графита, образуя хлориды редкоземельных и переходных металлов. Молекулы хлора способны образовывать ковалентную связь с атомами углерода, калий может находиться в графите в виде твердого раствора замещения, а сера – в свободном состоянии.
Удаление микропримесей после графитации, как правило, проводят путем выдержки полученных графитовых образцов в газовой среде или в вакууме при температуре 2500–3000°C [18]. Очистка в газовой среде характерна для отечественного марок графита. В качестве газа используют хлор и фтор или соединения их содержащие. Некоторый графит очищают с помощью фреона-12 (дифтордихлорметана, CCl2F2), гексафторида серы (SF6) и фреона-10 (тетрахлорметана, CCl4) [19]. Таким образом, очистка графитовых заготовок приводит, с одной стороны, к удалению большей части микропримесей, а, с другой стороны, к накоплению хлор- и серосодержащих соединений.
Обобщенные данные по содержанию микропримесей, приводящих к образованию радионуклида 36Cl, в необлученных графитовых элементах представлены в табл. 4.
Как видно из табл. 4, содержание микропримесей, приводящих к образованию радионуклида 36Cl, отличается для различных марок реакторного графита. По некоторым данным разброс превышает 100 раз.
Так, наиболее загрязненным является графит, производимый в США, а наиболее чистым – в Великобритании и России. Это объясняется тем, что американский реакторный графит исторически был произведен первым, и технология его очистки еще не была отработана. Французский графит (P3AN, 3JHA2N) имеет невысокую загрязненность, что объясняется использованием специализированных химически активных газов в процессе его очистки при производстве.
ОПРЕДЕЛЕНИЕ ФОРМЫ НАХОЖДЕНИЯ 36Cl
Химическая форма радионуклида 36Cl в структуре графитовых РАО будет зависеть от канала образования. Все источники образования данного радионуклида можно условно разделить на две группы: источники, накапливающиеся непосредственно в процессе производства ядерного графита и после (вплоть до момента выгрузки облученного графита из реактора). В процессе производства графита образование и накопление микропримесей происходит при подготовке кокса и пека, а также в процессе высокотемпературной очистки и графитации. После изготовления графита может происходить адсорбция различных хлорсодержащих и серосодержащих соединений, находящихся в окружающей среде, на поверхности графита (например, HCl, HOCl, NaCl, оксихлориды, SO2, H2S, (CH3)2S, ${\text{SO}}_{{\text{4}}}^{{{\text{2}} - }}$). Также могут адсорбироваться газообразные хлориды, находящиеся в продувочном газе вследствие неполной его очистки, при эксплуатации ядерного реактора. Для зарубежных графитовых элементов характерна их транспортировка до места эксплуатации в таре из поливинилхлорида ([−CH2−CHCl−]n), что также приводит к загрязнению поверхности необлученного графита.
СОСТАВ ПРОДУКТОВ РЕАКЦИИ ПРИ ГРАФИТАЦИИ И В ПРОЦЕССЕ УДАЛЕНИЯ МИКРОПРИМЕСЕЙ
С целью определения возможных химических соединений радионуклида 36Cl нами проводилось термодинамическое моделирование равновесного состава продуктов реакции при графитации и в процессе удаления микропримесей. Критерием достижения системой состояния термодинамического равновесия является достижение максимума ее характеристической функции. Для изолированной системы такой функцией является энтропия, а максимальное значение энтропии – критерий достижения равновесного состояния [23, 24]. Для моделирования использовалась специализированная программа ТЕРРА [25]. Состав фаз и характеристики равновесного состава моделировались с использованием справочной базы данных [26]. Исходное содержание примесей в необлученном графите выбиралось согласно данным, представленным в работе [20]. Расчет проводили в системе графит–газ, где в качестве последнего рассматривались Cl2, CCl2F2, SF6 и CCl4. Результаты расчета представлены на рис. 2.
Рис. 2.
Термодинамическое моделирование равновесного состава продуктов реакции при очистке необлученного графита различными газами: а − Сl2, б − CCl2F2, в − SF6, г − CCl4.
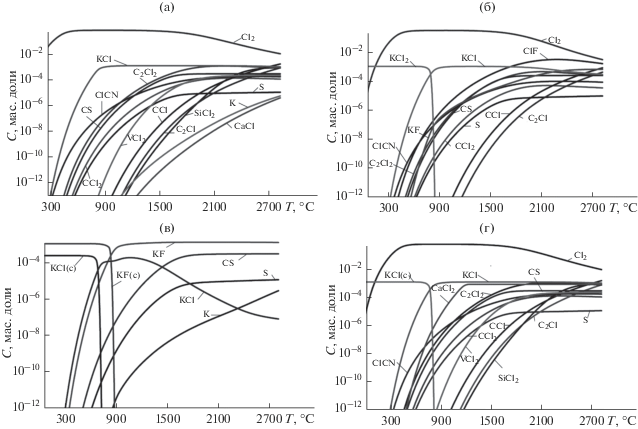
Из рис. 2 видно, что при использовании хлорсодержащих газов (рис. 2а, 2б, 2г) при очистке графитовых заготовок происходит накопление газообразного Cl2, который проникает внутрь графита через развитую систему пор и адсорбируется на поверхности. При использовании газов Cl2 и CCl4 большая часть продуктов реакции, которые в процессе облучения способны образовывать радионуклид 36Cl, представлены в виде хлоридов: C2Cl2, CCl, CCl2, ClCN, KCl, SiCl2, VCl2, CaCl2. В меньшей степени образуются соединения серы, которые, как правило, представлены в виде сероуглерода. При использовании в качестве очищающего газа дифтордихлорметана происходит одновременно два процесса: хлорирование и фторирование поверхности графита. Практически все имеющиеся примеси взаимодействуют с фтором и удаляются с очищаемой поверхности. Однако возможно образование соединений ClF и KF, которые в дальнейшем подвергаются облучению нейтронами.
Наиболее полная очистка графитовых заготовок происходит при использовании в качестве теплоносителя гексафторида серы SF6. Это связано с тем, что фтор взаимодействуют со всеми микропримесями и образует газообразные продукты реакции, а отсутствие хлора исключает появление хлоридов в структуре графита. При этом количество образующихся сульфатов и сульфидов незначительно. К основным соединениям, находящимся в необлученном графите после обработки гексафторидом серы можно отнести: CS2, K, KF, KCl.
Полученные результаты расчета справедливы только для процесса графитации и очистки. При извлечении заготовки из печей и камер может происходить взаимодействие соединений, находящихся в графитовой заготовке, с воздухом, атмосферными примесями и парами воды.
СОСТАВ ПРОДУКТОВ РЕАКЦИИ ПРИ ИЗВЛЕЧЕНИИ ЗАГОТОВОК ИЗ ПЕЧЕЙ И КАМЕР
Рассмотрим основные химические реакции, описывающие такие процессы:
(2)
${\text{HNCO}} + {{{\text{H}}}_{2}}{\text{O}} \to {\text{N}}{{{\text{H}}}_{3}} + {\text{C}}{{{\text{O}}}_{2}},$(3)
${\text{ClCN}} + {\text{N}}{{{\text{H}}}_{3}} \to {{{\text{H}}}_{2}}{\text{N - CN}} + {\text{HCl}},$(4)
${\text{4ClF}} + 2{{{\text{H}}}_{2}}{\text{O}} \to 2{\text{C}}{{{\text{l}}}_{2}} + {{{\text{O}}}_{2}} + 4{\text{HF}},$(6)
${\text{C}}{{{\text{S}}}_{2}} + 3{{{\text{O}}}_{2}} \to {\text{C}}{{{\text{O}}}_{2}} + 2{\text{S}}{{{\text{O}}}_{2}},$(7)
${\text{C}}{{{\text{S}}}_{2}} + 2{{{\text{H}}}_{2}}{\text{O}} \to {\text{C}}{{{\text{O}}}_{2}} + 2{{{\text{H}}}_{2}}{\text{S}}{\text{.}}$Реакции (1)–(2) отражают процесс гидролиза хлорциана парами воды с образованием изоциановой кислоты, которая, в свою очередь, гидролизуется до образования аммиака и диоксида углерода. Образующийся аммиак также может взаимодействовать с ClCN, в результате чего образуется HCl. Фторид хлора, взаимодействуя с парами воды и водородом, может образовывать молекулярный хлор Cl2 по реакции (4) и хлороводород HCl по реакции (5). Сероуглерод CS2 способен окисляться на воздухе до SO2 по реакции (6). При взаимодействии CS2 с водой происходит образование сероводорода H2S по реакции (7). Однако последняя реакция протекает при температуре выше 150°C, что достигается лишь при эксплуатации ядерного реактора и в случае разгерметизации технологического канала [27].
ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ ХИМИЧЕСКОЙ ФОРМЫ НАХОЖДЕНИЯ РАДИОНУКЛИДА 36Cl В ГРАФИТЕ
В работе [28] представлены результаты определения химической формы нахождения радионуклида 36Cl методом рентгеновской фотоэлектронной спектроскопии поверхности облученного ядерного графита. Показано, что хлор имеет ковалентную связь с углеродом на исследуемой поверхности. При этом происходит sp2 и sp3-гибридизация атомов углерода. Вероятнее всего, что рассматриваемый радионуклид находится в молекуле Cl2 или связан с углеродом C–Cl. С другой стороны, масс-спектрометрические исследования показывают наличие соединения HCl [29]. Исходя из этого, возможными реакциями между углеродом и хлором являются [30]:
− реакция замещения водорода хлором:
(8)
$--{\text{C}}{\kern 1pt} - {\kern 1pt} {\text{H}} + {\text{C}}{{{\text{l}}}_{2}} \to --{\text{C}}{\kern 1pt} --{\kern 1pt} {\text{Cl}} + {\text{HCl}};$– реакция присоединения к сопряженным двойным связям:
(9)
${\text{C}}{\kern 1pt} = {\kern 1pt} {\text{C}} + {\text{C}}{{{\text{l}}}_{2}} = {\text{ClC}}{\kern 1pt} --{\kern 1pt} {\text{CCl,}}$– реакция дегидрирования:
(10)
${\text{HC}}{\kern 1pt} --{\kern 1pt} {\text{CH}} + {\text{C}}{{{\text{l}}}_{2}} = {\text{C}}{\kern 1pt} = {\kern 1pt} {\text{C}} + 2{\text{HCl}}.$В работе [31] показано, что реакция (8) является многостадийной и включает в себя хемосорбцию газообразного Cl2, диффузию соединений внутрь поверхности графита (в том числе поверхности пор) и образование HCl. При этом реакция замещения водорода хлором необратима, а сам хлор не удаляется при нагревании или химической очистке [32]. В процессе обработки графита при температуре 500°C происходит необратимый процесс образования ковалентной связи С–Cl, в результате чего хлор занимает положение между слоями графита.
Кроме того, экспериментально определено, что радионуклид 36Cl (в меньшей степени) может находиться в соединениях: NaClO4, NaClO3, NaClO2, NaCl, [–CH2–CHCl–]n, HClO, CH3Cl, ClONO2, HClO, HClO2, HClO3, ClO, ClO2, ClO3 [33, 34].
ЗАКЛЮЧЕНИЕ
Рассмотренные каналы образования радионуклида 36Cl объясняют его локализацию в облученном графите. Это проявляется в отсутствии закономерностей его распределения как в объемах графита с характерными размерами не менее ≈1–2 мм (толщина образца), так и в объемах с характерными размерами в десятки сантиметров (размер блоков). Возможно, это одно из объяснений эффекта “самородка” (Nugget effect).
Представленные результаты экспериментов качественно согласуются с результатами термодинамического моделирования равновесного состава. Таким образом, наибольшее количество примесей, из которых образуется 36Cl при эксплуатации графита в ядерном реакторе, накапливается в процессе графитации, очистки в среде химически активных газов и при транспортировке готовых конструкционных элементов. При этом наиболее вероятными соединениями являются, в которых может находиться рассматриваемый радионуклид HCl, KCl и, в меньшей степени: NaClO4, NaClO3, NaClO2, NaCl, [–CH2–CHCl–]n, HClO, CH3Cl, ClONO2, HClO, HClO2, HClO3, ClO, ClO2, ClO3.
Список литературы
Pavliuk A.O., Kotlyarevskiy S.G., Bespala E.V. et al. // J. Environ. Radioactiv. 2018. V. 184. P. 22. https://doi.org/10.1016/j.jenvrad.2018.01.005
Poncet B., Petit L. // J. Radioanal. Nucl. Ch. 2013. V. 298. № 2. P. 941. https://doi.org/10.1007/s10967-013-2519-6
Lansdell T., Newland M. Magnox reactor graphite characterisation stage 2–final active analysis stage, Babcock Report TSG. 2012. V. 11(0801).
Бушуев А.В., Кожин А.Ф., Петрова Е.В. // Атомная энергия. 2006. Т. 101. Вып. 5. С. 359.
Hou X., Ostergaard L.F., Nielsen S.P. // Anal. Chem. 2007. V. 79. P. 3126. https://doi.org/10.1021/ac070100o
Narkunas E., Smaizys A., Poskas P. et al. // Prog. Nucl. Energy. 2016. V. 91. P. 265.
Black G. Irradiated Graphite Waste: Analysis and Modeling of Radionuclide Production with a View to Long Term Disposal. Manchester: The University of Manchester, 2014. P. 198.
TECDOC-1647. “Progress in Radioactive Graphite Waste Management”. IAEA, Vienna. 2010. URL: https://www-pub.iaea.org/books/iaeabooks/8421/ Progress-in-Radioactive-Graphite-Waste-Management.
Technical Report 1013091. Graphite Decommissioning: Options for Graphite Treatment, Recycling or Disposal, Including a Discussion of Safety-Related Issues. EPRI. 2006.
Бушуев А.В. и др. Радиоактивный реакторный графит: Монография. М.: НИЯУ МИФИ, 2015. 148 с.
Ragan S., Marsh H. // J. Mater. Sci. 1983. V. 18. № 11. P. 3161. https://doi.org/10.1007/BF00544139
Валявин Г.Г., Запорин В.П., Габбасов Р.Г. и др. // Переработка нефти и газа. 2011. № 8. С. 44.
Красюков А.Ф. Нефтяной кокс. Москва: Гостоптехиздат, 1963. 163 с.
Zhao H., Liang T., Zhang J., Li Z. et al. // Rare Metals. 2006. V. 25. P. 347. https://doi.org/10.1016/S1001-0521(07)60103-X
Вяткин С.Е. и др. Ядерный графит. М.: Атомиздат, 1967. 279 с.
Справочник коксохимика: В 6 т. / Под ред. инж. Шелкова А.К. М.: Металлургия, 1966. 391 с.
Авдеенко М.А., Багров Г.Н. // Конструкционные углеграфитовые материалы. 1964. № 1. С. 34.
Zhao H., Liang T., Zhang J. et al. // Nucl. Eng. Des. 2006. V. 236. P. 643. https://doi.org/10.1016/j.nucengdes.2005.10.023
Nightingale R.E. Nuclear Graphite. New York-London: Academic Press, 1962. 562 p.
Black G., Jones A.N., McDermott L. et al. // Materials Research Society Symposium Proceedings. 2012. V. 1475. P. 107. https://doi.org/10.1557/opl.2012.562
Comte J., Guy C., Tornabene A.L. et al. // J. Radioanal. Nucl. Ch. 2017. V. 314. № 2. P. 1245. https://doi.org/10.1007/s10967-017-5495-4
Parry S., Cox J. Graphite Characterisation (Stage 1-Define Characterisation Programme). Tech. Rep: UKAEA, 2010.
Трусов Б.Г. // III Междунар. симп. по теор. и прикл. плазмохимии. Сб. матер. Т. I. Иваново, 16–21 сентября. 2002. С. 217.
Белов Г.В., Трусов Б.Г. Термодинамическое моделирование химически реагирующих систем. М.: МГТУ имени Н.Э. Баумана, 2013. 96 с.
Пупышев А.А. Термодинамическое моделирование термохимических процессов. Екатеринбург: УГТУ-УПИ, 2007. 85 с.
Гурвич Л.В., Вейц И.В., Медведев В.А. Термодинамические свойства индивидуальных веществ: справочное издание в 4-х томах. М.: Наука, 1978–1982. 328 с.
Pavliuk A.O., Zagummenov V.S., Kotlyarevskiy S.G. et al. // Therm. Eng. 2018. V. 65. № 1. P. 51.
Vaudey C.E., Toulhoat N., Moncoffre N., Bérerd N., Favergeon L., Pijolat M., Raimbault L., Sainsot P., Rouzaud J.N. Thermal Behaviour of Chlorine in Nuclear Graphite; Presented at 9th International Nuclear Graphite Specialists Meeting, Egmond zur Zee, The Netherlands. September 2008 (Available at IAEA International Knowledge Base on Nuclear Graphite, www.iaea.org/NuclearPower/Graphite).
Vaudey C.E. Effets de la Température et de la Corrosion Radiolytique sur le Comportement du Chlore dans le Graphite Nucléaire: Conséquences pour le Stockage des Graphites Irradiés des Réacteurs UNGG. Lyon: Cote B.I.U., 2010. 186 p.
Gonzales J., Ruiz M. del C., Bohé A. Et al. // Carbon. 1999. V. 37. P. 1979. https://doi.org/10.1016/S0008-6223(99)00063-9
Pasquevich D. // Thermochim. Acta. 1990. V. 167. P. 91. https://doi.org/10.1016/0040-6031(90)80468-E
Tobias H., Soffer A. // Carbon. 1985. V. 23. P. 281. https://doi.org/10.1016/0008-6223(85)90113-7
Papirer E., Lacroix R., Donnet J.B. et al. // Carbon. 1995. V. 33. P. 63. https://doi.org/10.1016/0008-6223(94)00111-C
Soloman S. Progress Towards a Quantitative Understanding of Antarctic Ozone Depletion // Nature. 1990. V. 347. P. 347. https://doi.org/10.1038/347347a0
Дополнительные материалы отсутствуют.
Инструменты
Поверхность. Рентгеновские, синхротронные и нейтронные исследования


