Высокомолекулярные соединения (серия Б), 2020, T. 62, № 5, стр. 364-371
ПОЛИЭЛЕКТРОЛИТНЫЕ ГЕЛИ ДЛЯ СТАБИЛИЗАЦИИ ПЕСЧАНОЙ ПОЧВЫ ПРОТИВ ВЕТРОВОЙ ЭРОЗИИ
И. Г. Панова a, *, Л. О. Ильясов a, Д. Д. Хайдапова b, K. Ogawa c, Y. Adachi c, А. А. Ярославов a
a Московский государственный университет имени М.В. Ломоносова. Химический факультет
119991 Ленинские горы, Москва, Россия
b Московский государственный университет имени М.В. Ломоносова. Факультет почвоведения
119991 Ленинские горы, Москва, Россия
c Faculty of Life and Environmental Sciences, University of Tsukuba
305-8572 Ibaraki, 1-1-1, Tennodai, Tsukuba, Japan
* E-mail: igpan@mail.ru
Поступила в редакцию 06.04.2020
После доработки 21.04.2020
Принята к публикации 06.05.2020
Аннотация
Представлены интерполиэлектролитные комплексы линейного катионного полимера полидиаллилдиметиламмоний хлорида и частиц анионного микрогеля с карбоксильными группами в буферном растворе с рН 6. Дисперсии микрогеля и его комплексов – отрицательно заряженного с 3-кратным мольным избытком анионных групп микрогеля и положительно заряженного с 3-кратным мольным избытком катионных групп поликатиона – сохраняют агрегативную устойчивость в течение полугода. При нанесении 1 мас. % дисперсий микрогеля и комплекса на поверхность почвы с высоким содержанием песка формируются полимерно-почвенные покрытия с механической прочностью от 19 до 61 кг/м2 в зависимости от состава дисперсии. Эти показатели существенно превышают таковые для покрытий, полученных путем нанесения на поверхность почвы 1 мас.% раствора линейного анионного полимера, полиакриловой кислоты. Покрытия с участием микрогеля и его комплексов сохраняют устойчивость при скорости воздушного потока 190 км/ч.
ВВЕДЕНИЕ
Растущее использование полимеров для защиты почв от деградации и эрозии [1–3], сохранения и улучшения физических свойств пахотных земель [4–6], борьбы с опустыниванием [7, 8], рекультивации нарушенных и загрязненных почв [9–11] и удерживания влаги в почве [12–14] стимулировало появление многочисленных работ, посвященных этим проблемам. Было показано, в частности, что водорастворимые анионные полимеры линейного строения – гидролизованный полиакрилонитрил, лигносульфонат, полисахариды и их производные – действуют как эффективные стабилизаторы почв различного состава и происхождения [4, 15, 16]. Обработка такими полимерами песчаных и глинистых почв приводит к формированию полимерно-почвенных покрытий, которые эффективно защищают почвы от ветровой и водной эрозии [17, 18]. Противоэрозионная устойчивость таких покрытий объясняется множественными контактами полимеров с комплементарными областями на поверхности минеральных и органических частиц почвы, что влечет закрепление структуры почвы, повышение сопротивления частиц отрыву при механических нагрузках и их переносу в потоке воздуха и воды [19]. Однако полученные покрытия чувствительны к искусственному орошению и природным осадкам. При поступлении воды полимер перемещается вглубь слоя почвы и ее поверхность снова начинает подвергаться эрозионному разрушению [20, 21].
Дополнительный стабилизирующий эффект может быть достигнут за счет связывания анионного полимера в электростатический комплекс с катионным полимером. Полученный интерполиэлектролитный комплекс (ИПЭК) представляет собой блок-сополимер, в составе которого есть гидрофобные и гидрофильные участки; первые представлены блоками с взаимно скомпенсированными зарядами обоих полимеров, вторые свободными участками полимерных цепей [17]. Такое устройство поликомплексов повышает прочность полимерно-почвенных покрытий [20–23].
Ковалентно сшитые гидрофильные полимеры в современных агрохимических технологиях рассматриваются, как правило, в качестве водоудерживающих агентов [24]. Сетчатая структура и наличие ионных групп определяют способность сшитых полимеров поглощать значительное количество воды, бόльшая часть которой оказывается доступной для растений [12]. Набухшие в воде полимеры (гидрогели), чаще всего содержащие анионные группы, не проявляют фитотоксичности и безвредны для почвенных организмов [25, 26].
Между тем гидрогели представляют интерес и с точки зрения их применения в качестве стабилизаторов концентрированных дисперсных систем, к числу которых относятся почвы и грунты. Ранее было показано, что эффективность линейных полианионных стабилизаторов повышается с увеличением молекулярной массы полимера [27, 28]. Переход от линейного полимера к сетчатому аналогу сопровождается взрывным ростом молекулярной массы, что может положительным образом сказаться на эффективности стабилизирующего действия полимерных гидрогелей. Модификация анионного гидрогеля линейным катионным полимером может дополнительно усилить прочность полимерно-почвенных корок. Частицы гидрогеля могут выступать как “депо” для биологически активных веществ [29] и(или) адсорбента для связывания токсичных катионов тяжелых металлов [30]. Такой набор свойств делает рецептуры на основе гидрогелей перспективными кандидатами для подавления эрозионных процессов в почве и создания условий для развития растений, особенно на территориях с недостаточным содержанием влаги.
В настоящей работе описано получение ИПЭК из микроразмерных частиц анионного гидрогеля и линейного катионного полимера, агрегативная устойчивость ИПЭК в водно-солевом растворе и механическая прочность корок, полученных после нанесения ИПЭК на поверхность почвы с высоким содержанием песка (“песчаной почвы”). Подобные почвы преобладают в засушливых и полузасушливых районах мира. Особое внимание уделено устойчивости полимерно-почвенных корок в воздушно-сухом потоке воздуха; этот эксперимент моделирует сопротивляемость защитных корок воздушной эрозии. Полученные результаты сравниваются с данными по стабильности защитных покрытий, сформированных линейным анионным полимером.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Использовали катионный полимер полидиаллилдиметиламмоний хлорид (ПДАДМАХ) с Mw = = (200–350) × 103 и анионный полимер полиакриловую кислоту (ПАК) c Mw = 100 × 103 производства “Sigma-Aldrich” без дополнительной очистки.
Сетчатый сополимер синтезировали эмульсионной полимеризацией смеси N-изопропилакриламида (69 мас. %), акриловой кислоты (30 мас. %) и сшивателя N,N-метиленбисакриламида (1 мас. %) в водной среде [31]. Полученную водную суспензию частиц анионного микрогеля (АМГ) очищали методами кислотного диализа и ионообменной хроматографии с помощью колонок, заполненных ионообменными смолами “Amberlite IRA-400” (CL) и “Amberlite IR-120” (NA) (“Sigma-Aldrich”), и лиофильно сушили.
Средняя молекулярная масса сополимера, определенная методом статического светорассеяния на спектрометре (гониометре) “Photocor Complex” (“Photocor”, Россия), составила 81 × 106. Содержание карбоксильных групп в сополимере (2.85 × 10–3 моль/г) измеряли методом потенциометрического титрования.
Концентрация полидиаллилдиметиламмоний хлорида представлена в виде мольной концентрации катионных аминогрупп, [ПДАДМАХ], концентрация анионного микрогеля – в виде концентрации карбоксильных групп, [АМГ].
Объем частицы анионного микрогеля, равновесно набухшей в водном растворе, полагали равным Vн = 1/6π$d_{{\text{г}}}^{3}$ (dг – усредненный гидродинамический диаметр частицы, измеренный методом динамического светорассеяния). Объем высушенной частицы микрогеля оценивали как Vв = = 1/6π$d_{{\text{м}}}^{3}$, где dм – усредненный диаметр частицы, измеренный по микрофотографиям, полученным с помощью просвечивающего электронного микроскопа “LEO 912 AB Omega TEM” (“Karl Zeiss”, Германия). Образцы для электронной микроскопии готовили, нанося 0.002%-ную дисперсию анионного микрогеля в бидистиллированной воде на медную сетку с последующим высушиванием на воздухе при комнатной температуре в течение получаса. Контрастирования достигали добавлением раствора фосфорно-вольфрамовой кислоты. Коэффициент набухания анионного микрогеля рассчитывали по формуле, предложенной в работе [32]:
(1)
$\alpha = {{V}_{{\text{н}}}}{\text{/}}{{V}_{{\text{в}}}} = d_{{\text{г}}}^{3}{\text{/}}d_{{\text{м}}}^{3}$Интерполиэлектролитные комплексы готовили путем смешения раствора или дисперсии анионного полимера (ПАК или АМГ) и раствора катионного полимера (ПДАДМАХ). Состав ИПЭК характеризовали мольным соотношением ионных групп полианиона и поликатиона Z = [COO–]/[N+]. Гидродинамический диаметр и электрофоретическую подвижность μ частиц ИПЭК измеряли методами динамического светорассеяния и лазерного микроэлектрофореза на спектрометре “Brookhaven ZetaPlus” (США).
Образец почвы брали в верхнем десятисантиметровом слое на экспериментальном поле около деревни Ерохино в Псковской области РФ с координатами: 56.129474 с. ш. и 31.372435 в. д. Анализ почвы показал решающий вклад мелкого песка со средним размером частиц от 50 до 1000 мкм (85.7 мас. %), много меньшее содержание “пылевидного песка” с размером частиц от 0.01 до 50.0 мкм (12 мас. %) и тонкодисперсных частиц физической глины (2.2 мас. %) и незначительную долю органического вещества (1.1 мас. %). Гранулометрический состав почвы и содержание органического вещества определяли по ранее опубликованным стандартным методикам [33, 34].
Образцы почвы с защитным слоем на поверхности готовили двумя способами. Согласно первому, в пластиковый контейнер помещали 60 г почвы, высота слоя грунта составляла 5 см, площадь поверхности 8 см2. На поверхность равномерно наносили 3.6 мл 1 мас. % водный раствор (суспензию) полимера или ИПЭК (полимерную рецептуру) при норме расхода 2 л/м2. Образцы сушили до постоянной массы на воздухе и использовали для измерения прочностных характеристик полимерно-почвенных корок пенетрационным методом (погружением конуса) с помощью конического пластометра Ребиндера [35]. Следуя второму способу, в чашку Петри вносили 100 г почвы глубиной 1 см. На почву равномерно наносили 17.2 мл полимерной рецептуры при норме расхода 2 л/м2. В контрольных экспериментах на поверхность почвы наносили 17.2 мл дистиллированной воды. Образцы сушили до постоянной массы на воздухе и использовали для визуализации полимерно-почвенных корок и оценки их сопротивляемости воздушной эрозии.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Набухание сетчатого полимера в водном растворе
10 мг сетчатого сополимера помещали в стеклянный стакан с 100 мл 0.01 моль/л фосфатного буферного раствора с рН 6. Смесь оставляли при комнатной температуре на трое суток, что приводило к набуханию сополимера и появлению в растворе частиц анионного микрогеля. Кривая распределения частиц анионного микрогеля по размеру, полученная методом динамического светорассеяния, представлена на рис. 1а. Наличие одного узкого максимума свидетельствовало о монодисперсности образца. Средний гидродинамический диаметр частиц анионного микрогеля dг был равен 440 нм и не менялся при последующем увеличении времени выдерживания сетчатого полимера в буферном растворе. Следовательно, выдерживание полимера в буферном растворе в течение двух суток обеспечивало получение частиц максимально набухшего анионного микрогеля.
Рис. 1.
Распределение по размерам частиц АМГ в фосфатном буфере с рН 6 по данным динамического светорассеяния (а) и микрофотография частиц АМГ, полученная методом просвечивающей электронной микроскопии (б).
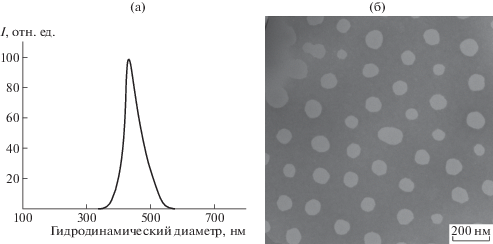
На рис. 1б представлена микрофотография того же образца анионного микрогеля, выполненная с помощью просвечивающей электронной микроскопии после высушивания образца на воздухе в течение получаса. Видно, что присутствует один тип преимущественно сферических частиц. Их диаметр dм, рассчитанный по данным пяти микрофотографий с общим количеством частиц ∼150, составил 71 нм. Сравнение данных динамического светорассеяния и электронной микроскопии позволило оценить степень набухания частиц анионного микрогеля в буферном растворе с рН 6: α = $d_{{\text{г}}}^{3}$/$d_{{\text{м}}}^{3}$ = 150.
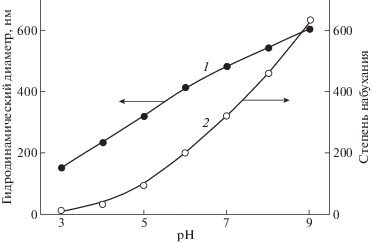
Описанный алгоритм был использован для оценки размера частиц предельно набухшего анионного микрогеля и степени набухания его в буферных растворах с другими значениями рН. Результаты, представленные на рис. 2, указывают на увеличение размера частиц анионного микрогеля по мере увеличения количества диссоциированных карбоксильных групп. Наименьший размер микрогеля был зарегистрирован при рН 3 (150 нм), наибольший при рН 9 (600 нм) с соответствующим возрастанием степени набухания с 5 до 450 при переходе от рН 3 к рН 9. Такое поведение характерно для микрогелей с ионными группами, оно отражает набухание гидрогелевых частиц по мере увеличения суммарного заряда полимерной сетки [36].
Взаимодействие анионного микрогеля с линейным катионным полимером
За формированием ИПЭК анионного микрогеля с катионным ПДАДМАХ следили, регистрируя поверхностный заряд частиц в системе. Эксперименты проводили в фосфатном буфере с рН 6. В этих условиях гидродинамический диаметр частиц анионного микрогеля был равен 440 нм при электрофоретической подвижности μ = –3.4 × 10–8 м2/Вс. Добавление раствора ПДАДМАХ к раствору анионного микрогеля приводило к нейтрализации заряда микрогелевых частиц, электрофоретическая подвижность μ = 0 была достигнута при соотношении Z = = [ПДАДМАХ]/[АМГ] = 0.76 (рис. 3, кривая 1). Сравнение данной величины со степенью диссоциации карбоксильных групп акриловых полимеров при pH 6 (∼0.5 [37]) позволило сделать вывод о том, что все ионизованные при рН 6 карбоксильные группы анионного микрогеля участвовали в образовании ионных связей с катионными группами ПДАДМАХ. Дополнительные ионные связи появлялись благодаря кооперативному вытеснению протонов из карбоксильных групп анионного микрогеля катионными группами ПДАДМАХ; подобные реакции с участием полиэлектролитов описаны в литературе [38]. Оставшаяся доля карбоксильных групп анионного микрогеля (0.24) не образовывала ионных связей с ПДАДМАХ. Таким образом, соотношение Z = 0.76 описывает состав электронейтрального (насыщенного) поликомплекса ПДАДМАХ/АМГ при pH 6. Последующее увеличение концентрации поликатиона придавало частицам ИПЭК положительный заряд с максимальным значением электрофоретической подвижности μ = 2 × 10–8 м2/Вс.
Рис. 3.
Зависимость электрофоретической подвижности (1) и гидродинамического диаметра (2) частиц поликомплекса ПДАДМАХ–АМГ от отношения Z. [АМГ] = 2.85 × 10-4 моль/л; 0.01 моль/л фосфатный буфер, pH 6.
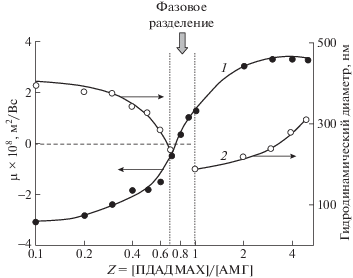
Размер частиц ИПЭК контролировали с помощью динамического светорассеяния. В исходном растворе анионного микрогеля присутствовали частицы с диаметром 400 нм. Добавление первых порций ПДАДМАХ к раствору анионного микрогеля сопровождалось уменьшением диаметра частиц (рис. 3, кривая 2). Так продолжалось до тех пор, пока отношение Z не достигало 0.7 и размер частиц комплекса не принимал своего минимального значения 250 нм. В интервале 0.7 < Z < 1.0 в системе была зарегистрирована опалесценция, что указывало на потерю растворимости поликомплекса при таких соотношениях компонентов. Частицы поликомплекса снова приобретали растворимость при Z ≥ 1 и увеличивали свой размер по мере повышения концентрации поликатиона вплоть до 300 нм при Z = 4.5.
Сравнение результатов электрофоретических экспериментов и данных светорассеяния позволяет нарисовать следующую картину процессов, развивающихся в системе ПДАДМАХ–АМГ. Добавление ПДАДМАХ к раствору анионного микрогеля приводит к его связыванию с частицами микрогеля, которое начинается с периферии частиц анионного микрогеля и развивается по мере продвижения макромолекул ПДАДМАХ внутрь анионных частиц. Это позволяет вовлечь в электростатическое взаимодействие максимальное количество карбоксильных групп микрогеля. Такой механизм описывает взаимодействие линейных катионных макромолекул с макроскопическими гидрогелями [38, 39]. Транспорт катионных макромолекул внутрь микрогеля сопровождается нейтрализацией зарядов карбоксильных групп и коллапсом микрогелевых частиц (рис. 3, части кривых 1 и 2 слева). При заряде частиц комплекса близком к нулю, они теряют стабильность и агрегируют, что выражается в помутнении раствора (появлении опалесценции). Связывание ПДАДМАХ сверх необходимого для достижения электрофоретической подвижности μ = 0 приводит к появлению положительного заряда на поверхности частиц микрогеля, что препятствует агрегации частиц (рис. 3, части кривых 1 и 2 справа). При этом размер частиц комплекса увеличивается за счет появления на поверхности микрогелевых частиц монослоя адсорбированных макромолекул ПДАДМАХ.
Характеристика 1 мас. % водных растворов полимерных рецептур
Для стабилизации почвы (грунта) водные растворы полимеров обычно используют в виде 1 мас. % рецептур [17]. Следуя данному протоколу, были подготовлены три рецептуры, представлявшие собой раствор анионного микрогеля: раствор комплекса ПДАДМАХ–АМГ с Z = 0.3 (ИПЭК(–)) и раствор комплекса ПДАДМАХ–АМГ с Z = 3.0 (ИПЭК(+)). Все растворы готовили в 0.01 моль/л фосфатном буфере с рН 6. В таблице 1 приведены характеристики рецептур, включающие электрофоретическую подвижность, размер частиц и вязкость растворов.
Частицы исходного анионного микрогеля характеризовались высоким отрицательным зарядом с электрофоретической подвижностью μ = = –3.4 × 10–8 м2/Вс, который обеспечивал стабильность раствора, по крайней мере, в течение полугода. Гидродинамический диаметр частиц анионного микрогеля составлял 440 нм, что соответствовало степени набухания α = 150. Формирование ИПЭК с Z = 0.3 понижало электрофоретическую подвижность частиц до –2.7 × 10–8 м2/Вс, их размер до 360 нм, а степень набухания до 85. Более выраженными были изменения в свойствах ИПЭК с Z = 3.0. При избытке ПДАДМАХ получался положительно заряженный ИПЭК с электрофоретической подвижностью μ = 2.6 × 10–8 м2/Вс. Его образование сопровождалось резким коллапсом микрогелевых частиц, их размер падал до 170 нм, а степень набухания опускалась до 8. Вместе с тем формирование отрицательно заряженного и положительно заряженного ИПЭК не сказывалось на агрегативной стабильности рецептур: они сохраняли устойчивость в течение полугода.
Кинематическая вязкость рецептур на основе АМГ (табл. 1) важна для оценки возможности их практического применения в распылительных системах ирригации. Раствор исходного анионного микрогеля с концентрацией 1 мас. % характеризуется довольно высокой вязкостью (320 сСт), которая, однако, позволяет наносить его с помощью обычного бытового пульверизатора. Связывание анионного микрогеля с ПДАДМАХ в отрицательно заряженный ИПЭК с Z = 0.3 влечет резкое понижение вязкости раствора до 6.8 сСт, что, очевидно, вызвано заметной контракцией микрогелевых частиц в комплексе с поликатионом. Дополнительное поджатие частиц комплекса в избытке ПДАДМАХ приводит в случае ИПЭК с Z = 3.0 к еще бόльшему снижению вязкости раствора (до 1.8 сСт). Таким образом, связывая анионный микрогель с линейным катионным полимером можно влиять на размер частиц микрогеля и вязкость полимерной рецептуры.
Механические свойства почвы, обработанной полимерными рецептурами
На рис. 4 представлены фотографии образцов почвы после ее обработки водным буферным раствором с рН 6 (контроль) и полимерными рецептурами с последующей сушкой на воздухе. Обработка почвы водным буферным раствором не способствовала формированию прочного покрытия: почва высыпалась из чашки Петри после того, как ее перевели в вертикальное положение (рис. 4а). Напротив, обработка почвы растворами анионного микрогеля, ИПЭК(–) и ИПЭК(+) привела к появлению на поверхности защитных полимерно-почвенных корок, которые предотвращали высыпание почвы (рис. 4б–4г).
Три образца почвы с защитными полимерно-почвенными корками и необработанная почва (контроль) были протестированы на предмет устойчивости к действию потока воздуха, создаваемого вентилятором (феном). Поток воздуха направляли на образец под углом 30 град с расстояния 15 см, чашку Петри с образцом располагали горизонтально. Согласно паспорту прибора, максимальная скорость воздушного потока составляла 54 м/с. Воздух подавали в течение 10 мин, затем фен выключали на 10 мин и снова включали на 10 мин. Таким образом моделировалась устойчивость полимерно-почвенных корок к сильным и непродолжительным порывам ветра. Количество унесенной ветром почвы определяли, взвешивая чашку Петри с образцом до и после воздушной обработки.
В контрольном образце потоком воздуха было унесено 100% почвы. В образцах с защитными полимерно-почвенными корками потери массы не наблюдалось. Полученные результаты указывали на то, что обработка почвы микрогелевыми рецептурами резко повышала их устойчивость к действию воздушного потока (ветровой эрозии). Полимерно-почвенные корки на поверхности почвы обеспечивали ее стабильность при скорости воздушного потока 54 м/с или 190 км/ч, что существенно превышает скорость ураганного ветра (120 км/ч).
Прочность полимерно-почвенных корок оценивали пенетрационным методом с использованием конического пластометра Ребиндера. В работах [19, 40] было показано, что такая характеристика композиционных покрытий (пенетрационная прочность) хорошо отражает эффективность их использования в качестве экранов, защищающих почву от воздушной эрозии. Под мерой прочности понимали нагрузку, которая вызывала появление трещины на поверхности полимерно-почвенных корок. Во всех случаях на поверхность почвы наносили одинаковое количество рецептуры (3.6 мл), поддерживая одинаковой общую концентрацию полимера (полимеров) 1 мас. %. Результаты представлены в виде гистограммы на рис. 5.
Рис. 5.
Прочность полимерно-почвенного покрытия (ППК), полученного нанесением 1 мас. % полимерной рецептуры АМГ (1), ИПЭК(–) (2), ИПЭК(+) (3) и ПАК (4) в 0.01 моль/л фосфатном буфере с рН 6. Норма расхода рецептур 2 л/м2.
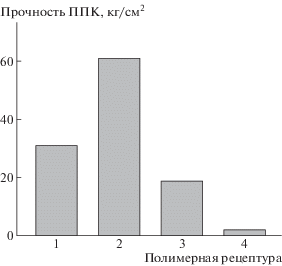
Прочность полимерно-почвенных корок из почвы и анионного микрогеля составила 31 ± 4 кг/cм2. Нанесение на почву отрицательно заряженного ИПЭК(–) повысило прочность корки до 61.0 ± ± 7.5 кг/cм2, в то время как нанесение положительно заряженного ИПЭК(+) понизило прочность корки до 19 ± 3 кг/cм2. Использование линейной полиакриловой кислоты привело к получению полимерно-почвенных корок с прочностью 2.3 ± ± 0.3 кг/cм2.
В литературе, посвященной использованию синтетических полимеров для структурирования почвы, отмечается прогрессивное повышение прочности защитных покрытий с ростом молекулярной массы полимера [27, 28]. Применительно к анионным полимерам (полиакриловой кислоте, гидролизованному полиакрилонитрилу и другим), предлагается следующий механизм стабилизирующего действия [19, 41, 42]. На поверхности частиц почвы присутствуют области (домены) различной аффинности: катионные, анионные, гидрофобные [43–45]. Анионные полимеры связываются с катионными областями на поверхности частиц. Помимо этого анионные полимеры могут связываться с присутствующими в почве поливалентными катионами, выступающими в роли “мостиков” между полимером и отрицательно заряженными областями на поверхности частиц почвы [46]. Возникающие контакты могут дополнительно стабилизироваться водородными связями и ван-дер-ваальсовыми силами между обоими компонентами. Увеличение молекулярной массы полианиона повышает вероятность взаимодействия полимера с несколькими частицами почвы и, следовательно, прочность всей полимерно-почвенной корки. Эксперименты подтверждают справедливость такого механизма. При переходе от линейной ПАК к анионному микрогелю масса полимера возрастает на несколько порядков, одновременно резко увеличивается размер анионной частицы, что позволяет ей заполнять пустоты между частицами почвы и “склеивать” их в единый кластер. Наконец, слабосшитые (сильнонабухающие) полимерные гели с мягкой структурой способны “растекаться” по межфазной границе, подстраиваясь под форму поверхности частиц почвы [47, 48]. Указанные изменения в поведении анионного связующего влекут резкое повышение прочности полимерно-почвенной корки с участием анионного микрогеля.
Связывание катионного ПДАДМАХ с анионным микрогелем дает два типа комплексов. Первый – ИПЭК(–), имеющий Z = 0.3 и валовый отрицательный заряд, способен взаимодействовать с частицами почвы за счет контактов своих анионных и катионных групп с соответствующими областями на поверхности частиц почвы. При его образовании размер частиц микрогеля меняется незначительно: с 440 до 360 нм. Таким образом, микрогель ИПЭК(–) может создать больше контактов с частицами почвы по сравнению с анионным микрогелем и при этом сохранить остальные свойства эффективного связующего (молекулярную массу, размер, степень набухания, “текучесть”), что отражается на повышении прочности полимерно-почвенных корок (рис. 5, рецептуры 1 и 2). Комплекс ИПЭК(+), имеющий Z = 3.0 и валовый положительный заряд, также способен предоставить свои анионные и катионные группы для связывания с комплементарными группами на поверхности частиц почвы. Однако избыток поликатиона приводит к заметному уменьшению размера и степени набухания частиц микрогеля, а значит, к существенному ограничению способности микрогеля “растекаться” по поверхности частиц почвы. Результатом таких изменений является наблюдаемое в эксперименте уменьшение прочности полимерно-почвенных корок (рис. 5, рецептуры 1 и 3).
Таким образом, в работе сделана оценка потенциала использования водорастворимого анионного микрогеля и ИПЭК на его основе для защиты песчаной почвы от воздушной эрозии. Сравнение влияния архитектуры полимеров акрилового ряда на механическую прочность защитных полимер-почвенных покрытий продемонстрировало преимущества сетчатого полиэлектролита (микрогеля) перед линейным аналогом. Наиболее эффективным стабилизатором почвы показал себя ИПЭК с 3-кратным избытком анионных групп анионного микрогеля, формировавший самые прочные защитные покрытия на поверхности почвы. Разработанные рецептуры на основе анионного микрогеля могут быть использованы для стабилизации почвы против ветровой эрозии и создания условий для развития растений, особенно на территориях с недостаточным содержанием влаги.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (проект № 19-29-05036) и программы JSPS KAKENHI (проект 16H06382).
Авторы выражают благодарность Университету Цукубы и профессору Усуяма Тошинобу за финансовую поддержку в виде стипендии по программе обмена JASSO.
Список литературы
Puoci F., Iemma F., Spizzirri U.G., Cirillo G., Curcio M., Picci N. // Am. J. Agric. Biol. Sci. 2008. V. 3. № 1. P. 299.
Izumrudov V.A., Mussabayeva B.K., Kassymova Z.S., Klivenko A.N., Orazzhanova L.K. // Russ. Chem. Rev. 2019. V. 88. № 10. P. 1046.
Малинина Т.А., Дюков А.Н., Голядкина И.В. // Лесотехнический журнал. 2012. № 3. С. 50.
Хабиров И.К., Сайфуллин Р.Р. // Изв. ОГАУ. 2018. Т. 6. № 74. С. 8.
Королев А.А. // Зерновое хозяйство. 2007. № 6. С. 16.
Кузин Е.Н., Кузина Е.Е. Изменение плодородия серой лесной почвы и продуктивности зерновых культур под действием химической и биологической мелиорации. Пенза: РИО ПГСХА, 2010.
Кубенкулов К.К., Наушабаев А.Х. // Гидрометеорология и экология. 2012. № 1. С. 98.
Zang Y.-X., Gong W., Xie H., Liu B.-L., Chen H.-L. // Environ. Technol. Rev. 2015. V. 4. № 1. P. 119.
Bimendina L.A., Yashkarova M.G., Orazzhanova L.K., Kudaibergenov S.E. // Eurasian Chem. J. 2005. V. 7. № 2. P. 139.
Голядкина И.В., Панков Я.В. // Усп. соврем. естествозн. 2016. № 6. С. 75.
Панков Я.В., Кондратьев В.Н., Голядкина И.В. // Лесотехнический журн. 2012. № 4. С. 148.
Данилова Т.H., Минникова Т.В., Мокриков Г.В., Казеев К.Ш., Акименко Ю.В., Колесников С.И., Якушев В.В. // Агрофизика. 2018. № 1. С. 1.
Годунова Е.И., Гундырин В.Н. // Достижения науки и техники АПК. 2015. Т. 29. № 5. С. 57.
Gilbert C., Peter S., Wilson N., Edward M., Francis M., Sylvester K., Erick B. // Open J. For. 2014. V. 04. № 01. P. 34.
Sojka R.E., Bjorneberg D.L., Entry J.A., Lentz R.D., Orts W.J. // Adv. Agron. 2007. V. 92. P. 75.
Bouranis D.L., Theodoropoulos A.G., Drossopoulos J.B. // Commun. Soil Sci. Plant Anal. 1995. V. 26. № 9–10. P. 1455.
Zezin A.B., Mikheikin S.V., Rogacheva V.B., Zansokhova M.F., Sybachin A.V., Yaroslavov A.A. // Adv. Colloid Interface Sci. 2015. V. 226. P. 17.
Tingle J.S., Newman J.K., Larson S.L., Weiss C.A., Rushing J.F. // Transp. Res. Rec. J. Transp. Res. Board. 2007. V. 1989–2. № 1. P. 59.
Liu J., Shi B., Jiang H., Huang H., Wang G., Kamai T. // Eng. Geol. 2011. V. 117. № 1–2. P. 114.
Panova I.G., Khaydapova D.D., Ilyasov L.O., Umarova A.B., Yaroslavov A.A. // Colloids Surf. A. 2020. V. 590. P. 124504.
Karol R.H. Chemical Grouting And Soil Stabilization. New York: Taylor & Francis, 2003.
Kudaibergenov S.E., Bimendina L.A., Yashkarova M.G., Orazzhanova L.K. // Res. J. Chem. Environ. 2006. V. 10. № 2. P. 25.
Shulga G., Betkers T., Brovkina J., Aniskevicha O., Ozolins J. // Environ. Eng. Manag. J. 2008. V. 7. № 4. P. 397.
Abobatta W. // Adv. Agric. Environ. Sci. Open Access. 2018. V. 1. № 2. P. 59.
Голядкина И.В., Панков Я.В. // Лесотехнический журн. 2013. Т. 4. № 12. С. 16.
Максимов А.Ю., Максимова Ю.Г., Демаков В.А., Будников В.И. // Вестн. Пермского ун-та. Сер. Биология. 2010. № 1. С. 1.
Lentz R., Sojka R., Ross C. // Int. J. Sediment Res. 2000. V. 15. P. 17.
Abu-Zreig M. // J. Soils Sediments. 2006. V. 6. № 3. P. 137.
Рабаданов Р.Г. // Аграрная Россия. 2017. № 6. С. 15.
Zhao B., Jiang H., Lin Z., Xu S., Xie J., Zhang A. // Carbohydr. Polym. 2019. V. 224. P. 115022.
Ito S., Ogawa K., Suzuki H., Wang B., Yoshida R., Kokufuta E. // Langmuir. 1999. V. 15. № 12. P. 4289.
Богдашкина Д.В., Дашян К.Э., Махаева Е.Е., Абрамчук С.С. // Вестн. Московского ун-та. Сер. Физика. Астрономия. 2017. № 1. С. 86.
Милановский Е.Ю., Хайдапова Д.Д., Поздняков А.И., Початкова Т.Н., Тюгай З. Практикум по физике твердой фазы почв. М.: Гриф и К, 2011.
Воробьева Л.А. Теория и практика химического анализа почв. М.: ГЕОС, 2006.
Хайдапова Д.Д., Пестонова Е.А. // Почвоведение. 2007. Т. 11. С. 1330.
Kramarenko E.Yu., Filippova O.E., Khokhlov A.R. // Polymer Science C. 2006. V. 48. № 7. P. 1.
Сергеев Б.М., Кирюхин М.В., Бахов Ф.Н., Сергеев В.Г. // Вестн. Московского ун-та. Сер. Химия. 2001. Т. 42. № 5. С. 308.
Кабанов В.А. // Успехи химии. 2005. Т. 74. № 1. С. 5.
Zezin A.B., Rogacheva V.B., Kabanov V.A. // Macromol. Symp. 1997. V. 126. P. 123.
Liu J., Bai Y., Song Z., Lu Y., Qian W., Kanungo D. // Polymers (Basel). 2018. V. 10. № 3. P. 287.
Laird D.A. // Soil Sci. 1997. V. 162. № 11. P. 826.
Караванова Е.И. // Почвоведение. 2013. № 8. С. 924.
Акимхан А.М. // Журн. физ. химии. 2013. Т. 87. № 11. С. 1898.
Курочкина Г.Н., Пинский Д.Л., Федотов Г.Н., Хайнос М., Соколовска З., Цесла И. // Почвоведение. 2013. № 8. С. 993.
Bachmann J., Guggenberger G., Baumgartl T., Ellerbrock R.H., Urbanek E., Goebel M.-O., Kaiser K., Horn R., Fischer W.R. // J. Plant Nutr. Soil Sci. 2008. V. 171. № 1. P. 14.
Abdel Khalek M., El-Midany A. // J. ore Dress. 2015. V. 17. № 34. P. 11.
Mourran A., Wu Y., Gumerov R.A., Rudov A.A., Potemkin I.I., Pich A., Möller M. // Langmuir. 2016. V. 32. № 3. P. 723.
Wellert S., Richter M., Hellweg T., von Klitzing R., Hertle Y. // Zeitschrift für Phys. Chemie. 2015. V. 229. № 7–8. P. 1225.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия Б)