Высокомолекулярные соединения (серия Б), 2020, T. 62, № 6, стр. 416-424
ИОНОМЕРЫ НА ОСНОВЕ СУЛЬФИРОВАННЫХ ПОЛИФЕНИЛХИНОКСАЛИНОВ: СИНТЕЗ, СВОЙСТВА В РАСТВОРЕ И БЛОКЕ
В. Г. Васильев a, *, М. И. Бузин a, Г. Г. Никифорова a, Н. М. Беломоина a, Е. Г. Булычева a, В. С. Папков a
a Институт элементоорганических соединений им. А.Н. Несмеянова Российской академии наук
119991 Москва, ул. Вавилова, 28, Россия
* E-mail: viktor@ineos.ac.ru
Поступила в редакцию 18.03.2020
После доработки 02.07.2020
Принята к публикации 16.07.2020
Аннотация
Взаимодействием ароматического ионогенного полимера – сульфированного полифенилхиноксалина с гидроокисями щелочных металлов (Li, Na и K) получен новый вид ароматических иономеров. Обнаружено, что введение металла оказывает существенное влияние на агрегацию макромолекул синтезированных иономеров, обусловленную как специфическим межмолекулярным взаимодействием ионных групп, так и взаимодействием гидрофобных участков основной цепи. В свою очередь, это влечет изменение растворимости и вязкости растворов иономеров, а также деформационно-прочностных характеристик пленок из них в сухом и в набухшем состоянии по сравнению с таковыми у пленок из исходного и сульфированного полифенилхиноксалина. Показано, что замещение атомов водорода в сульфогруппах на ионы щелочных металлов в сульфированном полифенилхиноксалине приводит к повышению термической и термоокислительной стабильности иономеров до уровня близкого к наблюдаемому для полифенилхиноксалина.
ВВЕДЕНИЕ
Полифенилхиноксалины (ПФХ) – один из перспективных классов полигетероариленов с высокими эксплуатационными характеристиками (термо-, хемо-, радиационной стойкостью). Во многом это связано с высокой степенью циклизации хиноксалиновых фрагментов макромолекулярной цепи, достигаемой при синтезе, и, соответственно, с наличием минимального количества структурных дефектов [1, 2]. Поскольку ароматические конденсационные полимеры, содержащие в своей структуре группы SO3H, успешно используют в качестве протонпроводящих мембран для топливных элементов, сульфирование ПФХ можно рассматривать как потенциально эффективный вид полимераналогичных превращений этого класса полимеров в термостойкие производные с новой расширенной сферой практического применения. К ним следует, в частности, отнести сульфированные полифенилхиноксалины (СПФХ), которые образуются при сульфировании ПФХ смесью серной кислоты с олеумом [3], а также имеют прекрасную растворимость в органических растворителях и хорошие пленкообразующие свойства.
Полимеры, содержащие сульфогруппы, традиционно используют для получения иономеров [4–9] – класса полимеров, специфическая молекулярная структура которых проявляется в сочетании в них свойств органических макромолекул и полиэлектролитов [10–12]. Иономеры получают частичной нейтрализацией сульфогрупп ионами металлов, приводящей к образованию ионных пар, их электростатическое взаимодействие, в свою очередь, ведет к возникновению мультиплетов, являющихся физическими узлами пространственной сетки [13–15]. Это позволяет успешно применять иономеры для создания ионных селективных мембран в электрохимических процессах, покрытий, топливных элементов и батарей [16–24].
В этой связи, СПФХ представляют интерес в качестве основы термостойких ароматических иономеров нового типа. Можно ожидать, что такие иономеры будут обладать повышенной термостабильностью по сравнению с исходными ПФХ. Дело в том, что наличие сульфогрупп в СПФХ приводит к более низкой его термостабильности, чем исходного ПФХ, из-за образования поперечных межмолекулярных сшивок выше 250°С в результате взаимодействия сульфогрупп [25, 26]. Так, формирование пространственной физической сетки в иономерах на основе СПФХ потенциально открывает возможность реализации нового подхода к термостабилизации сульфированных полиэлектролитов. Идеология данного подхода состоит в том, что “блокирование” сульфогрупп в образующихся физических узлах – мультиплетов ионных пар способно препятствовать развитию термохимического деструктивного взаимодействия этих групп. Таким образом, сульфированный полифенилхиноксалин и иономеры нового типа на его основе выглядят несомненно интересными объектами исследования в научном и прикладном плане.
В настоящей статье рассмотрены последовательные полимераналогичные превращения ПФХ в указанные полимеры и описаны их растворимость, поведение в растворах, гелеобразование, а также термостабильность и термические переходы в них. Эти ключевые свойства предопределяют возможность их успешного прикладного использования в качестве термостойких полимерных материалов, проявляющих электролитное поведение.
ОБЪЕКТЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Исходными мономерами для синтеза полимеров служили 1,4-бис-(фенилглиоксалил)дифенил-оксид и 3,3',4,4'-тетрааминодифенилоксид, последний по сравнению с обычным 3,3'-диаминобензидином обладает меньшей токсичностью и более высокой устойчивостью к окислению.
Сульфированные полифенилхиноксалины получали двумя методами – одностадийным и двустадийным.
При одностадийном методе СПФХ синтезировали непосредственно из соответствующих мономеров (3,3',4,4'-тетрааминодифенилоксида и 4,4'-бис-(фенилглиоксалил)-дифенилоксида) в среде серной кислоты. Предполагали, что серная кислота является в данном случае одновременно растворителем, катализатором образования хиноксалинового цикла и сульфирующим агентом:
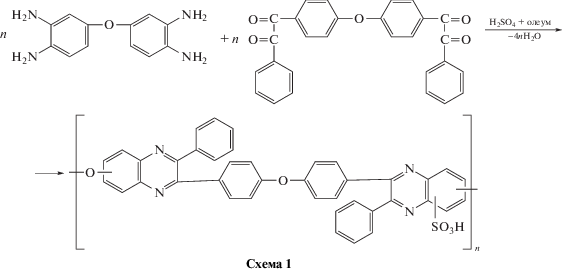
За основу брали ранее разработанный метод синтеза в смеси серная кислота : олеум = 4 : 1 [26], так как этим методом максимально удавалось достичь содержания серы в СПФХ (4.2 мас. %). В связи с тем что в настоящей работе планировали получить СПФХ с различным, в том числе и более высоким содержанием сульфогрупп, этот метод модифицировали, используя в качестве реакционной среды смесь серная кислота : олеум = 3 : 1.
После завершения реакции раствор охлаждали до комнатной температуры, полимер осаждали дистиллированной водой, далее отфильтровывали и многократно промывали дистиллированной водой до нейтральной реакции. Полученный СПФХ промывали ацетоном, отфильтровывали и высушивали вначале на воздухе, затем в вакууме при 50°С до постоянной массы. Полученные результаты приведены в табл. 1.
Таблица 1.
Условия получения и характеристики сульфированных полифенилхиноксалинов, синтезированных по одностадийному методу
| Опыт, № | Состав реакционной смеси | Температура реакции, °С | Продолжительность реакции, ч | ηпр*, дл/г | S, мас. % |
|---|---|---|---|---|---|
| 1 | Н2SO4 | 20 | 6 | 0 | – |
| 2 | Н2SO4 | 20 | 35 | 0 | – |
| 3 | Н2SO4 | 120 | 35 | 0.02 | 0.1 |
| 4 | Н2SO4 : олеум = 3 : 1 | 20 | 35 | 0 | – |
| 5 | Н2SO4 : олеум = 3 : 1 | 120 | 6 | 0.07 | 0.2 |
| 6 | Н2SO4 : олеум = 3 : 1 | 120 | 10 | 0.10 | 1.5 |
| 7 | Н2SO4 : олеум = 3 : 1 | 120 | 35 | 0.16 | 2.3 |
* Здесь и в табл. 2 – в N-метилпирролидоне при 25°C и концентрации 0.5 г/дл.
Установили, что при комнатной температуре образования хиноксалинового цикла не наблюдалось на протяжении 35 ч. (табл. 1, опыты 1 и 2). При повышении температуры до 120°С происходило образование низкомолекулярного СПФХ (табл. 1, опыт 3).
СПФХ, содержащие в своем составе от 0.2 до 2.3% серы, выделили из реакционной смеси при проведении реакции при 120°С в течение 6–35 ч (табл. 1, опыты 5–7). Оказалось, что и в использованных более жестких условиях получить высокомолекулярные СПФХ с высоким содержанием серы не удается.
Двустадийный метод: на первой стадии при 20–22°С в среде хлороформа с применением метанола в качестве донора протонов (соотношение 10 : 1) синтезировали ПФХ (схема 2). Из реакционного раствора их осаждали ацетоном, промывали ацетоном, отфильтровывали и высушивали вначале на воздухе, затем в вакууме при 50°С до постоянной массы. Полученные полимеры обладали пленкообразующими свойствами и растворимостью в хлороформе, бензиловом спирте, N-метилпирролидоне (МП), м-крезоле и H2SO4:
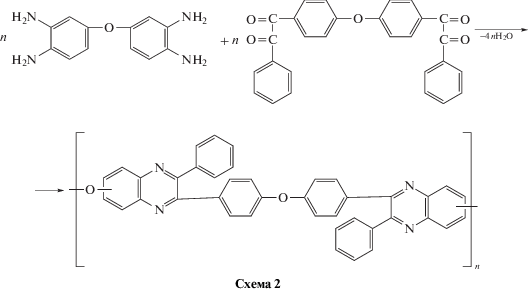
Последующее сульфирование ПФХ осуществляли при 120°С смесью серной кислоты с олеумом в соотношении 3 : 1 [19]:
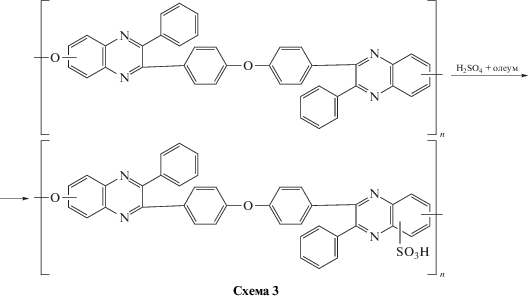
В табл. 2 приведены условия получения и характеристики СПФХ указанной выше общей формулы. Температура реакции во всех опытах составляла 120°C.
Таблица 2.
Условия получения и характеристики сульфированных полифенилхиноксалинов, синтезированных по двухстадийному методу
| Образец | Продолжи-тельность реакции, ч | ηпр, дл/г | S, мас. % | Группа (SO3H), мол. % |
|---|---|---|---|---|
| СПФХ-1 | 10 | 0.30 | 1.7 | 4.0 |
| СПФХ-2 | 15 | 0.30 | 2.7 | 6.8 |
| СПФХ-3 | 20 | 0.46 | 3.5 | 8.8 |
| СПФХ-4 | 25 | 0.61 | 4.2 | 10.6 |
| СПФХ-5 | 30 | 1.10 | 5.0 | 11.3 |
| СПФХ-6 | 35 | 1.12 | 9.1 | 23.0 |
После полимераналогичного превращения ПФХ в СПФХ реакционный раствор охлаждали до комнатной температуры, полимер осаждали дистиллированной водой, отфильтровывали и многократно промывали дистиллированной водой до нейтральной реакции. Полученный СПФХ промывали ацетоном, отфильтровывали и высушивали вначале на воздухе, затем в вакууме при 50°С до постоянной массы.
В связи с тем что реакцией полимераналогичных превращений ПФХ удалось получить СПФХ с хорошими вязкостными характеристиками и широким интервалом содержания сульфогрупп, для дальнейших исследований использовали СПФХ, полученные этим методом.
Реакцию синтеза иономеров на основе СПФХ с различной степенью сульфирования проводили в гетерогенных условиях:
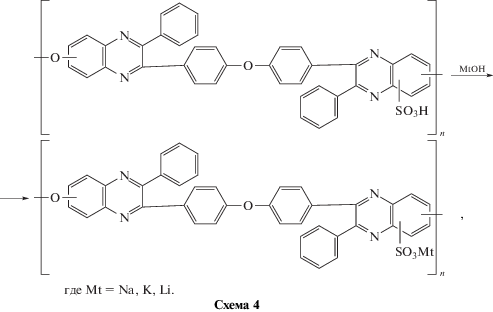
Полимер в виде порошка или пленки заливали 5 моль/л водными растворами гидроокисей лития, натрия или калия, реакцию проводили при комнатной температуре в течение 7 суток при перемешивании, после чего многократно промывали порошок (пленку) водой до установления нейтрального рН и сушили при 150°С до постоянной массы. О степени замещения атомов водорода в сульфогруппах судили по количеству вошедшего в полимер металла, определенного методами пламенной эмиссионной спектрометрии и(или) недеструктивного рентгенофлуоресцентного анализа.
В полученных иономерах практически все атомы водорода в сульфогруппах были замещены на катионы металлов.
Таблица 3.
Термические характеристики ПФХ, СПФХ и иономеров на их основе
| Образец | Содержание S, мас. % | Содержание влаги (мас. %) в образцах с металлами | Температура 5%-ной потери массы (°С) в образцах с металлами | Твердый остаток, мас. % | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| – | Li | Na | K | – | Li | Na | K | – | Li | Na | K | ||
| ПФХ | – | – | – | – | – | 497 | – | – | – | 1 | – | – | – |
| СПФХ-2 | 2.7 | 2.5 | 3.2 | 3.0 | 2.0 | 368 | 433 | 437 | 442 | 1 | 2.5 | 2.6 | 6 |
| СПФХ-3 | 3.5 | 3.5 | 5.7 | 4.5 | 2.5 | 390 | 440 | 450 | 442 | 1 | 5.5 | 7 | 10 |
| СПФХ-4 | 4.2 | 5.0 | 8.0 | 5.5 | 4.5 | 392 | 447 | 452 | 436 | 1 | 11.0 | 12 | 14 |
| СПФХ-5 | 5.0 | 10.5 | 12.0 | 6.5 | 5.5 | 392 | 460 | 440 | 464 | 1 | 13.6 | 15 | 19 |
| СПФХ-6 | 9.1 | 12.5 | 14.0 | 8.5 | 8.0 | 375 | 460 | 481 | 524 | 1 | 19.6 | 22 | 28 |
Вязкость разбавленных растворов полимеров в МП определяли с помощью капиллярного вискозиметра Уббелоде с “висящим” уровнем в диапазоне концентрации 0.1–1.0 дл/г при 25 ± 0.05°С. Молекулярную массу исходного ПФХ рассчитывали по уравнению Марка–Куна–Хаувинка, параметры которого были определены в работе [27]. Она составляла 20 × 10–3.
Термогравиметрические исследования выполняли на приборе “Derivatograth-C” (“МОМ”, Венгрия) на воздухе при скорости нагревания 10 град/мин на образцах массой ~15 мг.
Исследования методом дифференциальной сканирующей калориметрии осуществляли на приборе “DSC-822e” (“Меттлер-Толедо”, Швейцария) в атмосфере аргона при скорости нагревания 10 град /мин на образцах массой ~10 г.
Пленки для механических испытаний отливали из 10 мас. % раствора полимера в МП с последующим испарением растворителя при температуре 70°С и окончательным высыханием до постоянной массы при 120°С в вакууме.
Прочностные характеристики полимерных пленок определяли на универсальной испытательной машине “LLOYD Instruments LR5K Plus”.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
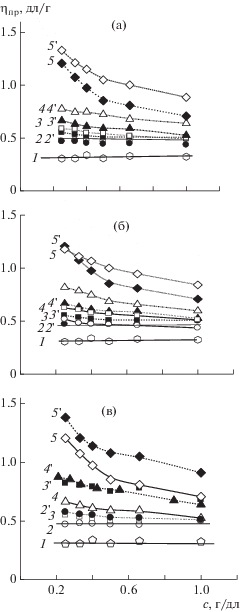
Сульфирование ПФХ сопровождается существенным изменением его растворимости и вязкостного поведения разбавленных растворов. Так, СПФХ, содержащие более 1.7 мас. % S, теряют растворимость в хлороформе, присущую исходному ПФХ, а при содержании более 8 мас. % S начинают растворяться в этаноле и набухать в воде. При увеличении степени сульфирования исходного полимера выше 2.7 мас. % S было обнаружено увеличение приведенной вязкости растворов СПФХ в МП и проявление так называемого полиэлектролитного эффекта, характерного для водных растворов полиэлектролитов (рис. 1). При содержании серы ≤2.7 мас. % полиэлектролитный эффект не наблюдается, полимер ведет себя, как исходный ПФХ (кривые 2). Вероятно, что такое поведение может быть связано с малой долей ионных групп.
Рис. 1.
Концентрационные зависимости приведенной вязкости в МП при 25°С ПФХ (1), СПФХ (2–5) и их солей (2 '–5 ') с литием (а), натрием (б) и калием (в). Содержание S в исходных СПФХ 2.7 (2), 3.5 (3), 4.2 (4) и 5.5 мас. % (5).
Полиэлектролитный эффект – это разворачивание макромолекул, проявляющееся в прогрессирующем возрастании приведенной вязкости раствора полиэлектролита при уменьшении его концентрации, в то время как для растворов неионогенных макромолекул характерно линейное уменьшение приведенной вязкости при разбавлении. Объясняется этот эффект тем, что при разбавлении растворов полиэлектролитов увеличивается объем, в котором распределяются противоионы, экранирующие кулоновское отталкивание между фиксированными зарядами полииона, вследствие чего возрастает их отталкивание и происходит прогрессирующее разворачивание полииона [28].
В последнее время аналогичный эффект обнаружен в неводных растворах полимеров, содержащих ионогенные группы, в случае высокополярных растворителей [29]. Иономеры на основе СПФХ с различным содержанием металла также растворяются в МП и проявляют полиэлектролитный эффект. Как видно из концентрационной зависимости приведенной вязкости, эффект этот тем больше, чем выше содержание металла. Вообще, критерием проявления полиэлектролитных или иономерных свойств полимеров, содержащих ионогенные сульфогруппы, и их солей является характерное поведение вязкости их разбавленных растворов.
Следует также отметить, что значения приведенной вязкости всех СПФХ и иономеров на их основе существенно выше значений для исходного ПФХ (рис. 1, кривая 1). Кроме того, вязкость растворов иономеров возрастает по сравнению с исходными сульфированными полимерами – свойство, характерное для растворов всех иономеров (рис. 1) [30–33].
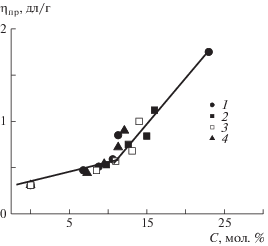
На рис. 2 представлена зависимость ηпр от содержания ионогенных групп в различных СПФХ (табл. 2) и солях на их основе. Представленная зависимость практически одинакова как для СПФХ, так и для солей, слабое отличие величины ηпр может быть связано с высокой полярностью растворителя и частичной диссоциацией ионных групп в неводном растворителе. На графике можно выделить два прямолинейных участка с различным наклоном, изменение наклона (точка перегиба) соответствует содержанию ионных групп порядка 10–12 мол. %. Возможно, что более интенсивный рост вязкости связан с изменением конформации макромолекул вследствие их разворачивания при постепенном переходе от иономера к полиэлектролиту.
Рис. 2.
Зависимость ηпр растворов от содержания ионогенных групп в СПФХ (1), в калиевых (2), натриевых (3) и литиевых (4) солях. Растворитель – МП, концентрация раствора 0.5 г/дл.
Влияние введения сульфогрупп на термическую стабильность ПФХ было исследовано методом ТГА. На рис. 3 приведены кривые ТГА для ПФХ и СПФХ с различным содержанием сульфогрупп. Обнаружено, что СПФХ содержат значительное количество сорбированной влаги воздуха. Это прослеживается в появлении на кривых ТГА области потери массы вблизи 100оС, связанной с ее десорбцией. Содержание влаги возрастает при увеличении содержания серы от 2.7 до 9.1 мас. % (табл. 3). Введение сульфогрупп в ПФХ приводит к понижению его термической стабильности: термоокислительная деструкция развивается в два этапа, и на кривых ТГА для СПФХ присутствует этап разложения в области 300–400°С, предшествующий высокотемпературному этапу потери массы, начинающемуся в области 500°С, в которой расположен единственный этап разложения на воздухе исходного ПФХ. Величина потери массы на первом этапе деструкции СПФХ возрастает при увеличении содержания сульфогрупп. Очевидно, что в области температуры 300–400°С происходят десульфирование и формирование сшитой структуры, как это наблюдали ранее в условиях длительного изотермического нагревания при 250°С [26].
Рис. 3.
Кривые ТГА для ПФХ (1), СПФХ-2 (2), СПФХ-3 (3), СПФХ-4 (4), СПФХ-5 (5) и СПФХ-6 (6); нагревание на воздухе со скоростью 10 град/мин.
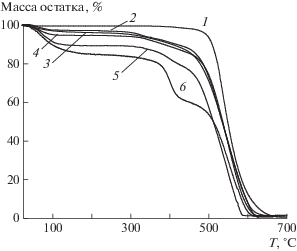
Введение в СПФХ ионов щелочных металлов существенно отражается на их способности к сорбции воды из воздуха. Например, при введении Li (рис. 4; табл. 3) количество теряемой при нагревании сорбированной влаги возрастает по сравнению с исходными СПФХ и ее содержание увеличивается при повышении содержания серы в СПФХ.
Рис. 4.
Кривые ТГА для литиевых солей СПФХ-2 (1), СПФХ-3 (2), СПФХ-4 (3), СПФХ-5 (4) и СПФХ-6 (5); нагревание на воздухе со скоростью 10 град/мин.
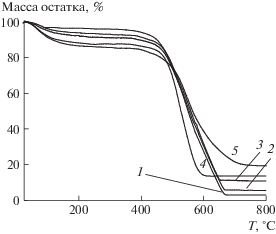
Замещение атомов водорода в сульфогруппах на Na приводит к незначительному увеличению количества сорбированной влаги по сравнению с литийсодержащими иономерами при невысоком количестве сульфогрупп в СПФХ и существенно уменьшается при возрастании содержания серы в СПФХ до 5.0 и 9.1 мас. % (табл. 3). Введение калия влечет заметное снижение сорбции воды иономерами по сравнению с исходными СПФХ и их литиевыми и натриевыми солями с сохранением тенденции к увеличению ее содержания при возрастании количества сульфогрупп в СПФХ и, соответственно, ионов металла (табл. 3).
Явление сорбции воды иономерами обусловлено гигроскопичностью солей металлов. Из солей щелочных металлов ионы лития имеют наименьший ионный радиус, что способствует образованию гидратов (обычно тригидратов), в большинстве этих соединений литий координирует шесть молекул воды. Чем больше радиус иона, тем ниже плотность заряда на его поверхности и тем сложнее иону удерживать молекулу воды. Поэтому в солях щелочных металлов гигроскопичность понижается в ряду Li+ > Na+ > K+, изменяя тип катиона в иономере возможно варьировать содержание в иономере воды и соответственно влиять на физические свойства полимера.
Следует отметить, что замещение атомов водорода в сульфогруппах на ионы щелочных металлов приводит к повышению термической стабильности иономеров по сравнению с СПФХ (табл. 3). Как и в случае СПФХ, разложение иономеров на воздухе протекает в два этапа, однако первый этап разложения, наблюдающийся в СПФХ вблизи 300–400°С, смещается в область более высоких значений температуры, а для калиевого иономера он частично налагается на окончательный и общий для всех исследованных полимеров этап деструкции, протекающий выше 500°С. Температура начала разложения $Т_{{\text{д}}}^{{5\% }}$ иономеров с увеличением содержания катионов металла демонстрирует тенденцию к возрастанию в ряду Li < Na < K (СПФХ-2, СПФХ-5, СПФХ-6). Аналогичная зависимость наблюдается и для количества твердого остатка после окончания термоокислительных превращений (табл. 3). Вероятно, наблюдаемые закономерности термического поведения связаны с увеличением ионного радиуса катиона щелочного металла при переходе от лития к натрию и калию и, как следствие, влиянием на процесс разложения и формирования твердого остатка.
Было обнаружено, что полимерные соли СПФХ хорошо набухают в воде, а равновесная степень их набухания также зависит от типа противоиона, например для солей СПФХ-6 массовая доля полимера в равновесно набухшем геле составляет 0.02, 0.09 и 0.27 для Li, Na и К солей соответственно.
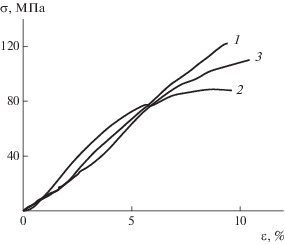
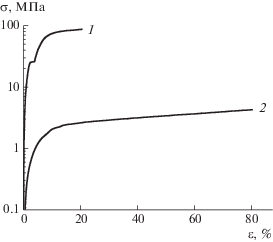
На рис. 5 представлены кривые растяжения пленок ПФХ, СПФХ и натриевой соли. Видно, что разрывная деформация для всех трех образцов составляет ~10%, прочность при разрыве уменьшается в ряду ПФХ > СПФХ-Na > СПФХ. Набухшие в воде пленки иономеров, представляющие собой гели, имеют существенно меньшее разрывное напряжение, но их деформация при разрыве достигает 80% (рис. 6). Вероятно, что образование водных гелей в иономерах обусловлено дифильностью макромолекул иономеров, имеющей гидрофобную основную цепь (исходный ПФХ не сорбирует влагу) и гидрофильные ионные группы.
Гели подобного типа представляют собой системы с незавершенным фазовым расслоением. Образующаяся в водном геле пространственная сетка устойчива к температурному воздействию и, в отличие от обратимых гелей с физическими узлами другой природы, не плавится вплоть до температуры кипения растворителя. Плавление гелей обусловлено разрушением физической (обратимой) сетки, оно не связано с деструкцией цепей.
На кривых ДСК для СПФХ и иономеров скачок теплоемкости, характерный для перехода из стеклообразного в высокоэластическое (вязкотекучее) состояние, отсутствует в отличие от исходного ПФХ с четко выраженным скачком теплоемкости в области Тс = 250°С. Тепловые эффекты наблюдаются только в области начала деструкционных процессов. Очевидно, что температура стеклования СПФХ и иономеров на их основе смещается в сторону высоких значений температуры и превышает температуру начала их деструкции.
ЗАКЛЮЧЕНИЕ
Последовательными реакциями полимераналогичных превращений полифенилхиноксалинов получены иономеры различного строения с широким диапазоном свойств.
Иономеры на основе СПФХ с разным содержанием металла так же, как и исходные СПФХ, растворяются в МП и проявляют полиэлектролитный эффект. Данный эффект тем больше, чем выше содержание металла, при этом вязкость растворов иономеров возрастает по сравнению с вязкостью растворов исходных сульфированных полимеров – свойство, характерное для растворов всех иономеров.
Замещение атомов водорода в сульфогруппах синтезированных СПФХ на ионы щелочных металлов приводит к образованию иономеров с существенно более высокой термической стабильностью по сравнению с СПФХ. Она сравнима с термостабильностью исходного ПФХ. В принципе, этот факт предполагает возможность термостабилизации полиэлектролитов, по крайне мере с ионогенными сульфогруппами, путем перевода их в соответствующие иономеры.
Обнаружена способность иономеров к гелеобразованию в водных растворах, что обусловлено дифильностью макромолекул СПФХ, имеющей гидрофобную основную цепь (исходный ПФХ не сорбирует влаги) и гидрофильные ионные группы.
Полученные системы на основе ПФХ являются потенциально интересными прекурсорами (в прикладном аспекте) для термостойких твердых полимерных иономеров и электролитов.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (код проекта 20-03-00348) и Министерства науки и высшего образования Российской Федерации (синтез и сульфирование полифенилхиноксалинов).
Определение элементного состава синтезированных полимеров проведено с использованием научного оборудования лаборатории элементного анализа ИНЭОС РАН при поддержке Министерства науки и высшего образования Российской Федерации. Исследования методом ДСК выполнены на оборудовании Учебно-научного центра функциональных и наноматериалов МПГУ при финансовой поддержке Министерства науки и высшего образования Российской Федерации.
Список литературы
Belomoina N.M., Rusanov A.L., Bruma M. // Polymer Science C. 2007. V. 49. № 4. P. 386.
Wrasidlo W.J., Augl M.J. // J. Polym. Sci. A. 1969. № 7. P. 3393.
Dobrovolsky Yu.A., Jannasch P., Lafitte B., Belomoina N.M., Rusanov A.L., Likhachev D.Y. // Russ. J. Electrochem. 2007. V. 43. № 5. P. 489.
Vasiliev V.G., Buzin M.I., Nikiforova G.G., Belomoina N.M., Bulycheva E.G., Papkov V.S. // Dokl. Phys. Chem. 2014. V. 458. № 2. P. 149.
Fitzgerald J.J., Weiss R.A. // J. Macromol. Sci., Rev. Macromol. Chem. Phys. 1988. V. C28. № 1. P. 99.
Tant M.R., Wilkis G.L. // J. Macromol. Sci., Rev. Macromol. Chem. Phys. 1988. V. C. 28. № 1. P. 1.
Hird B., Eisenberg A. // Macromolecules. 1992. V. 25. № 24. P. 6466.
Peiffer D.G., Hager B.L., Weiss R.A., Agarwal P.K., Lundberg R.D. // J. Polym. Sci., Polym. Phys. Ed. 1985. V. 23. № 9. P. 1869.
Hara M., Jar P., Sauer J.A. // Macromolecules. 1988. V. 21. № 10. P. 3183.
Khokhlov A.R., Dormidontova E.E. // Uspekhi Fizicheskikh Nauk. 1997. V. 167. № 2. P. 239.
Eisenberg A., Rinaudo M. // Polym. Bull. 1990. V. 24. № 6. P. 671.
Eisenberg A., Hird B., Moor R.B. // Macromolecules. 1990. V. 23. № 18. P. 4098.
Mauritz K.A. // J. Macromol. Sci., Rev. Macromol. Chem. Phys. 1988. V. C28. № 1. P. 65.
Besso E., LeGras R., Eisenberg A., Gupta R., Harris F.W., Steck A.E., Yeager H.L. // J. Appl. Polym. Sci. 1985. V. 30. № 7. P. 2821.
Wang B., Krause S. // Macromolecules. 1986. V. 19. № 11. P. 2877.
Chang Y., Brunello G.F., Fuller J., Hawley M., Kim Yu.S., Disabb-Miller M., Hickner M.A., Jang S.S., Bae C. // Macromolecules. 2011. V. 44. № 21. P. 8458.
Tierney N.K., Register R.A. // Macromolecules. 2003. V. 36. № 4. P. 1170.
Rikukawa M., Sanui K. // Prog. Polym. Sci. 2000. V. 25. № 10. P. 1463.
Park E.J., Maurya S., Lee A.S., Leonard D.P., Li D., Jeon J.Y., Bae C., Kim Y.S. // J. Mater. Chem. A. 2019. V. 7. P. 25040.
Kopitzke R.W., Linkous C.A., Anderson H.R., Nelson G.L. // J. Electrochem. Soc. 2000. V. 147. № 5. P. 1677.
Hsu S.L.-C., Liu C.-W., Tu C.-H., Chuang H.-Y., Bulycheva E., Belomoina N. // Polym. Bull. 2018. V. 75. № 11. P. 5321.
Tu C.H., Hsu S.L.-C., Bulycheva E., Belomoina N. // Polym. Eng. Sci. 2019. V. 12. P. 203.
Savadogo O. // J. New Mater. Electrochem. Syst. 1998. № 1. P. 47.
Булычева Е.Г., Беломоина Н.М., Бузин М.И., Васильев В.Г., Вассерман Л.А., Hsu S.L.-C. // Изв. Кабардино-Балкарского гос. ун-та. 2017. Т. VII. № 2. С. 22.
Polyanskii N.G., Tulupov P.E. // Usp. Khim. 1971. V. 40. № 12. P. 2250.
Беломоина Н.М., Русанов А.Л., Януль Н.A., Кирш Ю.Э. // Высокомолек. соед. A. 1996. Т. 38. № 2. С. 355.
Тимофеева Г.И., Кроян С.A., Ронова И.A., Павлова С.A., Кронгауз Е.С., Травникова A.Н., Коршак В.В. // Высокомолек. соед. A. 1979. Т. 21. № 1. С. 67.
Тэнфорд Ч. Физическая химия полимеров / Пер. с англ. под ред. Г.Л. Слонимского. М.: Химия, 1965. Tanford Ch. Physical Chemistry of Macromolecules. 1961. Wiley.
Rogovina L.Z., Nikoforova G.G., Ponomarenko A.T., Vasil’ev V.G., Dubrovina L.V., Bragina T.P., Ryabev A.N., Salazkin S.N., Papkov V.S. // Polymer Science. A. 2006. V. 48. № 11. P. 1218.
Lundberg R.D., Makowski H.S. // J. Polym. Sci. Polym. Phys. Ed. 1980. V. 18. № 8. P. 1821.
Lantman C.W., MacKnight W.J., Lundberg R.D. // Ann. Rev. Mater. Sci. 1989. V. 19. № 1. P. 295.
Hara M., Zhang D., Wu J., Lee A. // Polym. Prep. 1987. V. 28. № 1. P. 178.
Lundberg R.D., Phillips R.R. // Polym. Prepr. Am. Chem. Soc. Div. Polym. Chem. 1984. V. 25. № 2. P. 303.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия Б)