Высокомолекулярные соединения (серия Б), 2021, T. 63, № 2, стр. 122-130
КОМПЛЕКСЫ НА ОСНОВЕ ПОЛИСТИРОЛСУЛЬФОКИСЛОТЫ И ПОЛИЭТИЛЕНОКСИДА
П. И. Ветошева a, b, В. О. Бодаев a, О. А. Пышкина a, *, Е. А. Литманович a, В. Г. Сергеев a
a Московский государственный университет имени М.В. Ломоносова. Химический факультет
119992 Ленинские горы, Москва, Россия
b Автономная некоммерческая образовательная организация высшего образования
“Сколковский институт науки и технологий”
143026 Москва, Московская область, Большой бульвар, 30, Россия
* E-mail: pyshkina@genebee.msu.ru
Поступила в редакцию 02.11.2020
После доработки 07.12.2020
Принята к публикации 11.12.2020
Аннотация
Изучено комплексообразование в водных бессолевых полуразбавленных растворах полистиролсульфокислоты и полиэтиленоксида, приводящее к образованию растворимых комплексов полистиролсульфокислота–полиэтиленоксид. Показано, что взаимодействие компонентов в таких комплексах значительно ослабевает с ростом температуры, а также с уменьшением длины цепи полиэтиленоксида. Методами вискозиметрии и светорассеяния установлено, что в разбавленных водных и водно-солевых растворах комплексы между полистиролсульфокислотой и полиэтиленоксидом не образуются и система представляет собой совместимую смесь полимеров в общем растворителе.
ВВЕДЕНИЕ
В последнее время большой интерес вызывают интерполимерные комплексы, стабилизированные связями, отличающимися от кулоновских, такими как водородные и ион-дипольные связи [1, 2], поскольку их можно использовать в качестве pH- и термочувствительных компонентов при разработке микрокапсул, наночастиц, гидрогелей с контролируемым высвобождением, а также как полимерные электролитные мембраны [3]. Комплексы, стабилизированные водородными связями, образуются между полимерами, имеющими донор протона (как правило, поликислоты) и неионогенным полимером, содержащим в основной цепи сильный акцептор водорода. Среди водорастворимых неионогенных полимеров, которые изучали с точки зрения комплексообразования с поликислотами, можно выделить следующие группы: полимеры, содержащие эфирные группы в основной цепи (например, ПЭО, ППО) или в боковых заместителях (поливинилметиловый эфир); полимеры, содержащие лактамные группы, такие как поливинилпирролидон, поливинилкапролактам; акриловые полимеры (полиакриламид, полиизопропилакриламид); полимерные спирты (ПВС); другие синтетические полимеры, такие как полиэтилоксазолин, поли(N-ацетилиминоэтилен); полисахариды [4–11]. Кроме того, примеры доноров водорода в основном ограничены различными поликарбоновыми кислотами, исключение составляют те, которые содержат полифенол, полиспирты и полианилин [12, 13].
Образование комплексов на основе поликислот возможно только в кислых средах (pH < 7). Это обусловлено следующими причинами: кислота должна быть протонирована для образования водородной связи; электростатическое отталкивание между депротонированными кислотными остатками дестабилизирует интерполимерные комплексы (ИПК). Сульфоновые кислоты в отличие от карбоновых являются очень сильными и полностью диссоциируют даже в присутствии следов воды. Несмотря на это, в работе [14] была показана возможность формирования стехиометричных водонерастворимых комплексов между некоторыми полисульфокислотами и ПЭО в разбавленных водных растворах. Экспериментально образование комплекса между ПЭО и полистиролсульфоновой кислотой, а также фторированной полисульфокислотой (торговое название Nafion) было подтверждено измерением мутности и ИК-спектроскопией. В работе показано, что ПЭО образует комплексы с полистиролсульфоновой кислотой разной молекулярной массы при pH < 0.5. Такое неожиданное взаимодействие объясняется силой водородной связи между сульфогруппой и эфиром, которая стабилизирует ИПК за счет смещения кислотно-основного равновесия.
Показано, что свойства комплексов, образованных за счет водородных связей, можно регулировать за счет незначительных изменений начальных параметров и что при комплексообразовании происходит значительное изменение гидродинамических свойств растворов; это придает таким системам интерес для использования во многих практических задачах [15–17].
В настоящей работе исследовано комплексообразование в водных растворах ПССК и ПЭО в различных концентрационных режимах, при разной ионной силе растворов и молекулярной массе ПЭО (ПЭГ).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Поли(4-стиролсульфокислоту) (ПССК, Mw = = 7.5 × 104, “Sigma Aldrich”), полиэтиленоксид (ПЭО, Mw = 40 000, “Aldrich”), полиэтиленгликоль (ПЭГ, Mw = 2000, “Aldrich”) использовали без предварительной очистки. Для приготовления растворов брали бидистиллированную воду, деионизированную системой ионообменных колонок “MilliQ” (“Millipore”, США). Для приготовления солевых растворов использовали хлорид натрия (“Химреактив”, Россия).
Раствор ПЭО40 000 заданной массовой концентрации приготавливали растворением навески в течение 1 суток в рассчитанном объеме воды или 0.1 M раствора NaCl. Водный раствор ПССК заданной концентрации готовили разбавлением коммерческого 18 мас. % раствора. Для приготовления раствора ПССК в 0.1 M NaCl коммерческий 18 мас. % раствор сначала разбавляли в 2 раза 0.2 M раствором NaCl, а затем к полученному раствору добавляли 0.1 M NaCl до заданной концентрации. Водный раствор ПЭГ2000 заданной массовой концентрации готовили растворением навески в течение 1 суток в рассчитанном объеме воды. Водный раствор ПССК заданной концентрации готовили разбавлением коммерческого 18 мас. % раствора.
Водные растворы ПССК–ПЭО40 000 с заданным соотношением Z = (n(ПЭО40 000))/(n(ПЭО40 000) + + n(ПССК)) (Z = 0, 0.32, 0.59, 0.81, 0.91, 0.98, 1.0) приготавливали смешением разных объемов водных растворов ПЭО40 000 и ПССК одинаковой массовой концентрации при собственных рН исходных компонентов. Водные растворы ПССК–ПЭГ2000 готовили аналогичным образом. Солевые растворы комплексов и смесей приготавливали смешением растворов ПЭО40000 и ПССК в 0.1 M NaCl.
Относительную вязкость растворов ηотн определяли в капиллярном вискозиметре Уббелоде с подвешенным мениском, время истечения растворителя t0 = 47 с (25°С). Перед измерением образцы термостатировали в течение 15 мин, температуру в ячейке поддерживали с точностью ±0.2°С.
Динамическую вязкость рассчитывали, как η = = $\frac{{t\,{{\eta }_{0}}}}{{{{t}_{0}}}},$ где t – время истечения раствора, η0 – вязкость растворителя (воды) при данной температуре.
Удельную ηуд и приведенную вязкость ηпр находили по формулам
Статическое и динамическое светорассеяние измеряли на спектрометре “Photocor Complex” (“Photocor Instruments”, Россия), оснащенном He–Ne-лазером с мощностью 10 мВ (λ = 633 нм). Исследуемые растворы предварительно дважды фильтровали через фильтры Durapore® (“Millipore” США, гидрофилизованный тефлон, диаметр пор 0.22 мкм). Интенсивность рассеяния в экспериментах по статическому рассеянию усредняли по десяти независимым измерениям. Молекулярные массы ПССК, ПЭО и их смеси определяли при угле рассеяния 90°; результаты обрабатывали с использованием уравнения Дебая
где оптическая постоянная раствора K = $\frac{{4{{\pi }^{2}}{{n}^{2}}{{{\left( {\frac{{\partial n}}{{\partial c}}} \right)}}^{2}}}}{{\lambda _{0}^{4}{{N}_{{\text{A}}}}}}$, RΘ – отношение Рэлея, С – концентрация, А2 – второй вириальный коэффициент. Погрешность определения молекулярных масс не превышала 5%.Инкременты показателя преломления растворов ∂n/∂c находили с использованием дифференциального рефрактометра “Optilab T-Rex” (“Wyatt”, США) при λ = 633 нм, погрешность составляла 0.4–1.1%.
Корреляционные функции флуктуаций интенсивности рассеянного света в исследовании динамического светорассеяния измеряли с помощью 288-канального коррелятора “Photocor-FC” с псевдокросскорреляционной системой счета фотонов (“Photocor Instruments”, Россия). Данные обрабатывали программным обеспечением DynaLS. Гидродинамические радиусы макромолекул рассчитывали по коэффициентам диффузии с использованием уравнения Эйнштейна–Стокса
в котором k – постоянная Больцмана, η0 – вязкость растворителя, D – коэффициент диффузии.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Из литературных данных известно, что строение и свойства растворов интерполимерных комплексов в большинстве случаев зависят от концентрационного режима, в котором они находятся [18]. В разбавленных растворах такие комплексы обычно образуют индивидуальные частицы, а в полуразбавленных – межмолекулярные агрегаты, образующие сетку зацеплений. В связи с этим перед изучением комплексообразования в системе ПССК–ПЭО40 000 сначала находили границы концентрационных режимов отдельных компонентов ПССК и ПЭО40 000, а также смеси состава Z = = 0.81. Границы концентрационных режимов в растворах исходных полимеров и смеси определяли методом капиллярной вискозиметрии (рис. 1, 2). Растворы полимеров и их смеси готовили в воде в отсутствие низкомолекулярного электролита. ПЭО – неионогенный полимер, а ПССК в этих условиях – отрицательно заряженный полиэлектролит.
Рис. 1.
Зависимость логарифма удельной вязкости ПЭО40 000 (1) и ПССК (2) от логарифма концентрации. Цветные рисунки можно посмотреть в электронной версии.
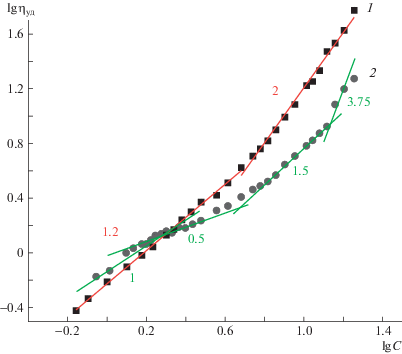
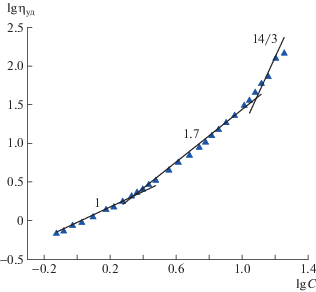
Рис. 2.
Зависимость логарифма удельной вязкости смеси ПССК и ПЭО40 000 (Z = 0.81) от логарифма концентрации.
Концентрационная зависимость удельной вязкости в логарифмических координатах для ПЭО40 000 (рис. 1, кривая 1) состоит из двух линейных участков. Начальный участок (С < 3.6%) имеет угловой наклон 1.2, т.е. в данном диапазоне концентраций ηуд ∝ С1.2, что, согласно скейлинговой модели [19], соответствует разбавленному раствору неионогенного полимера. Концентрация, при которой происходит изменение наклона зависимости, соответствует концентрации кроссовера С* (табл. 1). Угловой наклон второго линейного участка (3.6 < C ≤ 18%) равен двум. Скейлинговое соотношение ηуд ∝ С2 соответствует полуразбавленному режиму раствора без сетки зацеплений для незаряженного полимера. Важно отметить, что в исследованном нами интервале концентраций, вплоть до С = 18%, сетка зацеплений в растворах ПЭО40 000 не образуется.
Таблица 1.
Границы концентрационных режимов для ПЭО40 000, ПССК и смеси ПССК и ПЭО (Z = 0.81)
| Образец | С*, мас. % | Се, мас. % | Сd, мас. % |
|---|---|---|---|
| ПЭО40 000 | 3.6 | >18 | – |
| ПССК | 1.3 | 6.6 | 13 |
| ПССК–ПЭО40 000 | 1.1 | 2.3 | 12 |
Концентрационная зависимость удельной вязкости растворов ПССК (рис. 1, кривая 2) состоит из четырех участков и полностью соответствует скейлинговому описанию растворов полиэлектролитов [20, 21]. В области низких концентраций (С < 1.8%) ηуд ∝ С1, что характерно для разбавленного раствора полиэлектролита в присутствии соли. Несмотря на то, что эксперимент был проведен без добавления низкомолекулярного электролита, незначительное содержание остаточных солей в исходном растворе ПССК создает ненулевую ионную силу раствора. Эффект проявляется только при очень низких концентрациях полиэлектролита, при повышении концентрации вклад собственных противоионов его нивелирует. На втором участке (1.8 < C < 6.6%) ηуд ∝ С0.5, такой показатель степени совпадает со значениями скейлинговой модели для полуразбавленного раствора полиэлектролита без сетки зацеплений. Смена углового наклона после этого участка кривой отвечает концентрации образования зацеплений Ce. В интервале концентраций 6.6 < C < 12% ηуд ∝ С1.5, что соответствует полуразбавленному режиму с сеткой зацеплений. В области высоких концентраций (>13%) ηуд ∝ С3.75, что, согласно скейлинговой модели, соответствует полуразбавленному режиму раствора полиэлектролита с сеткой зацеплений в хорошем растворителе в условиях полного подавления электростатических взаимодействий.
Зависимость для раствора смеси ПССК и ПЭО40 000, Z = 0.81 (рис. 2), отличается как от данных для ПЭО40 000, так и от результатов для ПССК. Начальный участок (C < 2.3%) имеет такой же угловой наклон, как и зависимость ПССК, т.е. отвечает разбавленному раствору полиэлектролита при ненулевой ионной силе. Участок с наклоном 0.5, соответствующий полуразбавленному режиму для полиэлектролитов без сетки зацеплений, исчезает, что указывает на возможное взаимодействие между ПССК и ПЭО40 000. На втором участке (2.3 < C < 12%) угловой наклон составляет 1.7, этот концентрационный интервал можно интерпретировать как полуразбавленный режим для полиэлектролита с сеткой зацеплений. В области высоких концентраций (C > 12%) ηуд ∝ С14/3, что соответствует полуразбавленному раствору полиэлектролита с сеткой зацеплений при полном экранировании электростатических взаимодействий в θ-растворителе. Границы концентрационных режимов представлены в табл. 1.
При смешении двух полимеров разной химической природы в общем растворителе реализуется один из трех вариантов: совместимость (система представляет собой смесь невзаимодействующих компонентов, в которой не наблюдается фазового разделения), несовместимость (сопровождающуюся разделением на фазы, каждая из которых обогащена одним из полимеров) или взаимодействие (в данном случае в растворе образуется интерполимерный комплекс). Для комплексов полиакриловой кислоты с ПЭО, поливинилкапролактамом, поливиниловыми эфирами гликолей и эфирами целлюлозы [6, 22, 23] в разбавленных растворах было установлено значение pHкр, ниже которого происходит осаждение ИПК из раствора. Выше pHкр комплекс существует в растворе в виде гидрофильных растворимых ассоциатов. При pH > pHкр вязкость раствора резко возрастает вследствие разрушения компактной структуры ИПК. Иногда также выделяют pHкр 2, выше которого комплекс разрушается и полимеры сосуществуют в растворе как индивидуальные компоненты. Тогда в области pH < pHкр 1 интерполимерный комплекс существует в виде компактных гидрофобных агрегатов, а в области pHкр 1 < pH < pHкр 2 в виде гидрофильных ассоциатов, в области pH > pHкр 2 взаимодействия не происходит. Таким образом, интерполимерный комплекс (классический ИПК) образован кооперативной системой водородных связей, способствующей компактизации объема взаимодействующих (взаимопроникающих) клубков комплементарных макромолекул (модель “застежка-молния” с дефектами). Гидрофильный ассоциат формируется при участии значительно меньшего количества водородных связей, чем ИПК, при этом макромолекулы ПАК, включенные в состав ассоциата, имеют большую степень ионизации, чем макромолекулы ПАК, образующие обычный ИПК. Формирование интерполимерного гидрофильного ассоциата не сопровождается компактизацией взаимодействующих макроклубков.
Следует отметить, что растворы смесей ПССК–ПЭО40 000, ПССК–ПЭГ2000 и ПССNa–ПЭО40 000 во всем исследованном интервале концентраций и температур остаются прозрачными при любом соотношении полимерных компонентов. Это означает, что несовместимость в исследованных системах не проявляется.
Чтобы выяснить, происходит ли взаимодействие между полимерами в растворе, был использован метод вискозиметрии. В случае отсутствия взаимодействия вязкость смеси должна аддитивно складываться из вязкостей компонентов соответствующей концентрации. Сначала мы исследовали разбавленные растворы исходных компонентов и смесей. На рис. 3 (кривая 1, квадраты) представлена зависимость динамической вязкости смесей ПССК и ПЭО40 000 концентрации 0.5 мас. %. Значению Z = 0 соответствует 0.5%-ный раствор ПССК, значению Z = 1–0.5%-ный раствор ПЭО. Для сравнения на том же рисунке приведена зависимость аддитивной вязкости от состава смеси, рассчитанная в предположении отсутствия взаимодействий по алгоритму [24] (рис. 3, кривая 1').
Рис. 3.
Зависимости динамической вязкости смесей ПССК и ПЭО40 000 при концентрации 0.5 (1), 1 (2) и 3% (3) и соответствующие зависимости аддитивной вязкости смесей ПССК и ПЭО40 000 при концентрации 0.5 (1'), 1 (2') и 3% (3') от состава смеси Z.
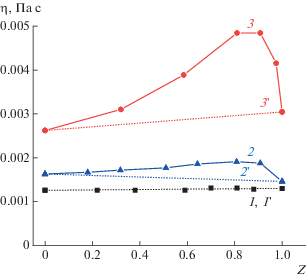
Как видно, динамическая вязкость смеси (рис. 3, кривая 1) практически не отличается от аддитивности (рис. 3, кривая 1'), что свидетельствует об отсутствии взаимодействия двух полимеров при концентрации 0.5%, т.е. в режиме разбавленных растворов. При повышении концентрации до 1 мас. % (рис. 3, кривая 2), что близко к концентрации кроссовера для смеси ПССК и ПЭО40000 состава Z = 0.8, наблюдается незначительное положительное отклонение от аддитивности. Это указывает на появление взаимодействия между компонентами смеси с образованием растворимых комплексов. И, как следует из рис. 3 (кривая 3), в полуразбавленных растворах (3%), динамическая вязкость смеси значительно увеличивается при возрастании Z от нуля до ~ 0.8, остается практически постоянной при повышении Z до 0.9, а затем заметно уменьшается при дальнейшем увеличении Z до 1. Другими словами, наблюдается существенное положительное отклонение от аддитивности (рис. 3, кривая 3'), которое свидетельствует о взаимодействии двух полимеров в системе. Наибольшее отклонение от аддитивности происходит при составах смеси Z = 0.8–0.9, что соответствует максимальной степени связывания полимерных компонентов. Подобное взаимодействие может осуществляться за счет комплексообразования между ПССК и ПЭО40 000 при образовании водородных связей между атомом кислорода в составе цепи ПЭО и атомом водорода в составе сульфогруппы цепи ПССК:
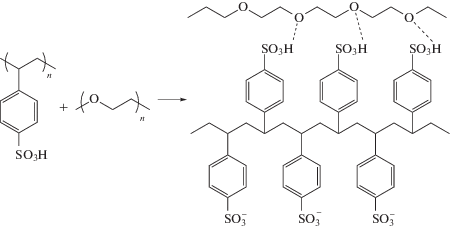
Образование комплексов между ПССК и ПЭО недавно было показано [14], однако только в сильно кислой среде (рН < 0.5) при дополнительном подкислении водных растворов HCl, и только для стехиометричных водонерастворимых комплексов. В настоящей работе впервые детально исследованы водные растворы на основе ПССК и ПЭО без добавления дополнительных подкисляющих агентов (pH ~ 2).
Несмотря на то, что ПССК относится к классу сильных полиэлектролитов, значительная часть сульфогрупп в водных растворах остается неионизованной благодаря эффекту конденсации противоионов [25]. Именно такие недиссоциированные группы способны образовывать водородные связи с атомами кислорода ПЭО, что приводит к формированию комплексов. Состав смесей в области составов Z ≈ 0.8 соответствует мольному соотношению звеньев [ПЭО] : [ПССК] ≈ 4 : 1. Учитывая степени полимеризации ПЭО40 000 (≈900) и ПССК (≈400) можно оценить, что при таком составе Z на одну макромолекулу ПССК в среднем приходится две макромолекулы ПЭО40 000. Избыточные звенья ПЭО40 000 и ионизованные участки ПССК обеспечивают растворимость комплекса. Ниже схематически показано строение комплекса ПССК–ПЭО с максимальными взаимодействиями.
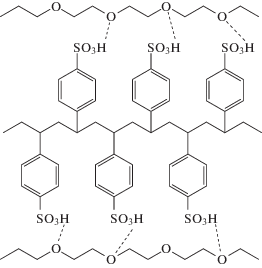
Методом статического светорассеяния были изучены исходные компоненты ПССК и ПЭО40 000 и их смесь состава Z = 0.8 (рис. 4). Все растворы готовили в 0.1 М NaCl, что позволяло проводить измерения в условиях изоионного разбавления. Концентрации рабочих растворов лежали в интервале 0.125–1 мас. %. Все три зависимости в координатах Дебая (КС/R90 от С) являются линейными в изученном интервале концентраций. Это позволяет определить среднемассовые молекулярные массы и вторые вириальные коэффициенты растворов (табл. 2).
Рис. 4.
Данные статического светорассеяния для растворов ПССК (1), ПЭО40 000 (2) и для смеси ПССК–ПЭО40 000 (3). Z = 0.81.
Таблица 2.
Данные статического светорассеяния для ПЭО40 000, ПССК и ПССК–ПЭО40 000 (Z = 0.81)
| Образец | Mw × 10–4 | A2, моль см3 /г2 | $\frac{{\partial n}}{{\partial c}}$, см3/г1 |
|---|---|---|---|
| ПЭО40 000 | 3.36 | 1.93 × 10–3 | 0.1323 |
| ПССК | 7.58 | 2.80 × 10–3 | 0.2019 |
| ПССК–ПЭО40 000 | 5.18 | 7.59 × 10–4 | 0.1677 |
Чтобы выяснить, существует ли комплекс ПССК–ПЭО40 000 в разбавленных водно-солевых растворах (концентрация 0.125–1 мас. %, концентрация NaCl 0.1 моль/л), необходимо рассчитать Мw для смеси в предположении отсутствия взаимодействий и сравнить полученную величину с результатом измерений. Смесь состава Z = 0.81 содержит равные массовые доли ПССК и ПЭО40 000, значит, в отсутствие взаимодействий Мw можно рассчитывать как
Отклонение расчетной величины от измеренной $\frac{{\Delta M}}{M} = 5\% $ не превышает погрешности метода статического светорассеяния. Инкремент показателя преломления $\frac{{\partial n}}{{\partial c}}$ также аддитивно складывается из инкрементов показателей преломления компонентов. Следовательно, в интервале концентраций 1% и ниже в водно-солевой среде комплекс не образуется, и система представляет собой смесь двух полимеров в общем растворителе.
Отсутствие взаимодействия в разбавленном водно-солевом растворе смеси ПССК и ПЭО40000 при концентрации 1% было подтверждено методом динамического светорассеяния. Ниже представлены эффективные гидродинамические радиусы клубков в растворах исходных полимеров и их смеси: Rh = 6 ± 1 для ПЭО40 000 и ПССК, 7 ± 1 для ПССК– ПЭО40 000. Размер клубков в смеси в пределах погрешности метода совпадает с размерами индивидуальных компонентов.
Таким образом, методами вискозиметрии и динамического и статического светорассеяния показано отсутствие взаимодействия в системе ПССК–ПЭО40 000 в режиме разбавленных растворов как в водной, так и в водно-солевой среде.
Из данных, полученных для комплексов ПАК–ПЭО, стабилизированных водородными связями, известно, что интенсивность взаимодействия в таких комплексах определяется длиной цепи ПЭО [26]: степень связывания в значительной степени уменьшается при снижении молекулярной массы ПЭО вплоть до полного отсутствия комплексообразования. В связи с этим необходимо установить, происходит ли образование комплексов ПССК с короткими цепями ПЭО в полуразбавленных растворах. На рис. 5 приведена зависимость динамической вязкости смесей ПССК и ПЭГ2000 от состава Z в сравнении с аналогичной зависимостью для ПССК и ПЭО40 000.
Рис. 5.
Зависимость динамической вязкости смесей ПССК и ПЭГ2000 (1) в сравнении с аналогичной зависимостью для ПССК и ПЭО40 000 (2) и зависимостью аддитивной вязкости смесей ПССК и ПЭГ2000 от состава смеси Z.
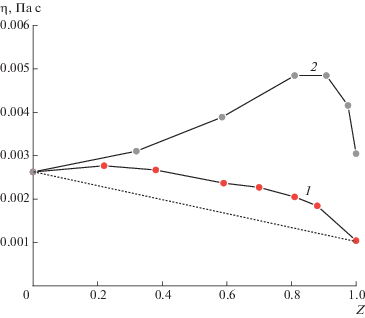
На зависимости, представленной на рис. 5 (кривая 1) видно, что для всех смесей ПССК–ПЭГ2000, как и для смесей ПССК–ПЭО40 000, наблюдается положительное отклонение динамической вязкости от аддитивности, однако оно выражено слабее по сравнению с системой ПССК–ПЭО40 000. Данный факт свидетельствует о том, что взаимодействия ослабевают, но комплексообразование между ПССК и коротким ПЭГ2000 сохраняется. Относительно небольшая величина отклонения от аддитивности не позволяет определить состав смеси, соответствующий максимальному связыванию в системе ПССК–короткоцепной ПЭГ.
Из литературных данных известно, что водородные связи ослабевают при повышении температуры [5], поэтому были измерены зависимости динамической вязкости от состава смеси для комплексов ПССК–ПЭО40 000 и ПССН–ПЭГ2000 (рис. 6) при разной температуре в интервале –60°С.
Рис. 6.
Зависимости вязкости смесей ПССК–ПЭО40 000 (а) и ПССК–ПЭГ2000 (б) от состава при 25 (1), 35 (2), 50 (3) и 60°С (4).
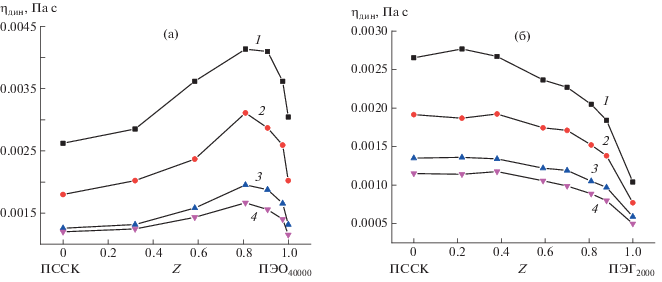
Для обоих комплексов при увеличении температуры положительное отклонение от аддитивности сохраняется, хотя и становится менее выраженным: это означает, что нагревание вплоть до 60°С не приводит к полному разрушению комплексов несмотря на то, что взаимодействия становятся слабее.
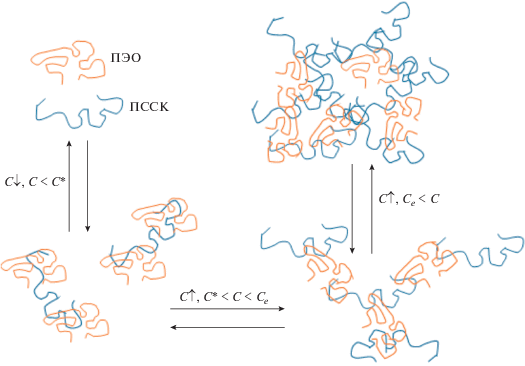
Схема образования и структура комплексов ПССК-ПЭО в различных концентрационных режимах представлена ниже.
ЗАКЛЮЧЕНИЕ
Таким образом, смешение ПССК с ПЭО в водных растворах приводит к образованию растворимых комплексов, максимальное связывание наблюдается при четырехкратном мольном избытке ПЭО. Взаимодействие компонентов существенно ослабевает с ростом температуры, а также с уменьшением длины цепи ПЭО. В полуразбавленном режиме раствора комплекс представляет собой сетку, узлами которой служат цепи ПЭО, связанные водородными связями с соседними клубками ПССК. При понижении концентрации происходит диссоциация комплекса, и в разбавленных водных и водно-солевых растворах система представляет собой совместимую смесь полимеров в общем растворителе. Полученные результаты позволяют предположить возможность аналогичного взаимодействия с другими неионными полимерами, такими как, например, поливиниловый спирт, поливинилпирролидон, полиакриламид, простые эфиры целлюлозы и т.д.
Работа выполнена в рамках проекта “Современные проблемы химии и физикохимии высокомолекулярных соединений” (Госконтракт, регистрационный номер АААА-А16-116031050014-6).
Список литературы
Khutoryanskiy V.V. // Int. J. Pharm. 2007. V. 334. № 1–2. P. 15.
Soldi V., Wilhelm H.M., Soldi M.D.S., Rodrigues J.R.S., Pires A.T.N., Sierakowski M.R. // Polym. Int. 2000. V. 49. № 1. P. 81.
Ye Y.-S., Rick J., Hwang B.-J. //Polymers. 2012. V. 4. P. 913.
Smith K.L., Winslow A.E., Petersen D.E. // Industr. Eng. Chem. 1959. V. 51. № 11. P. 1361.
Bailey Jr F.E., Lundberg R.D., Callard R.W. // J. Polym. Sci. A. 1964. V. 2. №. 2. P. 845.
Шайхутдинов Е.М., Мун Г.А. // Вестн. КазНУ. Сер. хим. 2012. Т. 65. № 1. С. 445.
Nurkeeva Z.S., Mun G.A., Khutoryanskij V.V. // Polymer Science B. 2001. V. 43. № 5. P. 146.
Khutoryanskiy V.V., Mun G.A., Nurkeeva Z.S., Dubolazov A.V. // Polym. Int. 2004. V. 53. P. 1382.
Wang Y., He J., Aktas S., Sukhishvili S.A., Kalyon D. // J. Rheol. 2019. V. 61. № 6. P. 1103.
Matsumura Y., Iwai K. // Polymers. 2019. V. 11. 1196.
Khutoryanskiy V.V., Staikos G. Hydrogen-Bonded Interpolymer Complexes: Formation, Structure and Applications. Singapore: World Scientific, 2009.
Erel I., Schlaad H., Demirel A.L. // J. Colloid Interface Sci. 2011. V. 361. P. 477.
Ma S., Yuan Q., Zhang X., Yang S., Xu J. // Colloids Surf. A. 2015. V. 471. P. 11.
Maldonado L., Debais G., Davia F., De Leo L.P.M., Tagliazucchi M. // Soft Matter. 2019. V. 15. № 45. P. 9318–9324.
Tsai C.-Yi., Chung C.-H., Hong J.-L. // ACS Omega. 2018. V. 3. P. 4423.
Hutchins K.M. // Roy. Soc. Open Sci. 2018. V. 5. P. 180564.
Wang Y., Sukhishvili S.A. // Soft Matter. 2016. V. 12. P. 8744.
Litmanovich E.A., Kotova E.V., Efremov V.V. // Colloid Polym. Sci. 2019. V. 297. № 3. P. 371.
Rubinstein M., Colby R.H. Polymer physics. New York: Oxford Univ. Press, 2003. V. 23.
Boris D.C., Colby R.H. // Macromolecules. 1998. V. 31. № 17. P. 5746.
Dobrynin A.V., Colby R.H., Rubinstein M. // Macromolecules. 1995. V. 28. № 6. P. 1859.
Suleimenov I., Shaltykova D., Sedlakova Z., Mun G., Semenyakin N., Kaldybekov D., Obukhova P. // Appl. Mechanics Materials. 2014. V. 467. P. 58.
Bo Y.J., Khutoryanskiy V.V., Mun G.A., Nurkeeva Z.S. // Polymer Science A. 2002. V. 44. № 10. P. 1094.
Бартенев Г.М., Вишницкая Л.А. // Высокомолек. соед. 1964. Т. 6. № 4. P. 751.
Manning G.S. // J. Chem. Phys. 1969. V. 51. № 3. P. 924.
Антипина А.Д., Барановский В.Ю., Паписов И.М., Кабанов В.А. // А. 1972. Т. 14. № 4. С. 941.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия Б)


