Высокомолекулярные соединения (серия Б), 2022, T. 64, № 2, стр. 116-123
ИЗУЧЕНИЕ ВЗАИМОДЕЙСТВИЯ ПОЛИФЕНИЛСИЛСЕСКВИОКСАНА С БОРНОЙ КИСЛОТОЙ В УСЛОВИЯХ МЕХАНОХИМИЧЕСКОЙ АКТИВАЦИИ
В. В. Либанов a, *, А. А. Капустина a, Н. П. Шапкин a
a Дальневосточный федеральный университет
690950 Владивосток, о-в Русский, пос. Аякс, 10, камп. ДВФУ, корп. L, Россия
* E-mail: libanov.vv@dvfu.ru
Поступила в редакцию 23.09.2021
После доработки 24.11.2021
Принята к публикации 08.12.2021
- EDN: NBQXMI
- DOI: 10.31857/S2308113922020036
Аннотация
В условиях механохимической активации полифенилсилсесквиоксана и борной кислоты синтезированы растворимые полиборфенилсилоксаны с различным мольным соотношением Si : B. Показано, что в условиях механохимической активации растворимый в органических растворителях полиборфенилсилоксан с заданным соотношением Si : B образуется при исходном соотношении полифенилсилсесквиоксана и борной кислоты 2 : 1. Установлено, что для выбранных соединений нецелесообразно увеличение времени активации свыше трех минут из-за деструкции формирующегося высокомолекулярного продукта. Плотность полиборфенилсилоксанов зависит от наличия в полимере кристаллической фазы, исходного соотношения реагирующих веществ и межплоскостного расстояния. Также высказано предположение о возможных механизмах протекающих твердофазных реакций.
ВВЕДЕНИЕ
Модификация полимерных материалов соединениями бора позволяет улучшить термостойкость [1–5], давая возможность применять их в качестве покрытий. Введение в силоксаны наполнителя, содержащего изотопы 10B, содействует эффективному экранированию нейтронного излучения, а также увеличивает стойкость к радиационной нагрузке [6]. Кроме того, силоксаны являются эффективными компонентами, влияющими на термоокислительную стабильность и ударную вязкость полимеров [7–9]. Введение бора и кремния в органические полимеры повышает степень графитизации с одновременным уменьшением размера кристаллитов графита в продуктах карбонизации. Пиролизованные соединения кремния и бора способствуют созданию слоя упорядоченного графитового углерода без пустот [3], усовершенствуют механические и абляционные свойства композитов, армированных волокном [10], а также усиливают адгезионные свойства материалов [11].
Существует множество методов синтеза полиэлементоорганосилоксанов, объединенных одним общим признаком, – все осуществляют в среде органического растворителя. Твердофазный синтез же обеспечивает ряд преимуществ: сравнительная простота процесса, малое время активации, понижение энергетических затрат. На сегодняшний день в условиях механохимической активации синтезированы полиэлементоорганосилоксаны, содержащие в полимерной цепи атомы магния, бора, алюминия, галлия, германия, олова, ванадия и некоторых других [12–19].
На состав и выход конечных продуктов при механохимической активации сильное влияние оказывают природа и соотношение реагирующих веществ [13, 15], наличие в системе воды [14, 20] либо других специально введенных или поступающих извне реагентов (кислород, углекислый газ и другие). Кроме того, необходимо учитывать параметры активатора и условия синтеза – время, число оборотов водила мельницы, соотношение “реагенты : мелющие тела”, температура и т.д. (см., например, работы [21–25]).
В настоящей работе изучено взаимодействие полифенилсилсесквиоксан и борной кислоты в условиях механохимической активации.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Фенилтрихлорсилан перегоняли при температуре 201–202°С. Коммерческие растворители (диэтиловый эфир и толуол) очищали по стандартной методике, физические константы совпадали с литературными данными [26]. Борную кислоту очищали перекристаллизацией из воды (Тпл = 171–172°С).
Синтез полифенилсилсесквиоксана (ПФССО) проводили следующим образом. К интенсивно перемешиваемой смеси 150 мл диэтилового эфира и 250 мл дистиллированной воды добавляли по каплям раствор 100.75 г фенилтрихлорсилана в 150 мл эфира. Синтез осуществляли при температуре –20°С и интенсивном перемешивании. Через 1 ч органический слой отделяли на делительной воронке, промывали дистиллированной водой до нейтральной реакции и сушили безводным сульфатом натрия сутки. Эфир отгоняли, остаток сушили в вакууме при 80°С. С выходом 93.7% получен полифенилсилсесквиоксан состава [C6H5SiO1.5 ∙ ∙ 0.17Н2О]n с содержанием 21.2% Si (вычислено 21.2%).
Взаимодействие ПФССО с борной кислотой в условиях механохимической активации показано в табл. 1. Синтез проводили в планетарной шаровой мономельнице “Pulverisette 6” (“Fritsch”). В качестве активирующей насадки использовали шары из нержавеющей стали диаметром 0.8 см и массой 4.05 г каждый. Соотношение массы насадки к массе полезной загрузки 1.8. Механохимическую активацию осуществляли при скорости 600 оборотов в минуту (10 Гц) в течение 1 мин (опыты 1, 4, 7), 3 мин (опыты 2, 5, 8) и 5 мин (опыты 3, 6, 9).
Таблица 1.
Доля (w) и элементный состав растворимых фракций
| Опыт, № | Время активации, мин | wфр, % | Найдено, % | Атомное соотношение Si : B | |
|---|---|---|---|---|---|
| B | Si | ||||
| Исходное мольное соотношение Si : B = 1 : 1 | |||||
| 1 | 1 | 67.9 | 3.6 | 19.5 | 2.1 |
| 2 | 3 | 70.4 | 3.8 | 20.8 | 2.1 |
| 3 | 5 | 71.2 | 4.1 | 21.6 | 2.0 |
| Исходное мольное соотношение Si : B = 2 : 1 | |||||
| 4 | 1 | 87.1 | 3.3 | 20.1 | 2.3 |
| 5 | 3 | 91.5 | 3.4 | 19.7 | 2.2 |
| 6 | 5 | 90.3 | 3.6 | 20.6 | 2.2 |
| Исходное мольное соотношение Si : B = 3 : 1 | |||||
| 7 | 1 | 92.0 | 2.3 | 21.3 | 3.6 |
| 8 | 3 | 93.8 | 2.6 | 21.9 | 3.2 |
| 9 | 5 | 92.5 | 2.4 | 21.4 | 3.4 |
Реакционную смесь делили на растворимую и нерастворимую фракции экстракцией толуолом в аппарате Сокслета. Фракции сушили в вакууме при температуре 70–75°С до постоянной массы. Содержание кремния и бора в растворимых фракциях представлено в табл. 1. Кремний определяли весовым методом [27], а бор – титриметрически в фильтрате, оставшемся после анализа на кремний [28]. Плотность полимеров оценивали объемным пикнометрическим методом.
ИК-спектры записывали на спектрометре “Hewlett Packard Series 1110 MSD” в бромиде калия. Рентгенофазовый анализ выполняли на приборе “Bruker – AXS D8 Advanced”.
Гель-проникающую хроматографию осуществляли на колонке длиной 980 мм и диаметром 12 мм, заполненной сополимером полистирола с 4% дивинилбензола. Диаметр зерен 0.08–1.0 мм, элюент – толуол, скорость потока 1 мл/мин, величина навески ~0.2 г. Детектирование выполняли весовым методом по содержанию сухого остатка во фракциях. Навеску вещества растворяли в 2 мл толуола и пропускали через колонку. Фракции раствора собирали по 3 мл, растворитель удаляли в сушильном шкафу. Колонку предварительно откалибровывали образцами ПС с различной молекулярной массой.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Взаимодействие ПФССО с борной кислотой в условиях механохимической активации было проведено при атомном соотношении Si : B = 1 : 1, 2 : 1 и 3 : 1, продолжительность активации варьировалась:
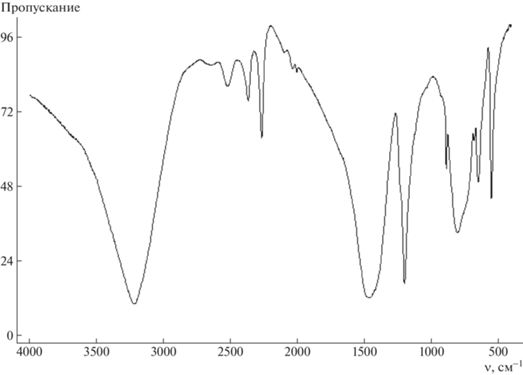
Растворимые фракции опытов 1–9 представляли собой стеклообразные продукты от белого до бледно-желтого цвета; нерастворимые – порошкообразные вещества серо-белого цвета. По данным ИК-спектроскопии, элементного и рентгенофазового анализа нерастворимыми фракциями всех опытов является борная кислота с незначительным содержанием исходного ПФССО и продуктов его превращений. На рис. 1 в качестве примера приведен ИК-спектр нерастворимой фракции опыта 2. Наблюдаемые на ИК-спектре полосы поглощения отвечают колебаниям связей в борной кислоте [29–31].
Рис. 1.
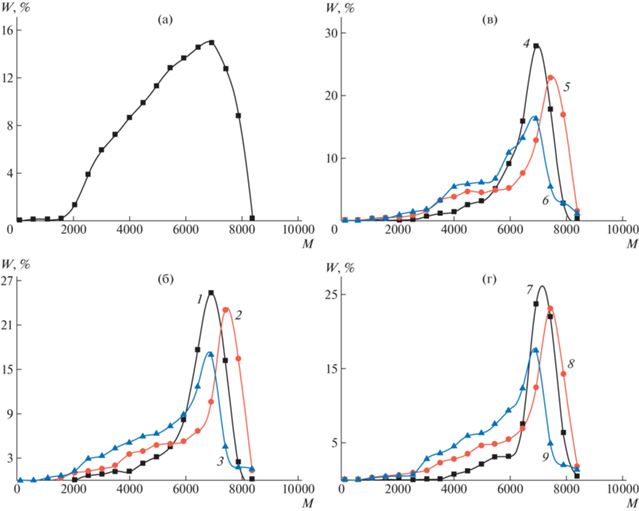
ИК-спектр нерастворимой фракции опыта 2. Здесь и на рис. 2–4 номера кривых соответствуют номерам опытов в таблицах.
Рефлексы на дифрактограммах нерастворимых фракций соответствуют рефлексам борной кислоты со следующими параметрами кристаллической решетки (в скобках приведены литературные данные [32]): а = 7.02501 (7.039) Å, b = = 7.03976 (7.053) Å, c = 6.57216 (6.578) Å; α = 92.5830° (92.58°), β = 101.1329° (101.17°), γ = 119.8058° (119.83о); V = 272.896 (274.07) Å3.
Согласно показаниям ГПХ в составе всех растворимых фракций отсутствуют низкомолекулярные соединения (рис. 2). По сравнению с исходным ПФССО (коэффициент полидисперсности 1.8) для продуктов опытов 1–9 наблюдается уменьшение разброса по молекулярной массе среди макромолекул. Наименее полидисперсными являются фракции 1, 4 и 7, полученные в течение одной минуты механохимической активации. Увеличение времени активации, а также исходного соотношения Si : B, приводило к увеличению полидисперсности.
Данные элементного анализа (см. табл. 1) показывают, что относительные массовые доли растворимых фракций при одинаковом исходном соотношении Si : B с изменением времени обработки менялись незначительно. Одновременно происходило и незначительное увеличение содержания бора в полимерной цепи.
Наиболее близкое к исходному соотношение Si : B было получено в опытах 4–6. Его повышение до 3 : 1 (опыты 7–9) привело к образованию бóльшей доли растворимой фракции, что может быть связано с увеличением длины силоксанового фрагмента в полимерной цепи. Наиболее близкое к заданному соотношение Si : B наблюдалось при трех минутах активации.
ИК-спектры растворимых фракций синтеза опытов 1–6, приведенные на рис. 3 на примере полиборфенилсилоксанов опытов 2 и 5, содержат полосы поглощения в области 1430 и 1130 см–1, соответствующие колебанию связи Si–С6Н5 в силсесквиоксанах, а также широкую полосу в области 1000–1100 см–1 валентных колебаний связи Si–О–Si.
Связь >В–О во фрагменте B–O–Si проявляется в области 1360 см–1, при этом характеристическая полоса становится более интенсивной с увеличением содержания бора в полимере. В области 3400–3200 см–1 прослеживаются колебания связей гидроксильных групп (>B–OH), а также ассоциированной воды (3620 см–1). Наиболее интенсивны эти полосы при исходном соотношении Si : B = 2 : 1. Обращает на себя внимание появление в ИК-спектре полос поглощения в области 1380 см–1, соответствующих колебаниям связи В–О–В.
Согласно данным элементного анализа, ГПХ и ИК-спектроскопии можно предположить, что растворимые фракции опытов 1–6 представляют собой разветвленные полиборфенилсилоксаны (ПБФС), состоящие из четырех звеньев:

Образование указанных структур в ПБФС не противоречит уже имеющимся данным по расщеплению силоксановой связи в условиях механохимической активации [33].
В отличие от опытов 1–6 реакция силоксановой связи борной кислотой при исходном соотношении Si : B = 3 : 1 (опыты 7–9) происходила без образования связи В–О–В, на что указывает отсутствие полос поглощения в области 1380 см–1 (рис. 3).
Кроме того, уменьшается интенсивность полос поглощения в области 3624 и 3414 см–1, свидетельствующая о более полном протекании реакций поликонденсации. Остальные характеристические полосы практически не отличаются от таковых для растворимых фракций опытов 1–6.
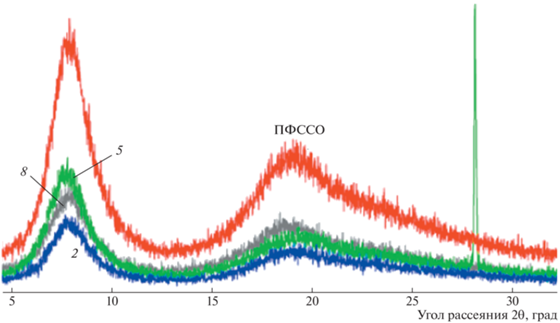
Для более детального изучения влияния атома бора на структуру полиборсилоксанов были сняты рентгенограммы растворимых полиборфенилсилоксанов и исходного ПФССО (рис. 4), а также определены их плотности.
Анализ полученных данных (табл. 2) показал, что значения d1 и d2 с увеличением содержания бора в продуктах опытов 1–3 возрастают.
Таблица 2.
Данные рентгенофазового анализа и значения плотности ПФССО и растворимых фракций опытов 1–9
| Опыт, № | ρ, г/см3 | 2θ, град | Межплоскостное расстояние, Å | ||
|---|---|---|---|---|---|
| d1 | d2 | d3 | |||
| ПФССО | 1.26460 | 8.30 | 11.0100 | – | – |
| 19.40 | – | 4.5500 | – | ||
| 1 | 1.23299 | 7.76 | 11.3946 | – | – |
| 19.40 | – | 4.5754 | – | ||
| 2 | 1.20070 | 7.80 | 11.3375 | – | – |
| 19.12 | – | 4.6409 | – | ||
| 3 | 1.18450 | 7.67 | 11.5208 | – | – |
| 18.78 | – | 4.7248 | – | ||
| 4 | 1.2807 | 7.62 | 11.6019 | – | – |
| 19.29 | – | 4.6008 | – | ||
| 28.17 | – | – | 3.1682 | ||
| 5 | 1.2563 | 7.82 | 11.3076 | – | – |
| 19.28 | – | 4.6049 | – | ||
| 28.03 | – | – | 3.1831 | ||
| 6 | 1.2422 | 7.99 | 11.0674 | – | – |
| 19.60 | – | 4.5297 | – | ||
| 28.08 | – | – | 3.1775 | ||
| 7 | 1.2557 | 7.55 | 11.7074 | – | – |
| 18.79 | – | 4.7238 | – | ||
| 8 | 1.2327 | 7.58 | 11.6577 | – | – |
| 19.16 | – | 4.6334 | – | ||
| 9 | 1.2630 | 7.53 | 11.7388 | – | – |
| 18.96 | – | 4.6801 | – | ||
Увеличение значения d1 свидетельствует об усложнении строения полимерной цепи и увеличении межцепного расстояния в аморфной фазе полимера с ростом содержания в нем бора, что может быть связано с образованием связи В–О–В. Величина d2 соответствует как внутрицепным, так и межцепным межатомным состояниям [34], которые также растут с повышением содержания бора и появлением связи B–O–B.
Сопоставление зависимости плотности ПБФС от содержания в нем бора с величинами межплоскостного расстояния продемонстрировало, что плотность обратно пропорциональна межплоскостному расстоянию. Таким образом, введение бора в силоксановую цепь в синтезе продуктов 1–3, 7–9 в условиях механохимической активации приводит к формированию более рыхлой структуры за счет менее плотной упаковки полимерных цепей.
Дифрактограммы растворимых фракций синтеза продуктов 4–6 заметно отличаются от дифрактограмм, описанных выше. Наряду с первым и вторым гало, соответствующим аморфному состоянию ПБФС, в них появляется третий узкий пик d3, соответствующий кристаллической фазе. Наибольшей интенсивности это отражение достигает в синтезе продукта 4. При переходе от этого образца к образцу 6 происходит уменьшение интенсивности пика, соответствующего кристаллической фазе, за счет повышения интенсивности гало, соответствующего аморфному состоянию.
Как видно из данных рентгенофазового анализа (табл. 2), межплоскостное расстояние d1 тем больше, чем меньше содержание в продукте кристаллической фазы. В отличие от образцов 1–3 и 7–9 плотность соединений 4–6 с ростом межплоскостного расстояния увеличивается, что, по-видимому, связано с наличием кристаллической фазы.
В условиях механохимической активации структура полимеров осложняется рядом других процессов, которые подлежат дальнейшему изучению.
Список литературы
Abdalla M.O., Ludwick A., Mitchell T. // Polymer. 2003. V. 44. № 24. P. 7353.
Lu Y., Gao J., Zhang R. // Polym. Degrad. Stab. 2002. V. 77. № 3. P. 495.
Chandran M.S., Sunitha K., Gayathri D.S., Soumyamol P.B., Mathew D. // J. Mater. Sci. 2018. V. 53. № 4. P. 2497.
Khelevina O.G. // Russ. J. Appl. Chem. 2012. V. 85. P. 277.
Khelevina O.G. // Russ. J. Appl. Chem. 2012. V. 85. P. 1142.
Labouriau A., Robison T., Shonrock C., Simmonds S., Cox B., Pacheco A., Cady C. // Radiation Phys. Chem. 2018. V. 144. P. 288.
Chiang C.-L., Ma C.-C.M. // Polym. Degrad. Stab. 2004. V. 83. № 2. P. 207.
Zhang Y., Lee S., Yoonessi M., Liang K., Pittman Ch.U. // Polymer. 2006. V. 47. № 9. P. 2984.
Zhuo D., Gu A., Liang G., Hu J., Yuan L., Chen X. // J. Mater. Chem. 2011. V. 21. № 18. P. 6584.
Yun J., Chen L., Zhao H., Zhang X., Ye W., Zhu D. // Macromol. Rapid Commun. 2019. V. 40. P. 1800702.
Pan Zh., Huang B., Zhu L., Zeng K. // J. Adhes. Sci. Technol. 2021. V. 35. № 6. P. 626.
Shapkin N.P., Kapustina A.A., Gardionov S.V., Khal’chenko I.G. // Russ. J. Gen. Chem. 2015. V. 85. № 6. P. 1487.
Kapustina A.A., Shapkin N.P., Libanov V.V. // Russ. J. Gen. Chem. 2014. V. 84. № 7. P. 1320.
Libanov V., Kapustina A., Shapkin N., Dmitrinok P., Puzyrkov Z. // Polymer. 2020. V. 194. 122367.
Libanov V.V., Kapustina A.A., Shapkin N.P., Rumina A.A. // Silicon. 2019. V. 11. № 3. P. 1489.
Либанов В.В., Капустина А.А., Шапкин Н.П., Касприк А.Э. // Бутлеровские сообщения. 2015. Т. 41. № 3. С. 18.
Kapustina A.A., Shapkin N.P., Ivanova E.B., Lyakhina A.A. // Russ. J. Gen. Chem. 2005. V. 75. № 4. P. 571.
Kapustina A.A., Shapkin N.P., Gavrilova N.I., Kalugina M.Yu., Bessonova V.I. // Russ. J. Gen. Chem. 2000. V. 70. № 2. P. 241.
Shapkin N.P., Kapustina A.A., Gardionov S.V., Khal’chenko I.G., Libanov V.V., Tokar E.A. // Silicon. 2019. V. 11. № 5. P. 2261.
Tumanov I.A., Michalchuk A.A.L., Politov A.A., Boldyreva E.V., Boldyrev V.V. // Cryst. Eng. Comm. 2017. V. 19. P. 2830.
Michalchuk A.A.L., Tumanov I.A., Boldyreva E.V. // Cryst. Eng. Comm. 2019. V. 21. P. 2174.
Smolyakov V.K., Lapshin O.V., Boldyrev V.V., Boldyreva E.V. // Russ. J. Phys. Chem. 2018. V. 92. P. 2542.
Fischer F., Fendel N., Greiser S., Rademann K., Emmerling F. // Org. Proc. Res. 2017. V. 21. № 4. P. 655.
Uzarevic K., Strukil V., Mottillo C., Julien P.A., Puskaric A., Friscic T., Halasz I. // Cryst. Growth Des. 2016. V. 16. № 4. P. 2342.
Tumanov I.A., Achkasov A.F., Myz S.A., Boldyreva E.V., Boldyrev V.V. // Dokl. Chem. 2014. V. 457. P. 154.
Новый справочник химика и технолога. Основные свойства неорганических, органических и элементоорганических соединений / Под общ. ред. Н.А. Скворцова. СПб.: Мир и семья, 2002.
Крешков А.П. Руководство по анализу кремнийорганических соединений. М.: Госхимиздат, 1962.
Немодрук А.А., Каралова З.К. Аналитическая химия бора (Сер. “Аналитическая химия элементов”). М.: Наука, 1964.
Khazikhanova B.K. // Russ. J. Inorg. Chem. 2013. V. 58. P. 1361.
Jiang W., Jia H., Li H., Zhu L., Tao R., Zhu W., Li H., Dai Sheng // Green Chem. 2019. V. 21. № 11. P. 3074.
Schott J., Kretzschmar J., Acker M., Eidner S., Kumke M.U., Drobot B., Barkleit A., Taut S., Brendler V., Stumpf Th. // Dalton Trans. 2014. V. 43. P. 11516.
Zachariasen W.H. // Acta Crystallogr. 1954. V. 7. P. 305.
Dubinskaya A.M. // Russ. Chem. Rev. 1999. V. 68. № 8. P. 637.
Цванкин Д.Я., Левин В.Ю., Папков В.С., Жуков В.П., Жданов A.A., Андрианов K.A. // Высокомолек. соед. А. 1979. Т. 21. № 9. P. 2126.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия Б)