Химия высоких энергий, 2019, T. 53, № 4, стр. 303-307
Фазовые превращения желирующих веществ в облученных водных растворах
Е. М. Холодкова a, *, А. И. Кастерин a, А. В. Пономарев a
a ФГБУН Институт физической химии и электрохимии им. А.Н. Фрумкина Российской Академии наук
119071 Москва, Ленинский просп., 31, корп. 4, Россия
* E-mail: kholodkova@ipc.rssi.ru
Поступила в редакцию 17.01.2019
После доработки 27.02.2019
Принята к публикации 27.02.2019
Аннотация
Пектин, крахмал, желатин и пшеничная мука в разбавленных водных растворах претерпевают необратимую агрегацию и осаждение уже при поглощенных дозах ниже 1 кГр. Облучение сужает размерное распределение взвешенных частиц в растворе. Отмечено, что эффект облучения обусловлен не только межмолекулярной сшивкой, но и электростатическим влиянием заряженных радиолитических интермедиатов. Снижение агрегативной устойчивости желирующих веществ при облучении их разбавленных растворов может использоваться для практической очистки воды и для направленного синтеза агрегатов с заданным размерным распределением.
ВВЕДЕНИЕ
Гели и суспензии природных загустителей и желирующих веществ широко используются в различных сферах повседневной жизни: в домашнем хозяйстве, фармацевтике, косметологии, терапии, пищевой промышленности, животноводстве, растениеводстве, и т.д. Природа желирующего вещества, его концентрация и температура студнеобразования оказывают существенное влияние на структуру и прочность пространственной упорядоченной сетки макромолекул, создаваемой сольватирующей водой и межмолекулярными водородными связями. Возможность изменять свойства гидрогелей и суспензий посредством ионизирующего излучения представляет практический интерес, прежде всего, для решения задач по очистке сточных вод и по созданию новых медикаментозных средств.
Гидрогели и суспензии довольно часто оказываются в составе производственных и коммунально-бытовых сточных вод [1, 2], затрудняя их очистку. В частности, гидрогели и стойкие суспензии могут замедлять коагуляцию и седиментацию других взвешенных веществ, затруднять применение некоторых реагентов, способствовать обрастанию внутренних поверхностей канализационных трубопроводов биологическими и окисными пленками и т.д. В ряде случаев радиолиз позволяет эффективно снижать агрегативную устойчивость дисперсий в воде и, тем самым, упрощать очистку водных растворов [3, 4].
Гидрогели и суспензии находят широкое применение в медицинской практике. В частности, они используются при лечении ожоговых поражений и кожных заболеваний, при уходе за лежачими больными и др. Однако во многих случаях биосовместимые гели нуждаются в упрочнении, снижении скорости старения, повышении термостойкости и т.п. Радиолиз мог бы служить надежным и чистым способом модифицирования их свойств [5–9].
С другой стороны, гели и суспензии могут служить исходной средой для синтеза нано- и микрочастиц с инкорпорированными лекарствами, катализаторами или стимуляторами, а также для медицинской дозиметрии [10–13]. В зависимости от конкретной задачи, синтезируемые частицы должны обладать специфической термостойкостью, химической активностью, лиофильностью, слипаемостью и т.п. Варьируя свойства синтезируемых оболочек, можно добиваться пролонгированного действия инкорпорированных препаратов. Соответственно радиолиз может служить инструментом для управляемого агрегирования дисперсных частиц и включения в них заданных препаратов.
Таким образом, радиационно-управляемая агрегация желирующих веществ и загустителей в воде является актуальным направлением исследований. В настоящей работе изучали изменение агрегативной устойчивости пектина, крахмала, желатина, пшеничной муки и некоторых их смесей в разбавленных водных растворах под действием ускоренных электронов при низких поглощенных дозах.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Пектин, кукурузный крахмал, желатин и пшеничная мука высшего сорта были приобретены в розничной торговой сети. Растворы готовили на дистиллированной воде в процессе 2-минутного кипячения с обратным холодильником при непрерывном перемешивании. Растворы облучались ускоренными электронами (линейный электронный ускоритель УЭЛВ-10-10Т энергия 8 МэВ, длительность импульса 6 мкс, частота повторения импульсов 300 Гц, средний ток пучка ≤ 800 мкА, ширина развертки 245 мм, частота развертки 1 Гц). Для дозиметрии использовали пленочные дозиметры СО ПД(Ф)Р-5/50 (ГСО 7865-2000). Мощность дозы составляла от 0.05 до 0.15 кГр/с.
Оптические измерения выполнялись с использованием спектрофотометра “Cary-100” UV-Vis. Следили за ослаблением света в растворах, которое соответствовало величине –lg10T, где T = I/I0 коэффициент пропускания образца (I0 и I – интенсивности падающего света и света, прошедшего через образец). Измеряемое ослабление представляло собой совокупность поглощения и рассеяние света. Мутность растворов анализировалась с помощью турбидиметра Turb 550 IR с использованием стандартных дисперсий (0.1-1000 NTU). Динамическое рассеяние света в образцах измерялось с помощью Delsa Nano C Beckman Coulter Particle Analyzer. Мутность и оптические спектры измерялись через 10 мин после облучения.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Желатин получают из белков (коллагена) и пептидов животного происхождения, тогда как пектин, крахмал, и мука являются материалами растительного происхождения, представляющими собой преимущественно полисахариды. В исходной муке, наряду с крахмалом, также содержатся белки (глютен), липиды и пектин, содержание которых составляло 12.5, 0.8 и 1.9 мас. % соответственно. Вместе с тем, все четыре исследуемых вещества – желатин, пектин, крахмал и мука – обладают желирующими свойствами и применяются на практике как загустители и желирующие агенты. При растворении в кипящей воде желатин, пектин и крахмал образуют прозрачные растворы, не содержащие визуально наблюдаемых взвешенных частиц. Соответственно, исходная мутность таких растворов, при концентрации желирующих добавок 0.5 мас. %, не превышает 6 NTU. В свою очередь, свежий раствор муки оказывается мутным. С течением времени наблюдается осаждение агрегатов, состоящих, в основном, из глютена. Остаточная мутность раствора муки перед облучением достигала 30 NTU.
Облучение при комнатной температуре вызывает изменение агрегативной устойчивости исследуемых водных дисперсий. В изначально прозрачном растворе 0.1 мас. % желатина, уже при поглощенной дозе 0.5 кГр, наблюдается образование взвешенных частиц сферической формы и их постепенное осаждение в течение примерно 30 мин. С ростом поглощенной дозы скорость осаждения частиц увеличивается.
В растворах 0.25 мас. % крахмала, также как в растворах пектина, облучение порождает бесформенные сгустки, хлопья и нити, которые медленно оседают на дно сосуда. В растворе крахмала быстрое снижение мутности наблюдается невооруженным глазом в течение первой минуты после облучения, тогда как в растворах пектина и муки мутность остается сравнительно высокой даже через 10 мин после облучения.
Оптические спектры необлученных растворов являются бесструктурными. Ослабление света, вызванное поглощением и рассеянием, монотонно уменьшается с ростом длины волны (рис. 1 и 2). Такие спектры характерны для неокрашенных растворов соединений, находящихся во взвешенном состоянии. Под действием ускоренных электронов, в оптических спектрах облученных растворов появляется специфическая полоса с максимумом ≈263 нм, которая указывает на изменение состояния примесей, обусловленное их взаимодействием с продуктами радиолиза воды. В растворе желатина эта полоса становится незаметной при дозах выше 2 кГр – спектр вновь становится бесструктурным. В свою очередь, в растворах других желирующих веществ интенсивность полосы возрастает монотонно с дозой.
Рис. 1.
Ослабление света (ОС) в индивидуальных водных растворах (0.25 мас. %) желатина (1), крахмала (2) и пектина (3) до облучения (а) и после облучения (б) при дозе 1 (1) и 6 (2, 3) кГр.

Рис. 2.
Ослабление света (ОС) в (а) смешанном водном растворе 0.5 мас. % желатина и 0.5 мас. % крахмала и (б) в водном растворе 0.25 мас. % пшеничной муки при дозах 0 (1), 0.5 (2) и 6 (3) кГр.

Облучение изменяет вклад рассеяния в общее ослабление света исследуемыми дисперсиями. В растворе крахмала ослабление света в видимой области спектра, измеренное через 10 мин после облучения, монотонно уменьшается с дозой (рис. 3). Напротив, в растворе желатина при поглощенных дозах 0.5–2 кГр наблюдается просветление, а при более высоких дозах прозрачность растворов вновь убывает. Измерение мутности показывает, что в растворах желатина и крахмала наблюдаются противоположные эффекты – через 10 мин после облучения в желатиновом растворе мутность тем выше, чем выше доза (вплоть до 3 кГр), тогда как в растворе крахмала мутность монотонно убывает с ростом дозы. Эти различия указывают на более быструю агрегацию и осаждение крахмала в облученных водных растворах. Несмотря на то, что мука на 80–82% состоит из крахмала, ослабление света в индивидуальных растворах крахмала и растворах муки изменяется с дозой по-разному. В растворе муки, ослабление света и мутность при низких дозах (до 4 кГр) возрастают (рис. 4).
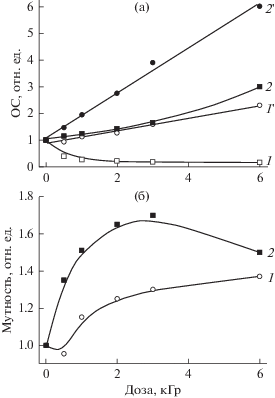
Рис. 3.
Влияние дозы на (а) ослабление света при 263 ± 2 нм (1 ' и 2 ') и 450 нм (1 и 2) и (б) на мутность в индивидуальных растворах желатина (1 и 1 ') и крахмала (2 и 2 ').

Рис. 4.
Влияние дозы на (а) ослабление света при 263 ± 2 нм (1' и 2') и 450 нм (1 и 2) и (б) на мутность в смешанном растворе 0.5 мас. % желатина и 0.5 мас. % крахмала (1 и 1 ') и в растворе 0.25 мас. % пшеничной муки (2 и 2 ').
После встряхивания отстоявшихся облученных растворов их просветление происходит быстрее, чем свежеоблученных. Такой эффект может указывать, с одной стороны, на пост-радиационное укрупнение агрегатов и, с другой стороны, на необратимость этого укрупнения и устойчивость получающихся укрупненных частиц.
Поскольку растворы желатина и крахмала существенно различаются по скорости осаждения радиационно-индуцированных агрегатов, представляет интерес поведение водных суспензий желатин/крахмал. Для исследования использовался комбинированный раствор желатина и крахмала, содержащий по 0.5 мас. % обоих компонентов. Как оказалось, эти компоненты взаимодействуют друг с другом в растворе еще до облучения и частично трансформируются в рыхлые взвешенные частицы, которые выпадают на дно. Тем не менее, растворы остаются мутными не менее получаса, и их мутность возрастает при облучении (рис. 4).
Результаты анализа динамического рассеяния света в растворах желатин/крахмал сразу после их встряхивания показывают, что в необлученном растворе мутность обусловлена частицами с широким разнообразием размеров (рис. 5а). В результате облучения образуется быстроосаждающая фракция крупных частиц, однако в растворе остаются мелкие взвешенные частицы. Рис. 5а показывает, что в остаточном рассеянии участвуют частицы с более узким размерным распределением, чем в необлученном растворе. Причем, чем выше доза, тем более мелкие частицы участвуют в остаточном рассеянии (рис. 5б и с).
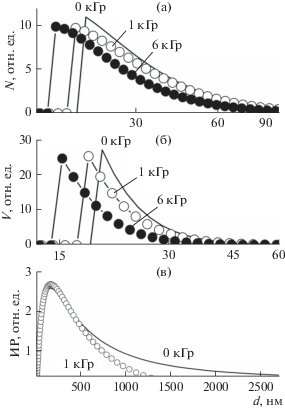
Рис. 5.
Влияние дозы на распределение (а) числа N и (б) объема V остаточных дисперсных частиц в смешанном растворе 0.5 мас. % желатина и 0.5 мас. % крахмала в зависимости от их диаметра d и (в) на вклад дисперсных частиц разного диаметра в интенсивность рассеяния света ИР.
Очевидно, радиолитическая трансформация растворенного вещества в разбавленном растворе происходит за счет косвенного действия излучения [14]. Поглощенная доза 0.5 кГр является сравнительно невысокой. Исходя из того, что выход образования наиболее реакционноспособных частиц (е-, ОН и Н) в объеме воды составляет около 6 молекул/100 эВ, можно оценить, что доза 0.5 кГр позволяет генерировать в воде примерно 3.1 × 10–4 М реакционноспособных ионов и радикалов. Причем большая часть этих частиц гибнут в реакциях друг с другом. Оцененная концентрация почти в 100 раз меньше, чем концентрация, например, альфа-глюкозных звеньев в 0.5% растворе крахмала. То есть, на каждую макромолекулу (мольная масса около 20 000) приходится в среднем по 1 или 2 короткоживущих интермедиата. В этих условиях косвенное действие излучения вряд ли может приводить к существенным химическим изменениям макромолекул. Следовательно, наряду с межмолекулярной сшивкой, на агрегацию мицелл могут оказывать влияние электростатические взаимодействия с участием радиолитических ионов [3, 15].
ЗАКЛЮЧЕНИЕ
Таким образом, агрегация и осаждение желирующих веществ, таких как желатин, крахмал, пектин, мука и их смеси в водных растворах, исходно обладающих кинетической стабильностью, могут инициироваться ионизирующим излучением без использования каких-либо вспомогательных реагентов. В результате происходит просветление растворов и снижение их остаточной мутности. Наиболее быстрое осаждение происходит в растворах крахмала. Параллельно уменьшается размерное разнообразие остаточных взвешенных веществ. Для эффективной агрегации и осаждения достаточны весьма невысокие поглощенные дозы – до 0.5 кГр. Данные эффекты могут найти практическое применение в подготовке питьевой воды, очистке сточных вод и в приготовлении микро- и наноагрегатов желирующих веществ.
Настоящая работа выполнена в рамках государственной темы АААА-А16-116121410087-6 с помощью оборудования, предоставленного Центром коллективного пользования физическими методами исследования ИФХЭ РАН.
Список литературы
Pikaev A.K., Ponomarev A.V., Bludenko A.V., Minin V.N., Elizar’eva L.M. // Radiation Physics and Chemistry. 2001. V. 61. Issue 1. P. 81.
Han B., Kim J., Kim Y., Choi J.S., Makarov I.E., Ponomarev A.V. // Water Science and Technology. 2005. V. 52. P. 317.
Bludenko A.V., Zhestkova T.P., Zhukova T.N., Pono-marev A.V. // High Energy Chemistry. 2006. V. 40. Issue 6. P. 370.
Metreveli P.K., Metreveli A.K., Ponomarev A.V., Bludenko A.V., Chulkov V.N. // High Energy Chemistry. 2014. V. 48. Issue 4. P. 225.
Zhou Y., Zhao Y., Wang L., Xu L., Zhai M., Wei S. // Radiat. Phys. Chem. 2012. V. 81. P. 553.
Singh B., Bala R. // Radiat. Phys. Chem. 2014. V. 103. P. 178.
Nho Y.-C., Park J.-S., Lim Y.-M. // Radiat. Phys. Chem. 2014. V. 94. P. 176.
Makuuchi K. // Radiat. Phys. Chem. 2010. V. 79. P. 267.
Furusawa K., Terao K., Nagasawa N., Yoshii F., Kubota K., Dobashi T. // Colloid Polym. Sci. 2004. V. 283. P. 229.
Queiroz R.G., Varca G.H.C., Kadlubowski S., Ulanski P., Lugão A.B. // Int. J. Biol. Macromol. 2016. V. 85. P. 82.
Demeter M., Virgolici M., Vancea C., Scarisoreanu A., Kaya M.G.A., Meltzer V. // Radiat. Phys. Chem. 2017. V. 131. P. 51.
Cieśla K., Sartowska B., Królak E. // Radiat. Phys. Chem. 2015. V. 106. P. 289.
Davies J.B., Bosi S.G., Baldock C. // Radiat. Phys. Chem. 2012. V. 81. P. 1263.
Woods R.J., Pikaev A.K. Applied Radiation Chemistry: Radiation Processing, Wiley-Interscience. New York, 1994.
Metreveli P.K., Kholodkova E.M., Ponomarev A.V. // Radiat. Phys. Chem. 2016. V. 124. P. 216.
Дополнительные материалы отсутствуют.
Инструменты
Химия высоких энергий


