Химия высоких энергий, 2022, T. 56, № 1, стр. 22-26
Хемосенсор с “включением” люминесценции для детектирования паров аммиака
Н. В. Петроченкова a, b, А. Г. Мирочник a, **, Т. Б. Емелина a, *, Д. С. Ионов c, И. В. Ионова c, В. А. Сажников c
a Институт химии Дальневосточного отделения РАН
690022 Владивосток, Россия
b Морской государственный университет им. адм. Г.И. Невельского
690059 Владивосток, Россия
c Центр фотохимии ФНИЦ “Кристаллография и фотоника” РАН
119421 Москва, Россия
** E-mail: mirochnik@ich.dvo.ru
* E-mail: maks-im2@mail.ru
Поступила в редакцию 27.06.2021
После доработки 24.08.2021
Принята к публикации 28.08.2021
- EDN: GMTNBP
- DOI: 10.31857/S0023119322010090
Аннотация
Обнаружены люминесцентные хемосенсорные свойства дибензоилметаната Eu(III) с капроновой кислотой. Показано, что взаимодействие хелата Eu(III) с парами аммиака приводит к увеличению интенсивности люминесценции комплекса. Экспериментально определенный предел обнаружения аммиака составил 3 ppm. Установлена обратимость оптического отклика. Полученная хемосенсорная композиция с эффектом “включения” люминесценции при воздействии аналита перспективна для мониторинга окружающей среды.
ВВЕДЕНИЕ
Анализ опубликованных данных показывает устойчивый рост числа исследований в области разработки смарт-материалов, характеризующихся люминесцентными хемосенсорными свойствами. Следует отметить, что люминесцентные редкоземельные координационные соединения являются перспективными объектами для разработки новых хемосенсоров [1–6].
Наличие сверхчувствительных f-f-переходов в спектрах европия(III) позволяет обнаружить тонкие изменения в координационной сфере люминесцентного центра при воздействии аналита. Преимуществом лантанидных хемосенсоров является наличие потенциально большого числа механизмов и типов взаимодействий “субстрат-аналит” (водородные связи, стекинг-взаимодействия и т.д.) [7–10]. Следует отметить, что в большинстве случаев при взаимодействии лантанидного комплекса с аналитом регистрируется тушение люминесценции [10]. Более перспективными являются хемосенсорные системы с “включением” люминесценции при взаимодействии с аналитом из-за их более высокой селективности и чувствительности [11]. Ранее нами обнаружены подобные хемосенсорные системы на основе комплексов европия(III) с “включением” люминесценции [12–14].
В данной работе исследовано взаимодействие комплекса европия Eu(Dbm)2Kapron (Dbm – дибензоилметанат-ион, Kapron – анион капроновой кислоты) с аммиаком. Аммиак токсичен, его высокие концентрации губительны для живых организмов [15], поэтому уверенное детектирование этого аналита является актуальным.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Комплекс Eu(Dbm)2Kapron, где Dbm – дибензоилметанат-ион, Kapron¯ – анион капроновой кислоты, синтезирован по методике, описанной в [16]. Навеску 0.0048 моль HDbm растворяли при нагревании (40–50°C) в 40 мл этанола, добавляли 0.0024 моль спиртового раствора Eu(NO)3·6H2O, к полученному раствору по каплям при постоянном перемешивании приливали 0.0024 моль кислоты HKapr. Реакционную смесь нейтрализовали при перемешивании спиртовым раствором аммиака до pH 8. Выпавший осадок отфильтровывали, промывали горячим этанолом и сушили на воздухе.
Элементный анализ выполнен на приборе EURO EA 3000. Данные элементного анализа EuC36H33O6:
Вычислено: С – 60.23; Н – 4.60; Eu – 21.03.
Найдено: С – 60.49; Н – 4.67; Eu – 21.43.
Хроматографические ТСХ пластины Sorbfil PTSKh-AF-A использовали как матрицу для иммобилизации комплекса европия. Для приготовления полиэтиленовых пленок смесь порошка полиэтилена (Alfa Aesar) тщательно перемешивали с комплексом европия и прессовали на гидравлическом прессе (p = 8 MPa, T = 130°C).
Спектры люминесценции и возбуждения люминесценции образцов при 300 K регистрировали на спектрофлуориметре RF-5301 (Shimadzu).
Количественные измерения люминесцентного отклика при воздействии аммония на комплекс европия проводили с использованием экспериментальной установки, детально описанной в [17], в состав которой входит 8-канальный оптоволоконный спектрометр S2000 (Ocean Optics).
Образцы размером 5 × 5 мм помещали в экспериментальную камеру, обращенную к газовому каналу. Отражательные зонды OceanOptics с 6 световыми волокнами и одним чувствительным волокном были размещены на передней поверхности образцов под углом 30° к нормали стекла. В качестве источника возбуждения использовались светодиоды Nichia NSHU591A с фильтрами UG-1. Генератор газовой смеси Microgas-F46, использующий метод проникающей трубки, использовался для создания концентрации аммиака в диапазоне 3–263 ppm. В качестве газа-носителя использовался воздух относительной влажности 10%. Чистый воздух или газовые смеси подавались в камеру с помощью автоматических клапанов. Газовые смеси подавались в камеру в течение 4 ч с последующей подачей чистого воздуха в течение 4 ч перед введением других смесей. Спектры регистрировались один раз в минуту.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
На рис. 1 приведены спектры люминесценции и возбуждения люминесценции комплекса Eu(Dbm)2Kapron (I) до воздействия и после воздействия паров аммиака. Воздействие паров аммиака приводит к заметному увеличению интенсивности люминесценции комплекса I, в отличие от большинства комплексов лантаноидов, для которых наблюдается тушение люминесценции под действием аналита [10, 12, 18, 19].
Рис. 1.
Спектры возбуждения люминесценции (a) (λлюм = 615 нм) и люминесценции (б) (λвозб = 370 нм) комплекса Eu(Dbm)2Kapron, адсорбированного на ТСХ-пластине: 1 – исходный образец, 2 – образец, обработанный аммиаком (300 К).
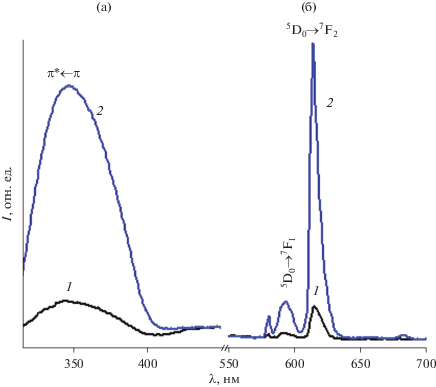
Следует отметить, что исследуемый комплекс европия обладает слабой люминесценцией при комнатной температуре. Однако при воздействии паров аммиака интенсивность свечения значительно возрастает (рис. 1).
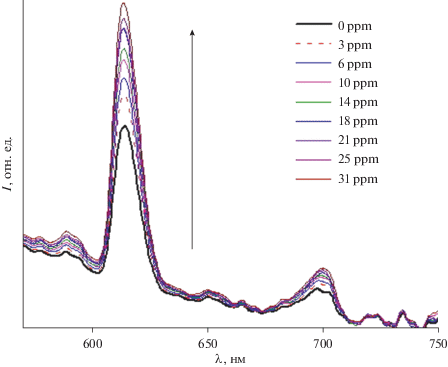
Результаты количественных измерений люминесцентного отклика хемосенсора I приведены на рис. 2: представлены зависимости интенсивности люминесценции I при низких концентрациях паров аммиака в ячейке от времени измерения. Как видно из рисунка, уже при низких концентрациях аналита наблюдается отчетливый люминесцентный отклик хемосенсора: при увеличении концентрации аналита в диапазоне 3–30 ppm последовательно растет интенсивность люминесценции Eu(III). Экспериментально определенный предел обнаружения аммиака составил 3 ppm (максимально допустимая концентрация для NH3 [16]).
Рис. 2.
Эволюция спектров люминесценции комплекса Eu(Dbm)2Kapron при низких концентрациях паров аммиака (λвозб = 370 нм) (300 K).
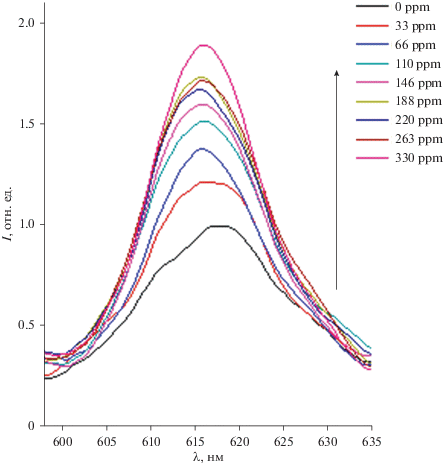
В настоящее время актуальной задачей является разработка высокочувствительных оптических лантанидных хемосенсоров на основе полимерных материалов, в частности, полиэтилена. Преимуществами полиэтилена являются инертность, негигроскопичность и относительная фотостабильность. Комплекс I показал хорошую совместимость с полиэтиленовой матрицей. На рис. 3 представлена эволюция спектра люминесценции при действии паров аммиака на комплекс I в полиэтилене (высокие концентрации аналита). Установлено, что в результате воздействия аммиака на полимерные композиты наблюдается значительный оптический отклик: регистрируется двукратное увеличение интенсивности люминесценции в диапазоне концентраций аналита 3–330 ppm (рис. 3).
Рис. 3.
Эволюция спектров люминесценции комплекса Eu(Dbm)2Kapron в полиэтилене при высоких концентрациях паров аммиака (λвозб = 370 нм) (переход 5D0–7F2) (300 K).
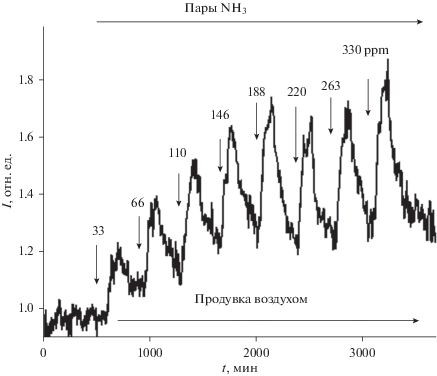
Установлена обратимость оптического отклика при подаче аммиака в ячейку с последующей ее продувкой воздухом (рис. 4). Регистрировалась интенсивность люминесценции полосы 615 нм под переменным потоком воздуха – насыщенного и ненасыщенного аммиаком. Из данных рис. 4 видно, что при воздействии паров аммиака наблюдается быстрое возрастание интенсивности люминесценции и быстрое восстановление сигнала почти до исходного значения при продувке воздухом.
Рис. 4.
Обратимость люминесцентного отклика комплекса Eu(Dbm)2Kapron в полиэтилене в присутствии паров аммиака и при продувке воздухом (λлюм = 615 нм, λвозб = 370 нм) (300 K).
Таким образом, установлено, что при взаимодействии исследуемого комплекса Eu(Dbm)2Kapron с парами аммиака в диапазоне концентраций 3–330 ppm наблюдается отчетливый люминесцентный отклик: возрастание интенсивности люминесценции электродипольного перехода 5D0–7F2 в два раза.
ВЫВОДЫ
Обнаружены люминесцентные хемосенсорные свойства комплекса Eu(Dbm)2Kapron. Показано, что взаимодействие хелата Eu(III) с парами аммиака приводит к увеличению интенсивности люминесценции Eu(III). В диапазоне концентраций 3–330 ppm наблюдается отчетливый люминесцентный отклик: возрастание интенсивности люминесценции электродипольного перехода 5D0–7F2 в два раза. Экспериментально определенный предел обнаружения аммиака составил 3 ppm (максимально допустимая концентрация для NH3). Установлена обратимость оптического отклика. Полученная хемосенсорная композиция с эффектом “включения” люминесценции при воздействии аналита перспективна для мониторинга окружающей среды.
Список литературы
Hu H., Cao C.-S., Kang X.-M., Zhao B. // Dalton Trans. 2016. V. 45. P. 18003. https://doi.org/10.1039/C6DT02213H
Bell T.W., Next N.M. Artificial receptors for chemosensors, C.A. Taitt (Eds.) // Optical Biosensors: Present and Future. Elsevier Science. 2002. P. 331.
Hu Z., Deibert B.J., Li J. // Chem. Soc. Rev. 2014. V. 43. P 5615. https://doi.org/10.1039/C4CS00010B
Cui Y., Yue Y., Qian G., Chen B. // Chem. Rev. 2012. V. 112. P. 1126. https://doi.org/10.1021/cr200101d
Rocha J., Carlos L.D., Paz F.A.A., Ananias D. // Chem. Soc. Rev. 2011. 40. P. 926. https://doi.org/10.1039/C0CS00130A
Roy1 S., Chakraborty A., Maji T.K. // Coord. Chem. Rev. 2014. V. 273–274. P. 139. https://doi.org/10.1016/j.ccr.2014.03.035
Cui Y., Chen B., Qian G. // Coord. Chem. Rev. 2014. V. 273–274. P. 76. https://doi.org/10.1016/bs.hpcre.2016.04.001
Mahata P., Mondal S.K., Singha D.K., Majee P. // Dalton Trans. 2017. V. 46 P. 301. https://doi.org/10.1039/C6DT03419E
Hu S.M., Niu H.L., Qiu L.G., Yuan Y.P., Jiang X., Xie A.J., Shen Y.H., Zhu J.F. // Inorg. Chem. Comm. 2012. V. 17. P. 147. https://doi.org/10.1016/j.inoche.2011.12.037
Aulsebrook M.L., Graham B., Grace M.R., Tuck K.L. // Coord. Chem. Rev. 2018. V. 375 P. 191. https://doi.org/10.1016/j.ccr.2017.11.018
Germain M.E., Knapp M.J. // Chem. Soc. Rev. 2009. V. 38. P. 2543.
Mirochnik A.G., Petrochenkova N.V., Shishov A.S., Bukvetskii B.V., Emelina T.B., Sergeev A.A., Voznesenskii S.S. // Spectrochim. Acta A. 2016. V. 155. P. 111. https://doi.org/10.1016/j.saa.2015.11.004
Voznesenskii S.S., Sergeev A.A., Mirochnik A.G., Leonov A.A., Petrochenkova N.V., Shishov A.S., Emelina T.B., Kulchin Yu.N. // Sensors and Actuators B: Chem. 2017. V. 246. № 7. P. 46. https://doi.org/10.1016/j.snb.2017.02.034
Petrochenkova N.V., Mirochnik A.G., Emelina T.B., Sergeev A.A., Leonov A.A., Voznesenskii S.S. // Spectrochim. Acta A. 2018. V. 200. P. 70. https://doi.org/10.1016/j.saa.2018.03.084
Timmer B., Olthuis W., Berg A. // Sens. Actuators. B. 2005. V. 107. P. 666. https://doi.org/10.1016/j.snb.2004.11.054
Karasev V.E., Petrochenkova N.V., Mirochnik A.G., Petukhova M.V., Lifar L.I. // Rus. J. Coord. Chem. 2001. V. 27. № 10. P. 746.
Khlebunov A.A., Ionov D.S., Komarov P.V., Aristarkhov V.M., Sazhnikov V.A., Petrov A.N., Alfimov M.V. // Instruments Exp. Tech. 2009. V. 52. P. 132. https://doi.org/10.1134/S0020441209010229
Mu Y., Ran Y., Du J., Wu X., Nie W., Zhang J., Liu H. // Polyhedron. 2017. V. 124. P. 125–130. https://doi.org/10.1016/j.poly.2016.12.030
Wang W., Yang J., Wang R., Zhang L., Yu J., Sun D. // Crystal Growth & Design. 2015. V. 15. № 6. P. 2589. https://doi.org/10.1021/acs.cgd.5b00381
Дополнительные материалы отсутствуют.
Инструменты
Химия высоких энергий


