Физикохимия поверхности и защита материалов, 2020, T. 56, № 2, стр. 132-137
Исследование структурной организации поверхностного слоя и состояния воды в ультрафильтрационных композиционных мембранах
С. И. Лазарев 1, *, Ю. М. Головин 1, И. В. Хорохорина 1, П. А. Хохлов 1
1 Федеральное государственное бюджетное образовательное учреждение высшего образования
Тамбовский государственный технический университет
392000 Тамбов, ул. Советская, 106, Россия
* E-mail: geometry@mail.nnn.tstu.ru
Поступила в редакцию 05.12.2018
После доработки 16.01.2019
Принята к публикации 12.02.2019
Аннотация
Исследованы структурная организация поверхностного (активного) слоя и состояние воды в ультрафильтрационных композиционных мембранах методами колебательной ИК-спектроскопии и дифференциально-сканирующей калориметрии (ДСК). Анализ формы полосы поглощения валентных колебаний гидроксильных групп при ν = 3366.2 см–1 с коэффициентом ассимметричности ~1 и активности колебаний метильных групп с ν = 2884.02 и 2942.35 см–1, показал, что обьемная надмолекулярная структура ацетат целлюлозного слоя сухого образца образована двумя типами водородных связей и диполь-дипольными взаимодействиями карбонильных групп. Взаимодействие макромолекул в экваториальной плоскости формируется сеткой водородных связей типа (ОН...О) с участием единственной гидроксильной группы пиранозного кольца в ацетатах целлюлозы. В аксиальном направлении надмолекулярная структура организована за счет водородных связей между метинными и карбонильными группами типа (СН…О=С) и дипольными взаимодействиями компланарно упорядоченных диполей (С=О) групп. Уменьшение интенсивности и коэффициента ассимметричности до 0.81 полосы поглощения гидроксильных групп и полосы поглощения метильных групп с частотами ν = 2884.02–2942.35 см–1 в 2.56 и 3.3 раза в водонасыщенных образцах происходит из–за разрушения надмолекулярной структуры и реорганизации водородных связей активных групп ацетата целлюлозы и молекул воды, которые блокируют межмолекулярные взаимодействия макромолекул. Проявление на полосе поглощения гидроксильных групп частот 3302.7 “пл” см–1, ν = 33105 “пл” см–1 и ν = 3600.6 “пл.” см–1 ν = 3598.8 “пл.” см–1 свидетельствует о взаимодействии ассоциированных молекул воды связанной и капиллярной формы. Отсутствие полосы поглощения с ν = 873.53 см–1 в воднонасыщенном образце объясняется как эмпирический показатель конформационного перехода макромолекул в линейную форму. Деконволюция эндотермического пика на кривой ДСК в интервале температур от 50 до 110°С на пять гауссианов доказывает многоуровневую структурную организацию молекул воды, сорбированной в порах и между макромолекулами аморфной фазы.
ВВЕДЕНИЕ
Мембранные методы разделения растворов привлекают внимание исследователей благодаря низкому потреблению энергии и экологичности, так. как затраты энергии используются только на разрыв межмолекулярных связей без фазовых превращений. При ультрафильтрационном получении ультрачистой воды, промышленной очистке сточных вод и концентрации биологических агентов, процессы отделения растворенного вещества от растворителя происходят в поверхностном (активном) слое. Однако при этом происходит осаждение и адсорбция макромолекулы на ультрафильтрационных мембранах, что вызывает загрязнение активного слоя мембраны, сокращая их срок службы [1–3]. Для этого мембранные материалы подвергают модификациям с последующим исследованием структурно-кинетических характеристик активного слоя. Например, авторы работ [4–6] применяют такие методы, как плазменная обработка, метод радикальной полимеризации с переносом атомов, синтез сшитых полимеров. Так, в работе [7] методом растровой электронной микроскопии проведен сравнительный анализ влияния структурных изменений мембран МА-40 и МА-41 на их физико-химические свойства в результате температурного воздействия в водной, щелочной и кислотной средах. Авторы работы [8] методами гидродинамики, электрооптики и компьютерного моделирования показали, что пленкообразующие аддитивный кремний, замещенный полинорборнен и кремний, замещенный полиацетилен, близкие по показателям газопроницаемости, обладают сходными конформационными свойствами цепей.
В работе [9] исследовали воздействие паров мезофазогенных растворителей на структуру и свойства порошкообразного полимера, где установлено, что модификация полимеров парами мезофазогенных растворителей позволяет управлять структурой и эксплутационными характеристиками ультрафильтрационных мембран. Так, в работе [10] установлены значения модуля упругости эритроцитов в зависимости от локализации области индентирования и времени воздействия зондом на поверхность мембраны. Показана существенная зависимость результатов оценки модуля упругости от скорости воздействия индентором на клеточную мембрану.
Проведенный анализ работ [1–10] позволил оценить значимость поверхностного слоя в процессах ультрафильтрационного разления растворов и его зависимость от стркутурных характеристик и состояния воды в нем. Поэтому целью данной работы явились исследования структурной организации активного слоя и состояния воды в ультрафильтрационных мембранах.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Композитные мембраны, изготовленные отливом раствора на подложку, представляют собой полимер, армированный каркасом из ткани. Образцы для съемки ИК-спектров поглощения готовили из коммерческих мембранах на тканевой подложке, полученной плетением (УАМ-50) и подложке – валяльным способом (УАМ-100). Затем высушенные образцы помещались в эксикатор. Перед регистрацией ИК-спектра поглощения в воднонасыщенном образце его помещали в дистиллированную воду на 5 мин, а затем поверхностная влага удалялась фильтровальной бумагой. Образцы помещали в ИК-Фурье спектрометр FT/IR-6200 (Jasco, Япония) с приставкой для неполного внутреннего отражения. Сканирование проводили в диапазоне волновых чисел от 600 до 4000 см–1. Время накопления сигнала – 3 мин. Теплофизические характеристики образцов УАМ-50 и УАМ-100 измерялись на дифференциальном сканирующем калориметре ДСК-2 со скоростью 10°С/мин и интервале температур от 45 до 300°С. Масса водонасыщенных образцов составляла 5.6 и 4.6 мг. Обработка спектральной информации и теплофизических характеристик проводилась с использованием пакета программы Оrigin 7.5 для визуализации и построения графиков.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
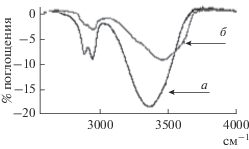
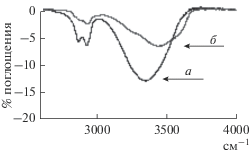
ИК-спектры сухого и водонасыщенного образцов ультрафильтрационных пленок УАМ-50 и УАМ-100 представлены на рис. 1–4 в интервалах частот от 600–2000 и 2750–4000 см–1 в разных масштабах для наглядности. Интервал от 2000 до 2750 см–1 не представляет интерес из-за отсутствия характерных полос поглощения. Положение и высокая интенсивность полос поглощения при 1740, 1430, 1341, 1234, 1022 см–1, согласно литературным данным, присущи ацетату целлюлозы [11, 12].
Характер спектра в этом интервале частот практически не изменяет свой неповторимый набор полос. Область частот от 2850 до 2950 см–1 соответствует суперпозиции валентных колебаний CН–, СН2–, СН3– групп, а 3050–3750 см–1 – валентным колебаниям гидроксильных групп, включенных в водородные связи. Значения частот и приведенная оптическая плотность полос валентных колебаний С=О, С–О и С–С–О групп представлены в табл. 1. Расчет оптической плотности проводили методом базовой линии по отношению к оптической плотности полосы деформационных колебаний СН2– групп при 1430 см–1.
Таблица 1.
Отнесение, приведенная оптическая плотность полос поглощения, значения частот мембран УАМ-50 и УАМ-100
| № п/п |
Мембрана УАМ-50 | Мембрана УАМ-100 | Отнесение | ||||||
|---|---|---|---|---|---|---|---|---|---|
| сухой образец | влажный образец |
сухой образец |
влажный образец | ||||||
| ν, см–1 | Dν/DδCH2 | ν, см–1 | Dν/DδCH2 | ν, см–1 | Dν/DδCH2 | ν, см–1 | Dν/DδCH2 | ||
| 1 | 3366.21 | 3302.7 “пл” | 3339.14 | 3310.5 “пл” | Валентные колебания ОН–групп | ||||
| 3452.82 | 3474.2 | ||||||||
| 3600.6 “пл” | 3598.8 “пл” | ||||||||
| 2 | Вк СН, СН2, СН3 | ||||||||
| 3 | 1741.4 | 0.65 | 1734.65 | 0.74 | 1738.1 | 0.6 | 1734.65 | 0.82 | Вк С=О |
| 4 | 1432.36 | 1.0 | 1431.4 | 1.0 | 1431.4 | 1.0 | 1431.4 | 1.0 | Деформационные колебания СН2 |
| 5 | 1369.21 | 1368.25 | 1367.71 | 1368.2 | Деформационные колебания СН3 | ||||
| 6 | 1225.54 | 0.74 | 1220.71 | 0.88 | 1225.57 | 0.72 | 1221.05 | 0.91 | Вк СО |
| 7 | 1033.65 | 0.81 | 1034.14 | 0.9 | 1032.4 | 0.79 | 1033.65 | 0.9 | С–С–О |
| 8 | 904.93 | 902.52 | 904.93 | 903.0 | Деформация кольца | ||||
| 9 | 873.59 | 870.7 | Колебания концевого кольца вокруг β(С1–С4) | ||||||
Оценочную информацию распределения водородных связей внутри цепочки и между ними можно получить по индексу асимметрии полосы поглощения гидроксильных (–ОН) групп [13, 14].
Индексы асимметрии рассчитывались, как отношение ширины правой (а) (высокочастотной) и левой (б) (низкочастотной) части максимума полосы поглощения (–ОН) групп на полувысоте пика. Для характеристики параметров водородной связи применялось уравнение, по которому можно рассчитать ее энергию [15]:
где ν0 – частота поглощения свободной гидроксильной группой (ν0 = 3650 см–1); ν – наблюдаемая частота поглощения гидроксильной группой, включенной в водородную связь; $\frac{1}{K} = 2.625 \times {{10}^{2}}\,\,\frac{{{\text{кДж}}}}{{{\text{моль}}}}.$Результаты расчетов сведены в табл. 2.
Известно, что если в ацетатцеллюлозе менее 55% связанной уксусной кислоты, то на пиранозное кольцо приходится одна свободная гидроксильная группа, которая участвует в образовании внутри- и межмолекулярных водородных связей типа –(ОН…О). Из таблицы видно, что для сухих образцов индекс асимметрии полосы поглощения для УАМ-50 равен 0.98, а для УАМ-100 равен 1.02. Это свидетельствует практически о равномерном распределении внутри- и межмолекулярных водородных связей. Следует отметить, что, согласно литературным данным [16], водородные связи между молекулами лежат в экваториальной плоскости. С другой стороны, образование связей можно объяснить взаимодействием макромолекул ацетата целлюлозы и в аксиальном направлении (т.е. в перпендикулярном к молекуле). Метинные группы (С–Н) ориентированы к плоскости кольца аксиально, следовательно, с большой вероятностью, могут быть включены в слабые водородные связи с кислородом карбонильной группы типа (С–Н…О=С).
Правомерность такого суждения подтверждает анализ полосы поглощения ν = 2884.02 и 2942.35 см–1, в которой доминируют колебания атомов СН3– групп. Метильная группа не участвует в водородных связях, но является донором электронов на сопряженные связи из-за индукционного эффекта карбонильной группы [17, 18]. То есть образование (С–Н…О=С) связи изменяет полярность метильной группы, что приводит к повышению интенсивности полосы поглощения при ν = 2884.02 и 2942.35 см–1 (рис. 1, 2). Учитывая, что СН3 группа имеет симметрию (С3v), а правилами отбора в ИК-спектре поглощения разрешено два типа валентных колебаний, то полоса при ν = 2884.02 см–1 идентифицируется, как валентное колебание А1 типа, а более широкая – ν = = 2942.35 см–1 – Е-типа. Отсутствие расщепления полосы поглощения ν = 2942.35 см–1 (Е-типа) свидетельствует о высокой локальной симметрии электростатического поля, образованного диполями карбонильных групп.
Таким образом, организация надмолекулярной структуры ацетатцеллюлозного активного слоя мембран УАМ-50 и УАМ-100 обусловлена двумя типами водородных связей – (ОН…О), (СН…О=С) и диполь-дипольным взаимодействием карбонильных групп.
В спектрах водно-насыщенных образцов наблюдается ряд изменений в области валентных колебаний атомов гидроксильных и ацетатных групп –3000–3700 и 2884.02–2942.35 см–1.
Прежде всего снижается интенсивность и изменяется форма полос поглощения (рис. 1 и 2). Индекс асимметрии полос поглощения гидроксильных групп уменьшается до 0.81 для УАМ-50, а для УАМ-100 до 0.82. Максимумы пиков смещаются в высокочастотную область спектра на 86.24 и 134.92 см–1 соответственно. Кроме этого, на полосах поглощения проявляются два “плеча” – одно при 3302.7 см–1 , второе при 3600.6 см–1 , для УАМ-50 а для УАМ-100 при 3310.5 и 3598.8 см–1. Данный факт может свидетельствовать, прежде всего, об уменьшении содержания гидроксильных групп, вовлеченных в межмолекулярные Н-связи, (уменьшается интенсивность), и о перераспределении водородных связей между ацетатом целлюлозы и молекулами воды с преобладанием слабых водородных связей.
Для уточнения, какой из фрагментов ацетатцеллюлозы вступает во взаимодействие с молекулами воды, была проведена оценка изменения приведенных оптических плотностей полос поглощения валентных колебаний атомов ацетильной группы – 1734.65, 1220.71, 1034.14 см–1 (табл. 1). Из данных таблицы следует, что в водно-насыщенных образцах частоты карбонильной (С=О) и эфирной (С–О) групп сдвигаются в низкочастотную область спектра на ( Δν = 6.7 см–1) и увеличивается оптическая плотность полос поглощения. На этом основании можно утверждать, что происходит разрыв слабых межмолекулярных связей (СН…О) и образование конкурирующих Н– связей карбоксильных групп с окружающими молекулами воды. Образование новых связей (Н2О…СО) приводит к частичному переносу заряда на сопряженные связи карбоксильных и метильных групп. Наиболее яркое проявление перераспределения электронной плотности на сопряженных связях наблюдается в уменьшении интегральных интенсивностей полос поглощения СН3– групп с частотами – ν = 2884.02 и 2942.35 см–1 для УАМ-50 в 2.56 раза, а для УАМ-100 в 3.3 раза, по отношению к сухому образцу (рис. 1–4).
Таким образом, в водно-насыщенных образцах, прежде всего, происходит разрыв водородных связей типа (С–Н…О) и образование новых Н-связей между молекулами воды и кислородом карбоксильных групп. Вследствие этого, увеличивается подвижность звеньев, а макромолекулы распрямляются, принимая линейную форму. В результате этого происходит пространственное упорядочение вытянутых макромолекул, между которыми образуются дополнительные, щелевидной формы микро- и мезо-поры. Подобные морфологические изменения молекулы ацетатцеллюлозы испытывают под влиянием низкомолекулярных жидкостей и, по мнению авторов, могут переходить в жидкокристаллическое состояние [19]. При этом полярные группы экранируются водородными связями с молекулами воды. образуя полимолекулярный слой связанной воды. Смещения частот колебаний С=О и С–О групп на Δν = 6.7 см–1 в низкочастотную область спектра, вероятнее всего, вызваны образованием Н-связей между молекулами воды и карбоксильными группами ацетата целлюлозы, из-за значительной полярности их молекул (дипольные моменты их равны Р = 1.84, D Н2О и Р = 2.4, D С=О) [20].
В ИК-спектре, на полосе поглощения водородных связей ацетатцеллюлозы, они проявляются в виде плеча с частотами ν = 3302.7 “пл” см–1, ν = 3310.5 “пл” см–1 для УАМ-50 и УАМ-100 соответственно, а величины энергий водородных связей равны ЕОН = 24.98 кДж/моль, ЕОН = 24.42 кДж/моль (табл. 2).
Таблица 2.
Индекс асимметрии полосы поглощения гидроксильных групп, значения энергий водородных связей мембран УАМ-50 и УАМ-100
| Состояние образца | Индекс асимметри a/в |
νmax (см–1) | ЕОН, кДж/моль | |
|---|---|---|---|---|
| Мембрана УАМ-50 |
Сухой | 0.98 | 3366.2 | 20.38 |
| Влажный | 3302.7 “пл” | 24.98 | ||
| 0.81 | 3452.82 | 14.17 | ||
| 3600.6 “пл” | 3.55 | |||
| Мембрана УАМ-100 |
Сухой | 1.02 | 3339.14 | 22.37 |
| Влажный | 3310.5 “пл” | 24.42 | ||
| 0.82 | 3474.2 | 12.65 | ||
| 3598.8 “пл” | 3.68 |
Полосы поглощения с максимумами ν = = 3452.82 см–1 и ν = 3474.06 см–1 являются комплексными, они включают внутримолекулярные и вновь образованные между молекулами воды и свободными активными группами ацетатцеллюлозы водородные связи, причем различной прочности с энергиями ЕОН = 14.17 кДж/моль и ЕОН = = 12.65 кДж/моль для УАМ-50 и УАМ-100 соответственно. Что касается высокочастотной части полосы поглощения с ν = 3600.6 “пл” см–1 ν = = 3598.8 “пл” см–1, то они свидетельствуют о проявлении слабых водородных связей (ОН…ОН), образованных между молекулами кластеров в капиллярной воде с энергиями равными ЕОН = = 3.55 кДж/моль и ЕОН = 3.68 кДж/моль. Становится понятным отсутствие полосы поглощения ν = 873.53 см–1 в водно-насыщенном образце. Данная частота обусловлена колебаниями концевых пиранозных колец, свободных от водородных связей, вокруг гликозидной связи (С1–С4)– типа колебания пластины, жестко закрепленной одним концом. Как отмечено выше, при сорбции воды разрушается жесткая надмолекулярная структура ацетата целлюлозы, макромолекулы принимают линейную форму, колебания которых, как правило, лежат в интервале более низких частот [19, 21]. Подобный эффект, очевидно, может быть использован как эмпирический показатель изменения конформации и перехода макромолекул в упорядоченную линейную форму. Подводя итог выше сказанному можно отметить, что вода нарушает структурную организацию ацетатцеллюлозного активного слоя на надмолекулярном уровне в результате разрыва межмолекулярных водородных связей. Во-вторых, активные группы ацетатцеллюлозы образуют новые водородные связи с молекулами воды, которые блокируют межмолекулярные взаимодействия выпрямленных макромолекул. В третьих, в структуре образуются дополнительные микро- и мезо- поры.
Таблица 3.
Параметры деконволюции кривых ДСК в интервале температур 50–110°С
| № | Мембраны | |||||
|---|---|---|---|---|---|---|
| УАМ-50 | УАМ-100 | |||||
| Тконв. | W, кДж/кг | % отн. | Тконв | W, кДж/кг | % отн. | |
| 1 | 62.38 | 10.42 | 5 | 60.38 | 12.23 | 5 |
| 2 | 74.33 | 68.33 | 34 | 73.85 | 85.14 | 37 |
| 3 | 87.14 | 83.06 | 42 | 85.38 | 82.59 | 36 |
| 4 | 95.06 | 25.6 | 13 | 92.92 | 36.84 | 16 |
| 5 | 98.82 | 11.46 | 6 | 97.1 | 13.8 | 6 |
Состояние воды можно количественно оценить при проведении термических исследований водно-насыщенных образцов. На кривых ДСК выделялся фрагмент в интервале температур 50–110°С, соответствующий эндотермическому пику испарения воды (рис. 3), затем проводили процедуру разложения на Гауссовы функции. Число элементарных гауссианов определялось из соображения максимального коэффициэнта регистрации. Видно, что экспериментальные кривые хорошо описываются суммарной кривой из пяти гауссовых компонент, при коэффициенте регрессии R2 = 0.998. Термические параметры результатов деконволюции эндотермических пиков сведены в табл. 3.
Рис. 5.
Фрагменты эндотермических пиков на кривых ДСК и их деконволюция на гауссовы контуры (1, 2, 3, 4, 5): (а) мембрана УАМ-50, (б) мембрана УАМ-100. Жирная линия – эксперимент. Сплошная линия – суперпозиция гауссовых кривых.

Из табл. 4 следует, что значения температур испарения воды и относительной плотности энергии гауссианов позволяют соотнести состояние воды в образцах с частотами, проявляемыми на полосе поглощения гидроксильных групп в ИК-спектре. Молекулы воды, удаляемые из образца при 98.82°С (97.1°С) (гауссиан-5), образуют мономолекулярный слой на свободных гидроксильных и карбонильных группах ацетата целлюлозы с энергией ЕНО = 24.98 кДж/моль (ЕНО = = 24.42 кДж/моль).
Вода, которая испаряется при температурах 74.33, 87.14, 95.06°С (гауссианы-2,3,4), образует полимолекулярный слой связанный с активными группами ацетатцеллюлозы и ассоциированными молекулами капиллярной воды. В ИК-спектре она проявляется колебаниями атомов гидроксильных групп с частотой поглощения ν = 3452.82 см–1 (ν = 3474.06 см–1) и средними энергиями ЕНО = = 14.17 кДж/моль (ЕНО = 12.65 кДж/моль). Молекулы воды удаляемые при температуре 62.38°С (гауссиан-1) – это вода со слабыми водородными связями и малыми энергиями ЕНО = 3.55 кДж/моль (ЕНО = 3.65 кДж/моль ) или поверхностная вода.
ЗАКЛЮЧЕНИЕ
В результате выполненных экспериментальных и теоретических исследований по колебательной спектроскопии и дифференциально-сканирующей калориметрии воздушно-сухого и водонасыщенного образцов композиционных ультрафильтрационных ацетатцеллюлозных мембран можно сделать следующие выводы:
1. Организация надмолекулярной структуры ацетатцеллюлозного активного слоя мембран УАМ-50 и УАМ-100 обусловлена двумя типами водородных связей – (ОН…О), (СН…О=С) и диполь-дипольным взаимодействием карбонильных групп. Вода нарушает структурную организацию ацетата целлюлозного активного слоя на надмолекулярном уровне в результате разрыва межмолекулярных водородных связей и образования новых водородных связей активных групп ацетатцеллюлозы с молекулами воды. Отсутствие полосы поглощения ν = = 873.53 см–1 в водно-насыщенном образце свидетельствует о конформационном переходе макромолекул в линейную форму с образованием узких мезопор между макромолекулами.
2. Термические исследования хорошо описываются пятью гауссианами, которые характеризуют физическое состояние молекул воды, традиционно разделяемую на связанную и капиллярную. Максимальная температура 98.82°С (97.1°С) соответствует образованию мономолекулярного слоя молекул воды на свободной гидроксильной и карбонильной группах с энергией ЕНО = 24.98 кДж/кг (ЕНО = = 24.42 кДж/кг) образует полимолекулярный слой, связанный с активными группами ацетатцеллюлозы и ассоциированными молекулами в капиллярной воде.
Список литературы
Мулдер М. Введение в мембранную технологию. М.: Мир, 1999. 514 с.
Рейдерман И.Б., Константинов В.А., Флисюк О.М. // Экология и промышленность России. 2010. № 11. С. 29.
Lie Jon Arvid, Hagg May-Britt. // J. Membr. Sci. 2006. V. 284. № 1–2. P. 79.
Ndmethy G., Scheraga H.A. // J. Phys. Chem. 1962. V. 36. P. 3401.
Gabrus E., Szaniawska D. // Przemysł Chemiczny. 2008. V. 87. № 5. P. 444–446.
Parna M., Jones Kimberly L., Abitoye Joshua O. // J. Membr. Sci. 2005. V. 254. № 1–2. P. 306.
Акберова Э.М., Малыхин М.Д. // Сорбционные и хроматографические процессы. 2014. Т. 14. Вып. 2. С. 232–239.
Евлампиева Н.П., Грингольц М.Л., Зайцева И.И., Рюмцев Е.И. // Высокомолекулярные соединения. Серия С. 2010. Т. 52. № 7. С. 1318–1328.
Потехина Л.Н., Седелкин В.М. // Вестник Саратовского государственного технического университета. 2011. Т. 1. № 1(52). С. 110–116.
Дрозд Е.С., Чижик С.А., Константинова E.Э. // Российский журнал биомеханики. 2009. № 4. С. 22–30.
Хаслам Дж., Виллис Г.И. Идентификация и анализ полимеров. М.: Химия, 1971. / Перевод с английского, под ред. Алешиной Л.А., Гуртова В.А., Мелех Н.В. Петрозаводск : Изд-во ПетрГУ, 2014. 240 с.
Воротынцев И.В. Автореферат дис. … докт. тех. наук. Нижний Новгород, 2011.
Жбанков Р.Г. Физика целлюлозы и ее производных. Минск: Наука и техника, 1983. 233 с.
Базарнова Н.Г., Карпова Е.В., Катраков И.Б. и др. Методы исследования древесины и ее производных: Учебное пособие. Издательство Алт. гос. ун-та. 2002. 160 с.
Popescu C.M., Singurel G., Popescu M.C. et al. // Carbohydr. Polym. 2009. V. 77. P. 851.
Renneckar Q., Li. S. // Biomacromolecules. 2011. V. 12. № 3. P. 650–659.
Беллами Л. Инфракрасные спектры сложных молекул. М.: Изд-во иностр. лит. 1963. 590 с.
Накасини К. Инфракрасные спектры и строение органических соединений. Практическое руководство / перевод с английского Куплетской Н.Б. и Эпштейн Л.М. / под ред. Мальцева А.А. М.: Мир, 1965. 220 с.
Папков С.П. Жидкокристаллическое состояние полимеров. М.: Химия, 1977. 240 с.
Осипов О.А. Справочник по дипольным моментам. М.: Высшая школа, 1971. 378 с.
Гилсон Т., Хендра П. Лазерная спектроскопия КР в химии / Перевод с английского / под ред. д.х.н. Алексаняна В.Т. М.: Мир. 1973. 306 с.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов