Физикохимия поверхности и защита материалов, 2021, T. 57, № 1, стр. 86-93
Физико-химические и биоцидные свойства покрытий никель–олово и никель–олово–диоксид титана
А. В. Пянко 1, *, И. В. Макарова 1, Д. С. Харитонов 2, И. С. Макеева 3, Д. С. Сергиевич 1, А. А. Черник 1
1 Белорусский государственный технологический университет
220006 Минск, ул. Свердлова, 13а, Беларусь
2 Jerzy Haber Institute of Catalysis and Surface Chemistry of Polish Academy of Sciences
30-239 Krakow, Niezapominajek, 8, Poland
3 Киевский национальный университет технологий и дизайна
01011 Киев, ул. Немировича-Данченко, 2, Украина
* E-mail: hanna.pianka@mail.ru
Поступила в редакцию 12.05.2020
После доработки 01.06.2020
Принята к публикации 08.06.2020
Аннотация
Методами сканирующей электронной микроскопии и элементного анализа изучены морфология и состав покрытий Ni–Sn и Ni–Sn–TiO2. Изучено электрохимическое поведение полученных покрытий в 3% растворе NaCl. Показано влияние включения диоксида титана в состав покрытия Sn–Ni на механические и антибактериальные свойства. Установлены зависимости влияния времени инкубирования и воздействия ультрафиолетового излучения на концентрацию жизнеспособных клеток на поверхности покрытия Ni–Sn–TiO2. На образцах покрытий Ni–Sn–TiO2, осажденных в электролите с содержанием TiO2 в количестве 2 г/дм3 концентрация жизнеспособных клеток Staphylococcus aureus уменьшается с 130 до 90 КОЕ/мл и с 70 до 30 КОЕ/мл без и при воздействии УФ излучения соответственно.
ВВЕДЕНИЕ
По данным Всемирной организации здравоохранения [1, 2], ежегодно в мире переносят инфекционные заболевания свыше 1 млрд человек, из которых, из-за вызванных осложнений умирает от 290 до 650 тыс. человек. Скорость распространения инфекционных заболеваний зависит от многих факторов [3–5]. Наиболее значимыми являются эпидемиологическая ситуация в стране, степень контагиозности заболевания и климатические условия. Степень контагиозности в свою очередь зависит от пути передачи заболевания, одним из которых является контактный путь [6, 7]. В данном случае возбудитель передается через кожные покровы при непосредственном соприкосновении или через поверхности общего пользования (поручни, ручки дверей и т.д.) [1–14]. Таким образом разработка нового класса металлических композиционных материалов, обладающих антибактериальными свойствами, является перспективным направлением в области материаловедения.
В качестве металлической основы для антибактериальных покрытий могут использоваться композиционные материалы на основе Cu [15–18], Ni [19–23], Fe [19, 20]. Сплав никель-олово обладает высокой коррозионной стойкостью и не оказывает раздражающего действия на кожу человека [10–14]. В предыдущей работе [24] описаны механизм формирования cплава никель–олово, структура и морфология формирующегося покрытия. Данный сплав применяется в промышленности в качестве защитно-декоративного покрытия для изделий из меди и стали [25, 26].
В качестве инертной фазы для композиционных покрытий могут использоваться наночастицы TiO2 [27–29], SiC [30, 31], Ag [32, 33]. Композиционные покрытия с внедрением таких наночастиц проявляют высокую эффективность против резистентных бактерий [13, 34–36] за счет подавления жизнедеятельности возбудителя инфекционной болезни в результате угнетения специфичного для микроорганизмов метаболического процесса [7].
Ввиду уникальных свойств наноразмерный TiO2 широко используется в качестве фотокатализатора для разложения органических загрязнителей и ингибиторов [37], модифицирующих микроорганизмы [38]. Широкое использование TiO2 основано на его эффективной фотокаталитической активности [39–41] и высокой химической стабильности [42–44]. В работах [42–48] изучена его антибактериальная эффективность под действием УФ-излучения. Следует отметить, что оксид титана, который встречается в природе в различных модификациях (анатаз, рутил, брукит), как правило, не является фотокатализатором. Для придания фотокаталитических свойств TiO2 должен быть синтезирован в определенных условиях и иметь наноразмерную структуру. В работах [39–41] отмечено, что наибольшей фотокаталитической активностью обладают частицы TiO2 размером от 10 до 50 нм.
Таким образом, электрохимически сформированный сплав никель–олово обладает рядом преимуществ по сравнению с покрытиями индивидуальными металлами. Введение наноразмерного диоксида титана в структуру сплава позволит придать металлической поверхности ряд уникальных свойств. В связи с этим, целью данной работы являлось исследование механических, трибологических, коррозионных и антибактериальных свойств покрытий никель–олово и никель–олово–диоксид титана.
МЕТОДИКА ЭКСПЕРИМЕНТА
Покрытия никель–олово и никель–олово–диоксид титана электрохимически осаждали из электролитов в соответствии с методикой [24]. В качестве анодов использовали оловянные и никелевые пластины с соотношением площадей 1 : 5. Покрытия осаждали на медные и стальные пластины, предварительно подготовленные согласно ГОСТ 9.305−84.
Наноразмерный диоксид титана синтезировали прямым окислением порошкообразного металлического титана по методике [49]. В результате получали смесь двух полиморфных модификаций диоксида титана − анатаза и рутила, с размером частиц 30−50 нм [50].
Электрохимические измерения проводили с помощью потенциостата Autolab PGSTAT 302N в трехэлектродной ячейке с насыщенным хлоридсеребряным электродом сравнения и платиновым вспомогательным электродом. В качестве коррозионной среды использовали 3% раствор NaCl. Поляризационные кривые снимали при скорости развертки потенциала 1 мВ/с через 30 мин после опускания рабочего электрода в раствор хлорида натрия для установления стационарного потенциала. Спектры электрохимического импеданса регистрировали в диапазоне частот от 10 кГц до 0.01 Гц с амплитудой переменного напряжения 10 мВ. Снятие частотных спектров импеданса проводили через 30 мин после выдерживания образца в исследуемом растворе. Обработку полученных данных проводили с использованием программного обеспечения Nova 2.1.
Морфологию поверхности полученных образцов изучали методом сканирующей электронной микроскопии (СЭМ) на микроскопе JEOL JSM–5610 LV и методом атомно-силовой микроскопии (АСМ) на микроскопе Nanosurf FlexAxiom с контроллером C3000 в прерывисто-контактном режиме “tapping mode” с использованием кремниевого кантиливера “n-тип” с радиусом острия иглы в пределах 8 нм (HQ:NSC15, MikroMasch). Элементный состав покрытий определяли методом энергодисперсионного рентгеновского микроанализа (EDX) с использованием системы химического микрорентгеноспектрального анализа EDX JED-2201.
Адгезию покрытий Ni–Sn и Ni–Sn–TiO2 к стальной подложке измеряли адгезиметром Defelsko Positest AT, а также испытывали методами нанесения сетки царапин и изгиба.
Микротвердость покрытий толщиной 20 мкм измеряли микротвердомером AFFRI-MVDM8 по ГОСТ 2999-75 при нагрузке на индентор 50 г.
Антибактериальные свойства покрытий изучали по отношению к грамположительным Staphylococcus aureus (S. aureus, ATCC 6538) и грамотрицательным Escherichia coli (E. coli, ATCC 8739) бактериям. Перед антибактериальными исследования-ми поверхность образцов стерилизовали в этаноле (70%) в течении 2 ч и сушили при комнатной температуре под УФ-облучением.
Тест-бактерии (одну колонию) переносили в пробирку с 2 мл питательного бульона (ПБ) и определяли количество бактерий. Жидкость с бактериями и ПБ разбавляли, чтобы полученный раствор содержал от 5.5 × 105 до 2.5 × 106 КОЕ/мл бактерий. Данный раствор использовали в качестве испытательной жидкости с бактериями. Жидкость объемом 0.1 мл высевали на испытуемый образец, накрывали пленкой, слегка прижимали, чтобы жидкость распределялась по всей поверхности. Облучение образца проводили в течение 1 ч при интенсивности ультрафиолетового излучения ~0.01 мВт/см2 и температуре 20 ± 1°С. Затем образцы промывали в стерильных полиэтиленовых упаковках содержащих 10 мл физиологического раствора и Тритон Х-100 (концентрация 0.1%) в течение 10 мин. Смытую жидкость немедленно высевали на питательный агар. Отбирали стерильной пипеткой 0.1 мл смытой жидкости и вносили в чашку Петри. Втирали раствор в агаризованную среду, накрывали чашки крышкой и оставляли при комнатной температуре на 5 мин. Засеянные чашки помещали в термостат, где инкубировали их в течении 48 ч при температуре 30 ± 1°С. Далее производили подсчет количества образовавшихся колоний в чашках и устанавливали концентрацию бактерий в промывной жидкости.
Оценку антибактериальной активности проводили по показателю K1 и K2:
(1)
${{K}_{1}} = 100 \times {{({{C}_{{{\text{конт}}}}} - {{С}_{{{\text{обр}}}}})} \mathord{\left/ {\vphantom {{({{C}_{{{\text{конт}}}}} - {{С}_{{{\text{обр}}}}})} {{{С}_{{{\text{конт}}}}}}}} \right. \kern-0em} {{{С}_{{{\text{конт}}}}}}},$(2)
${{K}_{2}} = {\text{lg}}({{{{C}_{{{\text{конт}}}}}} \mathord{\left/ {\vphantom {{{{C}_{{{\text{конт}}}}}} {{{C}_{{{\text{обр}}}}}}}} \right. \kern-0em} {{{C}_{{{\text{обр}}}}}}}),$Оценку антибактериальной активности самих пластинок с нанесенным покрытием также проводили без воздействия УФ-излучения. Для этого стерильные пластинки помещали в пакетики с 20 мл предварительно разведенной до концентрации 105 КОЕ/мл культурой тест-бактерий (S. aureus и E. coli) и инкубировали в течении 4 и 12 ч при температуре 30°С. Затем проводили высев из соответствующих разведений. Посевы инкубировали в течении 24 ч при температуре 30°С.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Cплавы никель–олово (рис. 1а) и никель–олово–диоксид титана (рис. 1б) осаждаются в виде гладких, блестящих, хорошо сцепленных с основой покрытий с плотной равномерной структурой. Введение в электролит TiO2 приводит к незначительному изменению характера покрытия, на поверхности наблюдается образование достаточно крупных сфероидов размером 6–8 мкм. По данным элементного анализа полученные покрытия Ni–Sn содержат 68–73 мас. % олова и 26–31 мас. % никеля. Данные соотношения являются оптимальным, так как в этом случае образуется механическая смесь NiSn2 и Ni3Sn2 [24, 51].
Рис. 1.
Микрофотографии сканирующей электронной микроскопии и элементный анализ покрытия Ni–Sn (а) и Ni–Sn–TiO2 (б).

Введение TiO2 в электролит приводит к изменению структуры поверхности покрытия с укрупнением формирующихся на поверхности кристаллитов. Как следует из данных АСМ (рис. 2), увеличение содержания TiO2 в электролите от 0 до 2 г/дм3 приводит к росту отдельных кристаллитов от 25 до 30 нм.
Рис. 2.
АСМ-изображения покрытий Ni–Sn и Ni–Sn–TiO2: Концентрация TiO2, г дм−3: (а–в) – 0, (г–е) – 1, (ж–и) – 2.

Адгезия и микротвердость сплава Ni–Sn и Ni–Sn–TiO2 представлены в табл. 1. Микротвердость покрытия Ni–Sn составила 405 HV, адгезия − 0.51 МПа/см2. Введение в электролит TiO2 в количестве 2 г/дм−3 приводит к росту микротвердости и адгезии до 439 HV и 0.65 МПа/см2 соответственно.
Таблица 1.
Свойства покрытий Ni–Sn и Ni–Sn–TiO2
| Ni–Sn | Ni–Sn–TiO2 | |
|---|---|---|
| Микротвердость, HV | 405 | 439 |
| Адгезия, МПа/см2 | 0.51 | 0.65 |
Поляризационные кривые сплавов, полученные в 3% растворе NaCl представлены на рис. 3. Катодные участки поляризационных кривых практически совпадают, что свидетельствует о незначительном влиянии состава и структуры покрытия на катодный процесс.
Рис. 3.
Потенциодинамические поляризационные кривые сплавов Ni–Sn и Ni–Sn–TiO2, полученные в 3% растворе NaCl.

На анодных участках поляризационных кривых наблюдается значительное отклонение в электроположительную сторону при введении в электролит TiO2. Так, начало анодного процесса для образцов без и с TiO2 наблюдается в диапазоне –50 и –25 мВ соответственно, при этом образцы сплава с TiO2 обладают более положительным стационарным потенциалом. По мере сдвига потенциала в электроположительную область до значения +50 мВ для сплава никель–олово наблюдается область относительной пассивации в диапазоне потенциалов 50–300 мВ с углом наклона приблизительно 0.4 В. Введение в электролит TiO2 приводит к активации поверхности в диапазоне потенциалов 0–0.2 В. На этом участке поляризационных кривых угол наклона составляет приблизительно 0.06 В. При потенциалах положительнее 0.2 В наблюдается область пассивации шириной 0.2–0.4 В. При этом плотность тока пассивации составляет 3.2 × 10–4 А/см2. Область потенциалов положительнее 0.4 В характеризуются достаточно активным протеканием анодного процесса как для образцов Ni–Sn, так и для образцов Ni–Sn–TiO2. Как следует из поляризационных кривых, введение диоксида титана в состав сплава Ni–Sn приводит к депассивации покрытия и способствует увеличению скорости анодного процесса.
Характеристики коррозионных процессов в 3% растворе хлорида натрия рассчитаны из поляризационных кривых и представлены в табл. 2. Плотность тока коррозии образцов, полученных из электролита с содержанием TiO2 2 г/дм3 уменьшается до 2.41 × 10−8 по сравнению с 5.41 × 10−8 А/см2 для покрытия без диоксида титана.
Таблица 2.
Характеристики коррозионного процесса сплава Ni–Sn и Ni–Sn–TiO2 (TiO2 2 г дм−3), полученные из анализа потенциодинамических поляризационных кривых
| ba, В | aa, В | |bk|, В | ak, В | iкор, А/см2 | |
|---|---|---|---|---|---|
| Sn–Ni | 0.0363 | 0.2072 | 0.0345 | –0.3073 | 5.41 × 10−8 |
| Sn–Ni–TiO2 | 0.0354 | 0.221 | 0.0278 | –0.2604 | 2.41 × 10−8 |
Данные электрохимической импедансной спектроскопии (рис. 4) также свидетельствуют о большей коррозионной стойкости покрытий Ni–Sn–TiO2. Диаграммы Найквиста, полученные для обоих типов покрытий в среде NaCl (рис. 4а), характеризуются емкостной полуокружностью в области высоких и средних частот, которая характерна для процессов с лимитирующей стадией переноса заряда на границе раздела электрод-электролит [52–57].
Рис. 4.
Диграммы Найквиста (а) и Боде (б) сплава Ni–Sn (1) и Ni–Sn–TiO2 (2), полученные в 3% растворе NaCl.
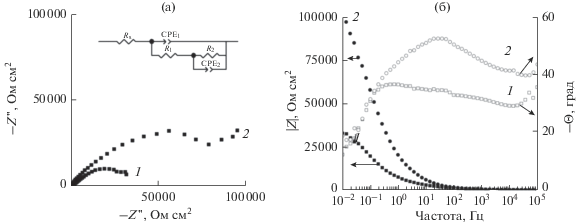
На диаграммах Боде для фазового угла в области средних частот присутствует широкий пик, что свидетельствует об относительно высоких значениях емкостного сопротивления и стойкости покрытия к коррозии. На диаграммах для модуля импеданса (рис. 4б) видно, что сопротивление переноса заряда покрытий, полученных в присутствии TiO2 (область низких частот) увеличивается от 3.30 × 104 до 8.95 × 104 Ом см2.
Для количественного анализа параметров полученных спектров использовалась эквивалентная схема, представленная на рис. 4. В использованной схеме Rs соответствует сопротивлению коррозионной среды, контур R1CPE1 описывает параметры процесса коррозии в дефектах покрытия, а контур R2CPE2 – сопротивление переноса заряда и емкость двойного электрического слоя на границе электрод-электролит. Вместо элемента конденсатора С, в схемах использовался элемент постоянной фазы CPE, учитывающий шероховатость поверхности. Результаты подбора параметров эквивалентных схем спектров импеданса представлены в табл. 3. Для покрытия Ni–Sn–TiO2 значения параметров R1 и R2 были выше, а параметров Y1 и Y2 – ниже, чем для покрытия Ni–Sn, что свидетельствует о большей коррозионной устойчивости полученных композитов. Значения параметра n1 для обоих покрытий близки к 0.5, что может свидетельствовать о протекании диффузионных процессов, вероятно, на дефектных участках покрытий.
Таблица 3.
Параметры эквивалентных схем спектров импеданса для покрытий Ni–Sn и Ni–Sn–TiO2, полученных в 3% NaCl
| Покрытие | Rs, Ом см2 | R1, Ом см2 | Y1, Ом–1 см–2 сn |
n1 | R2, Ом см2 | Y2, Ом–1 см–2 сn | n2 |
|---|---|---|---|---|---|---|---|
| Ni–Sn | 62.87 | 3.30 × 104 | 5.06 × 10–5 | 0.42 | 3.32 × 104 | 2.0 × 10–5 | 1 |
| Ni–Sn–TiO2 | 29.78 | 8.95 × 104 | 1.63 × 10–5 | 0.56 | 5.36× 104 | 9.16 × 10–6 | 1 |
Результаты исследований антибактериальных свойств полученных покрытий Ni–Sn и Ni–Sn–TiO2 по отношению к бактериям S. aureus и E. coli представлены на рис. 5. Как следует из представленных данных присутствие в покрытии диоксида титана значительно уменьшает количество бактериальных колоний на поверхности образцов. Данная тенденция наблюдается как для S. aureus, так и для E. coli. Концентрация жизнеспособных бактерий S. aureus на поверхности образцов при облучении УФ-излучением интенсивностью 0.01 мВ/м2 в течении 1 ч уменьшается от 130 до 70 КОЕ/мл (табл. 4). При облучении покрытий, полученных из электролита с 1 г/дм3 диоксида титана количество клеток уменьшается от 100 и до 20 КОЕ/мл. Это указывает на наличие антибактериального действия диоксида титана особенно при воздействии УФ. Для образцов, полученных в электролитах с 2 г/дм3 диоксида титана антибактериальный эффект увеличивается в 1.5 раза по сравнению с контрольным образцом.
Рис. 5.
Микрофотографии образцов колоний тест-бактерий (St. aureus и E. coli) после облучения УФ-излучением интенсивностью 0.01 мВ/м2 течение 4 ч: (а) контрольного образца с покрытием Ni–Sn и тест-бактерией St. aureus; (б) образца покрытия Ni–Sn–TiO2 после бактерицидного анализа тест-бактерией St. aureus; (в) контрольного образца с покрытием Ni–Sn и тест-бактерией E. coli; (г) образца покрытия Ni–Sn–TiO2 после бактерицидного анализа тест-бактерией E. coli.
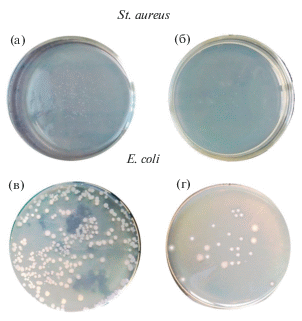
Таблица 4.
Концентрация жизнеспособных клеток Staphylococcus aureus на поверхности образцов (исходная концентрация: 5.6 × 105 КОЕ/мл)
| Условия опыта | Концентрация TiO2 в электролите, г/дм3 | Концентрация, КОЕ/мл | К1, % |
|---|---|---|---|
| Без обработки УФ | 0 | 1.3 × 102 | − |
| 1 | 1.0 × 102 | 23.08 | |
| 2 | 9.0 × 101 | 30.76 | |
| После обработки УФ излучением (I ∼ 0.01 мВт/см2, 1 ч) | 0 | 7.0 × 101 | − |
| 1 | 2.0 ×101 | 71.43 | |
| 2 | 3.0 × 101 | 57.14 |
Такое поведение образцов обусловлено, по всей видимости, фотокаталитической антибактериальной активностью композиционного электрохимичекого покрытия Ni–Sn–TiO2 в присутствии УФ-излучения [43–45] за счет повреждения клеточных мембран бактерий из-за поглощения излучения внутриклеточными хромофорами.
Антибактериальная активность образцов по отношению к тест-бактериям при инкубации в течение 4 и 12 ч увеличивается с ростом содержания диоксида титана в покрытии как для S. aureus, так и для E. coli (табл. 5).
Таблица 5.
Антибактериальная активность образцов по отношению к тест-бактериям при их инкубации в течении 4 и 12 ч
| Концентрация TiO2 в электролите, г/дм3 | S. aureus | E. coli | ||||||
|---|---|---|---|---|---|---|---|---|
| 12 ч | 4 ч | 12 ч | 4 ч | |||||
| КОЕ/мл | К2 | КОЕ/мл | К2 | КОЕ/мл | К2 | КОЕ/мл | К2 | |
| 0 | 2.9 × 107 | 1.96 | 2.6 × 104 | 1.33 | 2.8 × 107 | 1.51 | 2.4 × 104 | 1.40 |
| 1 | 1.6 × 107 | 2.23 | 2.0 × 104 | 1.44 | 2.1 × 107 | 1.64 | 1.9 × 104 | 1.50 |
| 2 | 9.8 × 106 | 2.44 | 1.0 × 104 | 1.74 | 1.3 × 107 | 1.84 | 2.1 × 104 | 1.29 |
| Контр. образец | 2.7 × 109 | − | 5.6 × 105 | − | 9.2 × 108 | − | 6.1 × 105 | − |
Показатель антибактериальной активности K2 увеличивается от 1.4 до 1.5 для E. coli и от 1.33 до 1.7 для S. aureus при времени инкубирования 4 ч. С увеличением времени инкубирования К2 также возрастает, достигая значения 1.84 для E. coli и 2.44 для S. aureus при концентрации диоксида титана в электролите 2 г/дм3.
ЗАКЛЮЧЕНИЕ
Таким образом, проведенные исследования показали, что введение наноразмерного диоксида титана в структуру сплава никель–олово позволяет получать покрытия с повышенной твердостью, адгезией и коррозионной стойкостью. Микротвердость и адгезия покрытий Ni–Sn–TiO2 составили 439 HV и 0.65 МПа/см2 соответственно, а плотность тока коррозии уменьшилась до 2.41 × 10−8 А/см2. Полученное композиционное покрытие характеризуется высокой биоцидной активностью по отношению к бактериям S. aureus и E. coli.
Список литературы
Кайгородова Т.В., Зимина Е.И., Иванов А.В. // Здравоохранение РФ. 2009. № 1. С. 23.
World Health Organization World health statistics 2018: monitoring health for the SDGs, sustainable development goals / Geneva: 2018. P. 64.
Beamer Paloma I., Plotkin Kevin R., Gerba Charles P. et al. // J. Occup. Environ. Hyg. 2015. V. 12. № 4. P. 266.
Julian T.R.A.O., Canales R.A.O., Leckie J.O. et al. // Risk Anal. 2009. V. 29. P. 617.
Nicas M., Best D. // J. Occup. Environ. Hyg. 2008. V. 5. P. 347.
Lopez G.U.P.H., Gerba C.P.H., Tamimi A.H. et al. // J. Appl. Environ. Microbiol. 2013. V. 79. P. 307.
Бартлетт Дж. Инфекции дыхательных путей / Пер. с англ. М.: Бином, 2000. С. 192.
Зайцев А.А., Клочков О.И., Миронов М.Б. и др. Острые респираторные вирусные инфекции: этиология, диагностика, лечение и профилактика / Пособие для врачей. Москва, 2008. С. 37.
Биличенко Т.Н., Чучалин А.Г. // Терапевт. арх. Т. 90. № 1. С. 22.
Woods J.B. // Biol. Weapons Def. N.J. 2005. P. 285.
Fluit A.C., Visser M.R., Schmitz F. // Clin. Microbiol. Rev. 2001. V. 14. № 4. P. 836.
Yim G., Wang H.H., Davies J. // Phil. Trans. R. Soc. B. 2007. V. 362. P. 1195.
Бeлoбopoдoв B.Б. // Con. Med. 2004. V. 6. № 1. P. 18.
Каркищенко Н.Н. // Биомедицина. 2009. № 1. С. 5.
Бабушкина И.В., Бородулин В.Б., Коршунов Г.В. и др. // Сарат. науч.-мед. журн. 2010. Т. 6, № 1. С. 11.
Зотова Е.С. // Дис. … канд. техн. наук: 05.02.01. М.: Моск. гос. вечер. металлург. ин-т, 2008. 114 с.
Yin M., Wu C.K., Lou Y. et al. // J. Am. Chem. Soc. 2005. V. 127. № 26. P. 9506.
Reisse J., Francois H., Vandercammen J. et al. // Electrochim. Acta. 1994. № 39. P. 37.
Ероклинцев В.Н., Лукьянова В.О. // Тенд. развития науки и образования. 2017. № 28-2. С. 17.
Бабушкина И.В., Бородулин В.Б., Коршунов Г.В. // Клин. лаб. диагностика. 2008. № 9. С. 85.
Бабушкина И.В., Бородулин В.Б., Коршунов Г.В. и др. // Сарат. науч.-мед. журн. 2010. Т. 6. № 1. С. 11.
Makarova I.V., Kharitonov D.S., Dobryden’ I.B. et al. // Russ. J. Appl. Chem. 2018. V. 91. P. 1441.
Makarova I., Dobryden’ I., Kharitonov D. et al. // Surf. Coat. Technol. 2019. V. 380. P. 125063.
Пянко А.В., Макарова И.В., Харитонов Д.С. и др. // Неорг. матер. 2019. Т. 55. № 6. С. 609.
Kuznetsov B.V., Vorobyova T.N., Glibin V.P. // Met. Finish. 2013. V. 111. № 3. P. 38.
Шеханов Р.Ф. // Изв. вузов. Химия и хим. технология. 2017. Т. 60. № 10. С. 75.
Wagner V. Übersichtsstudie Wasserknappheit & Technologie. Dusseldorf, 2004. P. 194.
Park N.-G., Van de Lagemaat J., Frank A.J. // J. Phys. Chem. 2000. V. 104. № 38. P. 8989.
Smestad G., Bignozzi C., Smestad R.A. // Sol. Energy Mater. Sol. Cells. 1994. V. 32. Iss. 3. P. 259.
Mills A., Le Hunte S. // J. Photochem. Photobiol. A Chem. 1997. 108. P. 1.
Kikuchi Y., Sunada K., Iyoda T. et al. // J. Photochem. Photobiol. A Chem. 1997. V. 106. P. 51.
Hoffmann M.R., Martin S.T., Choi W. et al. // Chem. Rev. 1995. V. 95. P. 69.
Matsunaga T., Tomoda R., Nakajima T. et al. // Appl. Environ. Microbiol. 1988. V. 54. P. 1330.
Woods J.B. // Biol. Weapons Def. N.J. 2005. P. 285.
Fluit A.C., Visser M.R., Schmitz F. // Clin. Microbiol. Rev. 2001. V. 14. № 4. P. 836.
Ollis D.F., Al-Ekabi H. // Open J. Inorg. Chem. 1993. P. 511.
Xu M., Huang N., Xiao Z. et al. // Supramol. Sci. 1998. № 5. P. 449.
Freitas R.A., Jr. // Int. J. Surg. 2005. № 3. P. 243.
Murashkevich A.N., Alisienok O.A., Zharskiy I.M. et al. // J. Sol-Gel Sci. Technol. 2019. V. 92. P. 254.
Kutuzau M., Shumskaya A., Kaniukov E. // Nucl. Instrum. Methods Phys. Res., Sect. B. 2019. V. 460. P. 212.
Murashkevich A.N., Chechura K.M., Novitskaya M.S. et al. // Inorg Mater. 2018. V. 54. P. 1223.
Кузьмичева Г.М., Савинкина Е.В., Оболенская Л.Н. и др. // Кристаллография. 2010. Т. 55. № 5. С. 919.
Ismagilov Z.R., Tsikoza L.T., Shikina N.V. et al. // Russ. Chem. Rev. 2009. V. 78. P. 873.
Герасименко Ю.В., Логачева В.А., Ховив А.М. // Конденсированные среды и межфазные границы. 2010. Т. 12. № 2. С. 113.
Kim B., Kim D., Cho D. et al. // Chemosphere. 2003. V. 52. P. 277.
Modesa T., Scheffela B., Metznera Chr. et al. // Surf. Coat. Technol. 2005. V. 200. P. 306.
Kleiman A., Mrquez A., Lamas D.G. // Surf. Coat. Technol. 2007. V. 201. P. 86.
Nishimoto S., Ohtani B., Kaijiwara H. et al. // J. Chem. Soc., Faraday Trans. I. 1985. V. 81. P. 61.
Коваленко И.В., Черненко Л.В., Хайнаков С.А. и др. // Укр. хим. журн. 2008. Т. 74. № 3–4. С. 52.
Коваленко И.В. / Дис. … канд. хим. наук: 02.00.01. Киев, 2009. 130 с.
Kuznetsov B.V., Vorobyova T.N., Glibin V.P. // Met. Finish. 2013. V. 111. № 3. P. 38.
Антихович И.В., Харитонов Д.С., Черник А.А. и др. // Журн. прикл. химии. 2017. Т. 90. № 4. С. 469.
Winiarski J., Niciejewska A., Ryl J. et al. // Materials. 2020. V. 13. P. 924.
Wysocka I., Kowalska E., Ryl J. et al. // Nanomaterials. 2019. V. 9. P. 1129.
Miszczyk A., Darowicki K. // Anti-Corros. Methods Mater. 2011. V. 58. № 1. P. 13–21.
Rudoy V.M., Ostanin N.I., Ostanina T.N. et al. // Russ. J. Non-ferrous Metals. 2019. V. 60. P. 632–638.
Nikitin V.S., Rudoi V.M., Ostanina T.N. et al. // J. Anal. Chem. 2017. V. 72. P. 390–395.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов


