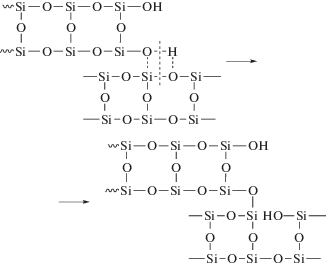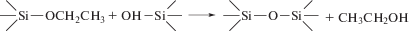Высокомолекулярные соединения (серия Б), 2021, T. 63, № 4, стр. 223-230
ОЛИГОМЕРНЫЕ СИЛСЕСКВИОКСАНЫ С 3-АМИНОПРОПИЛЬНЫМИ ГРУППАМИ
Н. С. Бредов a, *, Нгуен Ван Туан a, Д. С. Зайцева a, В. В. Киреев a, М. В. Горлов a, И. Б. Сокольская b, В. А. Поляков a
a Российский химико-технологический университет им. Д.И. Менделеева
125047 Москва, Миусская пл., 9, Россия
b Государственный научно-исследовательский институт химии и технологии элементоорганических соединений
111123 Москва, ш. Энтузиастов, 38, Россия
* E-mail: koljabs@rambler.ru
Поступила в редакцию 31.03.2021
После доработки 14.04.2021
Принята к публикации 28.04.2021
Аннотация
Гидролитической поликонденсацией 3-аминопропилтриэтоксисилана, а также его совместной конденсацией с фенилтриметоксисиланом в среде этанола синтезированы аминосодержащие олигосилсесквиоксаны. По данным спектроскопии ЯМР 1Н и ЯМР 29Si олигомеры наряду с лестничными фрагментами содержат незавершенные циклоцепные структуры. Сделано предположение о том, что самопроизвольное гелеобразование олигомеров при длительном хранении обусловлено протеканием межмолекулярных взаимодействий силоксановых цепей с силанольными и аминопропильными группами.
Водорастворимые олигоаминопропилсилсесквиоксаны являются весьма перспективными функциональными соединениями данного типа, которые можно использовать в качестве отвердителей термореактивных смол, для получения нанокомпозитов, а также для синтеза широкого спектра других функциональных олигосилоксанов модификацией реакционноспособных аминогрупп [1–6].
Впервые кубический окта-(3-аминопропил)силсесквиоксан [H2NCH2CH2CH2SiO1.5]8 (I) синтезирован гидролитической поликонденсацией 3-аминопропилтриэтоксисилана (АГМ-9) [7], однако деталей эксперимента и характеристик полученного соединения представлено не было. В работе [1] сообщалось о получении I гидролитической поликонденсацией АГМ-9 в среде метанола в присутствии концентрированной HCl при 25°С; при продолжительности реакции 6 недель выход I составил 30%.
Позже было установлено [8], что в этом случае образуется гидрохлорид I, ограниченно растворимый в большинстве органических растворителей, но легко растворимый в воде. Нейтрализация гидрохлорида I осуществлялась пропусканием его разбавленного раствора в смеси вода–этанол через колонку с ионитом “Amberlite IRA-400”. Раствор I оставался стабилен в течение 1–2 суток, но образовывал так называемый T-гель при более длительном хранении или удалении растворителя [1, 9, 10].
MALDI-TOF масс-спектр I, снятый перед образованием T-геля, показал наличие множества пиков с m/z < 3000 [1], при этом сигналы, которые можно было бы отнести к соединениям строения (RSiO1.5)n, где n = 6, 8, 10 или 12, отсутствовали. Это свидетельствует о преобладании в составе продуктов гидролитической поликонденсации АГМ-9 соединений с незавершенной полиэдрической структурой, подобной тем, которые были установлены в продуктах гидролиза [11, 12] и ацидолиза 3-метакрилоксипропилтриметоксисилана [13, 14].
При варьировании мольного соотношения вода : АГМ-9, природы и количества катализатора, в частности Et4NOH [6], выход I удалось повысить до 72%. Наиболее эффективным оказалось проведение процесса в водном растворе трифторметансульфокислоты с постепенным повышением температуры. В результате с выходом 93% получен октатрифторметансульфонат I [15, 16]. Установлен также факт перегруппировки каркасных структур типа T8 → Т10 под действием сульфокислоты [16, 17].
Некоторые особенности совместной гидролитической поликонденсации АГМ-9 и фенилтриметоксисилана представлены в работах [18–20].
С целью повышения стабильности аминопропилсилсесквиоксанов, их растворимости в органических средах и совместимости с другими олигомерами представлялось целесообразным синтезировать смешанные олигомеры, содержащие у атомов кремния помимо аминопропильных групп и другие инертные или функциональные радикалы. В качестве сомономера в настоящей работе использован фенилтриметоксисилан.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
3-Аминопропилтриэтоксисилан – продукт фирмы “Acros” (содержание основного вещества 98%, температура плавления Тпл = –70°С, температура кипения Ткип = 217°С, плотность ρ = 0.946 г/мл) применяли без дополнительной очистки. Спектр ЯМР 1Н (CDCl3), м.д.: 0.49 (т, –СН2–Si), 1.40 (м, –СH2CH2CH2–), 1.75 (с, –СH2CH2CH2NH2), 3.65 (с, CH3СН2О–), 1.08 (т, CH3СН2О–).
Фенилтриметоксисилан (ФТМС) – продукт фирмы “Acros” (содержание основного вещества 98%, Ткип = 211°С, $n_{D}^{{25}}$ = 1.468) использовали без дополнительной очистки. Спектр ЯМР 29Si (СDCl3), м.д.: –43.5 (с); спектр ЯМР 1Н (CDCl3), м.д.: 3.5 (с, СН3О–), 7.5 (с, Н), 7.7 (д, Н1).
Триэтиламин (ТЭА) – продукт фирмы “Acros” (содержание основного вещества 98%, Ткип = 89.5°С, $n_{D}^{{25}}$ = 0.728) применяли без дополнительной очистки.
Этанол – продукт фирмы “Acros” (содержание основного вещества 96%, Ткип = 78.4°С, ρ = = 0.812 г/см3 (20°С)).
Гидролитическую сополиконденсацию 3-аминопропилтриэтоксисилана и фенилтриметоксисилана проводили при их мольных соотношениях 1 : 1−1 : 10 по следующей методике. В круглодонную колбу, снабженную обратным холодильником с хлоркальциевой трубкой и перемешивающим устройством, приливали расчетное количество АГМ-9 и ФТМС в виде раствора в этаноле, объем которого обеспечивал выбранное мольное соотношение вода : силан = 6 : 1. Мольное соотношение ТЭА : силан = 0.01. Реакционную смесь перемешивали при 80–85°С в течение 10–50 ч, затем отгоняли в вакуумном испарителе растворитель и легколетучие продукты; остаток сушили в вакууме без нагревания, получая смолообразные олигомеры с выходом более 90%. Гидролитическую поликонденсацию только 3-аминопропилтриэтоксисилана или фенилтриметоксисилана осуществляли в аналогичных условиях.
Содержание аминогрупп в олигомере устанавливали методом обратного титрования по методике [18]. В колбу загружали 0.5 г образца, 20 мл 0.1 N раствора HCl и перемешивали полученную суспензию в течение 3 ч на магнитной мешалке при комнатной температуре. Далее осадок фильтровали, а фильтрат титровали водным раствором 0.1 N NaOH, используя фенолфталеин в качестве индикатора.
Спектры ЯМР 1Н и ЯМР 29Si снимали на приборах “Bruker СХP-200” и “Bruker AMX-360” при 25°С в растворах CDCl3 или D2O.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Для установления оптимальных условий сополиконденсации АГМ-9 с ФТМС уточнялись параметры его гомоконденсации в среде этанола при мольном соотношении вода : силан = 6 : 1 в присутствии каталитического количества триэтиламина:
(1)
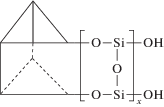
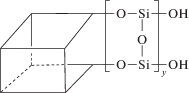
$n{\text{RSi}}{{({\text{OC}}{{{\text{H}}}_{2}}{\text{C}}{{{\text{H}}}_{3}})}_{3}} + {{{\text{H}}}_{2}}{\text{O}}\xrightarrow[{ - {{{\text{C}}}_{2}}{{{\text{H}}}_{5}}{\text{OH}}}]{{80 - 85^\circ {\text{C}}}}{{({\text{RSi}}{{{\text{O}}}_{{1.5}}})}_{n}}$Здесь и ниже R = –CH2CH2CH2NH2. По мере протекания процесса содержание этокси-групп в образующемся продукте гидролитической поликонденсации АГМ-9 по данным спектров ЯМР 1Н (рис. 1) постепенно уменьшается, и их полная конверсия наблюдается через 50 ч. В спектре ЯМР 13С олигомера прослеживаются сигналы ядер углерода 10.0 (–SiCH2), 24.6 (–SiCH2CH2–) и 42.32 м.д. (–СН2NH2) наряду с незначительными по интенсивности сигналами ядер углерода в этокси-группах в области 57 и 17 м.д. Анализ спектров ЯМР 29Si (рис. 2) позволил рассчитать содержание различных структурных фрагментов в составе продукта гидролитической поликонденсации мономера АГМ-9 (табл. 1). При анализе спектров ЯМР 29Si и описании строения полученных олигомеров использованы следующие условные формулы фрагментов молекул олигосилсесквиоксанов (радикалы R = –CH2CH2CH2NH2 на приведенных ниже формулах не показаны):
Рис. 1.
ЯМР 1Н-спектры АГМ-9 (а − спектр снят в CDCl3) и продуктов его гидролитической поликонденсации в среде этанола (б, в − спектры сняты в D2O) в присутствии каталитического количества триэтиламина; Т = 80°С, продолжительность – 10 (б) и 50 ч (в).
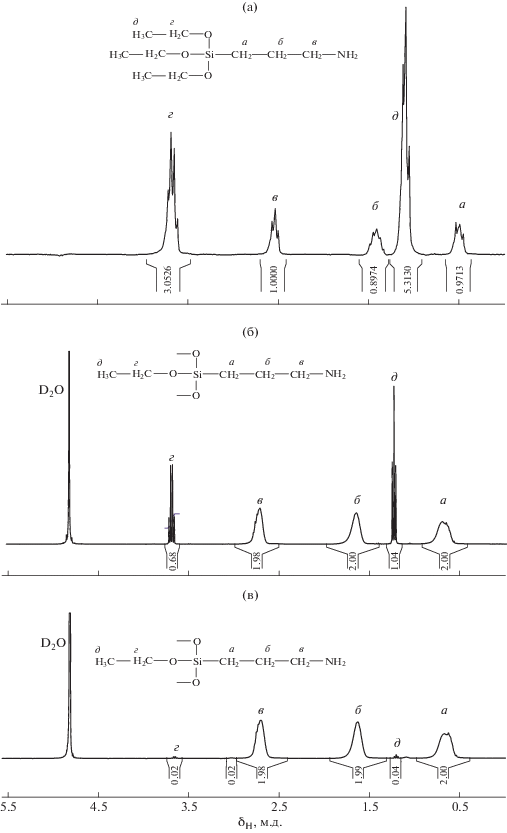
Рис. 2.
Спектр ЯМР 29Si продукта гидролитической поликонденсации АГМ-9, проводимой в течение 50 ч. Спектр снят в D2O.
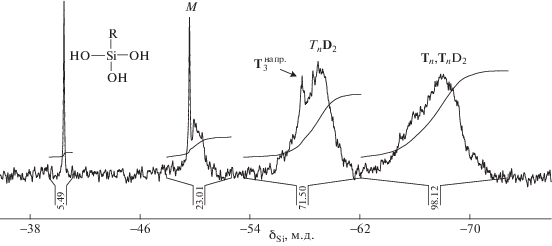
Таблица 1.
Содержание силанольных групп в продукте гидролитической поликонденсации АГМ-9 по данным спектра ЯМР 29Si
| Формула соединения или фрагмента | Усл. обозначения | Область хим. сдвигов сигналов δSi, м.д. | Содержание фрагмента в олигомере, мас. % | Содержание групп SiOH, мас. % | |
|---|---|---|---|---|---|
| во фрагменте | в олигомере* | ||||
| RSi(OH)3 | – | –40.5 | 3.4 | 37.2 | 1.3 |
| RSi(OH)2O0.5 | М | от –49 до –51 | 12.9 | 26.6 | 3.4 |
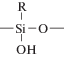 |
D | от –59 до –61 | 21.7 | 14.3 | 3.1 |
| RSiO1.5 | T | от –65 до –71 | 62 | – | – |
| T6+x** | – | – | 14.5(T) + 5.1(D) | 1.9–5.0 | 0.4–1.0 |
| T8+y** | – | – | 47.5(T) + 16.6(D) | 1.1–3.8 | 0.7–2.4 |
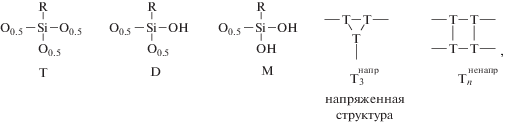
а также наиболее вероятностные структуры соединений типа
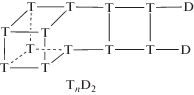
Расчет по интегральной интенсивности сигналов атомов кремния в различных структурах с учетом их относительной доли в продукте поликонденсации показал содержание силанольных групп в пределах 7–8%. Это свидетельствует о значительной незавершенности второй стадии гидролитической поликонденсации, а именно силанольной конденсации.
Как и в рассмотренных выше случаях, продукты гидролитической поликонденсации мономера АГМ-9 при длительном хранении в растворах образуют гели, а при выделении из раствора – нерастворимые полимерные продукты. Причина гелеобразования пока не ясна, но можно предположить, что это, скорее всего, не только реакция силанольной конденсации. Невысокое по данным спектроскопии ЯМР содержание в олигомере силанольных групп (табл. 1), тем более локализованных на концах жестких двутяжевых молекул типа Tn, позволяет рассмотреть еще один возможный путь образования трехмерной сетки за счет реакций межцепного обмена с участием силанольных групп и силоксановых связей молекул олигомера по типу хорошо известной деполимеризации линейных полисилоксанов:
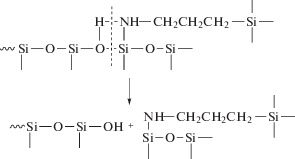
По мере образования разветвленных молекул, редкой пространственной сетки и затруднений контактов силанольных групп реакции “сшивания” по схеме (2) будут преобладать. Естественно реакция (2) может ускоряться как под каталитическим действием аминогрупп олигомера, так и по типу межцепного взаимодействия:
Для повышения стабильности аминопропилсодержащих олигосилсесквиоксанов была осуществлена совместная гидролитическая поликонденсация АГМ-9 с фенилтриметоксисиланом (ФТМС) в мольных соотношениях соответственно от 1 : 1 до 1 : 10. Условия реакции были аналогичны для гомополиконденсации АГМ-9.
Продукты реакций представляют собой прозрачные вязкие жидкости или твердые стеклообразные вещества белого цвета в зависимости от содержания фенилсилсесквиоксановых фрагментов. Условия реакции приведены в табл. 2.
Таблица 2.
Выход и аминное число продуктов гидролитической (co)поликонденсации АГМ-9 и ФТМС
| Мольное соотношение АГМ-9 : ФТМС |
Время реакции, ч | Выход олигомеров, % | Аминное число*, ммоль/г |
|---|---|---|---|
| 1 : 0 | 50 | 83 | – / 9.09 |
| 1 : 1 | 10 | 94 | – / 4.18 |
| 1 : 1 | 30 | 96 | – / 4.18 |
| 1 : 1 | 50 | 98 | – / 4.18 |
| 1 : 3 | 50 | 96 | 1.88 / 2.01 |
| 1 : 5 | 50 | 96 | 1.29 / 1.32 |
| 1 : 7 | 50 | 96 | 0.96 / 0.99 |
| 1 : 10 | 50 | 96 | 0.70 / 0.71 |
| 0 : 1 | 50 | 92 | – / – |
Процесс совместной гидролитической поликонденсации АГМ-9 и ФТМС в этаноле в присутствии 1 мол. % ТЭА от суммы молей силанов протекает с большими степенями конверсии по этокси- и метокси-группам. При проведении гидролитической поликонденсации только ФТМС из реакционной смеси выпадал белый осадок, в то время как в случае гидролитической поликонденсации АГМ-9 реакционная смесь являлась гомогенной. Это может быть связано с сильным взаимодействием аминогрупп с полярными этанолом и водой. При совместной гидролитической поликонденсации наличие или отсутствие гетерофазы зависит от мольного соотношения АГМ-9 и ФТМС. В случае мольного соотношения АГМ-9 : : ФТМС < < 3 : 1 в реакционной смеси можно видеть появление белого осадка. При указанном соотношении больше 3 : 1 реакционная смесь остается гомогенной, что, вероятно, связано с высоким содержанием аминогрупп в смешанных олиго(аминопропил)фенилсилсесквиоксанах, способствующих растворению в полярных средах.
По данным спектров ЯМР 1Н продуктов совместного гидролиза АГМ-9 и ФТМС найденное содержание аминогрупп в олигомерах несколько ниже по сравнению с вычисленными значениями. Эти результаты согласуются с данными работы [21] по модификации частиц кремнезема равномольным количеством АГМ-9 и тетраэтоксисилана: содержание аминопропильных звеньев в продуктах модификации не превышало 18.5 мол. % при расчетном 50 мол. %.
Важным моментом для практического использования синтезированных олигосилсесквиоксанов считается их растворимость в воде и органических растворителях (табл. 3).
Таблица 3.
Растворимость продуктов гидролитической (со)поликонденсации АГМ-9, ФТМС и АГМ-9/ФТМС в различных растворителях
| Мольное соотношение АГМ-9 : ФТМС |
Растворимость* | ||||
|---|---|---|---|---|---|
| H2O | CHCl3 | CH3COCH3 | ТГФ | ДМСО | |
| 1 : 0 | + | – | – | – | – |
| 5 : 1 | ± | – | – | – | – |
| 3 : 1 | ± | – | – | – | – |
| 1 : 1 | – | + | ± | + | + |
| 1 : 3 | – | + | + | + | + |
| 1 : 5 | – | + | + | + | + |
| 1 : 7 | – | + | + | + | + |
| 1 : 10 | – | + | + | + | + |
| 0 : 1 | – | + | + | + | + |
Олигомеры с преобладающим содержанием аминопропильных радикалов растворимы в воде, а олигомеры с большим количеством фенильных групп – в полярных органических растворителях.
Интересным остается факт образования нерастворимых или ограниченно растворимых в органических растворителях олигомеров при проведении согидролиза в ТГФ, диоксане, ацетоне и других подобных средах. В то же время, в среде этанола, даже несмотря на частичное выпадение продуктов из раствора, они, как правило, растворяются в полярных органических растворителях. Это, вероятно, связано с сольватацией групп и их возможным взаимодействием с этанолом:
хотя это равновесие и сильно сдвинуто влево.Изложенное выше позволяет заключить, что совместная гидролитическая поликонденсация АГМ-9 и ФТМС в среде этанола по сравнению с другими растворителями протекает со значительной долей реакции гетерофункциональной конденсации:
Спектр ЯMР 1Н продукта гидролитической сополиконденсации АГМ-9 и ФТМС при мольном соотношении 1 : 3 (рис. 3) показал, что гидролиз метокси- и этокси-групп протекает полностью после 50 ч реакции: сигналы протонов групп –OСH3 и –OCH2CH3 в спектре ЯМР 1Н олигомера почти отсутствует.
Рис. 3.
Спектр ЯМР 1H продукта гидролитической (со)поликонденсации при мольном соотношении АГМ-9 : ФТМС = = 1 : 3 в течение 50 ч.
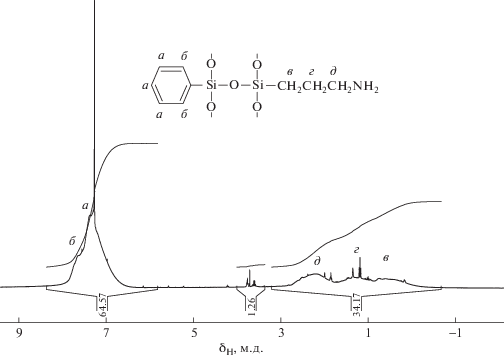
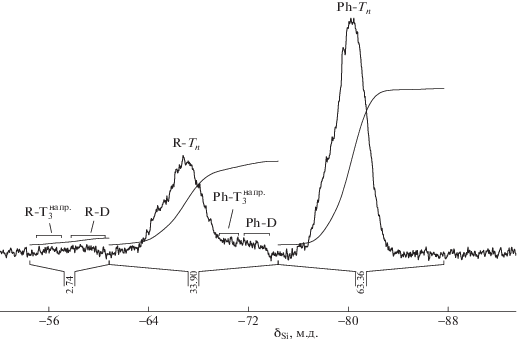
В кремниевых спектрах ЯМР продуктов сополиконденсации АГМ-9 и ФТМС при их мольном соотношении 1 : 3 (рис. 4) прослеживаются значительные по интенсивности сигналы атомов кремния, отнесенные, предположительно, к силсесквиоксановым структурам с фенильными (в области δSi = от –78 до –84 м.д.) и аминопропильными фрагментами (δSi = от –65 до –68 м.д.). Звеньям D c заместителями R и Ph соответствуют малоинтенсивные сигналы в областях от –58 до –60 и от –72 до –74 м.д. соответственно с относительной интенсивностью не более 1–5%.
Рис. 4.
Спектр ЯМР 29Si продукта гидролитической поликонденсации АГМ-9 и ФТМС при мольном соотношении 1 : 3 в течение 50 ч.
В отличие от олигосилсесквиоксанов только с аминопропильными радикалами у атомов кремния смешанные олигомеры являются более стабильными. Так, олигомеры, синтезированные при соотношении АГМ-9 : ФТМС = 1 : 1–1 : 10, не изменяются при хранении их растворов в хлороформе более 30 суток. Эти олигомеры представляют интерес в качестве модификаторов органических термореактивных олигомеров, например эпоксидных.
Список литературы
Feher F.J., Wyndham K.D. // Chem. Commun. 1998. P. 323.
Kim K., Adachi K., Chujo Y. // Polymer. 2002. V. 43. P. 1171.
Zhao Y., Song G., Chen G., Zhou Z., Li Q. // Polym. Plast. Technol. Mater. 2021. V. 60. № 1. P. 37.
Ni M., Chen G., Wang Y., Peng H., Liao Y., Xie X. // Composites. B. 2019. P. 107045.
Mohamed M.G., Kuo S.-W. // Polymers. 2016. V. 8. P. 225.
Zhang Z., Liang G., Lu T. // J. Appl. Polym. Sci. 2007. V. 103. P. 2608.
Weidner R., Zeller N., Deubzer B., Frey V. Pat. 5047492 USA. 1991.
Gravel M.-C., Laine R.M. // ACS Polym. Prepr. 1997. V. 38. P. 155.
Neyertz S., Brown D., Pilz M., Rival N., Arstad B., Mannle F., Simon C. // J. Phys. Chem. B. 2015. V. 119. № 21. P. 6433.
Feher F.J., Wyndham K.D., Soulivong D., Nguyen F. // J. Chem. Soc., Dalton Trans. 1999. P. 1491.
Zaikin V.G., Borisov R.S., Polovikov N.Yu., Filatov S.N., Kireev V.V. // Eur. J. Mass Spectrom. 2009. V. 15. P. 231.
Борисов Р.С., Половков Н.Ю., Заикин В.Г., Филатов С.Н. // Масс-спектрометрия. 2008. Т. 5. № 1. С. 25.
Bredov N.S., Shporta E.Yu., Liu Yanqing, Kireev V.V., Borisov R.S., Gorlov M.V., Posokhova V.F., Chuev V.P. // Polymer Science B. 2013. V. 55. № 7−8. P. 472.
Bredov N.S., Le Phu Soan, Kireev V.V., Bykovskaya A.A., Sokol’skaya I.B., Gorlov M.V., Esin A.S., Bekmukhamedova S.R., Polyakov V.A. // Polymer Science B. 2017. V. 59. № 3. P. 240.
Kaneko Y., Shoiriki M., Mizumo T. // J. Mater. Chem. 2012. V. 22. P. 14475.
Tokunaga T., Koge S., Mizumo T., Ohshita J., Kaneko Y. // Polym. Chem. 2015. V. 6. P. 3039.
Janeta M., John L., Ejfler J., Szafert S. // RSC Adv. 2015. V. 5. P. 72340.
Liu S., Lang X., Ye H., Zhang S., Zhao J. // Eur. Polym. J. 2005. V. 41. P. 996.
Wang H., Wang X., Yu C. // Appl. Mechan. Mater. 2012. V. 182–183. P. 114.
Liu S., Fu Y., Jiang Z., Zhao J., Zhang C. // J. Wuhan Univ. Technol. Mater. Sci. Ed. 2009. V. 24. P. 945.
Van Blaaderen A., Vrij A. // J. Colloid Interface Sci. 1993. V. 156. P. 1.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия Б)